Gli antipsicotici sono il pilastro del trattamento acuto e a lungo termine dei disturbi schizofrenici. Quanto prima inizia il trattamento antipsicotico, tanto maggiore è la possibilità di controllare o arrestare la progressione della psicosi.
Il termine schizofrenia è stato coniato da Eugen Bleuler e pubblicato per la prima volta nel 1911 nella sua monografia “Gruppo di schizofrenie”. Questo termine tecnico di 108 anni fa per il disturbo psicotico più importante è ancora in uso oggi. Sei anni fa, il DSM-5, il manuale diagnostico americano, ha introdotto il termine “disturbo dello spettro schizofrenico”. Tuttavia, il primo trattamento veramente efficace per il disturbo schizofrenico non fu disponibile negli ospedali psichiatrici fino al 1952/53. Questa terapia era basata sui farmaci: Clorpromazina. La clorpromazina fu portata direttamente dalla clinica universitaria psichiatrica di Parigi alla clinica universitaria di Basilea già nel 1952 da Felix Labhart. Si può presumere che questo sia stato fatto senza grandi sforzi burocratici all’epoca.
Breve storia dei neurolettici/antipsicotici
La clorpromazina/Largactil® ha portato, negli anni successivi, a uno sconvolgimento della psichiatria istituzionale dell’epoca. Secondo il Prof. Raymond Battegay, i reparti cosiddetti “irrequieti” con gli psicotici agitati sono diventati improvvisamente meno rumorosi e molto più rilassati. Erano ora possibili modi nuovi e più umani di trattare questi malati mentali gravi.
Il termine “neurolettico” deriva dal greco ed è stato introdotto nella letteratura scientifica da Delay e Deniker nel 1955. L’obiettivo era quello di sviluppare un modello ‘eziologico’ per la modalità d’azione dei nuovi farmaci antipsicotici. I due francesi avevano scoperto che la clorpromazina ha effetti sedativi e ansiolitici. Di conseguenza, è stato utilizzato per l’agitazione psicomotoria soprattutto nei pazienti schizofrenici.
L’introduzione dei neurolettici ha aperto una porta importante nel trattamento dei disturbi schizofrenici. In primo luogo, si trattava di un trattamento reversibile (ad esempio, in contrasto con le lobotomie ancora in uso all’epoca) e, in secondo luogo, l’effetto era rapido ed efficace. Questo ha portato a una massiccia riduzione della durata del soggiorno delle persone psicotiche negli istituti dell’epoca, che ha alleggerito gli ospedali sovraffollati. Le ricadute si sono verificate quando i pazienti hanno smesso di assumere il farmaco. I motivi erano la mancanza di conoscenza della malattia o effetti collaterali non trascurabili, come sedazione massiccia, parkinsonismo (EPMS) o fotosensibilità.
Scoperta della dopamina come neurotrasmettitore
All’incirca nello stesso periodo in cui la clorpromazina fu introdotta negli ospedali psichiatrici, Arvid Carlsson (1923-2018) in Svezia scoprì la dopamina, la sua struttura e la sua funzione come importante neurotrasmettitore nel cervello. Con il loro lavoro, Carlsson e Lindqvist hanno anche fondato l’ipotesi della dopamina nelle psicosi, che è stata successivamente stabilita da van Rossum e Snyder ed è tuttora valida. Questo afferma che gli antagonisti della dopamina, cioè i neurolettici o gli antipsicotici, occupano i recettori della dopamina (in particolare i recettori D2) a livello postsinaptico e quindi bloccano la neurotrasmissione della dopamina. Il risultato è un miglioramento dei sintomi positivi del disturbo schizofrenico. Mentre i neurolettici tipici migliorano principalmente le delusioni e le allucinazioni, hanno scarso effetto o addirittura peggiorano le caratteristiche della malattia in seguito definite sintomi negativi, come l’appiattimento affettivo, l’alogia, il ritiro sociale e l’apatia. In questo caso, la clozapina e gli antipsicotici atipici, meglio conosciuti come antagonisti della serotonina-dopamina, hanno portato un chiaro ampliamento dello spettro d’azione.
Introduzione di farmaci antipsicotici
Dopo l’introduzione della clorpromazina nel 1952, nei 20 anni successivi sono stati approvati diversi neurolettici cosiddetti triciclici, alcuni dei quali sono ancora oggi disponibili:
- Dal gruppo di sostanze fenotiaziniche (clorpromazina, levomepromazina, flufenazina, promazina e triflupromazina),
- Dal gruppo di sostanze dei tioxanteni (clorprotixene e flupentixolo).
Nello stesso periodo, sono stati approvati altri neurolettici con strutture non tricicliche ma con profili di effetti collaterali simili:
- Dal gruppo di sostanze dei butirofenoni (aloperidolo, pipamperone, melperone),
- Dal gruppo di sostanze delle difenilbutilpiperidine (fluspirilene e pimozide/ oggi non più in commercio).
La classificazione di cui sopra in base agli aspetti chimico-strutturali si basa sui libri di testo di Möller et al (2015) e Kaplan Sadock (2015).
Nel 1972, in Svizzera è stata approvata la clozapina (scoperta già nel 1959), che ha mostrato un profilo d’azione particolare e un diverso spettro di effetti collaterali rispetto ai neurolettici precedenti. L’FDA ha approvato la clozapina solo nel 1990, motivo per cui gli Stati Uniti hanno scoperto la sua unicità solo più tardi. È stato il primo “antipsicotico atipico”:
- Dal gruppo di sostanze dibenzodiazepine (clozapina): questo gruppo è anche chiamato “pini” da St. Stahl nel suo libro di testo a causa della loro fine: Cloza-pin; Questi includono olanzapina, quetiapina (entrambi strettamente correlati strutturalmente alla clozapina); asenapina e zotepina. Ciò che queste sostanze hanno in comune è il loro profilo multi-recettore.
Altri antipsicotici atipici:
- Dal gruppo di sostanze dei benzisoxazoli (risperidone e ziprasidone); per semplicità, il termine ombrello “dones” (risperi-dones) suggerito da St. Stahl viene utilizzato anche per le sostanze che sono simili in termini di recettori: Risperidone, Paliperidone, Lurasidone, Ziprasidone. Questi hanno una farmacologia recettoriale meno “ricca” rispetto ai “pini” e, a dosi più elevate con EPMS, hanno UAW simili agli antagonisti della sola dopamina. Risperidone e paliperidone possono anche provocare un aumento dose-indipendente della prolattina.
- Dal gruppo di sostanze dei derivati della piperazina (aripiprazolo, brexpiprazolo e cariprazina). Queste sostanze mostrano un effetto nuovo e farmacologicamente molto interessante. Sono agonisti parziali della dopamina. St. Stahl li chiama “due pipi e uno strappo”, che si rifà ai loro nomi: Ari-pip-razolo, Brex-pip-razolo e Ca-rip-razina; nel nostro Paese sono chiamati memotecnicamente l’ABC degli agonisti parziali della dopamina.
La caratteristica comune a tutte queste nuove sostanze (“pini/doni/due pipi e uno strappo”) è l’antagonismo combinato della serotonina (5-HT2A) e della dopamina D2. Sono stati introdotti in Svizzera dopo il 1990. L’aripiprazolo è disponibile in Svizzera dal 2004, la cariprazina e il brexpiprazolo dal 2018. A ciò ha fatto seguito, in Europa (non negli Stati Uniti), l’introduzione di altre nuove sostanze antipsicotiche del gruppo delle benzamidi (sulpiride nel 1972 e amisulpride nel 1999); anche l’amisulpride è considerata un antipsicotico atipico, sebbene sia prevalentemente un antagonista D2 e D3. A dosi più elevate, sono noti gli EPMS e soprattutto l’aumento significativo della prolattina.
Agonismo parziale della dopamina
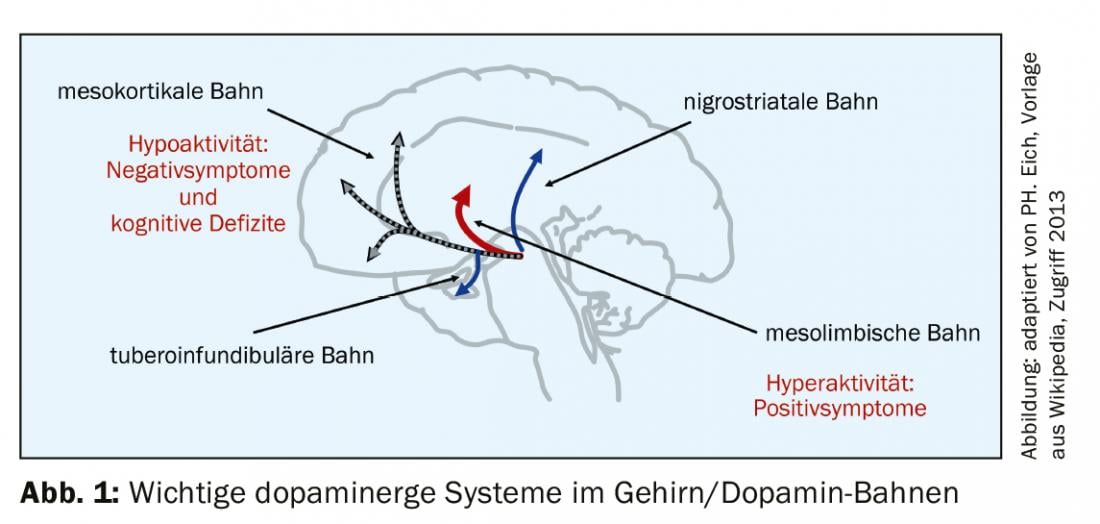
Il razionale dell’agonismo parziale della dopamina è la compensazione ottimale della disregolazione dopaminergica associata alla psicosi (ipotesi dopaminergica della psicosi). Lo sfondo è costituito dalle note vie della dopamina nel cervello (Fig. 1) . In queste condizioni ha senso,
- Diminuiscono l’attività dopaminergica nella via mesolimbica (migliorano i sintomi positivi come le illusioni e le allucinazioni attraverso un’azione antagonista).
- Aumenta l’attività dopaminergica nella via mesocorticale (i sintomi negativi e anche i deficit cognitivi migliorano grazie all’effetto agonistico sul recettore della dopamina).
- non hanno alcun effetto sulle vie nigrostriatali o tuberoinfundibolari (nessun cambiamento nella funzione motoria, nessuna EPMS e nessun aumento della prolattina).
L’aripiprazolo ottiene questo effetto bloccando contemporaneamente il recettore D2 postsinaptico e l’autorecettore presinaptico. Il risultato è un effetto agonistico parziale, ma anche un effetto intrinseco della dopamina di circa il 30%. Un eccesso di antagonismo avvicina la sostanza ai classici antagonisti della dopamina, un eccesso di agonismo porta ad un aumento dei sintomi psicotici.
Tutti e tre gli agonisti parziali della dopamina presentano la costellazione tipica degli antipsicotici atipici, con un antagonismo sull’asse della serotonina con 5-HT2A, ma con il già citato agonismo parziale per il recettore D2 e anche per il recettore 5-HT1A, che potrebbe essere una spiegazione dell’effetto antidepressivo delle sostanze.
L’aripiprazolo mostra poche prove farmacologiche di sedazione (basso blocco H1 e basso effetto muscarinergico/anticolinergico M1). Inoltre, ha uno scarso aumento di peso e un basso effetto diabetogeno. L’aripiprazolo è disponibile in Svizzera dal 2004 ed è a disposizione dei medici sia per via orale che intramuscolare e anche come depot.
Secondo St. Stahl, il brexpiprazolo è un agonista della dopamina più debole rispetto all’aripiprazolo, ma mostra un antagonismo più forte sul recettore 5-HT2A, un effetto agonista parziale più forte sul recettore 5-HT1A e un maggiore antagonismo alfa-1. Questo significa poca EPMS e soprattutto meno acatisia.
La cariprazina si comporta in modo simile al brexpiprazolo in termini di antagonismo (5-HT2A) e agonismo parziale (D2 e 5-HT1A), ma ha un ulteriore agonismo parziale per il recettore D3, che si pensa promuova il rilascio di dopamina nell’area mesocorticale. Questo sarebbe favorevole per il trattamento dei sintomi negativi. Le proprietà di riduzione dell’acatisia del brexpiprazolo sono meno presenti con la cariprazina. Inoltre, come con l’aripirazolo, il recettore dell’istamina è moderatamente bloccato, il che potrebbe spiegare una certa stanchezza (St. Stahl, 2013).
Le differenze tra i tre agonisti parziali della dopamina sono state raccolte da L. Citrome, 2018, anche se va notato che i confronti non sono ponderati testa a testa, ma indirettamente rispetto al placebo (Tabella 1).

Nomenclatura degli antipsicotici
La denominazione chimica strutturale delle sostanze attive antipsicotiche è stata utilizzata principalmente nelle pubblicazioni scientifiche e quando sono state introdotte nuove sostanze. Non era molto pratico nella pratica quotidiana della prescrizione. La maggior parte degli antipsicotici introdotti sul mercato prima della clozapina (CH 1972/USA 1990) si differenziavano per la gamma di dosi e per la sedazione (bassa potenza contro media potenza contro alta potenza), ma in termini di frequenza di EPMS ci sono solo differenze minori (Panoramica 1).

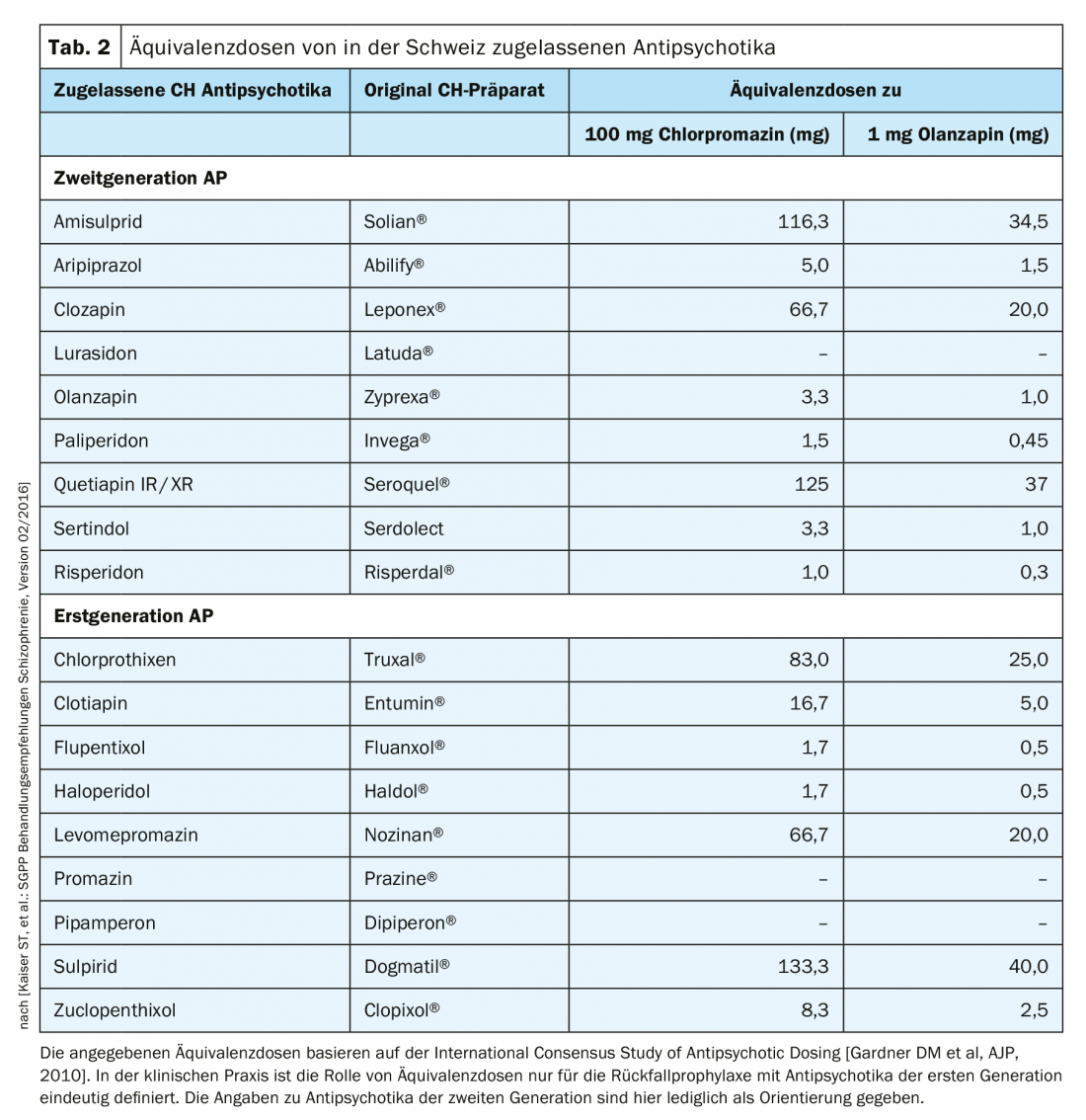
L’adozione di questa classificazione in base alla potenza antipsicotica e le tabelle di equivalenza della dose da essa derivate, tradizionalmente calibrate su 100 mg di clorpromazina, sono ormai superate per gli antipsicotici atipici e difficili da stabilire a causa dei profili di effetti collaterali molto diversi. Il gruppo di lavoro svizzero intorno a St. Kaiser et al. ha comunque incluso tale valutazione di equivalenza degli antipsicotici atipici, misurata a 1 mg di olanzapina, nelle raccomandazioni terapeutiche del 2016 (tab. 2). La clozapina non provoca EPMS, discinesia tardiva o aumento della prolattina. Il suo profilo di effetti collaterali è associato, ad esempio, ad agranulocitosi, aumento di peso o sialo-arrea. Pertanto, la clozapina è stata la prima ad essere assegnata al nuovo gruppo di antipsicotici atipici.
In contrasto con la psichiatria europea, soprattutto di lingua tedesca, il termine “antipsicotici” si è affermato presto nei Paesi di lingua inglese al posto di neurolettici. Al più tardi dall’introduzione della clozapina negli Stati Uniti nel 1990, si parla solo di antipsicotici e si fa una distinzione tra sostanze tipiche e atipiche. Sinonimi, e soprattutto nei libri di testo, sono classificati come antipsicotici di prima generazione (FGA) o antipsicotici di seconda generazione (SGA). Questo non significa una classe di sostanze uniforme, perché gli antipsicotici più recenti sono strutturalmente molto diversi e hanno un profilo recettoriale notevolmente differente. Fondamentalmente, nella letteratura scientifica in lingua inglese, tutte le sostanze antipsicotiche introdotte dopo il 1990 sono definite “antipsicotici atipici” (Linee guida Maudsley, 2018). Negli ultimi anni, il Collegio Europeo di Neuropsicofarmacologia (ECNP) ha diffuso una nuova nomenclatura, che classifica le sostanze in base alla farmacologia e alla modalità d’azione: Nomenclatura basata sulle neuroscienze (NbN2, 2018). Solo il tempo ci dirà se questa sofisticata classificazione prevarrà. Dopotutto, nel loro testo standard di psichiatria, Kaplan Sadock (2015) si riferisce agli antipsicotici tipici come antagonisti della dopamina e alle sostanze atipiche come antagonisti della serotonina-dopamina, poiché hanno questo principio d’azione in comune (sviluppo della nomenclatura).
Cosa fa questa discussione accademica per il paziente?
I pazienti di solito sono principalmente scettici/critici quando viene loro prescritto un antipsicotico. Soprattutto, per loro è importante un effetto efficace senza reazioni avverse ai farmaci.
Creare o mantenere buoni antipsicotici dal punto di vista del paziente (estratto):
- Nessun sintomo di crampi (EPMS)
- Nessuna irrequietezza (acatisia)
- Nessuna lingua pesante, nessun problema di deglutizione (EPMS, discinesia precoce).
- Peso corporeo stabile
- Nessuna sedazione/essere sedati
- Potenza/Libido
- Nessun appiattimento dell’effetto
- Nessuna “dipendenza
- Nessun “danno genico
Nella scelta di un antipsicotico, occorre quindi prestare attenzione alla sicurezza e alla tollerabilità ottimali con una buona efficacia (Panoramica 2) . Allo stesso tempo, i criteri sopra citati sono decisivi per consigliare il farmaco più adatto all’individuo. È importante procedere nel senso di un processo decisionale condiviso e tenere conto dei desideri del paziente.

Per i pazienti psicotici al primo episodio (FEP = First Episode Psychosis), la maggior parte delle linee guida internazionali raccomandano la somministrazione di un antipsicotico del tipo “a base di sangue”. 2a generazione, per cui quelli della Anche la terza generazione può essere inclusa in questa categoria. Questo vale anche per le raccomandazioni terapeutiche svizzere (Kaiser et al. 2016/18). Gli antipsicotici di prima generazione (ad esempio, l’aloperidolo) sono oggi la seconda scelta nel trattamento dei disturbi psicotici. L’eccezione è l’uso nel trattamento del delirio (Eich PH, Nick B. 2018).
Conclusione
La moderna farmacoterapia del disturbo schizofrenico deve svolgere molteplici funzioni, cioè la prospettiva di trattamento dei pazienti è multifocale. Lo farà allo stesso tempo:
- Conoscere gli antipsicotici di prima generazione ed essere consapevoli dei loro vantaggi e svantaggi.
- Essere efficace con il minor numero possibile di reazioni avverse ai farmaci (ADR).
- Essere personalizzato, cioè adattato alle persone interessate (se sono disponibili indicatori appropriati).
- Essere riparativi con l’obiettivo: Restitutio ad integrum, cioè preservare la funzione e riabilitare.
- Essere inseriti in un’assistenza basata sulla comunità e sui bisogni.
Da una prospettiva clinica, la Antipsicotici del 2. e Terza generazione vantaggi evidenti rispetto alle sostanze tipiche. Per quanto riguarda Ippocrate e il suo principio: “Primum non nocere – secundum cavere – tertium sanare” (primo, non nuocere/non provocare danni – secondo, prestare attenzione – terzo, curare/contribuire alla guarigione/traduzione dell’ autore), gli agonisti parziali della dopamina, con il loro profilo favorevole di effetti collaterali, sono sicuramente farmaci di prima scelta.
Messaggi da portare a casa
- Gli antipsicotici rimangono oggi il pilastro del trattamento acuto e a lungo termine dei disturbi schizofrenici. Storicamente, attualmente abbiamo una gamma abbastanza ampia di sostanze antipsicotiche moderne tra cui scegliere.
- L’ordine del trattamento farmacologico si basa sulla psicopatologia e sul livello di sofferenza dei pazienti affetti. Va notato che quanto prima inizia il trattamento antipsicotico, tanto maggiore è la possibilità di controllare o arrestare la progressione della psicosi.
- La non aderenza è il fattore di ricaduta più importante.
- L’uso degli antipsicotici deve essere discusso nel processo decisionale condiviso; una buona conoscenza della modalità d’azione e dei potenziali effetti avversi è un prerequisito.
- Gli antipsicotici di terza generazione (aripiprazolo, brexpiprazolo e cariprazina) sono un passo importante nella giusta direzione.
Ulteriori letture:
- Citrome L: Psichiatria attuale, 17(4), aprile 2018
- Eich PH, Nick B: Numero speciale “Schizofrenia”, Therapeutische Umschau, 01/2018.
- Kaiser ST, et al: Raccomandazioni di trattamento SGPP per la schizofrenia, versione febbraio 2016; www.psychiatrie.ch/sgpp/fachleute-und-kommissionen
- Kaiser ST, et al: Raccomandazioni di trattamento SGPP per la schizofrenia, Swiss Med Forum 2018; 18(25): 532-539.
- Taylor D, et al: The Maudsley Prescribing Guidelines in Psychiatry 13th edition, Wiley Blackwell, 2018.
- Nomenclatura basata sulle neuroscienze (NbN-2R), pubblicato da ECNP, 2018.
- Falkai P, Wittchen HU: Diagnostisches und Statistisches Manual Psychischer Störungen DSM-5, APA, 2013; Hogrefe 2015
- Kaplan & Sadock’s Synopsis of Psychiatry, 11ª edizione, Wolters Kluwer, 2015.
- Möller HJ, Laux G, Deister A: Psichiatria, psicosomatica e psicoterapia, 6a edizione, Thieme Verlag, 2015.
- Stahl ST: Essential Psychopharmacology, 4th ed, Cambridge University Press, 2013.
- Woggon B: Behandlung mit Psychopharmaka, 3a edizione, Huber Verlag, 2009.
InFo NEUROLOGIA & PSICHIATRIA 2019; 17(6): 16-21.














