Con l’aumento del numero di terapie sistemiche, i consigli pratici sulla scelta dell’opzione terapeutica più adatta stanno diventando sempre più importanti. La nuova edizione della linea guida S3 sulla dermatite atopica, pubblicata quest’anno, contiene numerose indicazioni basate sull’evidenza per l’uso di biologici e inibitori della Janus chinasi. Oltre a dupilumab, nella linea guida sono stati inclusi anche tralokinumab, abrocitinib, baricitinib e upadacitinib rispetto alla versione precedente, con le relative informazioni sull’attuazione della terapia.
Se utilizzati in modo appropriato, i biologici e gli inibitori JAK hanno un grande potenziale nella terapia sistemica dei pazienti con forme da moderate a gravi di dermatite atopica (AD). Ciò che accomuna tutti questi moderni principi attivi sistemici è che sono particolarmente adatti a determinati sottogruppi di pazienti e devono essere utilizzati come parte di un piano di trattamento personalizzato. Per ottenere i migliori risultati terapeutici possibili, è consigliabile soppesare i profili di rischio-beneficio sia a livello di classi di sostanze che per ogni singolo principio attivo [1]. Gli anticorpi monoclonali attualmente approvati per l’AD (dupilumab, tralokinumab) (Tabella 1) vengono somministrati per via sottocutanea e, a differenza degli inibitori della JAK, non richiedono esami di laboratorio o strumentali né prima dell’inizio del trattamento né durante il trattamento [1]. Tre inibitori della JAK (abrocitinib, baricitinib, upadacitinib) sono attualmente approvati per la terapia a lungo termine (Tabella 2) . Sono disponibili in forma di dosaggio orale, per cui è necessario uno screening prima di iniziare il trattamento e un monitoraggio durante la terapia [1].
Determinare la gravità dell’AD in base a parametri oggettivi e soggettivi.
I punteggi cutanei convalidati includono lo SCORAD (Scoring Atopic Dermatitis Index) e l’EASI (Eczema Area and Severity Index) [2]. Il punteggio massimo, cioè la massima gravità dell’AD, è di 83 punti per lo SCORAD, 103 punti per l’Indice SCORAD e 72 punti per l’EASI. Inoltre, gli studi clinici utilizzano spesso la più semplice IGA (Investigators’ Global Assessment), che di solito utilizza una scala di gravità dell’AD da 0 a un massimo di 4 punti. La linea guida raccomanda anche di registrare gli aspetti soggettivi riferiti dai pazienti utilizzando strumenti validati [3]. Oltre al prurito e all’insonnia, questo include anche la registrazione di altri sintomi (ad esempio, il questionario POEM) e della qualità di vita (ad esempio, il questionario CDLQI/DLQI). Anche le complicazioni dell’AD e le comorbidità extracutanee possono essere prese in considerazione per oggettivare la gravità della malattia [4].
Dupilumab e tralokinumab – non è richiesto il monitoraggio di laboratorio
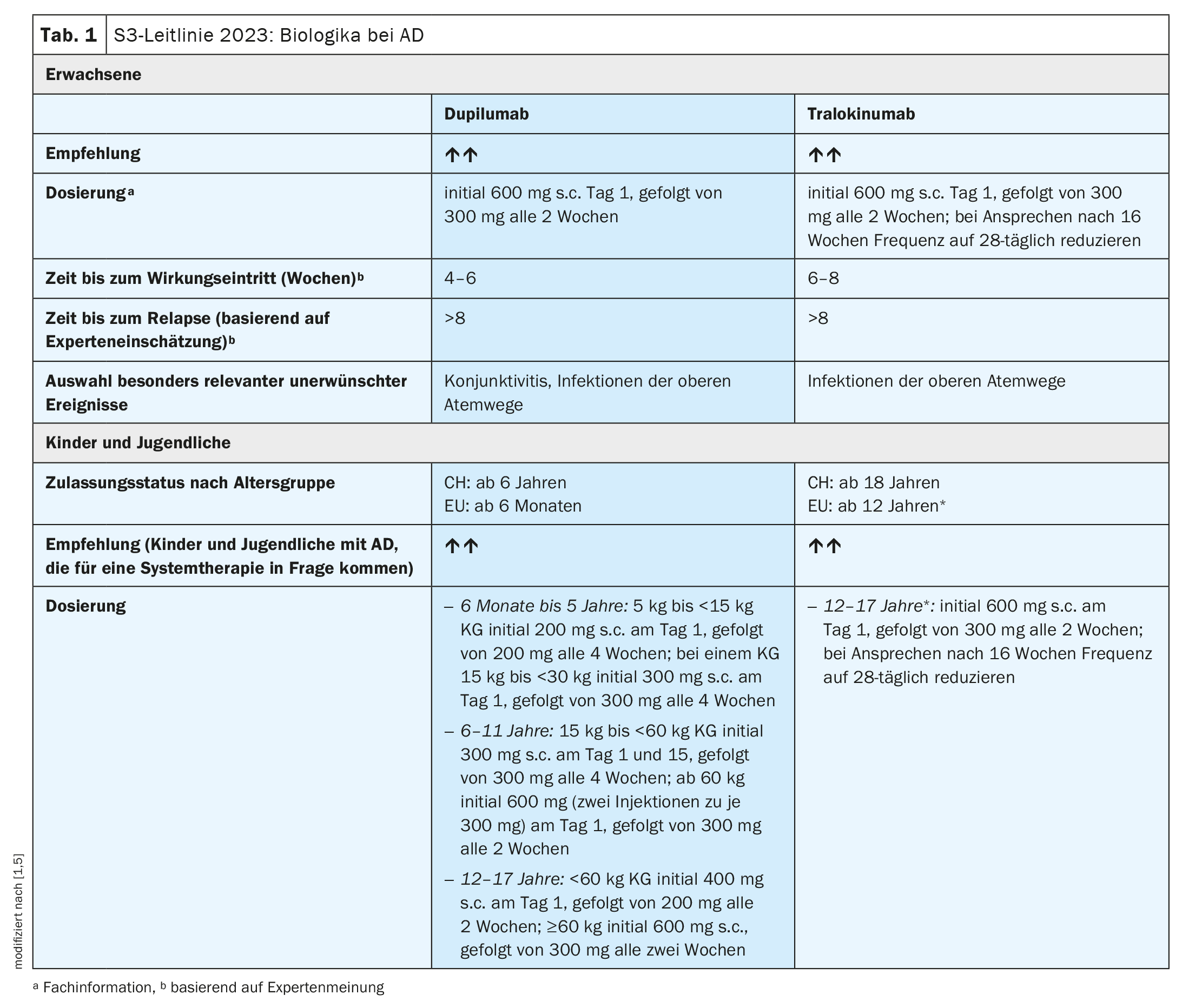
Sia dupilumab, un anticorpo monoclonale (mAb) che inibisce la segnalazione dell’interleuchina (IL)-4 e dell’IL-13, sia tralokinumab – un mAb che neutralizza l’IL-13 – sono raccomandati come terapia a lungo termine per l’AD da moderata a grave. In Svizzera, dupilumab è autorizzato a partire dall’età di 6 anni e tralokinumab a partire dall’età di 18 anni. Dupilumab è preferibile nei pazienti con asma bronchiale coesistente, rinosinusite cronica**, prurigo nodularis o esofagite eosinofila, in quanto sono disponibili prove specifiche di efficacia nei pazienti con AD con queste comorbidità.
** senza/con polipi nasali
Dupilumab (Dupixent®): Il dosaggio approvato negli adulti consiste in una dose sottocutanea iniziale di 600 mg, seguita da dosi di mantenimento di 300 mg ogni due settimane [1,5]. Per i bambini, si utilizzano regimi di dosaggio a seconda del gruppo di età e del peso corporeo (bw) (Tabella 1 ).
Tralokinumab (Adtralza®): Il dosaggio raccomandato dalla linea guida per gli adulti e gli adolescenti di età pari o superiore a 12 anni è di 300 mg ogni 2 settimane, dopo una dose iniziale di 600 mg all’inizio del trattamento [1]. In Svizzera, il tralokinumab è attualmente autorizzato solo a partire dai 18 anni di età [5]. La frequenza di dosaggio deve essere ridotta da ogni 14 giorni a ogni 28 giorni dopo 16 settimane, se c’è una risposta alla terapia [1]. Nel corso successivo, la frequenza di dosaggio (14 o 28 giorni) deve essere adattata alla manifestazione clinica.
Gli inibitori della JAK sono rapidamente efficaci – l’uso appropriato è fondamentale
Con gli inibitori della JAK, è particolarmente importante chiarire il rischio individuale di infezioni gravi prima di iniziare il trattamento [1]. L’uso non è raccomandato in caso di anamnesi di eventi tromboembolici o di un aumento del rischio di trombosi geneticamente determinato. La linea guida sottolinea che, secondo una procedura di valutazione del rischio pubblicata dalla Commissione Europea nel marzo 2023, gli inibitori della JAK dovrebbero essere utilizzati nei seguenti gruppi di pazienti solo se non sono disponibili alternative terapeutiche adeguate [1]: Età ≥65 anni, rischio cardiovascolare noto (ad esempio, infarto o ictus), fumatori (attuali o ex fumatori a lungo termine), aumento del rischio di cancro. Si consiglia cautela in presenza di fattori di rischio per coaguli di sangue nei polmoni e nelle vene profonde (tromboembolismo venoso), anche se i pazienti non appartengono ai gruppi di rischio sopra citati. Se gli inibitori della JAK vengono utilizzati in pazienti a rischio di tromboembolismo venoso, cancro o gravi problemi cardiovascolari, è necessario utilizzare una dose ridotta.
Baricitinib (Olumiant®) è un inibitore selettivo di JAK1 e JAK2, per il quale è raccomandata una dose giornaliera di 2 mg e 4 mg sia nella linea guida che secondo l’autorizzazione Swissmedic [1,5]. La linea guida sottolinea che il trattamento può essere iniziato con il dosaggio più alto nei pazienti di età inferiore ai 65 anni con MA grave, dopo aver escluso le controindicazioni. I pazienti affetti da AD con coesistente alopecia areata o artrite reumatoide in comorbidità traggono particolare beneficio da baricitinib, a condizione che siano soddisfatti i requisiti per la terapia sistemica con inibitori JAK.
Abrocitinib (Cibinqo®) è un inibitore selettivo di JAK1 che può essere utilizzato in una dose giornaliera di 100 mg o 200 mg secondo la linea guida [1]. Va notato che la terapia per l’MA grave può essere iniziata con il dosaggio più alto nei pazienti di età ≤64 anni, dopo aver escluso le controindicazioni, e il dosaggio deve essere adattato al decorso clinico dopo la risposta alla terapia. Secondo l’autorizzazione di Swissmedic, tuttavia, il dosaggio raccomandato è limitato a 100 mg/giorno [5].
Anche l’upadacitinib (Rinvoq®) è un inibitore selettivo di JAK1. La linea guida raccomanda dosi di 15 mg e 30 mg al giorno [1]. Come per gli altri due inibitori della JAK, va notato che upadacitinib può essere iniziato alla dose più alta nella DA grave, dopo aver escluso le controindicazioni, e la dose deve essere aggiustata nel corso del trattamento, se c’è una risposta. Secondo l’autorizzazione di Swissmedic, tuttavia, è disponibile una raccomandazione di dosaggio solo per 15 mg al giorno. I pazienti affetti da malattie concomitanti come l’artrite reumatoide, l’artrite psoriasica, la spondilite anchilosante e la spondiloartrite assiale o la colite ulcerosa sembrano trarre particolare beneficio da upadacitinib.
| La linea guida, aggiornata sotto gli auspici della Società Dermatologica Tedesca, ha come obiettivo principale quello di fornire un aggiornamento basato sull’evidenza su tutti gli aspetti della cura dei pazienti con dermatite atopica, al fine di fornire ai medici il miglior supporto possibile nel loro trattamento. Alla stesura delle linee guida hanno partecipato numerosi esperti di fama provenienti da Germania, Austria e Svizzera. Come nelle versioni precedenti, le opzioni di trattamento topico e la terapia sistemica sono trattate in capitoli separati. La gamma di biologici e di inibitori della Janus chinasi (JAK) è stata ampliata dall’ultimo aggiornamento delle linee guida. Oltre ai principi attivi autorizzati, la linea guida cita anche lebrikizumab, nemolizumab e omalizumab come promettenti candidati farmaci attualmente in fase di ricerca per il trattamento sistemico della dermatite atopica. |
| secondo [1] |
Terapia antipruriginosa: combinare le misure secondo le necessità.
Il prurito è uno dei principali sintomi clinici dell’AD e rappresenta anche una sfida e un peso psicologico particolare [1]. Il trattamento del prurito richiede un approccio multidimensionale che mira a influenzare diversi fattori, tra cui la secchezza della pelle, i processi infiammatori, i fattori scatenanti, l’alterazione dell’elaborazione degli stimoli e i cambiamenti neuroendocrini. La maggior parte degli agenti terapeutici utilizzati nel trattamento dell’AD sono mirati a trattare l’infiammazione e di solito hanno un effetto indiretto sul prurito. Gli effetti di alleviamento del prurito degli approcci terapeutici psicoeducativi, di riduzione dello stress e psicoterapeutici sono descritti nella linea guida in un capitolo separato (“Misure psicoeducative, psicosociali e psicoterapeutiche”) [1].
Aspetti generali della gestione della malattia
Il trattamento dell’AD richiede una serie di misure che devono essere adattate individualmente al paziente [1]. Oltre a evitare i fattori di esacerbazione individuali, questo include una terapia di base personalizzata e un trattamento antinfiammatorio topico e/o sistemico. Si consiglia di elaborare un piano di trattamento personalizzato. In generale, si raccomanda un approccio adattato alle fasi, per adattare la terapia alle diverse fasi individuali in base alla gravità e alla cronicità. Tuttavia, lo schema a tappe fornisce solo una linea guida; la terapia deve essere adattata individualmente a seconda dell’età, del decorso della malattia, della localizzazione e del livello di sofferenza individuale.
Mentre sono state incorporate nella linea guida alcune innovazioni per quanto riguarda i moderni terapici sistemici dei gruppi di farmaci biologici e inibitori della JAK, come già detto, le raccomandazioni relative agli agenti sistemici convenzionali sono rimaste in gran parte invariate rispetto alla versione precedente. Gli immunosoppressori convenzionali, più ampiamente efficaci, come i glucocorticosteroidi sistemici, la ciclosporina, l’azatioprina, il micofenolato mofetile e il metotrexato, venivano utilizzati in passato più frequentemente per il trattamento sistemico della dermatite atopica grave, rispetto a oggi [1]. Per le terapie sistemiche convenzionali, il rapporto tra beneficio atteso e rischio deve essere valutato individualmente rispetto alle alternative terapeutiche [1]. Con la ciclosporina, un agente terapeutico sistemico ancora oggi comunemente utilizzato, è particolarmente importante assicurarsi che i parametri della pressione arteriosa e della funzionalità renale siano attentamente monitorati.
Letteratura:
- Linea guida 1S3 “Dermatite atopica” (registro AWMF n. 013-027) 2023. Stato: 16/06/2023, valido fino al 15/06/2028.
- Schmitt J, et al.: Assessment of clinical signs of atopic dermatitis: A systematic review and recommendation. J Allergy Clin Immunol 2013; 132: 1337–1347.
- Schmitt J, et al.: Towards global consensus on outcome measures for atopic eczema research: results of the HOME II meeting. Allergy 2012; 67: 1111–1117.
- Charman CR, Venn AJ, Williams HC: The patient-oriented eczema measure – Development and initial validation of a new tool for measuring atopic eczema severity from the patients’ perspective. Archives of Dermatology 2004; 140: 1513–1519.
- Informazioni sui farmaci, www.swissmedicinfo.ch,(ultimo accesso 19/09/2023)
DERMATOLOGIE PRAXIS 2023; 33(5): 40–42