Il trattamento acuto dell’ictus ischemico ha fatto enormi progressi negli ultimi due decenni. Le pietre miliari della ricerca clinica sono la trombolisi endovenosa (IVT) e la ricanalizzazione meccanica. L’IVT viene eseguita dopo aver escluso l’infarto emorragico e altre controindicazioni. Il limite di tempo è stato esteso a 4,5 ore. Diversi studi del 2015 hanno dimostrato la superiorità della ricanalizzazione meccanica rispetto alla terapia conservativa nei pazienti con occlusioni prossimali dei vasi della circolazione anteriore. Sia nella IVT che nella ricanalizzazione meccanica, la grande sfida è ottimizzare le strutture e i processi per realizzare una riperfusione rapida nella pratica clinica quotidiana, anche al di fuori degli studi.
Nei Paesi industrializzati, l’ictus è la causa più comune di disabilità fisica persistente acquisita. I costi per il sistema sanitario derivanti dalle conseguenze di un ictus sono considerevoli. Mentre solo una piccola percentuale di ictus è dovuta a emorragia intracerebrale, la maggior parte ha una genesi ischemica (85-90%).
Il trattamento acuto dell’ictus ischemico ha fatto enormi progressi negli ultimi due decenni. In questo contesto, le pietre miliari della ricerca clinica includono soprattutto la dimostrazione dell’efficacia della trombolisi endovenosa nel 1995 [1] e la ricanalizzazione meccanica nel 2015 [2]. Il rapido ripristino della perfusione nel territorio vascolare interessato è l’obiettivo di entrambe le strategie. La trombolisi endovenosa richiede un impegno tecnico e di personale relativamente ridotto, mentre il trattamento interventistico può essere eseguito solo da un team interdisciplinare ben preparato e altamente specializzato in un centro ospedaliero. I risultati impressionanti degli studi corrispondenti giustificano questo sforzo nelle occlusioni vascolari prossimali.
Trombolisi endovenosa
La trombolisi endovenosa (IVT) con attivatore del plasminogeno tissutale (tPA) è parte integrante della terapia acuta dell’ictus ischemico da 20 anni. L’efficacia di questa terapia è stata successivamente confermata più volte [3–5]. La terapia viene somministrata per via i.v. nell’arco di un’ora a una dose di 0,9 mg/kg di peso corporeo (dose massima 90 mg) dopo aver escluso l’infarto emorragico (ad esempio mediante TAC cranica nativa) e altre controindicazioni, con il 10% della dose somministrata come bolo al basale. Il limite temporale originale di inizio della terapia fino a un massimo di tre ore dopo l’insorgenza dei sintomi è stato ora esteso a 4,5 ore [4]. Nonostante l’estensione della finestra temporale, tuttavia, non bisogna dimenticare che il successo della terapia dipende chiaramente dal tempo, e in nessun caso si deve ritardare la terapia [5]. Più tempo passa dalla comparsa dei sintomi alla terapia, meno il paziente ne trae beneficio e più alto è il rischio di gravi complicazioni.
Raccomandazioni della DGN sull’IVT
In base alla situazione dello studio attuale, le linee guida della Società tedesca di neurologia (DGN) sono state integrate con delle raccomandazioni [6]. Questi si riferiscono, da un lato, all’uso di IVT al di fuori dei criteri di approvazione stabiliti e, dall’altro, alla trombectomia meccanica. Le raccomandazioni più importanti saranno discusse brevemente di seguito. La novità è che le raccomandazioni per l’IVT non specificano più un limite massimo di età. Nei pazienti trattati con anticoagulazione orale, il trattamento al di fuori dei criteri di approvazione può essere preso in considerazione in determinate condizioni, se il rischio di sanguinamento è accettabile:
- in trattamento con antagonisti della vitamina K con un valore di INR fino a 1,7;
- sotto nuovi anticoagulanti orali se il tempo di trombina diluito o il livello di fattore Xa sono normali o se il paziente non ha assunto il farmaco nelle ultime 48 ore con una funzione renale normale.
L’inizio della terapia fino a sei ore dopo l’insorgenza dei sintomi non sembra portare a un aumento significativo del tasso di complicanze e può quindi essere preso in considerazione in casi individuali (ad esempio, imaging di mismatch, imaging collaterale). La terapia di lisi può essere eseguita anche in presenza dei cosiddetti segni precoci di infarto nella finestra temporale di 4,5 ore.
In sintesi, l’IVT presenta poche complicazioni nelle mani di un neurologo che ha familiarità con la terapia, in combinazione con l’assistenza acuta del paziente in una stroke unit e nel rispetto delle controindicazioni assolute.
Terapia endovascolare
Nonostante il successo indiscusso della IVT, il tasso relativamente basso di ricanalizzazione vascolare, soprattutto nelle occlusioni prossimali, ha spinto la ricerca di metodi alternativi [3,7]. In seguito alle procedure di terapia endovascolare consolidate in cardiologia, sono stati fatti vari tentativi per ottenere un tasso di ricanalizzazione più elevato e quindi un risultato clinico migliore mediante l’accesso diretto al trombo. Ci sono state alcune battute d’arresto nel processo, ma nel complesso hanno portato a un chiaro miglioramento della tecnica inizialmente applicata. Tra l’altro, la lisi locale intra-arteriosa con urochinasi, studiata sistematicamente per la prima volta nello studio PROACT, non ha ricevuto l’approvazione negli Stati Uniti a causa di un beneficio clinico insufficiente [8]. Questo processo è stato successivamente abbandonato a favore di processi puramente meccanici. Il posizionamento permanente di uno stent sull’area di occlusione del vaso ha aumentato il tasso di ricanalizzazione, ma ha portato a un aumento delle complicanze emorragiche, soprattutto a causa della doppia inibizione dell’aggregazione piastrinica necessaria dopo l’intervento [9]. Gli stent intracranici sono quindi utilizzati solo in casi eccezionali nella pratica clinica.
Nel 2013 sono stati pubblicati tre studi clinici che hanno analizzato le procedure di ricanalizzazione per le occlusioni vascolari cerebrali prossimali in cui il trombo veniva rimosso meccanicamente (Interventional Management of Stroke III [10], MR RESCUE [11], SYNTHESIS Expansion [12]). Questi studi non sono riusciti a dimostrare la superiorità della terapia endovascolare rispetto alla sola terapia farmacologica. Si possono identificare tre punti deboli per il fallimento di questi studi, che non solo sono stati evitati negli studi successivi (di successo), ma da cui si possono anche ricavare implicazioni per l’azione clinica quotidiana:
- In primo luogo, a volte si sono verificati ritardi drastici fino all’effettiva apertura del vaso, probabilmente dovuti principalmente al fatto che i processi dall’arrivo del paziente all’intervento non funzionavano in modo sufficientemente efficiente.
- In secondo luogo, la selezione dei pazienti è stata inadeguata, soprattutto a causa di una diagnostica per immagini inadeguata. In particolare, non si è riusciti a identificare rapidamente i pazienti idonei con un’occlusione del tronco principale e a escludere dallo studio i pazienti con un nucleo infartuale esteso.
- In terzo luogo, il successo della ricanalizzazione era relativamente basso anche nei pazienti idonei, a causa dell’uso di procedure di trombectomia più vecchie. In particolare, gli stent retriever che hanno avuto successo in seguito sono stati utilizzati solo sporadicamente.
I punti deboli menzionati sono stati affrontati negli studi successivi e hanno portato a risultati impressionanti negli studi finalmente pubblicati nel 2015 (Fig. 1 e 2) . MR-CLEAN è stato il primo studio randomizzato controllato a dimostrare chiaramente un beneficio della trombectomia meccanica [2]. Come diretta conseguenza, sono state condotte analisi ad interim in altri studi in corso (ESCAPE [13], EXTEND-IA [14], REVASCAT [15], SWIFT PRIME [16]), che hanno portato all’interruzione dello studio in tutti i centri, poiché la ricanalizzazione meccanica era già chiaramente superiore alla terapia conservativa a questo punto.
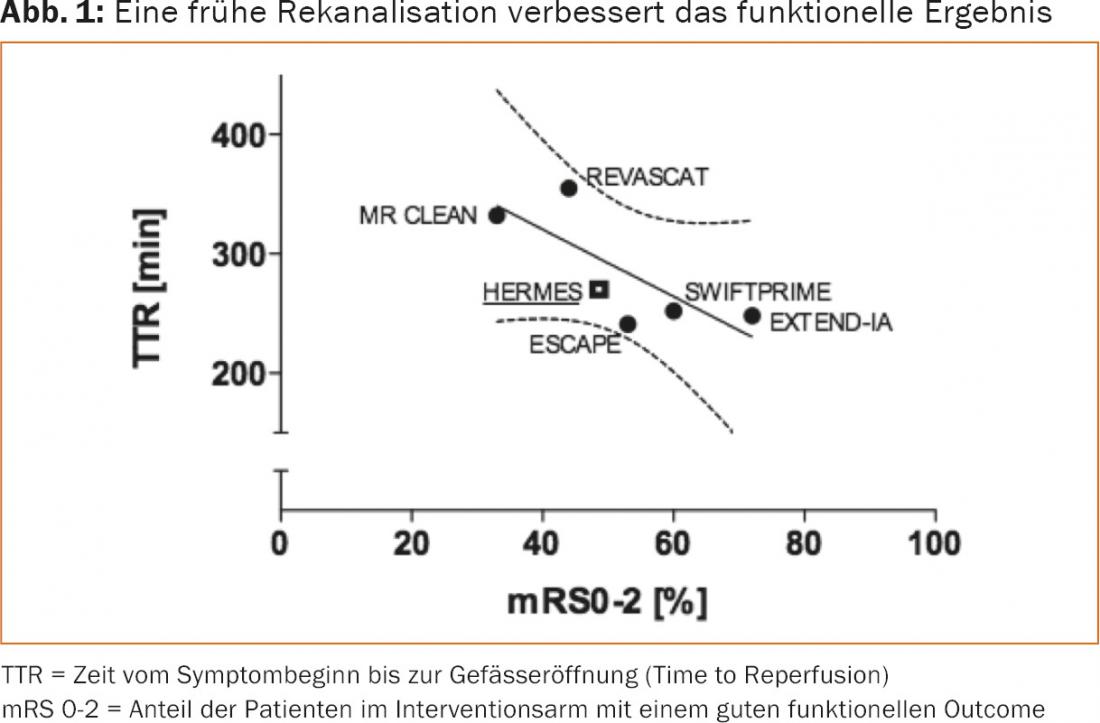
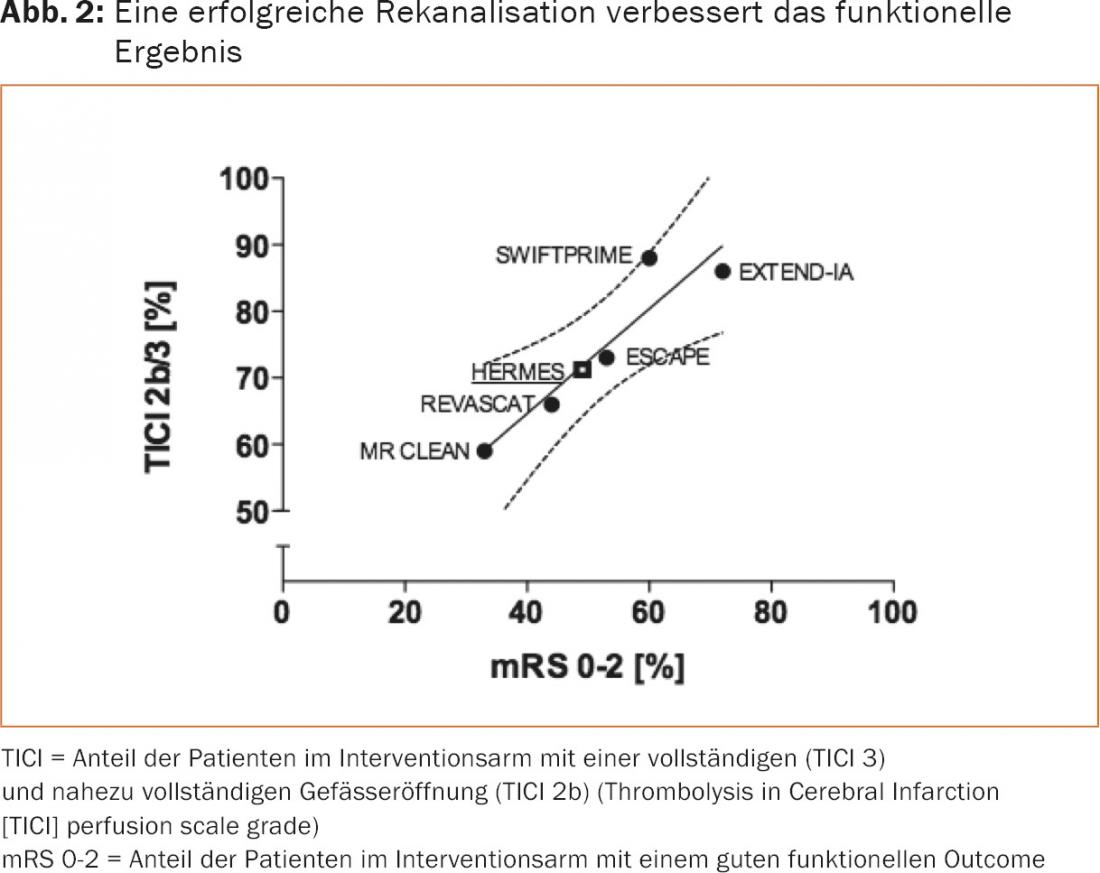
A parte alcune differenze nel disegno dello studio, che non possono essere discusse in dettaglio in questa sede, gli studi mostrano analogie rilevanti nei punti essenziali: I pazienti con occlusione dei vasi prossimali (carotide T e M1) e deficit clinico grave sono stati selezionati in modo specifico, le procedure ospedaliere sono state ottimizzate per una ricanalizzazione rapida (tempo mediano alla puntura inguinale 210-270 minuti) e sono stati utilizzati principalmente stent retrievers (81-100%). In parte, sono stati esclusi anche i pazienti con infarti grandi delimitati precocemente. Questi fattori hanno determinato un miglioramento significativo dell’esito clinico e una riduzione della mortalità a 90 giorni rispetto ai gruppi di controllo, grazie agli elevati tassi di ricanalizzazione (TICI2b/3: 59-88%) con poche complicanze (emorragia intracranica sintomatica: 0-8% ) (Tabella 1).
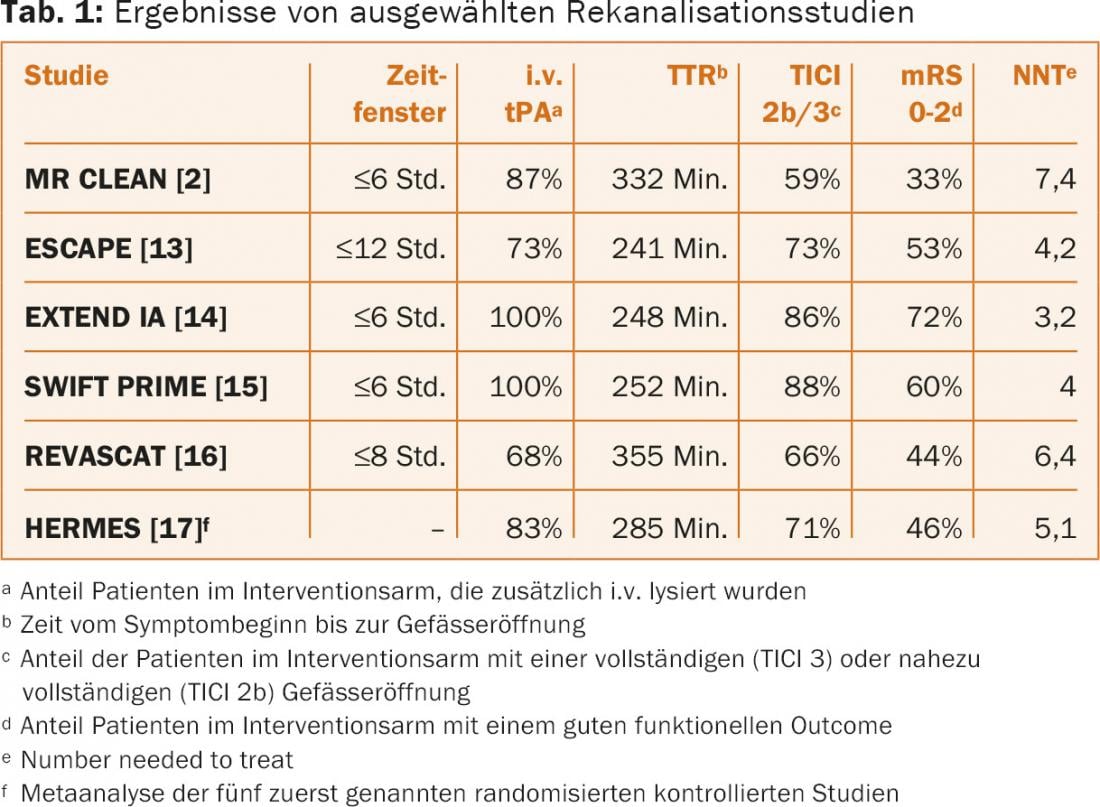
I risultati degli studi sopra citati sono stati recentemente esaminati in una meta-analisi in pool [17]. Questo ha dimostrato che la trombectomia meccanica ha un chiaro beneficio in quasi tutti i pazienti con occlusioni vascolari prossimali della circolazione anteriore, indipendentemente da altri fattori (come l’età).
Raccomandazioni della DGN per la ricanalizzazione meccanica
Come conseguenza degli studi sopra citati, le linee guida DGN per il trattamento dell’ictus ischemico sono state integrate con delle raccomandazioni, che sono brevemente riassunte di seguito.
Imaging vascolare: l’imaging vascolare (TC-A o RM-A) deve essere eseguito immediatamente per consentire una selezione rapida e significativa dei pazienti appropriati.
Finestra temporale: la ricanalizzazione meccanica è raccomandata per le occlusioni prossimali dei vasi della circolazione anteriore fino a sei ore dopo la comparsa dei sintomi. Un’estensione della finestra temporale oltre le sei ore può essere presa in considerazione in casi individuali (ad esempio, con l’aiuto dell’imaging mismatch o dell’imaging collaterale).
IVT: in assenza di controindicazioni, l’IVT deve sempre essere applicata entro 4,5 ore; se ciò non è possibile, la ricanalizzazione meccanica da sola è il trattamento di prima scelta. Le due procedure terapeutiche devono, se possibile, completarsi a vicenda e nessuna delle due procedure deve comportare un ritardo dell’altra. In particolare, non aspettare che l’IVT abbia successo e ritardare i preparativi per la ricanalizzazione meccanica.
Limiti di età: non esiste un limite di età superiore generale.
Durata delle procedure cliniche: per quanto riguarda le procedure cliniche, è richiesto che il tempo dall’arrivo alla puntura inguinale (“door to groin puncture”) non superi i 90 minuti e il tempo tra la puntura inguinale e l’apertura del vaso non superi i 30 minuti.
Fare da ponte: I pazienti indirizzati a ospedali senza possibilità di ricanalizzazione meccanica dovrebbero essere sottoposti a IVT dopo aver escluso le controindicazioni, e dovrebbero essere trasferiti immediatamente in un centro ospedaliero per la ricanalizzazione meccanica (“bridging”) mentre continuano la terapia.
Risultati: Come risultato della ricanalizzazione meccanica, l’apertura completa o quasi completa del vaso deve essere raggiunta in più del 75% dei pazienti (scala di trombolisi nell’infarto cerebrale [TICI]-perfusione di grado 3 o 2b).
Garanzia di qualità: i centri che offrono la ricanalizzazione meccanica sono tenuti a partecipare a programmi di garanzia di qualità e alla certificazione.
In sintesi, la ricanalizzazione meccanica apre nuove prospettive, soprattutto per i pazienti con occlusioni vascolari prossimali nella circolazione anteriore. Una sfida importante resta l’implementazione di strutture e processi per realizzare la riperfusione rapida al di fuori delle sperimentazioni nella pratica clinica quotidiana. Soprattutto, è importante ridurre al massimo le perdite per attrito derivanti dalla collaborazione di tre o più discipline (tra cui la medicina d’urgenza, la neurologia, la neuroradiologia e l’anestesia), perché nella cura dell’ictus ischemico acuto vale ancora l’unica regola d’oro: il tempo è cervello.
Letteratura:
- Attivatore del plasminogeno tissutale per l’ictus ischemico acuto. Il Gruppo di studio sull’ictus rt-PA del National Institute of Neurological Disorders and Stroke. N Engl J Med 1995; 333(24): 1581-1587.
- Berkhemer OA, et al: Uno studio randomizzato sul trattamento intraarterioso per l’ictus ischemico acuto. N Engl J Med 2015; 372(1): 11-20.
- Rha JH, Saver JL: L’impatto della ricanalizzazione sull’esito dell’ictus ischemico: una meta-analisi. Stroke 2007; 38(3): 967-973.
- Hacke W, et al: Trombolisi con alteplase da 3 a 4,5 ore dopo un ictus ischemico acuto. N Engl J Med 2008; 359(13): 1317-1329.
- Emberson J, et al: Effetto del ritardo del trattamento, dell’età e della gravità dell’ictus sugli effetti della trombolisi endovenosa con alteplase per l’ictus ischemico acuto: una meta-analisi dei dati dei singoli pazienti degli studi randomizzati. Lancet 2014; 384(9958): 1929-1935.
- Ringleb PA, et al: Terapia dell’ictus ischemico acuto – supplemento 2015; Terapia ricanalizzante. www.dgn.org/images/red_leitlinien/LL_2015/PDFs_Download/030140_LL_akuter-ischaemischer-schlaganfall_final.pdf, 2015.
- Lee KY, et al: Ricanalizzazione precoce dopo la somministrazione endovenosa di attivatore del plasminogeno tissutale ricombinante, valutata dall’angiografia pre e post-trombolitica nei pazienti con ictus ischemico acuto. Stroke 2007; 38(1): 192-193.
- Furlan A, et al: Prourochinasi intra-arteriosa per l’ictus ischemico acuto. Lo studio PROACT II: uno studio randomizzato e controllato. Prolyse nel tromboembolismo cerebrale acuto. JAMA 1999; 282(21): 2003-2011.
- Chimowitz MI, et al: Stenting rispetto alla terapia medica aggressiva per la stenosi arteriosa intracranica. N Engl J Med 2011; 365(11): 993-1003.
- Broderick JP, et al: Terapia endovascolare dopo t-PA endovenoso rispetto al solo t-PA per l’ictus. N Engl J Med 2013; 368(10): 893-903.
- Kidwell CS, et al: Uno studio sulla selezione dell’imaging e sul trattamento endovascolare per l’ictus ischemico. N Engl J Med 2013; 368(10): 914-923.
- Ciccone A, et al: Trattamento endovascolare per l’ictus ischemico acuto. N Engl J Med 2013; 368(10): 904-913.
- Goyal M, et al: Valutazione randomizzata del trattamento endovascolare rapido dell’ictus ischemico. N Engl J Med 2015; 372(11): 1019-1030.
- Campbell BC, et al: Terapia endovascolare per l’ictus ischemico con selezione di immagini di perfusione. N Engl J Med 2015; 372(11): 1009-1018.
- Jovin TG, et al: Trombectomia entro 8 ore dalla comparsa dei sintomi nell’ictus ischemico. N Engl J Med 2015; 372(24): 2296-2306.
- Saver JL, et al: Trombectomia con stent-retriever dopo t-PA endovenoso rispetto al solo t-PA nell’ictus. N Engl J Med 2015; 372(24): 2285-2295.
- Goyal M, et al: Trombectomia endovascolare dopo un ictus ischemico a grandi vasi: una meta-analisi dei dati dei singoli pazienti di cinque studi randomizzati. Lancet 2016: 387(10029): 1723-1731.
InFo NEUROLOGIA & PSICHIATRIA 2016; 14(4): 17-20.
PRATICA GP 2016; 11(10): 20-23











