Lo stimolatore carotideo è un dispositivo che attiva elettricamente il meccanismo baroreflesso. Questo ha l’effetto di indebolire il tono simpatico e di smorzare il sistema renina-angiotensina-aldosterone, provocando una riduzione della pressione sanguigna e della frequenza cardiaca. La terapia di attivazione del baroreflesso (BAT) porta a una riduzione media permanente della pressione arteriosa sistolica di 40-50 mmHg dopo quattro anni. Oltre all’effetto di abbassamento della pressione sanguigna, nei pazienti è stata osservata una riduzione dello spessore del muscolo cardiaco. L’effetto nei pazienti con insufficienza cardiaca è attualmente in fase di sperimentazione. L’impianto del dispositivo è considerato sicuro. Lo stimolatore carotideo è ora disponibile in diversi Paesi europei.
L’ipertensione arteriosa, definita come pressione arteriosa sistolica superiore a 140 mmHg o pressione arteriosa diastolica superiore a 90 mmHg, colpisce più del 30% degli adulti nel mondo occidentale. Un trattamento efficace della pressione arteriosa porta a una sostanziale riduzione del rischio di ictus, infarto e insufficienza cardiaca [1,2]. Nonostante l’ottimizzazione della terapia farmacologica e le modifiche dello stile di vita, solo il 25-34% dei pazienti raggiunge una pressione sanguigna target di 140/90 mmHg o inferiore [3]. Molti pazienti hanno un’ipertensione refrattaria alla terapia o soffrono di effetti collaterali indotti dai farmaci.
La terapia farmacologica è e rimane il pilastro terapeutico più importante per l’ipertensione arteriosa. Negli ultimi dieci anni, tuttavia, sono diventate pubbliche altre forme di terapia oltre a quella puramente medicamentosa:
- La stimolazione elettrica del barorecettore
- Biofeedback e altri trattamenti psicosomatici
- Denervazione dell’arteria renale
- La vaccinazione contro la pressione sanguigna (anticorpi angiotensina)
- La stimolazione elettrica del nervo vago.
Sia la denervazione dell’arteria renale che la vaccinazione per la pressione sanguigna non sono riuscite ad essere accettate [4,5]. E proprio di recente, all’ultimo Congresso ESC 2014 di Barcellona, sono stati presentati i risultati dello studio NECTAR-HF, che hanno dimostrato che la stimolazione del nervo vago non migliora la funzione cardiaca [6].
La terapia di attivazione del baroreflesso mediante uno stimolatore carotideo, invece, è stata in grado di dimostrare una riduzione sostenuta della pressione sanguigna nei pazienti con ipertensione arteriosa refrattaria.
La storia
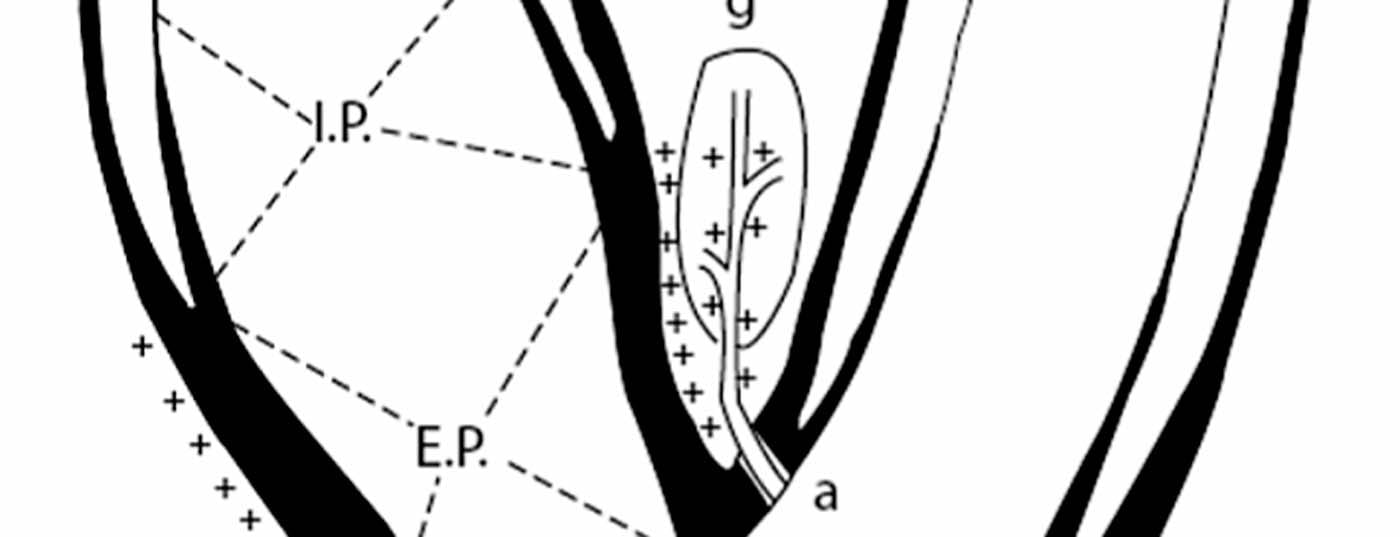
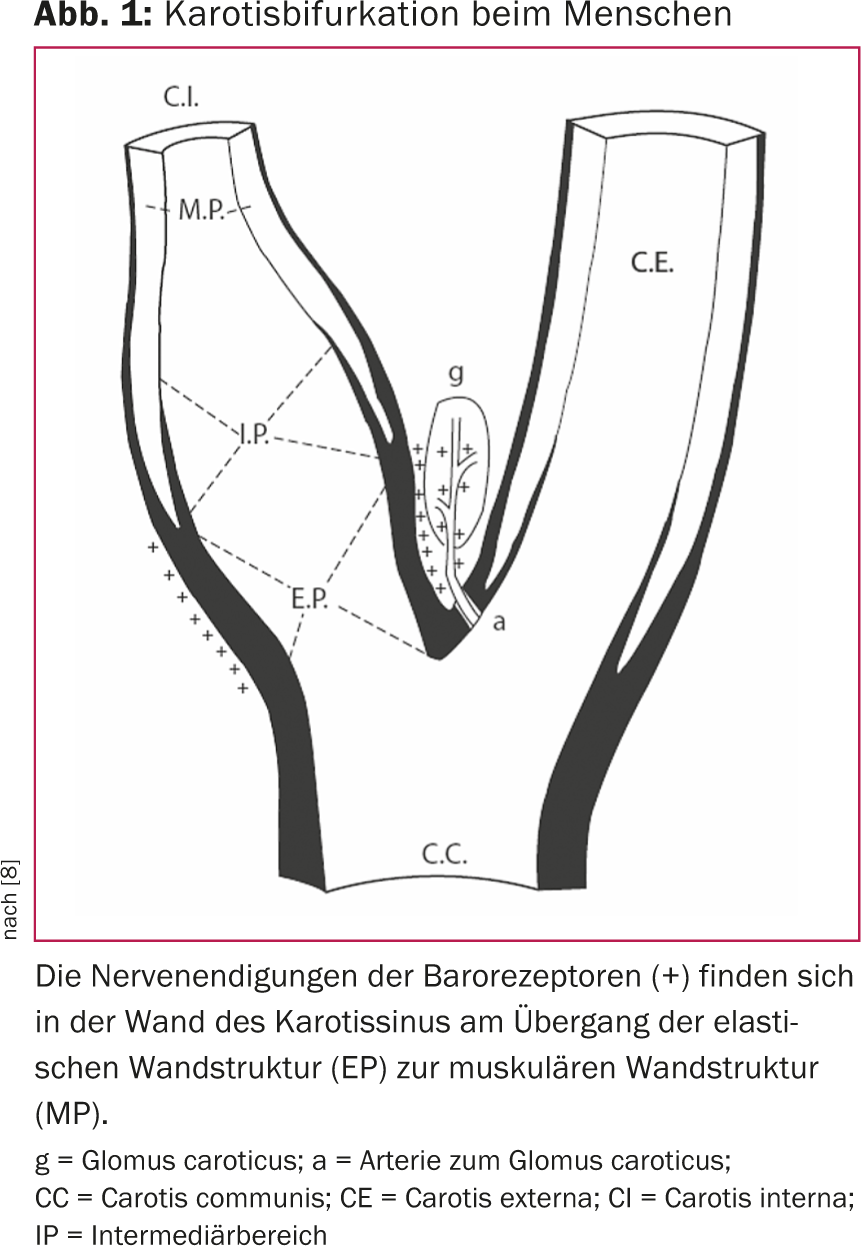
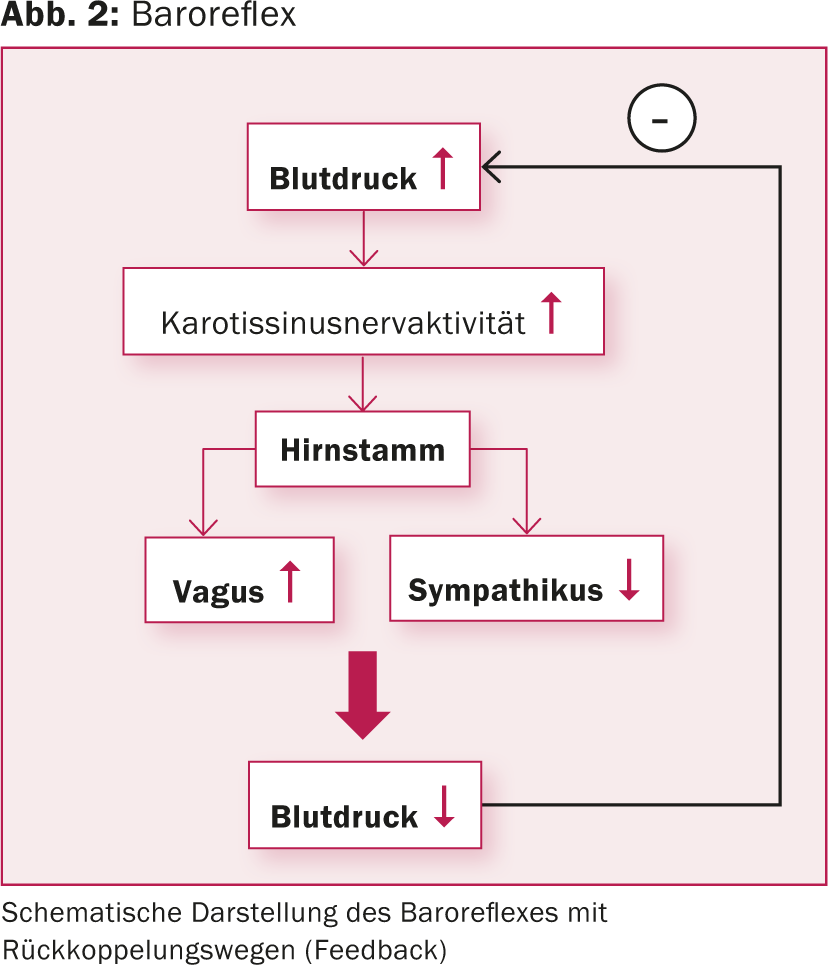
L’importanza del baroreflex per la regolazione della pressione arteriosa è stata riconosciuta più di 80 anni fa [7]. Negli esseri umani, i cosiddetti sensori della pressione sanguigna, cioè i barorecettori, si trovano principalmente nell’arco aortico, nelle arterie succlavie e nell’area del seno carotideo. I barorecettori nel seno carotideo sembrano essere dominanti. La distribuzione e il meccanismo di feedback delle fibre nervose barorecettoriali sono stati studiati intensamente (Fig. 1) [8]. In sostanza, un aumento della pressione sanguigna provoca un aumento della tensione della parete del seno carotideo. Questo attiva i barorecettori nella parete del seno carotideo, che si manifesta con un aumento della frequenza e dell’ampiezza degli impulsi nervosi afferenti. Gli impulsi sono interconnessi nel cervello e portano, sia a livello neuro-umorale che attraverso la modulazione del sistema nervoso autonomo, a un’attenuazione del tono simpatico. Di conseguenza, la pressione arteriosa viene influenzata dalla funzione cardiaca, dai reni e dalla resistenza vascolare periferica (Fig. 2).
Già negli anni ’60, gli stimolatori carotidei sono stati utilizzati in uno studio su pazienti con ipertensione arteriosa refrattaria [9]. Tuttavia, per motivi tecnici e perché sono stati sviluppati farmaci migliori per la pressione sanguigna, questo approccio terapeutico è stato abbandonato e l’industria ha rivolto la sua attenzione allo sviluppo di pacemaker. L’idea della stimolazione elettrica dei barorecettori è stata ripresa solo all’inizio di questo secolo. Sia gli studi sugli animali che quelli a lungo termine sull’uomo hanno dimostrato un effetto positivo e duraturo sulla regolazione della pressione sanguigna [10,11].
Specifiche del dispositivo e tecnica di impianto
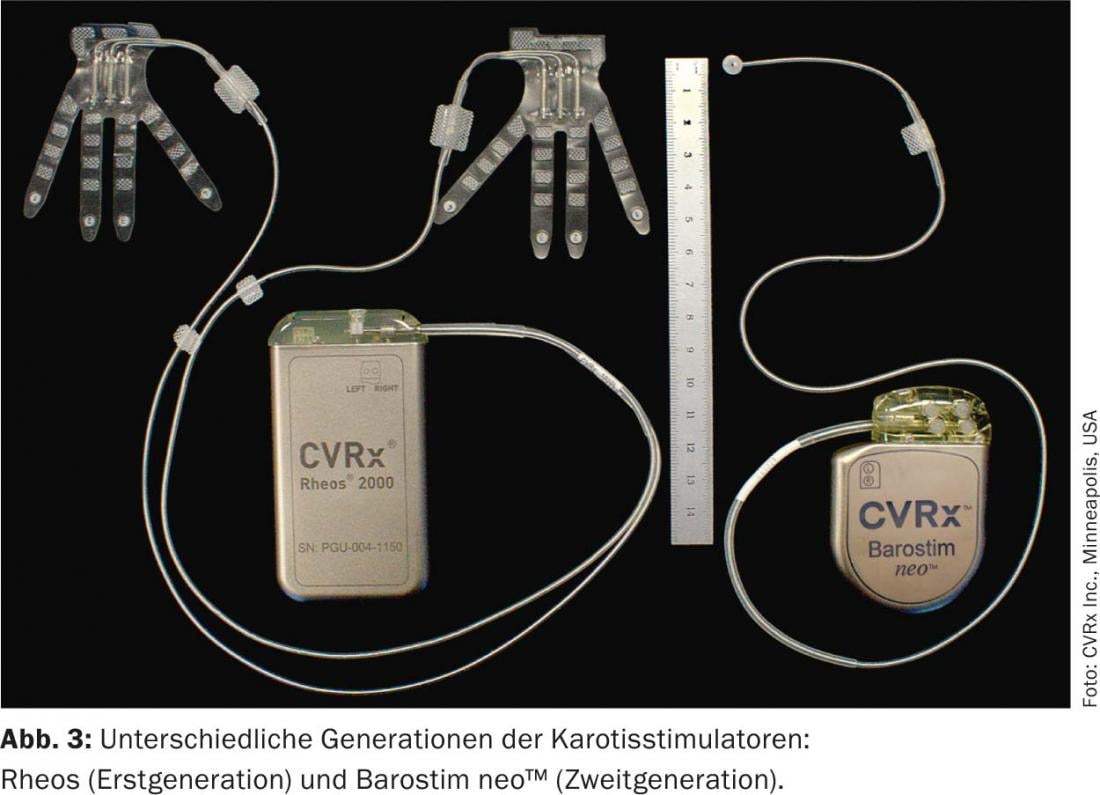
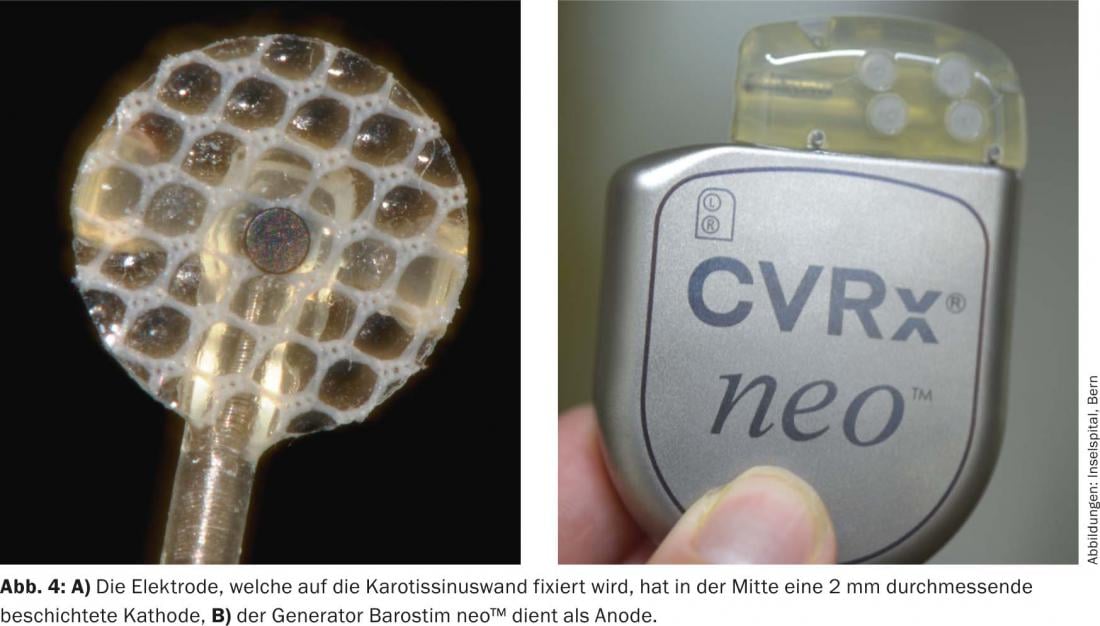
Il dispositivo di prima generazione (Rheos-System Baroreflex Activation Therapy Device®, CVRx Inc., Minneapolis, MN, USA) richiedeva l’impianto di un generatore e di due sonde. Gli elettrodi sono stati posizionati intorno al seno carotideo su entrambi i lati. Il dispositivo di nuova generazione (Barostim neo™), invece, ha una sola sonda, che viene impiantata preferibilmente sul lato destro. Inoltre, il generatore e l’elettrodo sono stati notevolmente ridotti nelle dimensioni e la durata della batteria è stata estesa a 48 mesi in media. Nella stimolazione monopolare, il generatore funge da elettrodo attivo (fig. 3 e 4). Inoltre, la corrente viene applicata in modo costante e non più intermittente.
L’impianto del dispositivo avviene in anestesia. La procedura richiede 60-90 minuti. La biforcazione carotidea e la parete anteriore del seno carotideo vengono visualizzate con un approccio chirurgico attraverso la biforcazione carotidea destra. Poi verifica quale area del seno carotideo ha la risposta più forte (cioè l’abbassamento della pressione arteriosa sistolica e/o del polso). Successivamente, l’elettrodo viene fissato con suture sottili. Si forma una tasca infraclaveare a destra per il generatore, simile all’impianto di un pacemaker. L’elettrodo viene tunnellizzato lungo l’arteria carotidea fino al livello del giugulo e poi sottocute fino alla tasca del generatore e collegato al generatore. Nell’area dell’arteria carotide comune si forma un’ansa di rilievo, che dovrebbe impedire la trazione sull’elettrodo quando si gira la testa. L’anestesia deve essere pianificata in modo specifico, in quanto gli anestetici per inalazione, in particolare, possono attenuare il baroreflesso. L’operazione non è stressante e può essere eseguita bene durante un breve ricovero. Il dispositivo viene poi acceso solo da due a quattro settimane dopo l’impianto. I farmaci antipertensivi devono essere continuati e, a seconda della risposta della pressione arteriosa alla stimolazione barorecettoriale, possono essere gradualmente ridotti nel tempo.
Studi clinici
Nell’ambito di uno studio acuto (BRASS, BaroReceptor Activation System Study), abbiamo attivato elettricamente il baroreflesso durante un intervento alla carotide comune [12]. Con una stimolazione crescente, è stato possibile ottenere una riduzione significativa della pressione sanguigna e del polso dipendente dal voltaggio. La risposta più forte è stata rilevata quando è stata stimolata con 4-6 volt. Questo ha dimostrato in modo riproducibile che la stimolazione elettrica del baroreflesso porta a un cambiamento immediato della pressione sanguigna. Si tratta di uno studio importante per quanto riguarda l’impianto permanente del dispositivo per abbassare la pressione sanguigna nei pazienti con ipertensione refrattaria.
Pazienti con ipertensione refrattaria
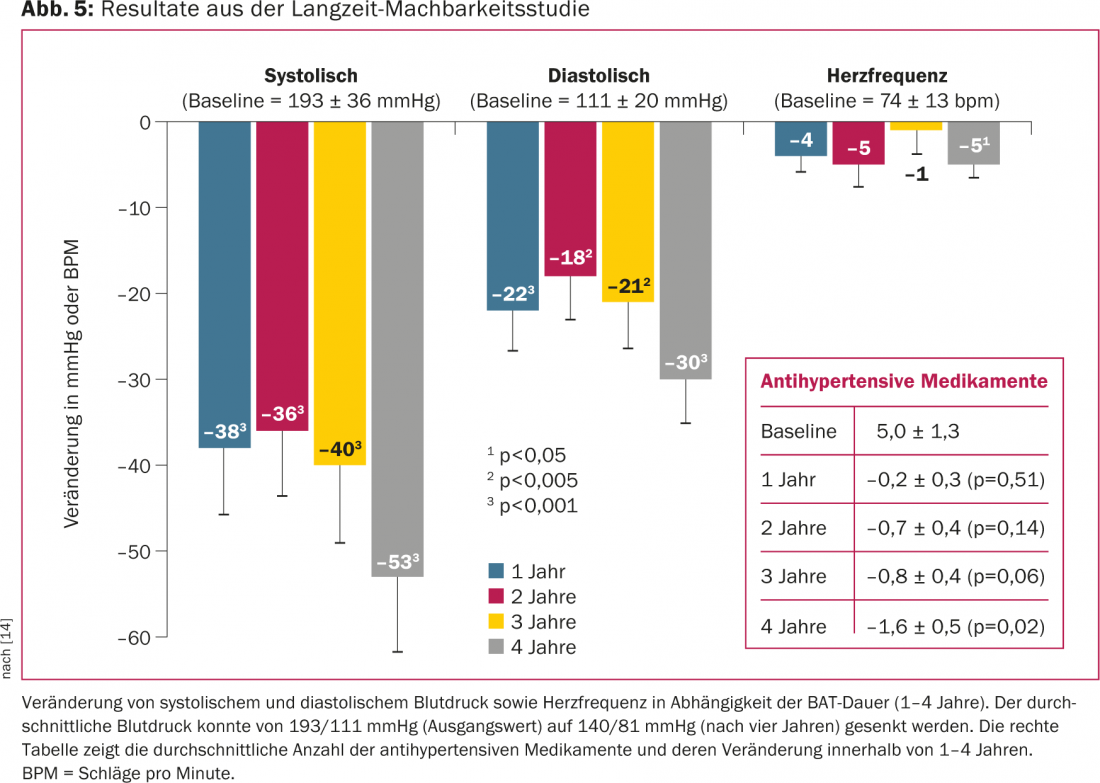
Lo studio DEBuT-HT(Device Based Therapyin Hypertension Trial) è stato uno studio multicentrico europeo prospettico, non randomizzato, che ha analizzato la sicurezza e la fattibilità dello stimolatore carotideo in 45 pazienti con ipertensione refrattaria. Il criterio di inclusione era una pressione arteriosa sistolica superiore a 160 mmHg nonostante un regime farmacologico con tre farmaci antipertensivi, uno dei quali doveva essere un diuretico [13]. I farmaci antipertensivi non sono stati modificati durante il periodo di studio. L’endpoint principale era una riduzione della pressione arteriosa sistolica di almeno 10 mmHg tre mesi dopo il BAT. Nel corso di tre anni, sono stati monitorati tutti gli eventi gravi e tutte le complicanze legate all’impianto e al dispositivo. Prima dell’impianto, la pressione arteriosa sistolica media e la frequenza del polso erano rispettivamente di quasi 180 mmHg e 180 mmHg. 80 battiti al minuto con un’assunzione media di 5,5 farmaci antipertensivi per paziente. Dopo tre mesi, la pressione arteriosa media si è ridotta di oltre 20 mmHg. Semmai, la riduzione della pressione sanguigna era ancora maggiore dopo due e tre anni di follow-up [13]. Dopo quattro anni, la pressione arteriosa sistolica era addirittura ridotta di una media di 53 mmHg (Fig. 5) [14]. La procedura di impianto si è rivelata sicura. Il posizionamento dell’elettrodo intorno al seno carotideo non ha provocato stenosi dell’arteria carotidea. La soddisfazione dei pazienti è stata molto alta e i pazienti hanno riferito una migliore qualità del sonno, meno mal di testa e una migliore concentrazione.
Negli Stati Uniti e in Europa è stato avviato uno studio di fase III (Rheos Pivotal Trial) con 265 pazienti. Si trattava di uno studio randomizzato in doppio cieco controllato con placebo su pazienti con ipertensione refrattaria. Un mese dopo l’impianto del sistema Rheos, i pazienti sono stati randomizzati 2:1, cioè in due terzi dei pazienti il dispositivo è stato acceso subito dopo la randomizzazione e negli altri solo dopo sei mesi. Entrambi i gruppi di pazienti sono stati seguiti per dodici mesi dopo la randomizzazione. Lo studio ha mostrato una riduzione della pressione arteriosa sistolica media di 35 mmHg dopo dodici mesi. Più del 50% dei pazienti ha raggiunto un valore target di pressione arteriosa di ≤140 mmHg [15,16]. Dopo l’accensione del dispositivo, è stata osservata una leggera diminuzione iniziale della velocità di filtrazione glomerulare. Questo è stato interpretato come una reazione alla riduzione della pressione sanguigna. Nel decorso a lungo termine, tuttavia, la funzione renale è rimasta stabile [17].
In un’analisi di sottogruppo dello studio DEBuT-HT, l’effetto dell’alterazione della pressione sanguigna sulla regolazione autonomica cardiaca è stato studiato in 21 pazienti [18]. È stato osservato un cambiamento nella variabilità della frequenza cardiaca, che si è correlato all’attenuazione simpatica o all’attivazione parasimpatica con una corrispondente riduzione della pressione sanguigna. Un altro studio ha dimostrato che il BAT porta a un rimodellamento inverso del ventricolo sinistro e degli atri e a un miglioramento della compliance arteriosa [19]. Inoltre, è stato osservato che i pazienti con insufficienza cardiaca sintomatica che assumono il BAT hanno migliorato le prestazioni funzionali di oltre il 37% (come misurato dal test del cammino di 6 minuti). Inoltre, l’ecocardiografia ha rivelato una riduzione significativa della massa ventricolare sinistra e dello spessore della parete posteriore, come segno di “rimodellamento inverso” del ventricolo sinistro [20].
Tutti gli studi citati sono stati condotti con il dispositivo di abbassamento della pressione sanguigna di prima generazione (Rheos). In uno studio recente con l’impianto di seconda generazione (Barostim neo™), è stato ottenuto lo stesso effetto sulla riduzione della pressione sanguigna come con il sistema Rheos [21].
Contrariamente al timore che il BAT possa portare a un blocco del baroreflesso (“reset del baroflex”), nei pazienti con ipertensione refrattaria è stata osservata una riduzione sostenuta e dose-dipendente della pressione sanguigna e della frequenza cardiaca [22].
I risultati degli studi condotti finora hanno portato all’inclusione del BAT come opzione terapeutica nelle linee guida sull’ipertensione dell’ESH/ESC nel 2013. Si raccomanda di prendere in considerazione la BAT nei pazienti con ipertensione refrattaria (classe di raccomandazione IIb, livello di evidenza C). Allo stesso tempo, però, è stato raccomandato che lo stimolatore barorecettoriale venga impiantato solo da specialisti esperti e in centri selezionati per il trattamento dell’ipertensione, fino a quando non saranno disponibili ulteriori prove sull’efficacia e la sicurezza a lungo termine (Classe I, Livello C) [23].
Il rapporto costo-efficacia del BAT è stato analizzato in un altro studio su pazienti affetti da ipertensione refrattaria. Allo stesso tempo, è stata studiata anche l’influenza della terapia sulla morbilità e mortalità cardiovascolare [24]. In questo studio condotto in Germania, gli autori hanno concluso che nei pazienti con ipertensione refrattaria, la stimolazione dei barorecettori per tutta la vita ha ridotto il rischio di ictus del 35%, di infarto del miocardio del 19% e di insufficienza renale che richiede la dialisi del 23%. In media, i pazienti vivrebbero 1,66 anni in più, con un aumento di 2,17 anni di vita aggiustati per la qualità (QALY). Il costo di un QALY è stato stimato in 7797 euro. Questo valore è molto inferiore alla soglia di costo-efficacia generalmente accettata di 35.000 euro per un QALY [25]. Si è concluso che il BAT può essere conveniente rispetto al trattamento farmacologico ottimale dell’ipertensione nei pazienti con ipertensione refrattaria.
BAT nei pazienti con insufficienza cardiaca
Poiché il BAT non solo abbassa la pressione sanguigna, ma ha anche un effetto benefico sulla funzione cardiaca, sono stati condotti degli studi su pazienti con insufficienza cardiaca. Recentemente, è stato pubblicato uno studio su undici pazienti con insufficienza cardiaca (classe NYHA III, EF <40%) in cui non era possibile effettuare la terapia di risincronizzazione cardiaca. Per sei mesi, il BAT è stato utilizzato in parallelo alla terapia farmacologica ottimale. L’efficacia del trattamento è stata misurata dalla variazione dell’attività del nervo simpatico muscolare. Inoltre, sono stati raccolti parametri clinici per la qualità della vita e le prestazioni funzionali. I pazienti hanno mostrato un’attenuazione significativa dell’attività del nervo muscolare simpatico con miglioramenti significativi della sensibilità baroreflessa, della frazione di eiezione, della classe NYHA, della qualità della vita e del test del cammino di 6 minuti. Inoltre, il numero di riospedalizzazioni dovute al peggioramento dell’insufficienza cardiaca è stato ridotto in modo significativo [26]. Il BAT si è dimostrato compatibile con il defibrillatore cardioverter impiantabile (ICD) e le due terapie sono sembrate funzionare in modo complementare [27].
Nell’aprile 2013, è stato avviato uno studio sull’insufficienza cardiaca che include pazienti con una frazione di eiezione ventricolare sinistra ≤35% e una classe NYHA III (Barostim Health Outcomes Prospective Evaluation for Heart Failure, Barostim HOPE4HF). Si tratta di uno studio di fase II che testa l’efficacia e la sicurezza del sistema Barostim neo™ nei pazienti con insufficienza cardiaca. Questo studio prospettico multicentrico randomizzato e controllato arruolerà 140 pazienti negli Stati Uniti e in Europa, con l’intento di confrontare la terapia Barostim neo™ con la terapia standard per l’insufficienza cardiaca. Gli endpoint dello studio sono le variazioni della frazione di eiezione, del test del cammino di 6 minuti, della classificazione NYHA, della qualità della vita e della funzione renale e di altri parametri. I primi risultati dopo sei mesi sono attesi a breve.
Situazione attuale
All’inizio di settembre 2014, erano stati impiantati in tutto il mondo 420 dispositivi Rheos e 380 stimolatori Barostim neo™. L’impianto si è rivelato sicuro e i rischi di impianto sono paragonabili a quelli di altri dispositivi impiantabili, come pacemaker o ICD.
In Europa, Barostim neo™ è certificato CE e disponibile in Italia, Germania, Svizzera e Olanda. La compensazione finanziaria non è ancora universalmente regolamentata, ma si stanno compiendo sforzi in questa direzione, nella consapevolezza che la BAT può essere conveniente nei pazienti con ipertensione refrattaria [24].
Sommario
Lo stimolatore carotideo può essere impiantato con basso rischio e produce una riduzione significativa e sostenuta della pressione sanguigna nei pazienti con ipertensione refrattaria. L’efficienza emodinamica è maggiore del previsto e addirittura sostenuta per più di cinque anni. L’obiettivo del trattamento è modulare il sistema nervoso autonomo e quindi smorzare il tono simpatico. Oltre alla riduzione della pressione arteriosa, si osserva anche un rimodellamento cardiaco con diminuzione dello spessore della parete miocardica del ventricolo sinistro. Tutti questi risultati hanno portato all’integrazione del BAT nelle linee guida ESH/ESC 2013 sull’ipertensione arteriosa. L’efficacia di questo trattamento nei pazienti con insufficienza cardiaca è attualmente oggetto di studi; tuttavia, sono già stati dimostrati effetti positivi in popolazioni di pazienti selezionate.
Letteratura:
- Fields LE, et al: Il peso dell’ipertensione negli adulti negli Stati Uniti dal 1999 al 2000: una marea crescente. Ipertensione 2004; 44: 398-404.
- Hajjar I, Kotchen TA: Tendenze nella prevalenza, consapevolezza, trattamento e controllo dell’ipertensione negli Stati Uniti, 1988-2000. JAMA : la rivista dell’Associazione Medica Americana 2003; 290: 199-206.
- Chobanian AV, et al: Il settimo rapporto del Comitato Nazionale Congiunto sulla prevenzione, l’individuazione, la valutazione e il trattamento dell’ipertensione arteriosa: il rapporto JNC 7. JAMA : la rivista dell’Associazione Medica Americana 2003; 289: 2560-2572.
- Campbell DJ: Vaccinazione contro l’ipertensione. Current pharmaceutical design 2012; 18: 1005-1010.
- Wienemann H, et al: Trattamento dell’ipertensione resistente con nuovi dispositivi. Minerva cardioangiologica 2014; 62: 235-241.
- Zannad F, et al: Stimolazione vagale cronica per il trattamento dell’insufficienza cardiaca a bassa frazione di eiezione: risultati dello studio randomizzato e controllato sulla terapia cardiaca neurale per l’insufficienza cardiaca (NECTAR-HF). European heart journal 2014 [Epub ahead of print].
- Koch E: L’autocontrollo riflesso della circolazione. Dresda, Steinkopff 1931.
- Muratori G: Osservazioni istologiche sulla struttura del seno carotideo nell’uomo e nei mammiferi. Oxford, Pergamon 1967.
- Brest AN, Wiener L, Bachrach B: Stimolazione bilaterale del nervo del seno carotideo nel trattamento dell’ipertensione. American journal of cardiology 1972; 29: 821-825.
- Lohmeier TE, et al: L’attivazione prolungata del baroreflesso produce ipotensione sostenuta. Ipertensione 2004; 43: 306-311.
- Scheffers IJM, et al: Riduzione sostenuta della pressione arteriosa mediante la terapia dell’ipertensione baroreflessa con un sistema impiantato cronicamente: dati a 3 anni dello studio Rheos DEBuT in pazienti con ipertensione resistente. J Hypertens 2009; 27: S421.
- Schmidli J, et al: Riduzione acuta della pressione arteriosa basata su un dispositivo: attivazione elettrica del baroreflesso carotideo nei pazienti sottoposti a chirurgia carotidea elettiva. Vascolare 2007; 15: 63-69.
- Scheffers IJ, et al: Una nuova terapia di attivazione del baroreflex nell’ipertensione resistente: risultati di uno studio di fattibilità multicentrico europeo. Journal of the American College of Cardiology 2010; 56: 1254-1258.
- Kroon AA, et al: Sistema impiantato cronicamente: dati a 4 anni dello studio Rheos® DEBuT-HT in pazienti con ipertensione resistente. Journal of hypertension 2010; 28: 278.
- Bakris GL, et al: La terapia di attivazione del baroreflesso fornisce un beneficio duraturo nei pazienti con ipertensione resistente: risultati del follow-up a lungo termine nel Rheos Pivotal Trial. Journal of the American Society of Hypertension: JASH 2012; 6: 152-158.
- Bisognano JD, et al: La terapia di attivazione del baroreflesso abbassa la pressione sanguigna nei pazienti con ipertensione resistente: risultati dello studio pivotale rheos in doppio cieco, randomizzato, controllato con placebo. Journal of the American College of Cardiology 2011; 58: 765-773.
- Alnima T, et al: Risposte renali alla terapia di attivazione del riflesso carotideo a lungo termine nei pazienti con ipertensione resistente ai farmaci. Ipertensione 2013; 61: 1334-1339.
- Wustmann K, et al.: Effetti della stimolazione cronica dei barorecettori sulla regolazione autonomica cardiovascolare nei pazienti con ipertensione arteriosa resistente ai farmaci. Ipertensione 2009; 54: 530-536.
- Bisognano JD, et al: Miglioramento della struttura e della funzione cardiaca con il trattamento cronico mediante un dispositivo impiantabile nell’ipertensione resistente: risultati degli studi europei e statunitensi sul sistema Rheos. Journal of the American College of Cardiology 2011; 57: 1787-1788.
- Mohaupt MG, Schmidli J, Luft FC: Gestione dell’ipertensione incontrollabile con un dispositivo di stimolazione del seno carotideo. Ipertensione 2007; 50: 825-828.
- Hoppe UC, et al: Il sistema minimamente invasivo per la terapia di attivazione del baroreflesso abbassa cronicamente la pressione sanguigna con un profilo di sicurezza simile a quello di un pacemaker: risultati dello studio Barostim neo. Journal of the American Society of Hypertension: JASH 2012; 6: 270-276.
- Alnima T, et al: Diminuzione acuta sostenuta della pressione arteriosa voltaggio-dipendente con attivazione prolungata del baroreflesso carotideo nell’ipertensione resistente alla terapia. Giornale dell’ipertensione 2012; 30: 1665-1670.
- Task Force for the Management of Arterial Hypertension of the European Society Of H, Task Force for the Management of Arterial Hypertension of the European Society Of C: Linee guida ESH/ESC 2013 per la gestione dell’ipertensione arteriosa. Pressione sanguigna 2013; 22: 193-278.
- Borisenko O, et al.: Costo-efficacia della terapia Barostim per il trattamento dell’ipertensione resistente in contesti europei. Giornale dell’ipertensione 2014; 32: 681-692.
- Eichler HG, et al.: Uso dell’analisi costo-efficacia nel processo decisionale di allocazione delle risorse sanitarie: come si prevede che emergano le soglie di costo-efficacia? Valore Salute 2004; 7: 518-528.
- Gronda E, et al: Effetti dell’attivazione cronica del baroreflex sul traffico nervoso simpatico, sulla funzione baroreflessa e sull’emodinamica cardiaca nell’insufficienza cardiaca: uno studio proof-of-concept. European journal of heart failure 2014; 16: 977-983.
- Madershahian N, et al: Terapia di attivazione del baroreflesso nei pazienti con preesistente cardioverter-defibrillatore impiantabile: terapie compatibili e complementari. Europace 2014; 16: 861-865.
CARDIOVASC 2014; 13(6): 6-11