Una diagnosi accurata pone le basi in presenza di una doppia patologia valvolare stenosi della valvola aortica / stenosi della valvola mitrale. Poiché le due patologie si influenzano a vicenda, un approccio multimodale con valutazione invasiva, di imaging e funzionale è un prerequisito, ma rimane una sfida anche in mani esperte. Una strategia terapeutica individuale viene formulata in base alle condizioni anatomiche, all’età e alle comorbidità, nonché all’obiettivo terapeutico desiderato. Si deve prendere in considerazione l’intera gamma di interventi chirurgici, percutanei e combinati. I complessi chiarimenti diagnostici e l’esecuzione di varie operazioni e interventi percutanei suggeriscono il coinvolgimento di un team cardiaco ampio.
La stenosi della valvola aortica sintomatica è il rappresentante più comune della malattia cardiaca valvolare degenerativa. Le opzioni di trattamento sono di conseguenza innovative e diversificate, e coprono un’ampia gamma di terapie curative, dalla sostituzione chirurgica della valvola aortica alla sostituzione della valvola con catetere (TAVI). Oggi, il rischio di letalità perioperatoria per la sostituzione chirurgica isolata della valvola aortica è inferiore al 3,5% e il rischio di mortalità a 30 giorni per i pazienti ad alto rischio trattati con la valvola TAVI è inferiore al 15% [1,2]. Nella chirurgia a doppia valvola, il rischio perioperatorio aumenta a %–13% [3,4]. Se la stenosi della valvola aortica è accompagnata dal rigurgito della valvola mitrale (MI), questo può influenzare in modo significativo l’approccio strategico al trattamento della stenosi della valvola aortica. La prevalenza della stenosi della valvola aortica accompagnata da un MI almeno moderato è riportata fino al 33% [2]. L’ampia variazione nella prevalenza può essere spiegata dalle definizioni parzialmente diverse di una MI rilevante nella letteratura. Resta il fatto, tuttavia, che in una percentuale rilevante di pazienti con stenosi della valvola aortica, si pone la questione di una MI concomitante che richiede un trattamento. I numerosi metodi di terapia chirurgica e interventistica oggi disponibili consentono di adattare la terapia al rischio individuale e alle caratteristiche anatomiche del paziente, contribuendo così a mantenere al minimo il rischio peri-interventistico.
Strategia di trattamento per AS grave e MI concomitante
I punti chiave che definiscono la terapia nella complessa malattia combinata della valvola aortica e mitrale sono una diagnosi approfondita dei meccanismi e una valutazione del decorso spontaneo della MI dopo la correzione della stenosi della valvola aortica. Pertanto, nel determinare la strategia di trattamento ottimale, vale la pena di condurre un esame accurato della MI che identifichi le cause sottostanti e le collochi nel contesto della fisiopatologia risultante. In base alle conoscenze acquisite, si può scegliere la terapia più sensata per il paziente tra le varie opzioni terapeutiche.
Causa del rigurgito della valvola mitrale
In genere, si distingue tra MI organico e MI funzionale. Mentre nella MI organica è l’apparato valvolare strutturale (valvole a foglietto, corde, muscoli papillari, anulus) a generare la perdita, nella MI funzionale l’apparato valvolare in quanto tale è intatto e la valvola mitrale perde come risultato di un cambiamento geometrico strutturale del ventricolo sinistro. I rappresentanti tipici della MI organica sono le rotture o gli allungamenti dei filamenti tendinei, nonché le alterazioni mixomatose o aterosclerotiche, con le alterazioni mixomatose che sono le più comuni. Le insufficienze funzionali della valvola mitrale hanno in comune il fatto che, a causa della mutata geometria ventricolare, l’apparato valvolare effettivamente intatto non garantisce più una coaptazione pulita dei lembi. La MI non deve necessariamente basarsi su un disturbo globale della geometria ventricolare, poiché i disturbi regionali possono già portare a una MI rilevante. Non è raro che ciò sia dovuto a una causa ischemica. Spesso l’MI deriva anche da una combinazione di diverse cause funzionali e organiche, che alla fine influenzano negativamente la geometria ventricolare e la superficie di coaptazione, portando alla perdita.
Diagnostica
Il work-up per la malattia bivalvolare prevede diverse modalità diagnostiche. Questi includono il cateterismo cardiaco destro-sinistro, l’ecocardiografia transtoracica e transoesofagea e, in singoli casi, l’ecocardiografia da sforzo per valutare l’MI sotto sforzo. Le misure di performance come l’ergometria o il test del cammino di 6 minuti possono essere utilizzate anche per smascherare i sintomi, l’ischemia concomitante o misurare indirettamente il volume dell’ictus profondo. La difficoltà nell’analisi della patologia valvolare è che entrambe le patologie si influenzano a vicenda. Una stenosi valvolare aortica grave può portare a un MI rilevante semplicemente a causa dell’elevato postcarico e del conseguente sovraccarico di pressione nel ventricolo sinistro. Tuttavia, l’MI grave può anche portare a una riduzione significativa del volume di corsa in avanti, e quindi ridurre il gradiente transvalvolare attraverso la valvola aortica, il che può portare a un’interpretazione errata della gravità della stenosi della valvola aortica. In questo caso, l’ecocardiografia da sforzo con dobutrex può essere utile per valutare meglio la reale gravità della stenosi della valvola aortica. Un fattore di complicazione è spesso la ridotta funzione ventricolare sinistra, che può anche falsificare il grado di patologia valvolare. Pertanto, la corretta valutazione della causa e della gravità della patologia valvolare spesso non si basa su una singola misurazione, ma è spesso il risultato di una moltitudine di esami complementari, che alla fine portano a un’interpretazione logica fisiologicamente comprensibile dei risultati.
Opzioni terapeutiche
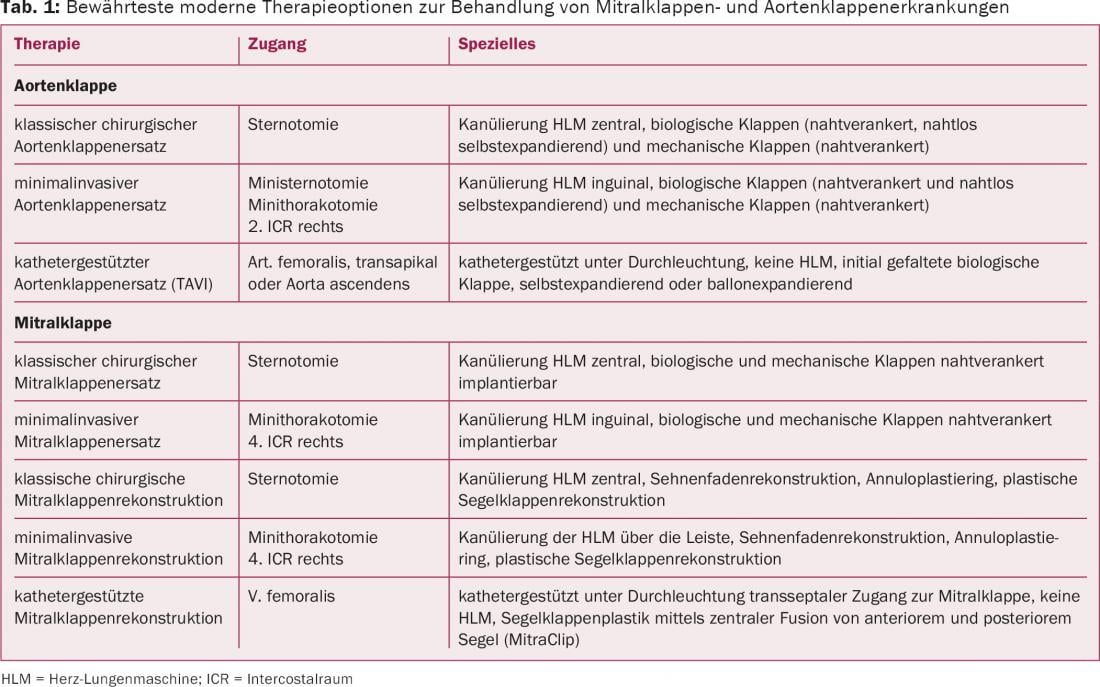
Negli ultimi anni, le opzioni terapeutiche per il trattamento della patologia valvolare hanno subito un forte sviluppo sia nel settore chirurgico che in quello interventistico. La Tabella 1 offre una panoramica delle opzioni di trattamento oggi comunemente utilizzate.
Discussione
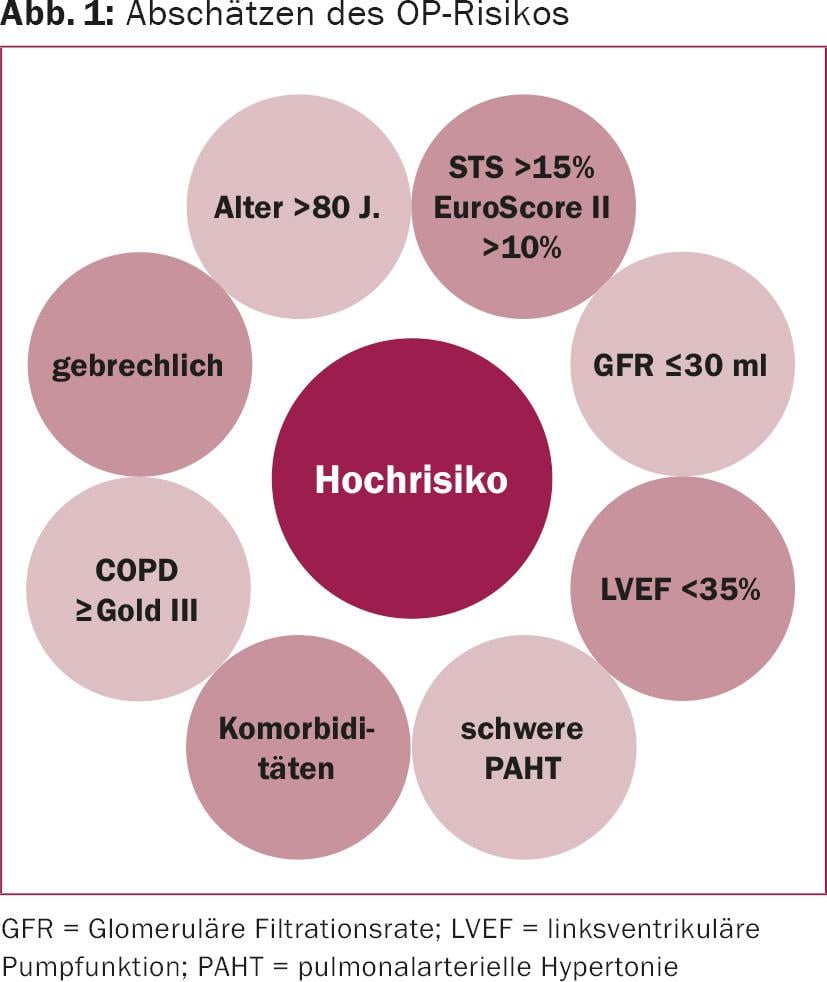
I seguenti risultati si applicano al trattamento delle insufficienze concomitanti della valvola mitrale nella stenosi valvolare aortica grave: Per quanto riguarda la mortalità e la sopravvivenza a lungo termine, al momento sembrano possibili solo affermazioni prudenti. È chiaro, tuttavia, che una MI moderata persistente favorisce lo sviluppo di un’insufficienza cardiaca rilevante a medio e lungo termine [5–8]. C’è un numero crescente di dati che suggeriscono che il rigurgito mitralico funzionale, in particolare, trae beneficio dalla chirurgia della valvola aortica isolata [2,5,6,9–11]. Per valutare meglio il decorso post-operatorio dell’MI funzionale, i parametri clinici predittivi sfavorevoli concomitanti, come la compromissione della funzione di pompa del ventricolo sinistro, l’ipertensione polmonare, fibrillazione atriale concomitante, dilatazione atriale sinistra >5 cm, un gradiente di picco transaortico preoperatorio <60 mmHg e un concomitante rigurgito della valvola aortica con un diametro endosistolico <45 mm possono essere aggiunti [8,9].
Tuttavia, a causa della complessità che può essere alla base dell’MI e dei singoli rischi concomitanti periinterventistici, una proposta di terapia generica per la stenosi valvolare aortica grave con MI moderata concomitante è insufficiente. Ciò si riflette nelle linee guida ECS/EACTS e ACC/AHA, che raccomandano essenzialmente il trattamento in base alla malattia valvolare e alla funzione ventricolare [1,12].Gli studi suggeriscono che l’MI funzionale in particolare trae beneficio dall’intervento isolato sulla valvola aortica. In questo caso, la caduta di pressione del ventricolo sinistro e il rimodellamento associato della geometria ventricolare sembrano favorire maggiormente la MI. Tuttavia, va notato che il miglioramento post-terapeutico della MI può essere atteso solo in quei pazienti in cui la MI funzionale è una conseguenza diretta della stenosi della valvola aortica e il rimodellamento è ancora possibile. Una circostanza che non è più necessariamente data nei pazienti in cui l’aumento cronico del postcarico ha già portato a un grave indebolimento del ventricolo sinistro. Nelle insufficienze della valvola mitrale causate organicamente, anche il rimodellamento dopo la sostituzione isolata della valvola aortica sembra avere un’influenza favorevole. Tuttavia, a causa dei difetti strutturali della valvola, questo effetto non è ugualmente pronunciato. A nostro avviso, un approccio sistematico e interdisciplinare che tenga conto dei rischi individuali e delle caratteristiche anatomiche specifiche della MI è decisivo per il successo del trattamento della MI concomitante (Fig. 1-3) .
La Figura 2 e la Figura 3 illustrano il concetto di strategia per il rigurgito mitralico organico e funzionale, rispettivamente. È ovvio che una diagnosi accurata pone le basi per un trattamento di successo. Poiché le due patologie si influenzano a vicenda, un approccio multimodale con chiarimenti invasivi, di imaging e funzionali è un prerequisito. In questo caso, sono utili un catetere cardiaco destro-sinistro, un’ecocardiografia transtoracica e transoesofagea e, se necessario, un’ecocardiografia da sforzo. Quest’ultima può essere particolarmente utile nella MI isolata indotta da stress. Inoltre, è possibile eseguire l’angiografia TC della radice aortica e delle arterie periferiche in preparazione alla terapia interventistica. L’analisi della diagnosi e la terapia che ne consegue devono essere effettuate da un team cardiaco interdisciplinare (composto da cardiologi interventisti e non, cardioanestesisti e cardiochirurghi). La natura interdisciplinare della proposta terapeutica non solo apre un ampio spettro di opzioni di trattamento, ma consente anche un approccio personalizzato in base alle esigenze e ai rischi individuali. Dalle diverse opzioni di trattamento elencate nella tabella 1, si può finalmente determinare il concetto terapeutico più sensato per il paziente. Per esempio, il trattamento chirurgico di una MI che richiede un trattamento con un ventricolo sinistro inizialmente indebolito può diventare possibile solo dopo il recupero attraverso la riduzione del postcarico con una procedura TAVI più delicata.
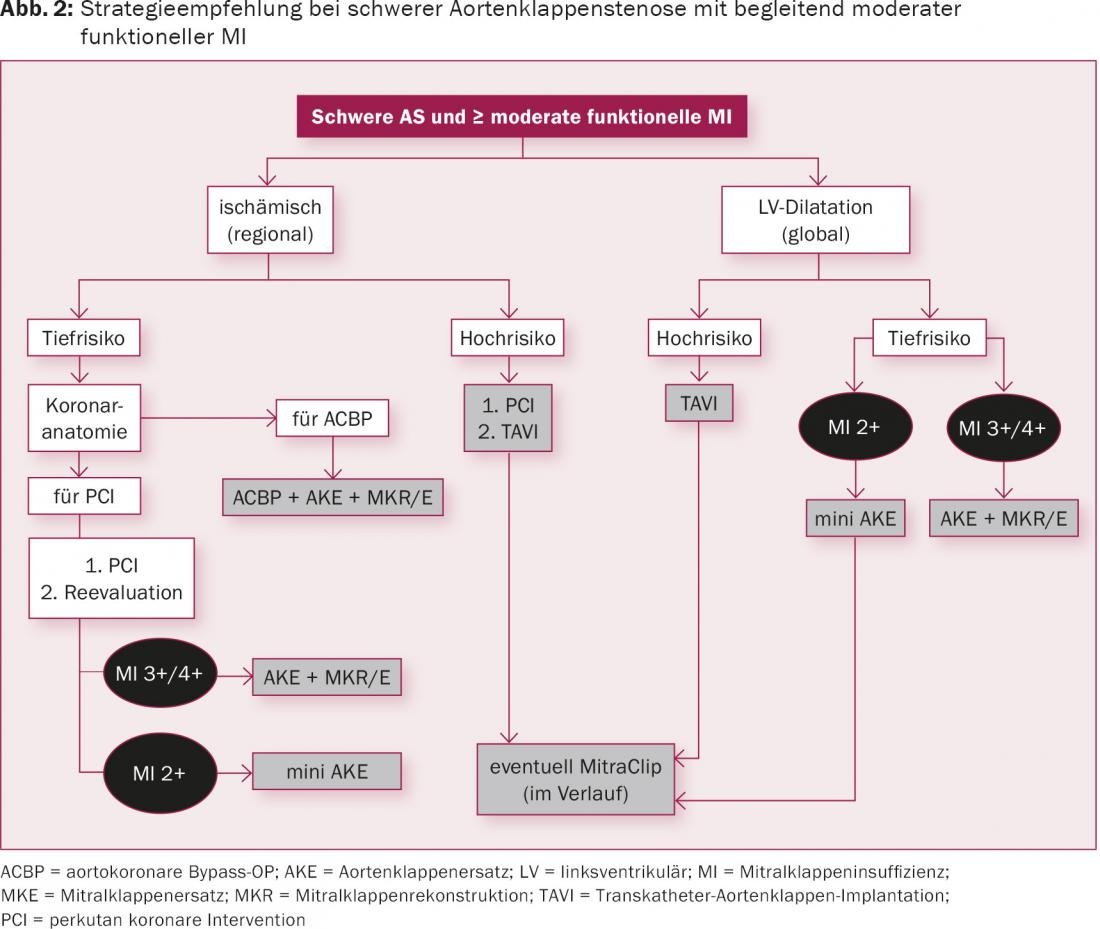
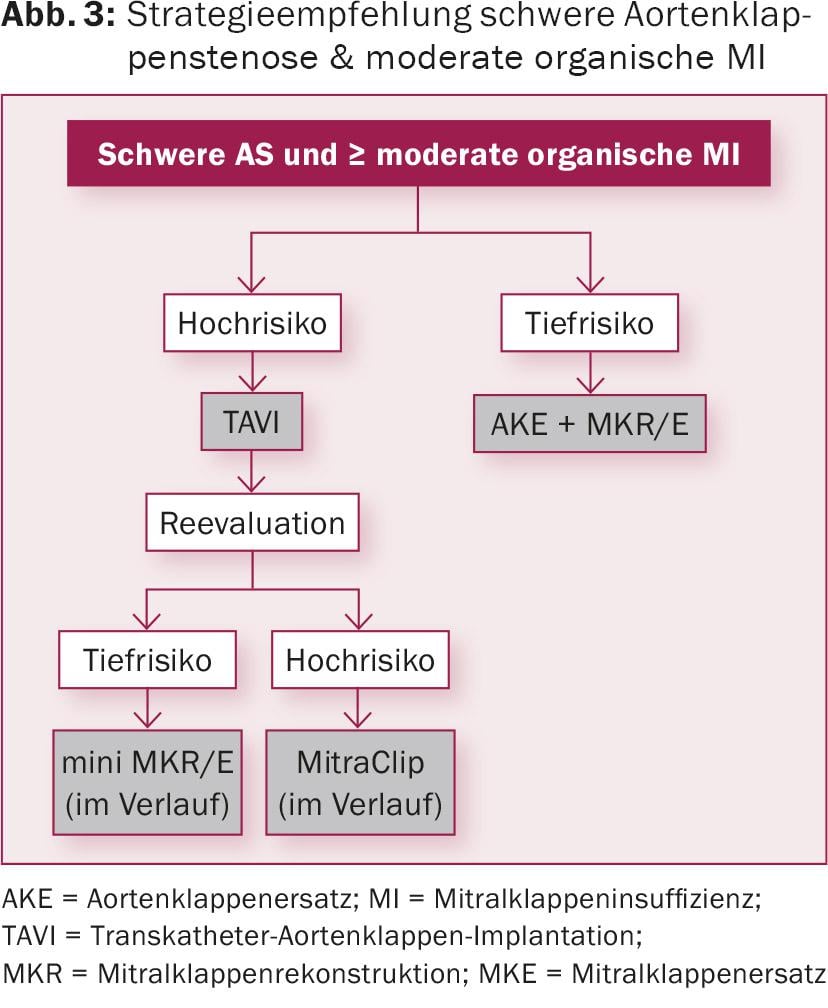
In sintesi, si può affermare che soprattutto le concomitanti insufficienze funzionali della valvola mitrale possono migliorare dopo la sostituzione isolata della valvola aortica. Il rigurgito organico della valvola mitrale concomitante beneficerà di una strategia a doppia valvola a lungo termine. Il rigurgito della valvola mitrale grave concomitante, sia organico che funzionale, deve essere indirizzato alla terapia con doppia valvola. Se il rischio peri-interventistico è corrispondentemente alto, può essere utile una procedura ibrida ritardata (prima valvola interventistica, poi seconda valvola chirurgica minimamente invasiva). La natura interdisciplinare di un Heart Team non solo apre un ampio spettro di opzioni terapeutiche diverse, ma permette anche di adattare la terapia alle esigenze e ai rischi individuali.
Letteratura:
- Vahanian A, et al: Linee guida sulla gestione della cardiopatia valvolare: la Task Force sulla gestione della cardiopatia valvolare della Società Europea di Cardiologia. Eur Heart J 2007; 28: 230-268.
- Nombela-Franco L, et al: Rigurgito mitralico significativo non trattato al momento della sostituzione della valvola aortica: una revisione completa di un’entità frequente nell’era della sostituzione transcatetere della valvola aortica. J Am Coll Cardiol 2014; 63: 2643-2658.
- Litmathe J, et al: Fattori di rischio predittivi nella sostituzione a doppia valvola (AVR e MVR) rispetto alla sostituzione della valvola aortica isolata. Thorac Cardiovasc Surg 2006; 54: 459-463.
- Harling L, et al: Sostituzione della valvola aortica per stenosi aortica in pazienti con concomitante rigurgito mitralico: si deve trattare la valvola mitrale? Eur Cardiothorac Surg 2011; 40: 1087-1096.
- Barreiro CJ, et al: Sostituzione della valvola aortica e concomitante rigurgito della valvola mitrale negli anziani: impatto sulla sopravvivenza e sull’esito funzionale. Circolazione 2005; 112: 1443-1447.
- Takeda K, et al: Impatto del rigurgito mitralico da lieve a moderato non trattato al momento della sostituzione isolata della valvola aortica sugli esiti avversi tardivi. Eur J Cardiothorac Surg 2010; 37: 1033-1038.
- Coutinho GF, et al: Gestione del rigurgito mitralico secondario moderato al momento della chirurgia della valvola aortica. Eur J Cardiothorac Surg 2013; 44: 32-40.
- Ruel M, et al: Storia naturale e predittori di esito nei pazienti con concomitante rigurgito mitralico funzionale al momento della sostituzione della valvola aortica. Circolazione 2006; 114: 1541-1546.
- Toggweiler S, et al: Sostituzione transcatetere della valvola aortica: esiti dei pazienti con rigurgito mitralico moderato o grave. J Am Coll Cardiol 2012; 59: 2068-2074.
- Wyler S, et al: Cosa succede al rigurgito mitralico funzionale dopo la sostituzione della valvola aortica per la stenosi aortica? Forum di cardiochirurgia 2013; 16: E238-E242.
- Nombela-Franco L, et al: Impatto clinico ed evoluzione del rigurgito mitralico dopo la sostituzione transcatetere della valvola aortica: una meta-analisi. Cuore 2015; 101: 1395-1405.
- Nishimura RA, et al: Linea guida AHA/ACC 2014 per la gestione dei pazienti con cardiopatia valvolare: un rapporto della Task Force on Practice Guidelines dell’American College of Cardiology/American Heart Association. J Thorac Cardiovasc Surg 2014; 148: e1-e132.
CARDIOVASC 2016; 15(1): 22-27