I pazienti con embolia polmonare necessitano di anticoagulazione per almeno tre mesi. Prima di iniziare la terapia, bisogna fare diverse considerazioni: Quale anticoagulante è più appropriato per questo paziente, quale dovrebbe essere la durata dell’anticoagulazione? E qual è il rapporto rischio-beneficio?
L’embolia polmonare acuta è considerata la manifestazione più grave del tromboembolismo venoso (TEV). Per la fase acuta e di mantenimento, l’obiettivo della terapia antitrombotica è prevenire la progressione della trombosi e dissolvere il materiale trombotico. Nella fase iniziale, la routine clinica viene solitamente eseguita per via parenterale utilizzando eparina non frazionata (UFH), eparine a basso peso molecolare (NMH) e fondaparinux.
Fase iniziale
Le eparine a basso peso molecolare e il fondaparinux sono la terapia di scelta per l’anticoagulazione parenterale iniziale nei pazienti che non sono classificati come ad alto rischio. Rispetto all’UFH, l’NMH e il fondaparinux offrono vantaggi in termini di efficacia, sicurezza e praticabilità, ad esempio un livello di farmaco più stabile e quindi un effetto anticoagulante, un’efficacia maggiore, un rischio minore di emorragie gravi o di trombocitopenia indotta dall’eparina (HIT) e una via di somministrazione più semplice tramite iniezione sottocutanea 1-2 volte al giorno. Questi vantaggi superano lo svantaggio di un inizio d’azione leggermente più lento. In alternativa all’anticoagulazione parenterale, la terapia con gli inibitori orali del fattore Xa, apixaban e rivaroxaban, può essere presa in considerazione anche per i pazienti non ad alto rischio.
La situazione è diversa per i pazienti emodinamicamente instabili e con un rischio molto elevato di embolia. In questi casi, l’anticoagulazione terapeutica con UFH deve essere iniziata immediatamente, cioè non appena viene formulato un sospetto diagnostico, scrivono il dottor Matthias Ebner e la dottoressa Mareike Lankeit della Charité – Universitätsmedizin Berlin (D) [1]. Secondo lo studio, i pazienti con embolia polmonare emodinamicamente instabile sono a rischio di un alto tasso di mortalità, soprattutto nelle prime ore. Secondo gli scienziati, la somministrazione di UFH in bolo endovenoso (di solito 5000 UI) è superiore alle alternative NMH e Fondaparinux somministrate per via sottocutanea. Soprattutto se c’è una centralizzazione con ridotta perfusione tissutale nello shock ostruttivo. Come infusione continua successiva, raccomandano una dose iniziale di 1000 UI all’ora con l’obiettivo di prolungare di 1,5-2,5 volte il tempo di tromboplastina parziale (aPTT).
Fase acuta e di mantenimento
Gli antagonisti della vitamina K (VKA) sono stati a lungo i preparati più utilizzati per l’anticoagulazione terapeutica. Tuttavia, sono limitati da fattori quali la ristretta finestra terapeutica, le interazioni farmacologiche e alimentari e la necessità di regolare la dose, compreso il monitoraggio (misurazione dell’INR). Un’alternativa ai VKA sono gli anticoagulanti orali non vitamina K-dipendenti (NOAK), che comprendono dabigatran, apixaban, edoxaban e rivaroxaban. Nel 2019, la Società Europea di Cardiologia (ESC), in collaborazione con la Società Europea di Respirazione (ERS), ha pubblicato la sua nuova linea guida, secondo la quale i NOAK dovrebbero essere preferiti ai VKA per l’anticoagulazione orale dei pazienti con embolia polmonare (in assenza di controindicazioni). Le controindicazioni ai NOAK includono l’insufficienza renale grave, la funzionalità epatica compromessa, la gravidanza o l’allattamento e la sindrome antifosfolipidica.
Attualmente sono disponibili diverse strategie per la terapia dell’anticoagulazione orale dei pazienti con embolia polmonare, scrivono il Dr. Ebner e il Dr. Lankeit: il regime “tradizionale” consiste nella sovrapposizione di una doppia anticoagulazione con NMH e nel passaggio a un VKA (INR target 2,0-3,0). Inoltre, è prevista una duplice terapia sequenziale con NMH iniziale per almeno 5 giorni e successivo passaggio alla terapia con dabigatran o edoxaban (in dose di mantenimento), nonché monoterapia con rivaroxaban o apixaban (in ogni caso in dose iniziale più elevata). Secondo gli esperti, una riduzione della dose di NOAK dovrebbe essere effettuata solo dopo un esame critico e in modo restrittivo nei primi 6 mesi dopo un’embolia polmonare. Nei pazienti con embolia polmonare che hanno anche un cancro, l’anticoagulazione deve essere continuata fino a quando il cancro non è considerato guarito.
Profilassi secondaria
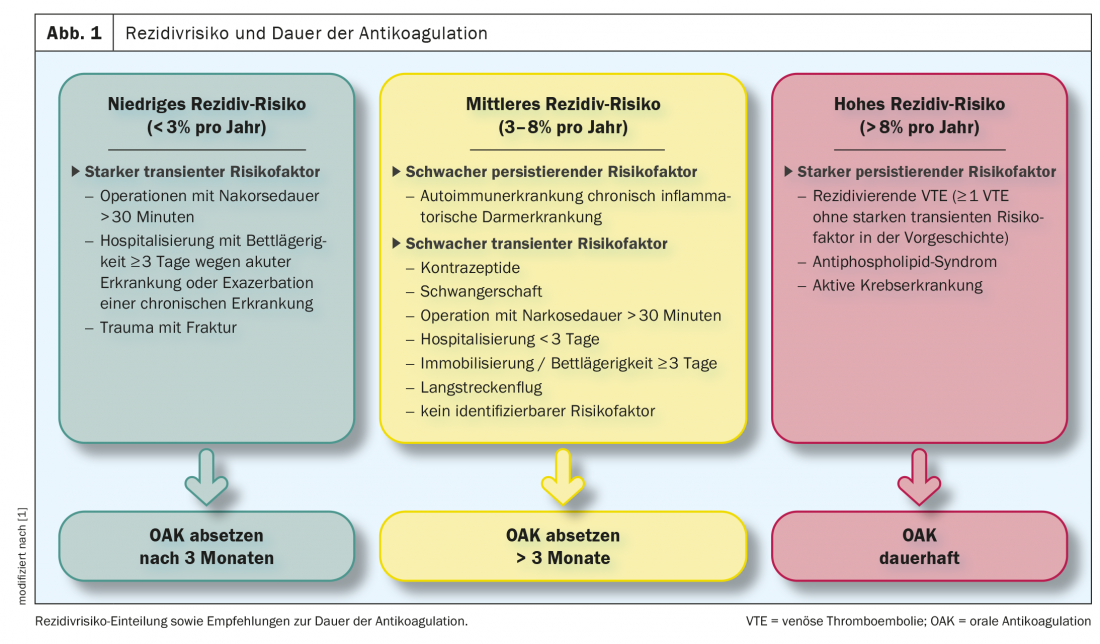
La profilassi secondaria serve a prevenire una nuova tromboembolia. Nella linea guida ESC 2019 [2], i pazienti con embolia polmonare sono suddivisi in 3 gruppi in relazione al rischio di recidiva. Gruppi divisi (Fig.1). Di conseguenza, nei pazienti che avevano un forte fattore di rischio transitorio/reversibile all’insorgenza dell’EPP (ad esempio, un intervento di sostituzione dell’anca o del ginocchio o un trauma con frattura), il rischio di recidiva può essere considerato basso e l’anticoagulazione può essere interrotta dopo 3 mesi. Un rischio medio di recidiva con la considerazione di continuare l’anticoagulazione a tempo indeterminato (con valutazione regolare del rischio-beneficio) è associato ai pazienti che hanno un debole fattore di rischio transitorio/reversibile (per esempio, un intervento chirurgico minore, un volo a lunga distanza), un debole fattore di rischio persistente (per esempio, malattie autoimmuni attive, malattia infiammatoria cronica intestinale) o per i quali non è possibile identificare alcun fattore scatenante. I pazienti ad alto rischio di recidiva e raccomandati per l’anticoagulazione permanente hanno un forte fattore di rischio persistente (ad esempio, cancro attivo, sindrome antifosfolipidica o episodi ricorrenti di TEV non spiegati da forti fattori di rischio transitori).
Letteratura:
- Ebner M, Lankeit M: Terapia antitrombotica nell’embolia polmonare. DMW – Deutsche Medizinische Wochenschrift 2020; 145(14): 970-977; doi: 10.1055/a-0955-3379.
- Konstantinides SV, Meyer G, Becattini C, et al: Linee guida ESC 2019 per la diagnosi e la gestione dell’embolia polmonare acuta sviluppate in collaborazione con la European Respiratory Society (ERS). Eur Heart J 2019; doi: 10.1093/eurheartj/ehz405.
InFo PNEUMOLOGIA & ALLERGOLOGIA 2021; 3(1): 39-40