Il carcinoma della prostata è il tumore maschile più comune nei Paesi occidentali ed è la seconda causa di morte legata al cancro in Svizzera. In particolare, il cancro alla prostata metastatico resistente alla castrazione (mCRPC) è una sfida che può essere affrontata terapeuticamente in molti modi. L’attuale situazione dei dati sui nuovi principi attivi è stata discussa in occasione del Simposio sulla prostata tenutosi a San Gallo a novembre.
“Cosa promettono i nuovi farmaci e gli sviluppi nel campo del carcinoma prostatico metastatico?” è stata la domanda posta da Aurelius Omlin, MD, dell’Ospedale Cantonale di San Gallo. “Non molto tempo fa, la chemioterapia con docetaxel era l’unica opzione di trattamento che offriva un beneficio in termini di sopravvivenza globale ai pazienti con cancro alla prostata metastatico resistente alla castrazione (progressione nonostante la soppressione del testosterone) (mCRPC).
La situazione è cambiata solo negli ultimi quattro anni, quando è stato possibile dimostrare l’efficacia dei seguenti farmaci in studi prospettici randomizzati: l’immunoterapia con sipuleucel-T, una chemioterapia con legame alla tubulina analoga al docetaxel con cabazitaxel, il nuovo inibitore della sintesi ormonale abiraterone, il radionuclide radium-223 e il nuovo antagonista del recettore degli androgeni enzalutamide (Tabella 1)”.

Cabazitaxel: è approvato in Svizzera dopo il fallimento della chemioterapia con docetaxel. In combinazione con il prednisone, mostra un vantaggio significativo nella sopravvivenza globale rispetto alla combinazione con il mitoxantrone [1].
Abiraterone: è approvato in Svizzera dopo e, come unica delle nuove sostanze, anche prima della chemioterapia con docetaxel. In combinazione con il prednisone, mostra un vantaggio significativo nella sopravvivenza globale rispetto al placebo più prednisone, dopo la terapia di prima linea con docetaxel [2]. In combinazione con il prednisone, migliora anche significativamente la sopravvivenza libera da progressione come terapia di prima linea rispetto al placebo più prednisone e mostra un trend nella sopravvivenza globale [3].
Enzalutamide: non ancora approvato in Svizzera, ma previsto per il 2014. Dopo la chemioterapia, mostra un vantaggio significativo rispetto al placebo nella sopravvivenza globale [4].
Radium-223: è attualmente disponibile in Svizzera nell’ambito di un programma di accesso ampliato.
Monitoraggio e uso sequenziale
“Il livello di PSA può aumentare con le nuove terapie nelle prime dodici settimane, quindi la misurazione del PSA deve essere effettuata con cautela in questo periodo. In seguito, però, dovrebbe essere effettuato ogni tre o quattro settimane”, afferma il dottor Omlin. Il monitoraggio comprende anche:
- TAC e scintigrafia ogni dodici settimane
- Risonanza magnetica della colonna vertebrale lunga in caso di coinvolgimento osseo esteso: al basale e se clinicamente indicato (dolore, deficit neurologici).
Attualmente non sono disponibili dati raccolti in modo prospettico sull’uso sequenziale e sulla possibile resistenza incrociata delle nuove sostanze. Tuttavia, esistono studi più piccoli con una potenza limitata, ad esempio che studiano il docetaxel dopo l’abiraterone: L’attività del docetaxel è stata inferiore a quella prevista dopo l’abiraterone e non c’è stata una risposta significativa del PSA o dei tessuti molli in otto pazienti che non avevano risposto all’abiraterone o erano progrediti durante la terapia con abiraterone. [5]. L’enzalutamide ha mostrato un beneficio significativo in alcuni pazienti in sequenza dopo docetaxel e abiraterone [6]; allo stesso modo, l’abiraterone sembra avere un effetto moderato dopo docetaxel ed enzalutamide [7]. Attualmente, mancano fattori predittivi che permettano di selezionare una terapia personalizzata.
“Nel complesso, quindi, ci sono molte nuove opzioni terapeutiche con tassi di sopravvivenza migliori, che a loro volta rendono ancora più importante la gestione degli effetti collaterali e la prevenzione delle complicanze (eventi ossei). Il monitoraggio della terapia è comunque impegnativo, in alcuni casi ci si può aspettare una resistenza incrociata alle nuove terapie e, cosa da non dimenticare, i costi delle nuove terapie sono considerevoli”, ha concluso il dottor Omlin. “A causa delle crescenti possibilità e complessità, i pazienti con cancro alla prostata resistente alla castrazione dovrebbero essere discussi in modo interdisciplinare e, se possibile, anche inclusi in studi clinici per ottenere ulteriori progressi nel trattamento di questa malattia”.
Come trattare le metastasi ossee?
Il PD Dr. med. Dr. Friedemann Honecker dello ZeTuP di San Gallo ha parlato del tema delle metastasi ossee e del trattamento diretto all’osso: “Oltre il 90% di tutti i pazienti con mCRPC sviluppa metastasi ossee. Questo è associato a una mortalità e a una morbilità significative. Queste metastasi osteoblastiche maggioritarie causano un aumento del tasso di eventi ossei (“eventi correlati allo scheletro”, SRE). Le possibili complicazioni sono: Dolore, immobilizzazione, fratture patologiche, ipercalcemia o compressione nervosa/spinale”.
Poiché le sostanze messaggere PTHrP, RANKL, TGF-β, FGF, MET e VEGF sul lato del tumore e TNF-α ed ET-1 sul lato dell’osso sono significativamente coinvolte nelle metastasi scheletriche, rappresentano anche possibili bersagli per una terapia mirata.
Ad esempio, il denosumab, un anticorpo anti-RANKL, viene già utilizzato specificamente per trattare le metastasi ossee. È particolarmente efficace per ridurre il rischio di SRE. In uno studio di fase III, è stata ottenuta una riduzione relativa di circa il 18% rispetto allo zoledronato (Fig. 1) [8].
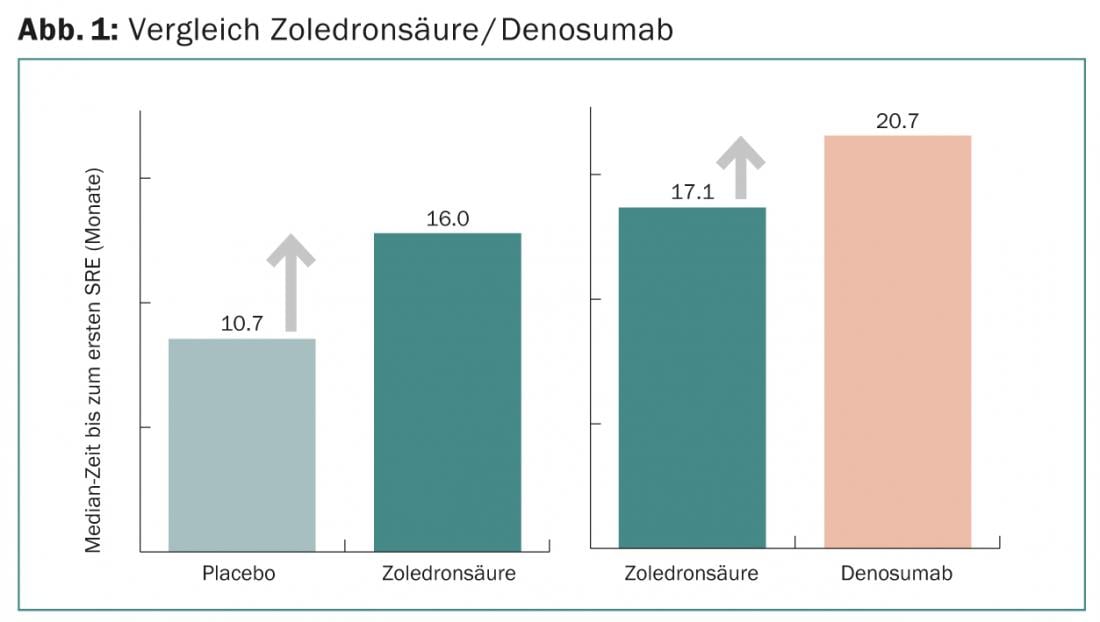
Tuttavia, anche il bifosfonato zoledronato previene significativamente le SRE rispetto al placebo [9]. “Le reazioni avverse ai bifosfonati includono sintomi simil-influenzali (reazione di fase acuta) nel 10-20% dei casi, effetti collaterali renali (diminuzione della clearance della creatinina), ipocalcemia (diminuzione del livello di calcio nel siero) e osteonecrosi della mascella (evento multifattoriale). La clearance della creatinina deve essere sempre controllata prima di ogni infusione; se aumenta, la dose deve essere modificata. La durata dell’infusione non deve essere ridotta, ma trattenuta o prolungata. La raccomandazione al paziente di bere 1-2 litri di acqua nel giorno dell’infusione è ragionevole”, ha spiegato il Dr. Honecker.
Il radio-223 ha persino mostrato un effetto positivo sulla sopravvivenza globale nei pazienti sintomatici con metastasi ossee, per cui l’approvazione in Svizzera è attualmente in fase di esame. Infine, anche la sostanza già approvata abiraterone mostra una buona efficacia per quanto riguarda la comparsa di SRE e la palliazione del dolore osseo.
Cabozantinib, un inibitore VEGFR2/MET, è particolarmente promettente tra gli agenti attivi completamente nuovi e non ancora approvati e ha indotto una risposta molto chiara delle metastasi ossee nella scintigrafia scheletrica nel 60-70% e un sollievo dal dolore in un buon 50% dei pazienti parzialmente pretrattati negli studi di fase II. Il composto è attualmente in fase di sperimentazione III. Si devono anche osservare gli effetti collaterali, a volte gravi, di cabozantinib in particolare.
Radio-223
Infine, il dottor Joachim Müller, dell’Ospedale Cantonale di San Gallo, ha approfondito il radionuclide radio-223 (nome commerciale nuovo Xofigo®): “Si tratta del primo radiofarmaco emittente particelle alfa clinicamente disponibile per la terapia medica nucleare delle metastasi ossee nella mCRPC.
Rispetto agli emettitori beta (stronzio-89, samario-153, renio-188) che sono stati utilizzati per molto tempo, che consentono una terapia palliativa del dolore ma non prolungano la sopravvivenza, gli emettitori alfa mostrano alcuni vantaggi fisici: trasferiscono la loro energia al tessuto nel modo più breve possibile, per cui le aree vicine, come il midollo osseo adiacente, non ricevono alcuna dose di radiazioni o ne ricevono una molto bassa”.
Il noto studio di fase III ALSYMPCA [10] ha recentemente portato all’approvazione da parte della FDA. La sopravvivenza complessiva è stata significativamente prolungata rispetto al placebo, così come l’intervallo di tempo fino al primo evento scheletrico. Gli effetti collaterali erano solo lievi e comprendevano diarrea e nausea. L’emotossicità di grado 3-4 è rara: Neutropenia 2%, trombocitopenia 3%, anemia 6%.
Le possibili combinazioni con altri farmaci non sono ancora state determinate.
Fonte: 5° Simposio interdisciplinare sul cancro alla prostata, 7 novembre 2013, San Gallo.
Letteratura:
- De Bono JS, et al: Prednisone più cabazitaxel o mitoxantrone per il carcinoma prostatico metastatico resistente alla castrazione in progressione dopo il trattamento con docetaxel: uno studio randomizzato in aperto. The Lancet 2010; 376(9747): 1147-1154. doi:10.1016/S0140-6736(10)61389-X.
- De Bono JS, et al: Abiraterone e aumento della sopravvivenza nel cancro alla prostata metastatico. N Engl J Med 2011; 364: 1995-2005. doi: 10.1056/NEJMoa1014618.
- Ryan CJ, et al: Abiraterone nel cancro alla prostata metastatico senza precedente chemioterapia. N Engl J Med 2013; 368: 138-48. doi: 10.1056/NEJMoa120909.
- Scher HI, et al: Aumento della sopravvivenza con enzalutamide nel cancro alla prostata dopo la chemioterapia. N Engl J Med 2012 Sep 27; 367(13): 1187-97. Epub 2012 Aug 15.
- Mezynski J, et al: Attività antitumorale del docetaxel dopo il trattamento con l’inibitore del CYP17A1 abiraterone: prove cliniche di resistenza incrociata? Ann Oncol 2012 Nov; 23(11): 2943-7. doi: 10.1093/annonc/mds119. Epub 2012 Jul 5.
- Schrader AJ, et al: Enzalutamide nei pazienti con cancro alla prostata resistente alla castrazione che progrediscono dopo Docetaxel e Abiraterone. Eur Urol 2013 Jul 2. pii: S0302 2838(13)00657-X. doi: 10.1016/j.eururo.2013.06.042. [Epub ahead of print].
- Noonan KL, et al: Attività clinica di abiraterone acetato nei pazienti con carcinoma prostatico metastatico resistente alla castrazione in progressione dopo enzalutamide. Ann Oncol 2013. doi: 10.1093/annonc/mdt138 Prima pubblicazione online: 12 aprile 2013.
- Fizazi K, et al: Denosumab rispetto all’acido zoledronico per il trattamento delle metastasi ossee negli uomini con cancro alla prostata resistente alla castrazione: uno studio randomizzato, in doppio cieco. Lancet 2011 Mar 5; 377(9768): 813-22. doi: 10.1016/S0140-6736(10)62344-6. Epub 2011 Feb 25.
- Saad F, et al: Uno studio randomizzato, controllato con placebo, sull’acido zoledronico nei pazienti con carcinoma prostatico metastatico ormono-refrattario. J Natl Cancer Inst 2002 Oct 2; 94(19): 1458-68.
- Parker C, et al: Radio-223 emettitore di alfa e sopravvivenza nel cancro alla prostata metastatico. N Engl J Med 2013; 369: 213-23. doi: 10.1056/NEJMoa1213755.
InFo Oncologia & Ematologia 2013; 1(1): 33-36