L’8ª Accademia del Ferro non riguardava solo il ferro in sé, ma collocava la carenza di ferro in un contesto pratico più ampio. Tra le altre cose, si è parlato della diagnosi precoce e della cura dei pazienti oncologici e del paziente con insufficienza renale nell’ambulatorio di famiglia.
Secondo il Prof. Dr. med. Daniel Betticher, Clinica di Medicina Interna Generale e Clinica di Oncologia, Ospedale di Friburgo, la prevenzione del cancro consiste inizialmente nel ridurre i fattori di rischio attraverso uno stile di vita non sano (smettere di fumare, consumo moderato di alcol, protezione dal sole, dieta sana, ecc.) Il secondo imperativo è la diagnosi precoce. I sintomi non specifici come il dolore, la stanchezza, l’astenia o la costipazione sono molto più frequenti delle “bandiere rosse”, cioè dei sintomi specifici come l’emottisi, la melena, l’alternanza costipazione/diarrea, ecc. Il National Institute for Health and Care Excellence (NICE) ha dedicato linee guida speciali a sintomi specifici nel 2005. I medici di base in Inghilterra sono stati istruiti a indirizzare i pazienti con questi sintomi ai centri oncologici. È stato dimostrato che questo potrebbe effettivamente ridurre in modo significativo l’intervallo tra la prima comparsa dei sintomi e la diagnosi in alcuni tipi di cancro [1].
Ma l’intervallo più breve è anche associato a migliori possibilità di cura (o a un tempo più lungo tra la diagnosi e la morte)? Secondo un documento di Tørring et al. L’accorciamento dell’intervallo – almeno per i sintomi specifici – contribuisce a ridurre il rischio di mortalità nei pazienti con cancro colorettale [2]. Nell’area dei sintomi non specifici, invece, non è stato possibile dimostrare una correlazione significativa. Questo include, tra l’altro, la stanchezza, che spesso è dovuta a una carenza di ferro. Uno studio ha dimostrato che il 42,6% di 1513 pazienti oncologici aveva una saturazione di transferrina (TSAT) inferiore al 20% [3]. Il 33% era anemico. Quindi, quando dovrebbe avvenire la sostituzione [4]?
- AIDA (“anemia da carenza assoluta di ferro”, ad esempio il carcinoma del colon): TSAT <20%, ferritina <30 ng/ml. Qui è indicato il ferro i.v..
- FIDA (“anemia funzionale da carenza di ferro, ad esempio avversione alla carne, carcinoma gastrico metastatico): TSAT <20%; ferritina 30-800 ng/ml. Questo gruppo potrebbe beneficiare della sostituzione del ferro per via endovenosa.
- FIDA: TSAT 20-50%, ferritina 30-800 ng/ml. È improbabile che questo gruppo tragga beneficio dalla sostituzione i.v. del ferro.
Se i valori sono ancora più alti, c’è un sovraccarico di ferro e non è necessario sostituirlo.
Programmi di diagnosi precoce
Il terzo imperativo della prevenzione del cancro è rappresentato dai programmi di diagnosi precoce. “L’obiettivo dovrebbe essere quello di diagnosticare il carcinoma prima che si sviluppi completamente, cioè quando è ancora una displasia moderata o grave”, afferma il Prof. Betticher. Un esempio è la diagnosi precoce del carcinoma cervicale con la diagnosi di lesioni precancerose con un semplice test di striscio (ogni anno per i primi tre anni, poi ogni tre anni). Gli studi non randomizzati hanno mostrato una diminuzione della mortalità dopo l’introduzione del test. Il test dello striscio cervicale è consigliato a tutte le donne di età superiore ai 21 anni.
Carcinoma mammario: lo screening mammografico cerca il carcinoma in fase iniziale. In una revisione Cochrane, gli studi randomizzati hanno dimostrato che il rischio di mortalità può essere ridotto del 23% dopo 13 anni. Ma qual è la situazione in Svizzera? “Se tutte le donne svizzere di età compresa tra i 50 e i 69 anni venissero sottoposte a screening, ogni anno se ne potrebbero salvare 160 dalla morte”, ha detto il Prof. Betticher. “Rispetto allo screening ‘selvaggio’, un’infestazione dei linfonodi ascellari è del 50% meno frequente se si organizza una diagnosi precoce. Questo è un vantaggio spesso dimenticato, perché uno stadio avanzato richiede anche una terapia più intensa. Nel complesso, si può affermare che la mammografia è efficace e conveniente. Ecco perché è consigliato a tutte le donne sopra i 50 anni”.
Carcinoma del colon: le opzioni di esame per il carcinoma del colon includono il rilevamento di sangue nelle feci o la colonscopia (virtuale). L’obiettivo è quello di individuare una fase iniziale di sviluppo con polipi o un carcinoma precoce che è ancora curabile con la chirurgia e la chemioterapia. L’analisi del sangue ha un beneficio comprovato (riduce il rischio di mortalità del 16% secondo una revisione Cochrane di quattro studi randomizzati [5]), ma si perde molto. Il tasso di falsi negativi è fino al 75%. Il gold standard è quindi la colonscopia. Secondo le stime (non ci sono studi randomizzati), questo riduce la mortalità della metà e consente la resezione dei polipi nella stessa seduta. Tuttavia, si tratta di una procedura (anche se piccola) con i relativi effetti collaterali. La colonscopia virtuale non comporta un intervento chirurgico, ma non consente di rimuovere i polipi. Inoltre, per essere rilevato con la colonscopia virtuale, un polipo deve avere una dimensione di >9 mm. “In generale, se si ha un rischio normale o una predisposizione familiare, è consigliabile una colonscopia a partire dai 50 anni , poiché la probabilità di carcinoma aumenta da questo momento in poi”, ha spiegato il Prof. Betticher.
Carcinoma polmonare: nel carcinoma polmonare, non è possibile identificare uno stadio precanceroso. Il National Lung Screening Trial (NLST) ha dimostrato che la TAC annuale a basso dosaggio riduce la mortalità specifica per cancro al polmone e la mortalità per tutte le cause (rispettivamente del 20 e del 6,7%). Tuttavia, ci sono stati anche molti risultati che necessitano di chiarimenti. Il tasso di sovradiagnosi era relativamente alto e il rapporto costi-benefici era scarso. Pertanto, al momento lo screening non è raccomandato globalmente ai fumatori. Bisogna scoprire qual è la popolazione di screening migliore.
Carcinoma prostatico: lo studio di Göteborg ha dimostrato che il rischio di mortalità nel carcinoma prostatico può essere ridotto di un significativo 44% dopo 15 anni con il test del PSA [6]. Tuttavia, è stato necessario trattare dodici uomini perché uno fosse guarito. La morbilità dopo l’intervento chirurgico (incontinenza urinaria 15-50%, disfunzione sessuale 20-70%) o dopo la radioterapia (incontinenza urinaria 2-16%, disfunzione sessuale 20-45%) è elevata. A causa della scarsa specificità e sensibilità del test, lo screening di massa non è raccomandato – a meno che non vi siano chiari fattori di rischio (colore della pelle nera, padre o fratello con cancro alla prostata) o il paziente informato desideri esplicitamente essere sottoposto allo screening. L’aspettativa di vita deve essere di almeno dieci anni.
Il paziente con insufficienza renale nell’ambulatorio di famiglia
Secondo il Prof. Dr. med. Rudolf P. Wüthrich, Clinica di Nefrologia, Ospedale Universitario di Zurigo, circa 500.000 persone in Svizzera hanno un tasso di filtrazione glomerulare (GFR) compromesso. La prevalenza dell’insufficienza renale cronica è in aumento nella popolazione generale. Lo screening della malattia renale è quindi consigliabile ogni uno o due anni per i gruppi a rischio. Questi includono i diabetici, gli ipertesi e le persone con una storia familiare di diabete. Vengono misurati la creatinina sierica (stima del GFR), le proteine/creatinina o l’albumina/creatinina e il sedimento urinario. Alla fine del chiarimento, si dovrebbe determinare quanto segue:
- Stadio e tendenza alla progressione dell’insufficienza renale (creatinina sierica, eventualmente cistatina C, valori precedenti, tendenza alla progressione).
- Insufficienza renale acuta o cronica? (Anamnesi; ecografia: reni rimpiccioliti, struttura, singolarità).
- Pre-renale, postrenale, renale? (anamnesi, pressione sanguigna, vene del collo; ecografia: ostruzione, ritenzione di urina).
- Se renale: glomerulare, tubulo-interstiziale, vascolare? (sedimento, proteine/creatinina, profilo proteico dell’urina, catene leggere libere nel siero).
La malattia renale cronica (CKD) è classificata in cinque stadi (Tab. 1) . Inoltre, esiste la classificazione CGA della malattia renale cronica in base alla malattia di base(causa), alla velocità di filtrazione glomerulare(GFR) e all’albuminuria. La GFR è suddivisa in sei categorie, l’albuminuria in tre. È stato dimostrato che il rischio di mortalità nell’insufficienza renale cronica dipende dall’entità dell’albuminuria (più alta, più pericolosa).

Evitare la progressione
La progressione dell’insufficienza renale può essere generalmente inibita da un controllo ottimale della pressione arteriosa con ACE-inibitori o bloccanti del recettore dell’angiotensina II [7], statine e bicarbonato. Il doppio blocco con ACE-inibitori e bloccanti del recettore dell’angiotensina II deve essere evitato, come ha dimostrato uno studio del 2008 [8]. Gli obiettivi di pressione arteriosa nella malattia renale sono valori di <140/90 mmHg. Nelle popolazioni a rischio, come i pazienti con diabete, si dovrebbe puntare a valori di <135/85 mmHg, e nella nefropatia cronica con proteinuria inferiore a 1 g/d, a valori di <130/80 mmHg e <125/75 mmHg rispettivamente (proteinuria >1 g/d). Uno studio di Baigent e colleghi dimostra la riduzione significativa dell’incidenza di eventi aterosclerotici gravi con simvastatina più ezetimibe nei pazienti con malattia renale cronica avanzata [9].
Le complicazioni dell’insufficienza renale cronica progressiva sono principalmente la morbilità cardiovascolare nello stadio 2 della CKD, l’iperparatiroidismo e l’anemia nello stadio 3, l’acidosi metabolica e l’iperkaliemia nello stadio 4 e la dialisi nello stadio 5.
Anemia renale
La patogenesi dell’anemia renale avviene attraverso la riduzione della massa dei nefroni, con conseguente diminuzione della produzione di eritropoietina. La perdita cronica di sangue causa una carenza di ferro, la malnutrizione a sua volta causa una carenza di vitamine. Inoltre, l’emivita degli eritrociti si accorcia. Un valore di emoglobina (Hb) <11 g/dl è un’indicazione per la terapia (prima della dialisi). Mirare a un’Hb compresa tra 11 e 12 g/dl (o 13), ma non superiore. I prerequisiti sono riserve di ferro “piene”: ferritina >100 ug/l e saturazione della transferrina >20%. Il ferro viene somministrato per via parenterale (Ferinject® o Venofer®), poiché è più rapido ed efficiente della somministrazione orale [10].
In Svizzera, esistono i preparati di eritropoietina Mircera®, Aranesp®, Recormon® ed Eprex®. Se il livello di emoglobina sale troppo (valori di 13 g/dl e superiori), diventa pericoloso, poiché eventi come morte, infarto, ricovero in ospedale per insufficienza cardiaca e ictus si verificano frequentemente [11].
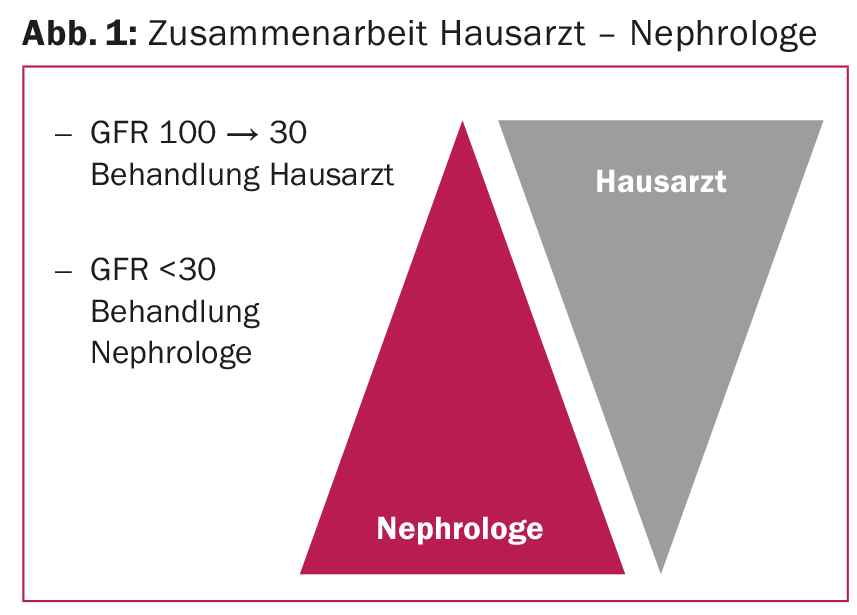
“In generale, è molto importante che la collaborazione tra medico di base e nefrologo funzioni bene nel trattamento dei pazienti con malattia renale”, ha detto il relatore. La Figura 1 mostra un esempio di come potrebbe apparire un tale approccio.
Fonte: 8a Accademia del Ferro, 30 aprile 2015, Zurigo-Oerlikon
Letteratura:
- Neal RD, et al: Confronto degli intervalli diagnostici del cancro prima e dopo l’implementazione delle linee guida NICE: analisi dei dati del database di ricerca della medicina generale del Regno Unito. Br J Cancer 2014 Feb 4; 110(3): 584-592.
- Tørring ML, et al: Tempo alla diagnosi e mortalità nel cancro del colon-retto: uno studio di coorte nell’assistenza primaria. Br J Cancer 2011 Mar 15; 104(6): 934-940.
- Ludwig H, et al: Prevalenza della carenza di ferro in diversi tumori e la sua associazione con lo scarso rendimento, lo stato di malattia e l’anemia. Ann Oncol 2013 Jul; 24(7): 1886-1892.
- Gilreath JA, Stenehjem DD, Rodgers GM: Diagnosi e trattamento dell’anemia correlata al cancro. Am J Hematol 2014; 89(2): 203-212.
- Hewitson P, et al: Revisione sistematica Cochrane dello screening del cancro colorettale con il test del sangue occulto fecale (emoccult): un aggiornamento. Am J Gastroenterol 2008 Jun; 103(6): 1541-1549.
- Hugosson J, et al: Risultati sulla mortalità dello studio randomizzato di screening del cancro alla prostata basato sulla popolazione di Göteborg. Lancet Oncol 2010 Aug; 11(8): 725-732.
- Brenner BM, et al: Effetti del losartan sugli esiti renali e cardiovascolari nei pazienti con diabete di tipo 2 e nefropatia. N Engl J Med 2001 Sep 20; 345(12): 861-869.
- Mann JF, et al: Esiti renali con telmisartan, ramipril, o entrambi, in persone ad alto rischio vascolare (studio ONTARGET): uno studio multicentrico, randomizzato, in doppio cieco, controllato. Lancet 2008 Aug 16; 372(9638): 547-553.
- Baigent C, et al: Gli effetti della riduzione del colesterolo LDL con simvastatina più ezetimibe nei pazienti con malattia renale cronica (Study of Heart and Renal Protection): uno studio randomizzato controllato con placebo. Lancet 2011 Jun 25; 377(9784): 2181-2192.
- Van Wyck DB, et al: Uno studio randomizzato e controllato che confronta il ferro saccarosio per via endovenosa con il ferro per via orale nei pazienti anemici con CKD non dipendenti dalla dialisi. Kidney Int 2005 Dic; 68(6): 2846-2856.
- Singh AK, et al: Correzione dell’anemia con epoetina alfa nella malattia renale cronica. N Engl J Med 2006 Nov 16; 355(20): 2085-2098.
CARDIOVASC 2015; 14(4): 35-37











