Esistono nuovi approcci terapeutici per il mieloma multiplo. Ad esempio, si stanno studiando l’efficacia e la sicurezza delle cellule CAR-T. In particolare, potrebbero essere applicabili in futuro nella situazione di refrattarietà e recidiva.
La lenalidomide è sempre più utilizzata per la terapia di induzione nei pazienti con mieloma multiplo. Tuttavia, a causa della resistenza alla lenalidomide nel mieloma multiplo, che spesso si verifica nel prosieguo del trattamento, la ricerca di terapie di follow-up efficaci è necessaria dal punto di vista medico.
OPTIMISMM: ha dimostrato di essere più che un semplice ottimismo.
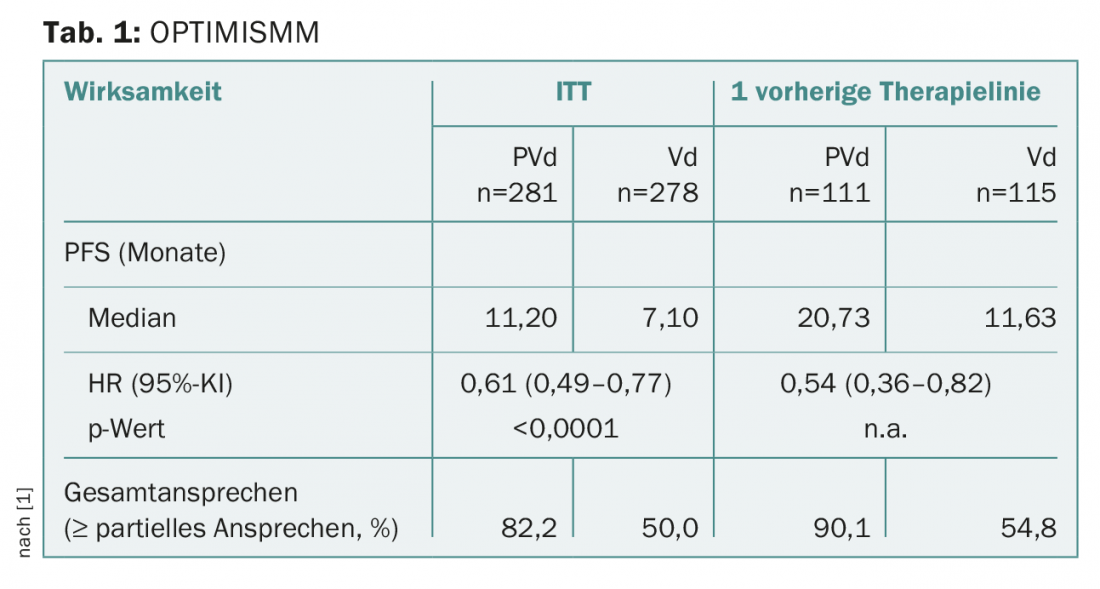
La pomalidomide è oggi generalmente utilizzata nel trattamento del mieloma multiplo recidivato/refrattario e spesso si è dimostrata efficace anche contro le cellule resistenti alla lenalidomide [1]. Lo studio di fase III presentato, denominato OPTIMISMM, su pazienti trattati con lenalidomide con mieloma multiplo recidivato/refrattario (di cui circa il 70% era precedentemente refrattario alla lenalidomide) ha rivelato, tra l’altro, un significativo prolungamento della sopravvivenza libera da progressione: Nella popolazione intention-to-treat, ma anche dopo un solo pre-trattamento (inclusa la lenalidomide), sia la PFS che il tasso di risposta globale (ORR) erano migliori per pomalidomide, bortezomib e desametasone a basso dosaggio rispetto a bortezomib e desametasone da soli. (Tab. 1) [1].
Risposta al trattamento sostenuta grazie all’immunoterapia?
Al congresso EHA di quest’anno, si è discusso in modo molto vivace anche di un altro nuovo approccio terapeutico per il mieloma multiplo, l’immuno-oncologia che utilizza le cellule CAR-T. Soprattutto per i pazienti con MM refrattario e pesantemente pretrattati, l’immunoterapia potrebbe rappresentare un’opzione terapeutica in futuro.
Come bersaglio terapeutico, l’antigene di maturazione delle cellule B (BCMA in breve) sembra attualmente molto promettente. Il BCMA è espresso prevalentemente sulla superficie delle plasmacellule e si trova in pochissimi altri tessuti del corpo umano. Questo lo rende un marcatore tumorale adatto e un possibile bersaglio per l’immunoterapia [2].
In uno studio multicentrico iniziale di fase I [2], gli ematologi stanno utilizzando bb2121, cellule T chimeriche del recettore dell’antigene (CAR) di seconda generazione, in grado di riconoscere il BCMA con precisione millimetrica. La fase di dose-escalation dello studio ha già fornito risultati promettenti per quanto riguarda l’efficacia e la sicurezza di bb2121 nei pazienti con mieloma multiplo recidivato/refrattario.
Una buona metà dei pazienti presentati ha partecipato alla fase di escalation. In precedenza, dovevano essere sottoposti ad almeno tre terapie (tra cui un inibitore del proteasoma e un immunomodulatore) o essere doppiamente refrattari alla terapia. Sulle loro plasmacellule, questi pazienti hanno portato il BCMA nel ≥50% dei casi [2]. La seconda parte dello studio in corso, la cosiddetta fase di espansione della dose, prevedeva la pre-terapia con daratumumab per i restanti pazienti presentati. Inoltre, la malattia doveva essere refrattaria all’ultima terapia. Al contrario, non era più necessaria una comprovata espressione di BCMA.
I risultati hanno mostrato che bb2121 ha funzionato in modo molto promettente a dosi di ≥150 × 106 cellule CAR-T (Tab. 2) [2]:
- C’è stata una risposta sostenuta alla terapia, la neurotossicità e la sindrome da rilascio di citochine (CRS) sono state controllabili, per lo più di grado 1-2.
- Nel complesso, la terapia con cellule T CAR contro il BCMA con bb2121 sembra certamente rappresentare una nuova opzione terapeutica per i pazienti con mieloma multiplo recidivato/refrattario.

Tema caldo: Immunoterapia
Da un punto di vista genetico, il mieloma multiplo è molto eterogeneo, il che lo rende una malattia complessa. Oggi, il sequenziamento di nuova generazione (NGS) va già ben oltre l’importanza diagnostica della citogenetica convenzionale e ha aiutato, tra l’altro, a decifrare importanti percorsi di segnalazione e processi di mutazione che possono influenzare la prognosi di un paziente con mieloma multiplo. Allo stesso tempo, i progressi nell’ambito della diagnostica genetica sono il punto di partenza per nuove procedure terapeutiche come l’immunoterapia, che naturalmente comprende la procedura delle cellule CAR-T o l’anticorpo anti-CD38 daratumumab.
L’anticorpo monoclonale anti-CD38 daratumumab è già un fattore importante nella lotta contro il mieloma multiplo. Il meccanismo d’azione è tanto semplice quanto efficace: l’anticorpo anti-CD38 induce la morte cellulare delle cellule del mieloma, da un lato attraverso effetti immunitari diretti e dall’altro attraverso l’eliminazione delle cellule immunosoppressive. Gli studi hanno anche dimostrato che le combinazioni di anticorpi monoclonali come daratumumab o elotuzumab e farmaci immunomodulatori o inibitori del proteasoma possono aumentare la loro efficacia terapeutica, ma senza provocare maggiori effetti tossici.
In futuro, si prevede che la gamma di immunoterapie per il mieloma multiplo aumenterà ulteriormente, secondo gli esperti presenti al congresso EHA. Ad esempio, si sta discutendo di coniugati composti da un anticorpo e un farmaco o dell’uso di inibitori del checkpoint per il trattamento del mieloma multiplo [3].
Gli ematologi e gli oncologi dovrebbero tenerlo presente.
Negli ultimi anni, ci sono stati alcuni sviluppi notevoli nel campo delle opzioni terapeutiche per il mieloma multiplo. Tuttavia, non bisogna dimenticare che il MM è ancora una malattia tumorale che non può essere trattata in modo curativo. Soprattutto nel mieloma multiplo recidivato/refrattario, la scelta delle opzioni terapeutiche è considerata limitata. L’immunoterapia potrebbe offrire nuove possibilità in futuro, ma molti approcci per il trattamento del MM, tra cui le cellule CAR-T, sono attualmente ancora in fase di sviluppo e purtroppo non sono ancora disponibili per la pratica quotidiana.
L’approvazione di diverse nuove combinazioni di farmaci (ad esempio carfilzomib-lenalidomide-desametasone, daratumumab-lenalidomide-desametasone o elotuzumab-lenalidomide-desametasone, nonché bortezomib-desametasone-daratumab) ha migliorato la terapia per i pazienti con mieloma multiplo recidivato/refrattario. Tuttavia, questo ha anche complicato il processo decisionale terapeutico da parte di medici e pazienti. In ogni caso, la terapia deve essere ottimizzata per il singolo paziente, soprattutto in caso di ricaduta [3].
Fonte: Congresso EHA, 14-17 giugno 2018, Stoccolma
Letteratura:
- Richardson P, et al: OPTIMISMM: studio di fase 3 di pomalidomide, bortezomib e desametasone a basso dosaggio vs bortezomib e desametasone a basso dosaggio in pazienti esposti a lenalidomide con mieloma multiplo recidivato/refrattario. EHA 2018; Abstract S847.
- Raje N, et al: terapia con cellule t anti-bcma car bb2121 nei pazienti con mieloma multiplo recidivato/refrattario: risultati aggiornati di uno studio multicentrico di fase I. EHA 2018; Abstract S138.
- Van de Donk N: Immunoterapia nel mieloma: perché, quando e come? Argomento: 3ec Mieloma plasmacellulare (mieloma multiplo). EHA 2018; 219162.
InFo ONCOLOGIA & EMATOLOGIA 2018; 6(4): 39-40.