La sarcoidosi è una malattia granulomatosa multisistemica dall’eziologia ancora poco chiara. La diagnosi di sarcoidosi si basa sul quadro clinico tipico e sull’evidenza istologica di granulomi non necrotizzanti a cellule epitelioidi, dopo l’esclusione di altre diagnosi differenziali. Poiché oltre il 90% dei pazienti con sarcoidosi presenta un’infiammazione polmonare o dei polmoni, è importante che i polmoni non vengano danneggiati. Se sono coinvolti anche i linfonodi intratoracici, la diagnosi viene spesso effettuata mediante biopsie ottenute con la broncoscopia. Se indicato, la terapia viene effettuata con immunosoppressori o farmaci immunosoppressivi. Immunomodulatori.
La sarcoidosi è una malattia granulomatosa multisistemica dall’eziologia ancora poco chiara [1]. È caratterizzata da granulomi a cellule epitelioidi non necrotizzanti in vari organi e quindi ha una clinica variabile a seconda del coinvolgimento dell’organo. Non esiste un test diagnostico specifico, quindi la diagnosi si basa sui risultati clinici tipici, sul rilevamento dei granulomi tipici e sull’esclusione delle diagnosi differenziali.
La prevalenza della sarcoidosi è stimata in 1-40/100.000 abitanti in tutto il mondo, anche se le diverse definizioni dei casi, la presentazione clinica variabile e, infine, l’occasionale difficoltà nel fare una diagnosi rendono difficile una quantificazione accurata [2,3]. Inoltre, è stato descritto un “divario Nord-Sud” con una maggiore prevalenza in Scandinavia [4]; lo studio ACCESS ha confermato che gli afroamericani soffrono della malattia più frequentemente e più gravemente [5].
In Svizzera, è stata rilevata una prevalenza nell’arco della vita di 121/100.000 per la diagnosi di sarcoidosi (130/100.000 uomini, 112/100.000 donne). È stata calcolata una prevalenza di 44/100.000 per la sarcoidosi attiva e di 16/100.000 per la sarcoidosi che richiede un ricovero ospedaliero. L’incidenza media annuale in Svizzera è stimata a 7/100.000 abitanti [6].
La malattia è possibile a qualsiasi età, anche se gli adulti più giovani (<40 anni) hanno maggiori probabilità di sviluppare la malattia; un secondo picco di malattia esiste per il sesso femminile all’età di >50 anni [7]. In Svizzera, l’età media alla diagnosi è di 45 +/- 15 anni (41 +/- 14 anni per gli uomini, 48 +/- 15 anni per le donne) [6].
Causa e patogenesi
Le cause della sarcoidosi non sono note. In letteratura sono state discusse diverse ipotesi. La malattia è probabilmente innescata dall’inalazione di un agente/antigene (patogeno, aerosol) in pazienti geneticamente predisposti, come dimostra l’osservazione di un’incidenza raggruppata di sarcoidosi nel primo anno dopo l’attacco terroristico dell’11 settembre al World Trade Center di New York, tra i vigili del fuoco esposti alle polveri [8]. In Svizzera, è stata osservata una maggiore prevalenza nelle regioni con industrie di lavorazione dei metalli e con l’agricoltura (lavorazione di patate e cereali e coltivazione di prati) [6]. A causa della caratteristica di una malattia granulomatosa, è stata discussa anche l’esposizione a micobatteri o altri agenti patogeni, ma non è mai stata provata.
L’osservazione di un accumulo familiare ed etnico suggerisce l’esistenza di un background genetico [9]. Sono stati studiati diversi alleli – principalmente del complesso di istocompatibilità maggiore (MHC) e del gene ACE – identificando i genotipi più frequentemente associati alla sarcoidosi [10]. Alcuni genotipi, a loro volta, sono stati associati alla sindrome di Löfgren e a un decorso benigno, tra gli altri [11].
I processi immunologici sono coinvolti nella patogenesi della sarcoidosi, anche se non sono ancora stati compresi nel dettaglio. La risposta immunitaria è presumibilmente innescata dalla presentazione di un antigene non definito da parte dei macrofagi ai linfociti T CD4+ tramite i recettori MHC di classe II. Le micochine e le citochine rilasciate nel processo (tra cui TNF-α, IL-2) portano alla formazione dei tipici granulomi costituiti da cellule epitelioidi, cellule giganti multinucleate e linfociti T CD4+ [12–14]. Non si sa quali siano i meccanismi che determinano l’autolimitazione della malattia da un lato e la sua progressione cronica dall’altro.
Diagnosi
La diagnosi di sarcoidosi viene fatta con un quadro clinico tipico, l’evidenza istopatologica di granulomi a cellule epitelioidi non necrotizzanti (Fig. 1) e dopo l’esclusione delle diagnosi differenziali.
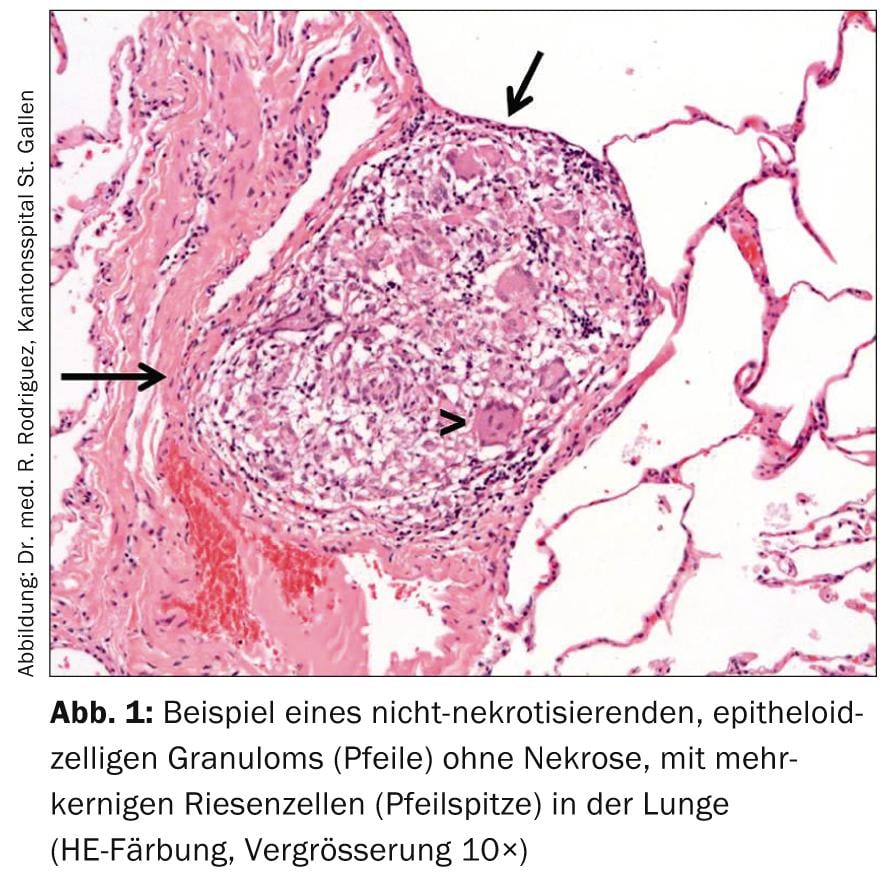
Un possibile algoritmo diagnostico è riassunto nella Figura 2 [15].
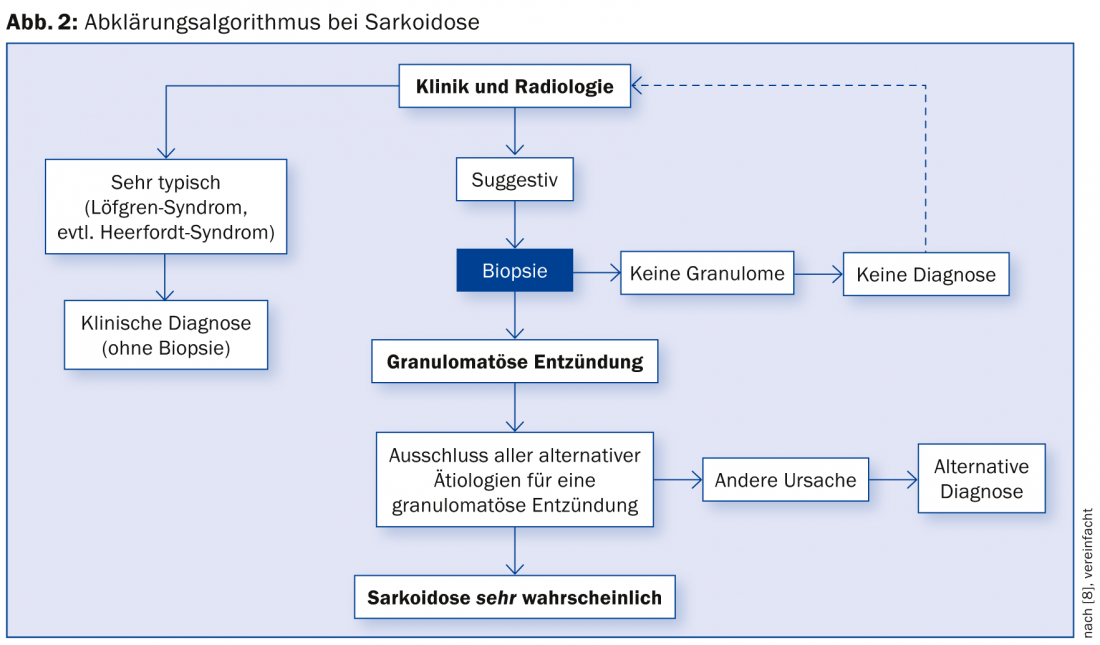
Sintomi tipici
I granulomi tipici possono svilupparsi in qualsiasi organo. Sono frequentemente colpiti i linfonodi ilari e mediastinici, il tessuto polmonare, la pelle e le stazioni linfonodali extratoraciche. Meno frequentemente, viene descritto un coinvolgimento oftalmologico, neurologico o cardiaco (tab. 1); quando questi organi sono colpiti, la compromissione clinica, la morbilità e la mortalità sono significative [16]. Non esiste un’unica sintomatologia tipica della sarcoidosi, in quanto possono essere colpiti praticamente tutti gli organi.

I pazienti sono spesso asintomatici, quindi non è raro che la sarcoidosi sia un reperto incidentale nella linfoadenopatia biliare quando viene eseguita una radiografia convenzionale [17].
Poiché le manifestazioni polmonari sono presenti in oltre il 90% dei pazienti, sono comuni sintomi come tosse non produttiva, dispnea e dolore toracico. Spesso vengono descritti anche sintomi generali non specifici come febbre, perdita di peso, stanchezza cronica, malessere, debolezza muscolare e intolleranza all’esercizio fisico.
Sindrome di Löfgren e sindrome di Heerfordt
La combinazione di linfoadenopatia biliari, febbre, eritema nodoso e artralgie/artriti si chiama sindrome di Löfgren. Questa clinica è caratteristica, per cui l’evidenza istologica dei granulomi può essere omessa in questa situazione. La sindrome di Löfgren ha una buona prognosi. La rara ma specifica combinazione di parotite con uveite e paresi facciale periferica (“paralisi di Bells”) con granulomi sarcoidi istologicamente provati è nota come sindrome di Heerfordt.
Manifestazione intratoracica
Le manifestazioni intratoraciche variano dalla sola linfoadenopatia bifilare alla grave distruzione parenchimale del polmone e all’ipertensione polmonare (anche senza alterazioni polmonari). La gravità polmonare è classificata in cinque stadi radiologici secondo Siltzbach e Scadding sulla base della radiografia convenzionale (Tab. 2 e Fig. 3) [18,19].

La stadiazione è importante perché da essa si possono ricavare informazioni prognostiche. Due terzi dei pazienti sperimentano una remissione spontanea entro 2-5 anni. Questo è particolarmente vero per gli stadi radiologici I e II al momento della diagnosi.
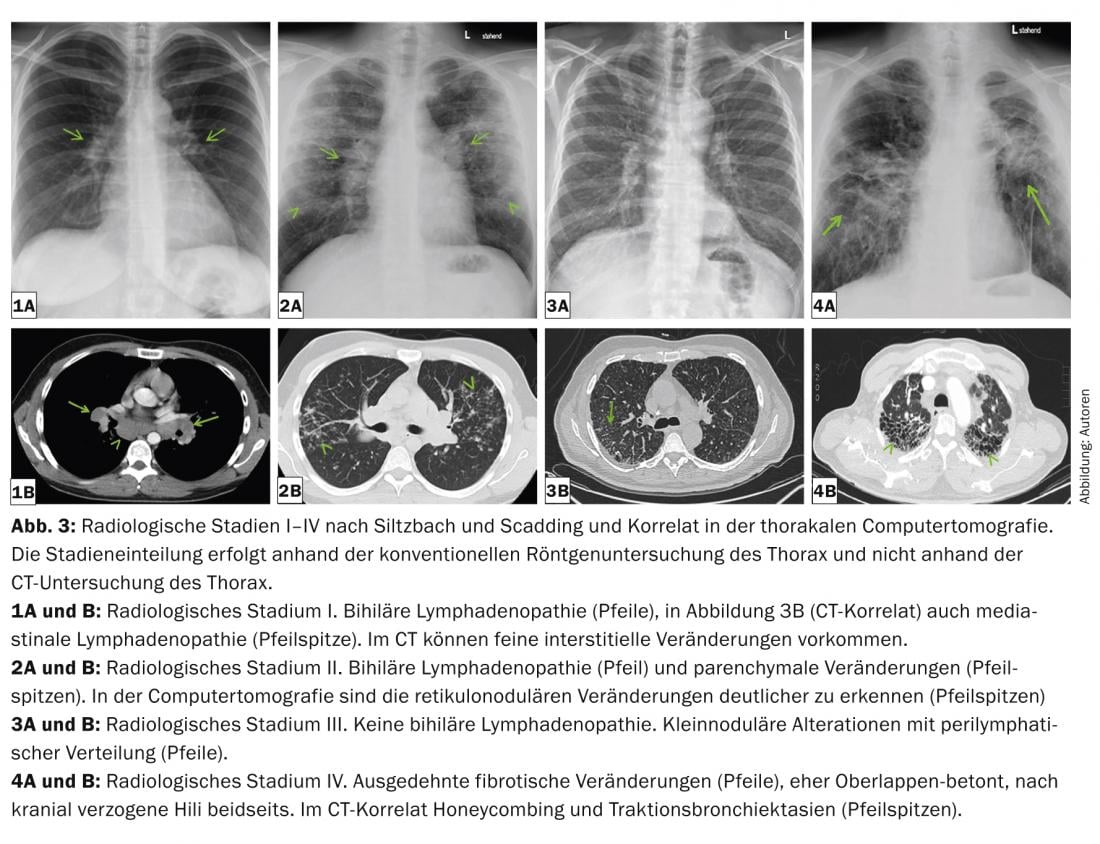
I quadri radiologici polmonari tipici sono una linfadenopatia mediastinica bifilare, ma anche simmetrica, micronoduli (diametro <3 mm) con distribuzione tipica (campi superiori e medi, lungo i fasci broncovascolari, subpleurici e lungo i setti interlobulari), macronoduli bilaterali che raramente possono fondersi (come espressione di necrosi ischemica del nucleo del granuloma), opacità a vetro smerigliato, proliferazione del disegno reticolare, fibrosi con alveolatura, nonché bronchiectasie da trazione con enfasi sui campi superiori. (Fig. 3 e 4). La tomografia computerizzata ad alta risoluzione (HRCT) è più sensibile per valutare i cambiamenti discreti nel parenchima polmonare.
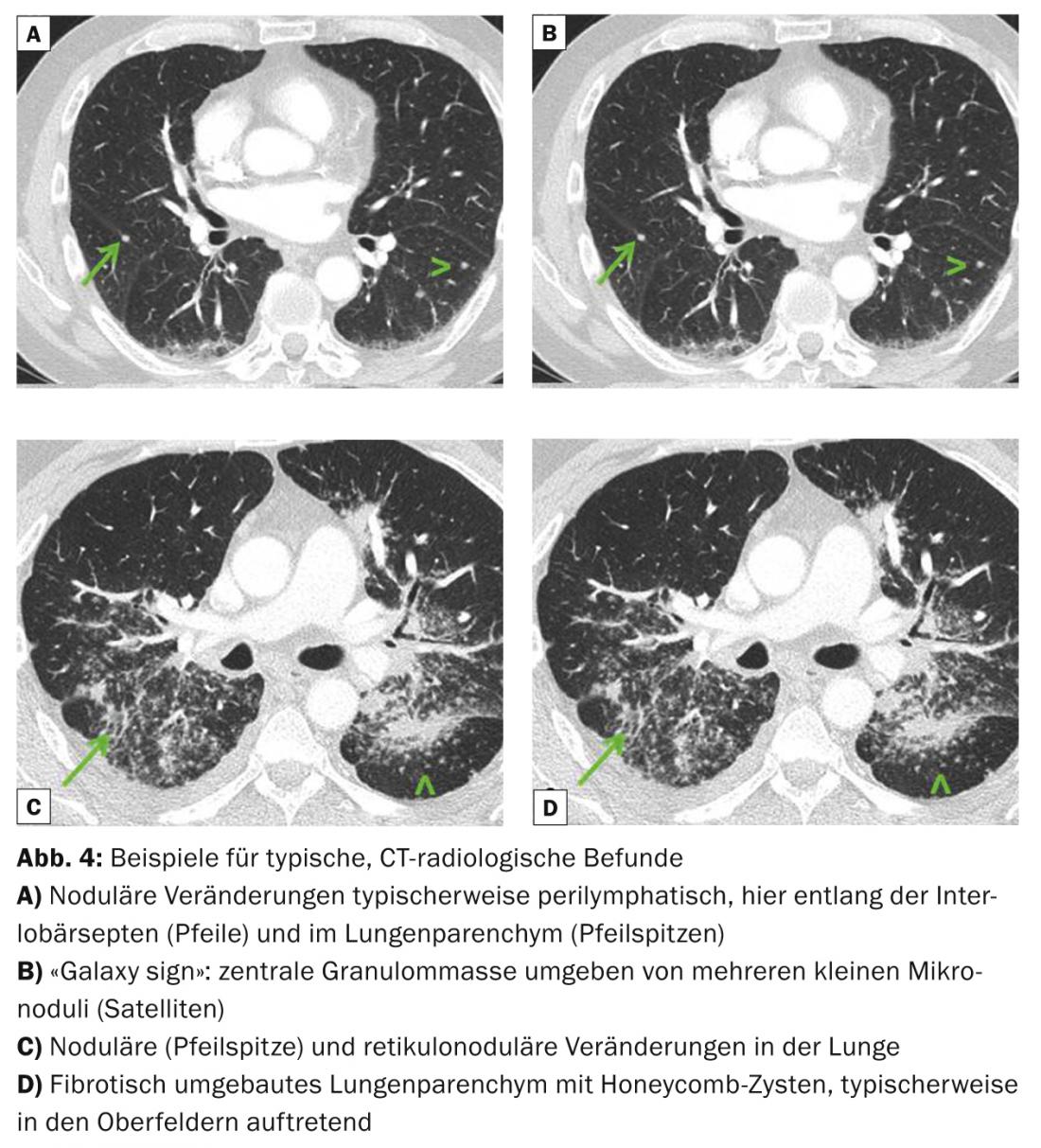
Manifestazioni neurologiche, cardiache o oftalmologiche
Nella sarcoidosi cardiaca, spesso sono presenti disturbi della conduzione nel senso di un blocco AV o disturbi della conduzione intraventricolare nell’ECG. I pazienti possono essere asintomatici, avvertire palpitazioni o avere sincope o dispnea. soffrono di aritmie fino alla morte cardiaca improvvisa. Se il miocardio è gravemente coinvolto, può verificarsi una cardiomiopatia con il quadro clinico dell’insufficienza cardiaca. Può anche verificarsi una pericardite.
Il coinvolgimento oftalmologico si manifesta spesso come uveite, neurite del nervo ottico e gonfiore delle ghiandole lacrimali.
In caso di coinvolgimento neurologico, sono più comuni la neuropatia cranica (paresi facciale) o periferica, l’irritazione meningea con evidenza di linfociti nel liquido cerebrospinale o l’infiltrazione dell’ipofisi o della ghiandola pituitaria. della regione dell’ipotalamo con le relative complicazioni endocrinologiche.
La comparsa di ipercalcemia può essere minacciosa, come conseguenza dell’aumento dell’idrossilazione della vitamina D3 nelle cellule epitelioidi dei granulomi.
Manifestazione cutanea
Spesso vengono descritte diverse manifestazioni cutanee. Tipici sono il lupus pernio resp. Eritema nodoso, ma anche alterazioni maculo-papulari e nodulari (Fig. 5) – frequentemente anche nell’area dei tatuaggi e delle cicatrici. A seconda della localizzazione (viso), le alterazioni cutanee possono portare a una significativa compromissione soggettiva dovuta alla deturpazione.
Evidenze istologiche di granulomi sarcoidi
Tranne che nella sindrome di Löfgren, l’evidenza istologica dei tipici granulomi è raccomandata per la diagnosi; questi sono non necrotizzanti, piccoli, nettamente circoscritti con una certa enfasi perivascolare e tendenza all’aggregazione, e possibilmente fibrosi centripeta fine-lamellare. (Fig. 2). La scelta del sito bioptico deve consentire la procedura meno invasiva possibile (ad esempio, biopsia della pelle, biopsia della ghiandola lacrimale, escissione dei linfonodi periferici).
Solo il 2% circa di tutti i pazienti con sarcoidosi extrapolmonare non presenta un coinvolgimento polmonare [16]. Per questo motivo, si ricorre a tecniche broncoscopiche per cercare di identificare le caratteristiche istologiche o di per prelevare campioni citologici. Nelle lesioni endobronchiali (mucosa alterata simile a un ciottolo in un massimo del 50% dei pazienti [20]), si può ottenere una biopsia mucosa mediante una biopsia con pinza; si può prevedere un risultato positivo in oltre il 60% dei pazienti [21]. Le biopsie polmonari transbronchiali possono essere utilizzate per ottenere campioni diagnosticamente utili nel 60-97% dei pazienti (a seconda del numero di biopsie prelevate e dell’estensione delle alterazioni parenchimali polmonari radiologiche) [22–24], e l’agoaspirato transbronchiale (TBNA) ecograficamente guidato dei linfonodi mediastinici e/o ilari in circa l’80% dei pazienti [25]. La combinazione di queste tecniche migliora la resa diagnostica, per cui la mediastinoscopia, che un tempo era spesso necessaria, oggi viene utilizzata solo molto raramente.
La broncoscopia di solito comporta un lavaggio broncoalveolare. La sarcoidosi è probabile – ma non provata – se c’è un’evidenza di alveolite linfocitaria (>15% di linfociti), un aumento del quoziente CD4/CD8 >3,5 ed è esclusa un’infezione (compresi i micobatteri). La sensibilità del quoziente CD4/CD8 è del 42-59% e la specificità del 76-96% per l’aumento del quoziente >3,5 [26,27].
Utilizzando la tecnologia PET/CT, i focolai infiammatori possono essere rappresentati come regioni con una maggiore captazione di FDG in casi selezionati. Se il sito della biopsia non può essere definito chiaramente a causa dei risultati clinici, si può utilizzare la tecnologia PET/CT per cercare di identificare un focus infiammatorio.
Diagnosi differenziali da escludere
La diagnosi di sarcoidosi con un quadro clinico tipico e l’evidenza dei reperti istopatologici appropriati può essere fatta quando sono state escluse altre malattie granulomatose. Le diagnosi differenziali includono malattie infettive come la tubercolosi, infezioni fungine (istoplasmosi, coccidioidomicosi), brucellosi o tularemia. Queste malattie possono essere escluse mediante un work-up del lavaggio broncoalveolare, se c’è un sospetto clinico. Le diagnosi differenziali includono anche malattie maligne, soprattutto linfomi e carcinomi (esclusione in base ai risultati istopatologici). La berilliosi cronica può causare un quadro polmonare molto simile alla sarcoidosi. Per differenziare la berilliosi, è importante fare un’anamnesi professionale precisa. In caso di sospetto, la diagnosi viene effettuata mediante la stimolazione in vitro delle cellule mononucleari dal sangue o dal liquido del lavaggio broncoalveolare. Inoltre, bisogna escludere l’alveolite allergica esogena (anamnesi, quoziente CD4/CD8 abbassato), la polmonite indotta da farmaci (anamnesi) e i granulomi nel contesto di una reazione da corpo estraneo (istologia). Poiché i granulomi della sarcoidosi possono anche presentarsi a livello perivascolare, la differenziazione da una vasculite nel materiale bioptico può essere difficile.
Piccoli granulomi ben definiti nei linfonodi drenanti, nello stroma circostante, ma anche nel fegato o nella milza di pazienti con malattie maligne sono definiti “reazione simil-sarcoidea”; tali granulomi si verificano in circa il 4% dei pazienti con carcinomi (incluso il carcinoma mammario e i carcinomi renali e gastrointestinali) e un po’ più frequentemente nei pazienti con tumori maligni Hodgkin (14%) e non Hodgkin (7%). [28].
Un’altra importante diagnosi differenziale quando viene rilevata una malattia granulomatosa è l’immunodeficienza comune variabile (CVID). È caratterizzata da bassi livelli di immunoglobuline nel siero, infezioni batteriche ricorrenti e una risposta anticorpale ridotta. Alcuni pazienti sviluppano un’infiammazione granulomatosa con granulomi non necrotizzanti nei polmoni, nella milza, nel fegato e nei linfonodi, tra gli altri [29].
La sarcoidosi viene trattata, tra l’altro, con inibitori del TNF-α. Paradossalmente, l’infiammazione granulomatosa è stata descritta durante la terapia con gli inibitori del TNF-α, soprattutto etanercept nell’artrite reumatoide, ma anche infliximab [30]. I granulomi non calcificanti possono verificarsi anche in relazione alla terapia con interferone-γ (ad esempio, nell’epatite cronica C) [31].
Valutazione del lavoro e dei progressi
Una volta fatta la diagnosi di sarcoidosi, si raccomanda di eseguire un work-up per verificare l’estensione della malattia. In particolare, devono essere esaminate le manifestazioni d’organo che potrebbero portare a una morbilità significativa (Tab. 3).
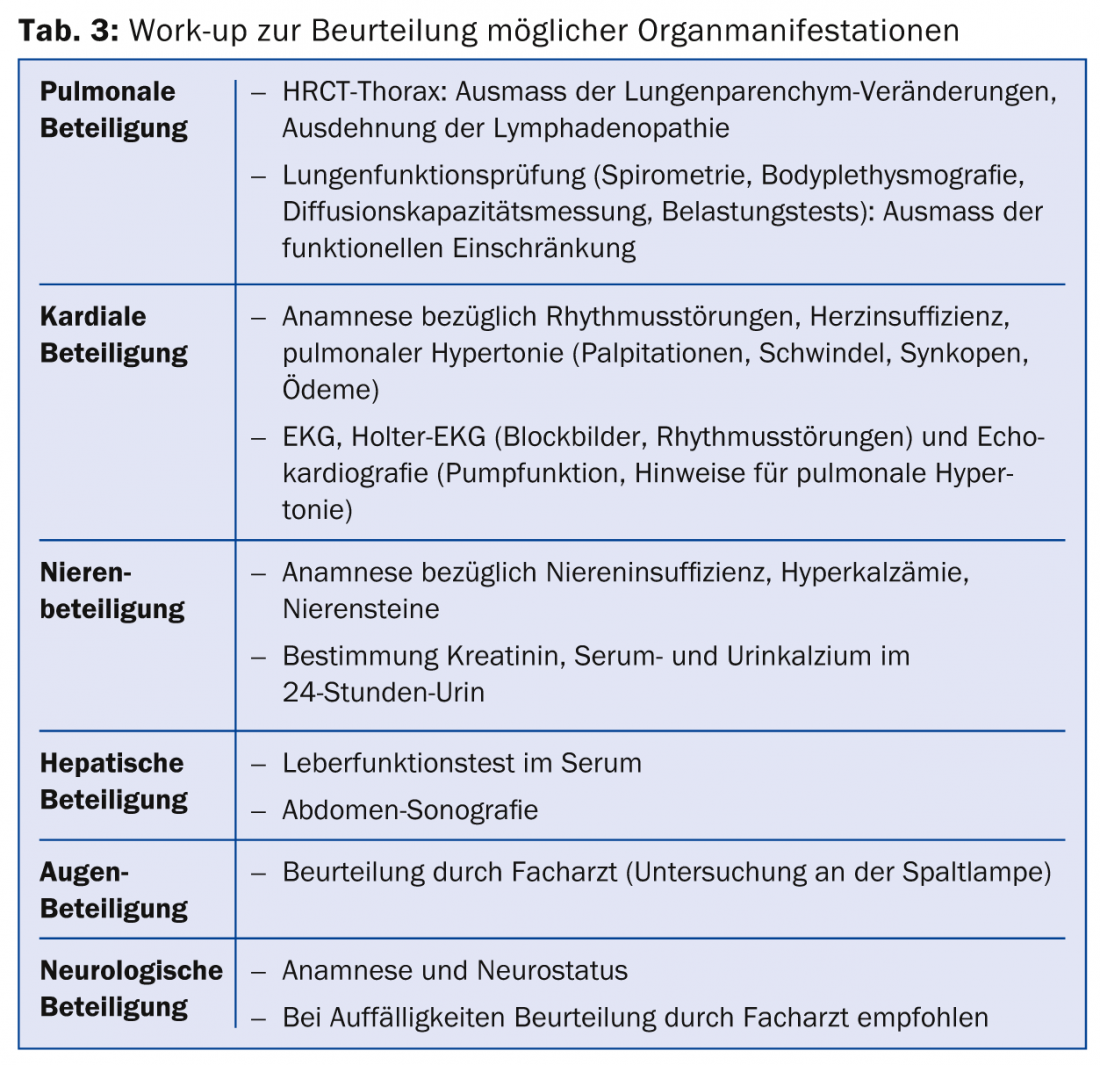
Inoltre, occorre definire quali parametri possono essere utilizzati per la valutazione del decorso (ad esempio, anche sotto terapia). L’enzima di conversione dell’angiotensina (ACE) viene determinato per valutare il possibile coinvolgimento midollare. L’ACE è prodotto, tra l’altro, nelle cellule epitelioidi dei granulomi nella sarcoidosi [32]. Tuttavia, a causa della bassa sensibilità, l’ACE non è adatto come test diagnostico. Se elevato alla diagnosi, l’ACE è un possibile parametro di follow-up. Un altro possibile fattore di progressione è il recettore solubile dell’interleuchina-2: le cellule presentanti l’antigene producono interleuchina 2 (IL-2) in relazione alla formazione del granuloma. Questo porta all’attivazione delle cellule T. Questo rilascia una forma solubile del recettore dell’interleuchina-2 (recettore sIL-2) nel flusso sanguigno. Poiché l’aumento del recettore sIL-2 riflette l’attivazione non specifica dei linfociti T, è possibile determinare l’attività della malattia e quindi valutare il decorso.
Prognosi e indicazione alla terapia
Il decorso della malattia non può essere previsto. Tuttavia, la prognosi è favorevole in circa due terzi dei pazienti: la remissione avviene entro un decennio e in circa il 50% dei pazienti entro tre anni. In circa un terzo dei pazienti, la malattia progredisce in modo cronico, con una rilevante compromissione funzionale degli organi colpiti. Meno del 5% di tutti i pazienti muore a causa della sarcoidosi. La mortalità è dovuta principalmente a fibrosi polmonare con insufficienza respiratoria, coinvolgimento cardiaco o neurologico o ipertensione polmonare [33].
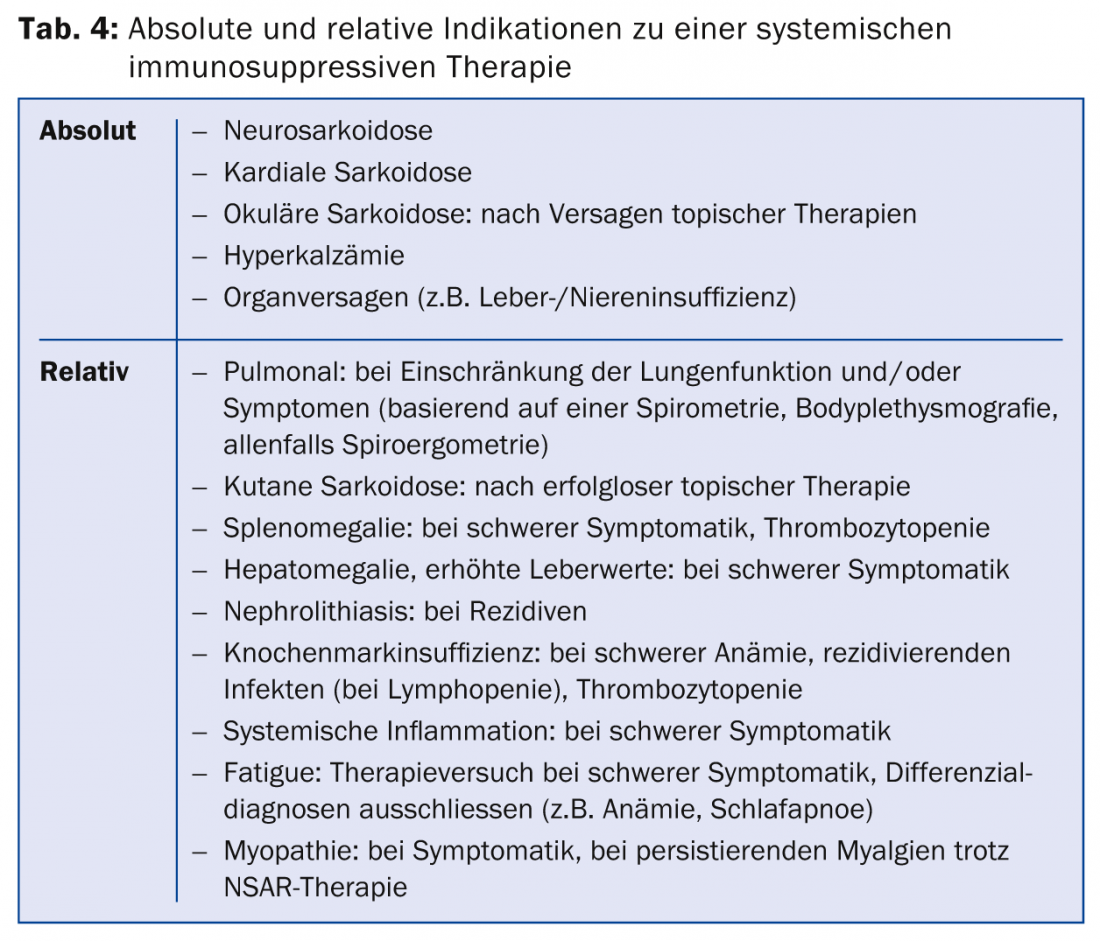
L’indicazione alla terapia deve essere fatta con molta attenzione, sapendo che il decorso della malattia è per lo più spontaneamente favorevole, i potenziali effetti collaterali della terapia e l’aumento del tasso di recidiva dopo la terapia con immunosoppressori (l’antigene postulato persiste nell’organo colpito, per cui la formazione del granuloma può ripresentarsi dopo l’interruzione della terapia). Un’indicazione assoluta per la terapia esiste nei casi di neurosarcoidosi, sarcoidosi cardiaca o oculare con coinvolgimento del segmento medio o posteriore dell’occhio, nonché nei casi di grave compromissione funzionale degli organi colpiti, tipicamente insufficienza epatica o renale, ma anche grave disfunzione polmonare. In caso di limitazione lieve e moderata, è possibile un’attenta osservazione clinica del decorso: se i sintomi sono presenti e la limitazione funzionale è progressiva, e quindi ci sono indicazioni di attività della malattia, di solito si inizia la terapia.
Terapia con immunosoppressori/immunomodulatori
Se esiste un’indicazione per la terapia (tab. 4), vengono utilizzati immunosoppressori o farmaci immunosoppressivi. vengono utilizzati immunomodulatori (tab. 5).
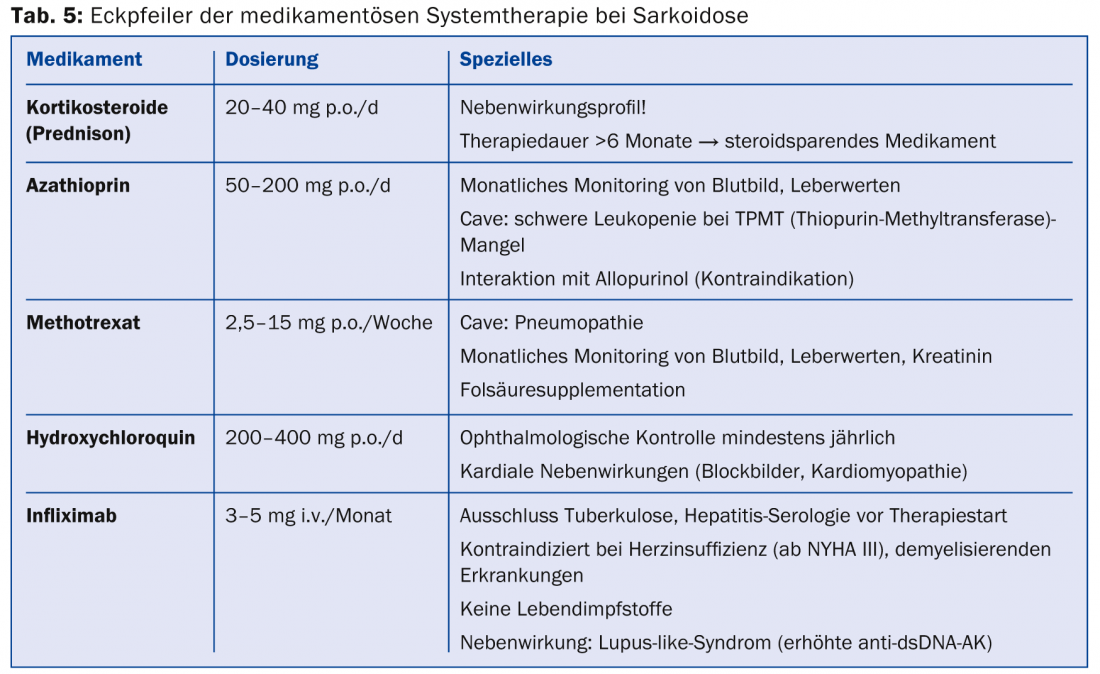
Grazie alla loro buona e rapida efficacia, i corticosteroidi sono la prima scelta. Si raccomandano dosi di 20-40 mg in un dosaggio graduale nell’arco di circa un semestre, ma non esistono studi randomizzati e controllati. L’uso di sostanze che risparmiano gli steroidi (azatioprina, metotrexato, leflunomide, micofenolato) per gli effetti collaterali associati agli steroidi deve essere valutato precocemente. Tuttavia, il metotrexato deve essere prescritto con cautela nella sarcoidosi polmonare, a causa della possibilità di polmonite da metotrexato. Poiché il TNF-α è coinvolto nella formazione dei granulomi, gli antagonisti del TNF-α (soprattutto l’infliximab) sono una buona terapia alternativa di seconda linea [34,35]. Si è potuto dimostrare un beneficio soprattutto per la terapia della sarcoidosi cutanea (lupus pernio) e delle manifestazioni polmonari e neurologiche. Il farmaco antimalarico idrossiclorochina ottiene buoni risultati nella sarcoidosi cutanea e nell’ipercalcemia. Nella sindrome di Löfgren, viene stabilita una terapia sintomatica con farmaci antinfiammatori non steroidei.
Letteratura:
- Hunninghake GW, et al: Dichiarazione ATS/ERS/WASOG sulla sarcoidosi. American Thoracic Society/European Respiratory Society/World Association of Sarcoidosis and other Granulomatous Disorders. Sarcoidosi Vasc Diffuse Lung Dis 1999; 16(2): 149-173.
- Fernandez FE: [Epidemiology of sarcoidosis]. Arch Bronconeumol 2007; 43(2): 92-100.
- Rybicki BA, Iannuzzi MC: Epidemiologia della sarcoidosi: progressi recenti e prospettive future. Semin Respir Crit Care Med 2007; 28(1): 22-35.
- Pietinalho A, et al: La frequenza della sarcoidosi in Finlandia e Hokkaido, Giappone. Uno studio epidemiologico comparativo. Sarcoidosi 1995; 12(1): 61-67.
- Rossman MD, Kreider ME: Lezione appresa da ACCESS (A Case Controlled Etiologic Study of Sarcoidosis). Proc Am Thorac Soc 2007; 4(5): 453-456.
- Deubelbeiss U, et al.: La prevalenza della sarcoidosi in Svizzera è associata a fattori ambientali. Eur Respir J 2010; 35(5): 1088-1097.
- Hosoda Y, et al.: Epidemiologia globale della sarcoidosi. Quale storia ci raccontano la prevalenza e l’incidenza? Clin Chest Med 1997; 18(4): 681-694.
- Izbicki G, et al: Malattia polmonare granulomatosa “sarcoidea” del World Trade Center nei soccorritori dei Vigili del Fuoco di New York. Chest 2007; 131(5): 1414-1423.
- McGrath DS, et al: Epidemiologia della sarcoidosi familiare nel Regno Unito. Thorax 2000; 55(9): 751-754.
- Rossman MD, et al: HLA-DRB1*1101: un fattore di rischio significativo per la sarcoidosi nei neri e nei bianchi. Am J Hum Genet 2003; 73(4): 720-735.
- Berlin M, et al: HLA-DR predice la prognosi nei pazienti scandinavi con sarcoidosi polmonare. Am J Respir Crit Care Med 1997; 156(5): 1601-1605.
- Baughman RP, et al: Rilascio del fattore di necrosi tumorale da parte dei macrofagi alveolari di pazienti con sarcoidosi. J Lab Clin Med 1990; 115(1): 36-42.
- Iida K, et al: Analisi delle sottopopolazioni di cellule T e delle beta-chemochine nei pazienti con sarcoidosi polmonare. Thorax 1997; 52(5): 431-437.
- Pinkston P, Bitterman PB, Crystal RG: Rilascio spontaneo di interleuchina-2 da parte dei linfociti T polmonari nella sarcoidosi polmonare attiva. N Engl J Med 1983; 308(14): 793-800.
- Judson MA: La diagnosi di sarcoidosi. Clin Chest Med 2008; 29(3): 415-427, viii.
- Baughman RP, et al: Caratteristiche cliniche dei pazienti in uno studio caso-controllo sulla sarcoidosi. Am J Respir Crit Care Med 2001; 164(10 Pt 1): 1885-1889.
- Thomas KW, Hunninghake GW: Sarcoidosi. JAMA 2003; 289(24): 3300-3303.
- Siltzbach LE: Sarcoidosi: caratteristiche cliniche e gestione. Med Clin North Am 1967; 51(2): 483-502.
- Scadding JG: Prognosi della sarcoidosi intratoracica in Inghilterra. Una revisione di 136 casi dopo cinque anni di osservazione. Br Med J 1961; 2(5261): 1165-1172.
- Chapman JT, Mehta AC: Broncoscopia nella sarcoidosi: interventi diagnostici e terapeutici. Curr Opin Pulm Med 2003; 9(5): 402-407.
- Shorr AF, Torrington KG, Hnatiuk OW. Biopsia endobronchiale per la sarcoidosi: uno studio prospettico. Chest 2001; 120(1): 109-114.
- Koerner SK, et al: Biopsia polmonare transbronchinale per la diagnosi di sarcoidosi. N Engl J Med 1975; 293(6): 268-270.
- Gilman MJ, Wang KP: Biopsia polmonare transbronchiale nella sarcoidosi. Un approccio per determinare il numero ottimale di biopsie. Am Rev Respir Dis 1980; 122(5): 721-724.
- Mitchell DM, et al: Biopsia polmonare transbronchiale attraverso il broncoscopio a fibre ottiche nella diagnosi di sarcoidosi. Br Med J 1980; 280(6215): 679-681.
- Agarwal R, et al: Efficacia e sicurezza dell’EBUS-TBNA con sonda convessa nella sarcoidosi: una revisione sistematica e una meta-analisi. Respir Med 2012; 106(6): 883-892.
- Costabel U: Rapporti CD4/CD8 nel liquido di lavaggio broncoalveolare: di valore per la diagnosi di sarcoidosi? Eur Respir J 1997; 10(12): 2699-2700.
- Zaiss AW, et al: [Rapporto T4/T8 nel liquido di lavaggio broncoalveolare: sensibilità e specificità per la diagnosi di sarcoidosi]. Prax Klin Pneumol 1988; 42 Suppl 1: 233-234.
- Chowdhury FU, et al: Reazione simil-sarcoide a malignità sulla PET/CT integrata (18)F-FDG del corpo intero: prevalenza e modello di malattia. Clin Radiol 2009; 64(7): 675-681.
- Ardeniz O, Cunningham-Rundles C: Malattia granulomatosa nell’immunodeficienza comune variabile. Immunologia clinica 2009; 133(2): 198-207.
- Khasnis AA, Calabrese LH: Inibitori del fattore di necrosi tumorale e malattia polmonare: un paradosso di efficacia e rischio. Semin Arthritis Rheum 2010; 40(2): 147-163.
- Goldberg HJ, et al: Sarcoidosi dopo il trattamento con interferone-alfa: una serie di casi e una revisione della letteratura. Respir Med 2006; 100(11): 2063-2068.
- Studdy PR, Bird R: L’enzima di conversione dell’angiotensina nel siero nella sarcoidosi – il suo valore nella pratica clinica attuale. Ann Clin Biochem 1989; 26(Pt 1): 13-18.
- Siltzbach LE, et al: Decorso e prognosi della sarcoidosi nel mondo. Am J Med 1974; 57(6): 847-852.
- Judson MA, et al: Efficacia di infliximab nella sarcoidosi extrapolmonare: risultati di uno studio randomizzato. Eur Respir J 2008; 31(6): 1189-1196.
- Baughman RP, et al: Terapia con infliximab nei pazienti con sarcoidosi cronica e coinvolgimento polmonare. Am J Respir Crit Care Med 2006; 174(7): 795-802.
PRATICA GP 2015; 10(3): 10-18











