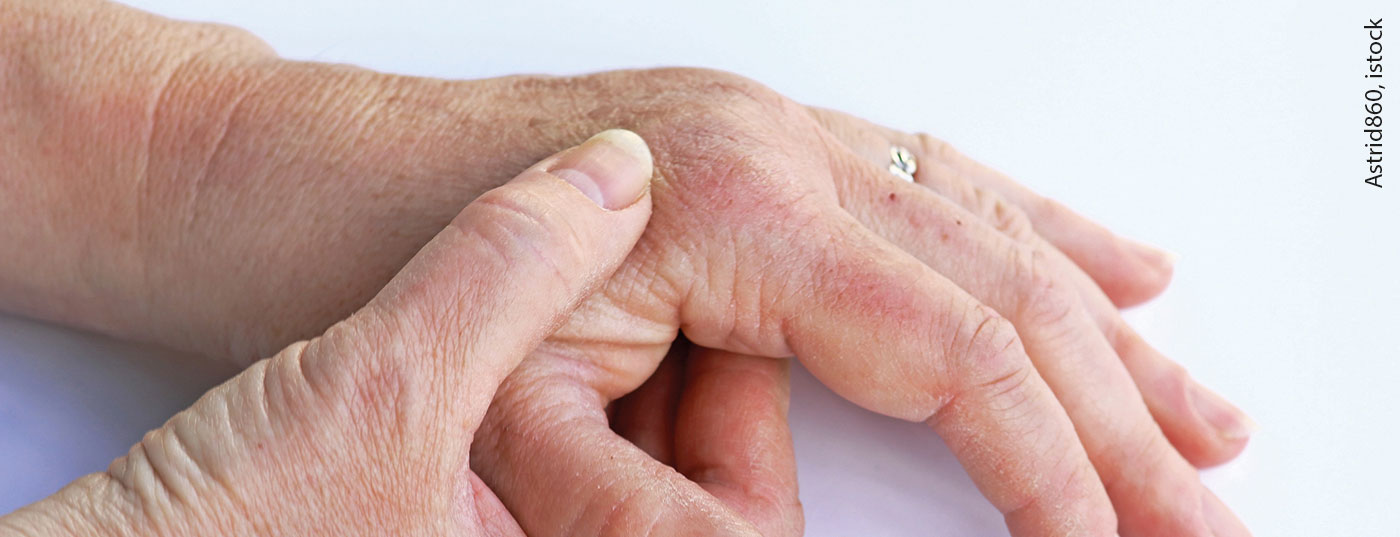
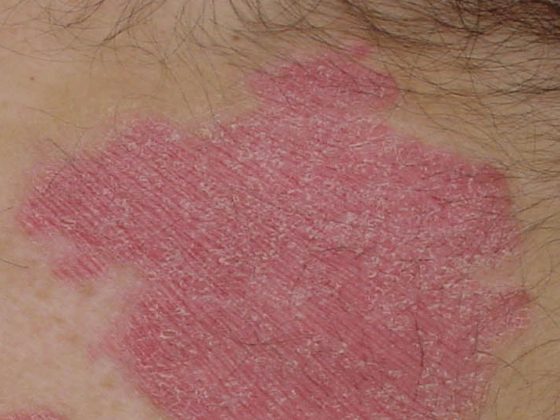
L’anticorpo monoclonale anti-IL-17A ixekizumab è già stato approvato per il trattamento della psoriasi a placche da moderata a grave e dell’artrite psoriasica dal 2016. Nel 2020, è stata aggiunta la spondiloartrite assiale (axSpA) come ulteriore indicazione per la quale ixekizumab rappresenta un’opzione terapeutica. Sulla base del programma di studi COAST, è stata dimostrata l’efficacia e la tollerabilità di ixekizumab nell’axSpA non radiografica e radiografica in pazienti con o senza pre-trattamento con inibitori del TNF-α.
L’anticorpo monoclonale anti-IL-17A ixekizumab è già stato approvato per il trattamento della psoriasi a placche da moderata a grave e dell’artrite psoriasica dal 2016. Nel 2020, è stata aggiunta la spondiloartrite assiale (axSpA) come ulteriore indicazione per la quale ixekizumab rappresenta un’opzione terapeutica. Sulla base del programma di sperimentazione COAST, sono state dimostrate l’efficacia e la tollerabilità di ixekizumab nella axSpA non radiografica e radiografica in pazienti con o senza pre-trattamento con inibitori del TNF-α [1–4].
Artrite psoriasica
Le strategie terapeutiche approvate per l’artrite psoriasica (PsA) comprendono l’uso di FANS, csDMARDs, biologici (inibitori del TNF, inibitori dell’IL-12/23 e dell’IL-17, modulatori delle cellule T) e tsDMARDs (inibitori della PDE4, inibitori della JAK). Quali agenti utilizzare in quali pazienti è determinato individualmente in base al modello di manifestazione e ad altri fattori (ad esempio, comorbidità, fattori sociali, modalità di applicazione e malattie concomitanti).
Con l’American College of Rheumatology (ACR), la European League Against Rheumatism (EULAR) e il Group for Research and Assessment of Psoriasis and Psoriatic Arthritis (GRAPPA), sono disponibili raccomandazioni terapeutiche da parte di tre istituzioni internazionali che forniscono un orientamento per la prescrizione [5]. Come strategia di prima linea nel trattamento della PsA, si raccomanda ancora l’uso di farmaci antinfiammatori non steroidei (FANS), che possono essere utilizzati alla comparsa dei sintomi, ma anche prima che la diagnosi sia confermata. Nella cura quotidiana, occorre prestare attenzione ai rischi gastrointestinali, cardiovascolari e renali specifici della sostanza. I glucocorticoidi sistemici (GC), invece, svolgono solo un ruolo minore nella PsA. Tuttavia, l’iniezione intra-articolare può essere presa in considerazione per il trattamento di modelli di coinvolgimento mono o oligoarticolare o come aggiunta alla terapia esistente con terapie antireumatiche modificanti la malattia (DMARD). I DMARD vengono utilizzati dopo che è stata fatta una diagnosi confermata e se i sintomi persistono.
Miglioramento significativo già dopo 6 settimane
Ixekizumab è indicato nel trattamento della PsA negli adulti che hanno avuto una risposta inadeguata o sono intolleranti a uno o più farmaci antireumatici modificanti la malattia (DMARD), da soli o in combinazione con il metotrexato. Questo può portare a un miglioramento significativo delle florescenze cutanee, con una quasi normalizzazione della struttura della pelle dopo solo 6 settimane di terapia. Inoltre, sono stati descritti una rapida riduzione del prurito e un miglioramento della qualità della vita per il principio attivo.
Attualmente, è stato riportato un miglioramento del dolore per ixekizumab nei pazienti con e senza infiammazione misurabile nell’artrite psoriasica [6]. Avendo dimostrato in precedenza l’efficacia di ixekizumab (IXE) e adalimumab (ADA) nei pazienti con PsA con riferimento ai tassi di risposta all’ACR50 e al PASI (Psoriasis Area and Severity Index)-100 [7,8]Lo studio ha analizzato l’efficacia della monoterapia con IXE o ADA sulla riduzione del dolore al di là dell’infiammazione misurabile nei pazienti con PsA attiva e proteina C-reattiva (CRP, <5 mg/l) bassa al basale.
Lo studio SPIRIT-H2H ha incluso 95 pazienti in monoterapia. Le caratteristiche basali erano simili tra i due bracci di trattamento. Nei pazienti con bassa infiammazione persistente (misurata dalla CRP), non c’è stata alcuna differenza nel miglioramento del dolore articolare tra i pazienti trattati con IXE e ADA. Tuttavia, nei pazienti con infiammazione fluttuante, i pazienti trattati con IXE hanno mostrato un miglioramento medio numericamente maggiore del dolore articolare (VAS) rispetto ai pazienti trattati con ADA alla settimana 16 (IXE: -31,64, ADA: -25,33). Questo è continuato fino alla settimana 52 (IXE: -47,69, ADA: -20,67). La significatività a favore dell’IXE è stata misurata alle settimane 32 (p=0,0045) e 52 (p=0,0288). Allo stesso modo, i pazienti con un miglioramento sostenuto del gonfiore articolare e con un miglioramento fluttuante (valutato da SJC) hanno avuto miglioramenti medi numericamente maggiori nel dolore articolare nel braccio IXE rispetto ai pazienti trattati con ADA, rispettivamente dalla quarta e dalla sedicesima settimana, che sono stati mantenuti fino alla 52esima settimana.
Questa analisi suggerisce modelli differenziali di miglioramento del dolore nei pazienti con CRP bassa al basale trattati con IXE o con monoterapia ADA, con un risultato di riduzione del dolore più favorevole per i pazienti trattati con IXE. Questo è evidente anche quando l’infiammazione, misurata dal miglioramento della CRP o dell’SJC, fluttua. Lo studio supporta quindi l’ipotesi che l’IXE migliori il dolore articolare nei pazienti con PsA con e senza infiammazione misurabile.
Spondiloartrite assiale
La spondiloartrite assiale (axSpA) è una malattia infiammatoria cronica composta da axSpA non radiologica e axSpA radiologica (r-axSpA). Quest’ultima, nota anche come spondilite anchilosante (AS), è caratterizzata da un dolore infiammatorio alla schiena e dall’evidenza radiologica di un danno all’articolazione sacroiliaca [9]. Queste manifestazioni, così come i segni e i sintomi muscolo-scheletrici periferici ed extra-articolari, possono contribuire alla limitazione della mobilità, alla disabilità progressiva e alla riduzione della qualità di vita (QoL). I farmaci biologici antireumatici modificanti la malattia (bDMARDs), compresi gli inibitori del fattore di necrosi tumorale (TNFi) e un antagonista dell’interleuchina (IL)-17A, sono raccomandati per il trattamento dei pazienti con axSpA che non rispondono o non possono tollerare i farmaci antinfiammatori non steroidei (FANS). Tuttavia, fino al 40% dei pazienti non raggiunge un controllo soddisfacente della malattia con gli inibitori del TNF [10] e il trattamento con TNFi può essere controindicato in alcuni pazienti.
La via di segnalazione dell’IL-17 svolge un ruolo chiave nella patogenesi dell’axSpA. Due studi clinici randomizzati e controllati di fase 3 (COAST-V e COAST-W) hanno valutato l’efficacia e la sicurezza di ixekizumab come anticorpo monoclonale ad alta affinità che ha come bersaglio selettivo l’IL-17A per un periodo fino a 52 settimane in pazienti con spondiloartrite assiale radiografica attiva (r-axSpA). I partecipanti a COAST-V erano bDMARD-naïve, quelli a COAST-W con esperienza di inibitori del TNF.
In COAST-V, 341 pazienti con r-axSpA attiva sono stati randomizzati 1:1:1 a 80 mg di ixekizumab (IXE) ogni 2 o 4 settimane, placebo o 40 mg di adalimumab (ADA) a cadenza quindicinale. In COAST-W, 316 pazienti hanno ricevuto ixekizumab 1:1:1 ogni 2 o 4 settimane o placebo. Alla settimana 16, i pazienti che ricevevano ixekizumab hanno continuato il trattamento assegnato, mentre i pazienti che assumevano placebo o ADA sono stati passati 1:1 a IXE Q2W o IXE Q4W fino alla settimana 52.
Buona efficacia e sicurezza
Entrambe le terapie con ixekizumab hanno dimostrato di migliorare l’attività della malattia, la funzione fisica, i marcatori oggettivi dell’infiammazione, la qualità della vita, lo stato di salute e la funzione generale per un periodo fino a 52 settimane.
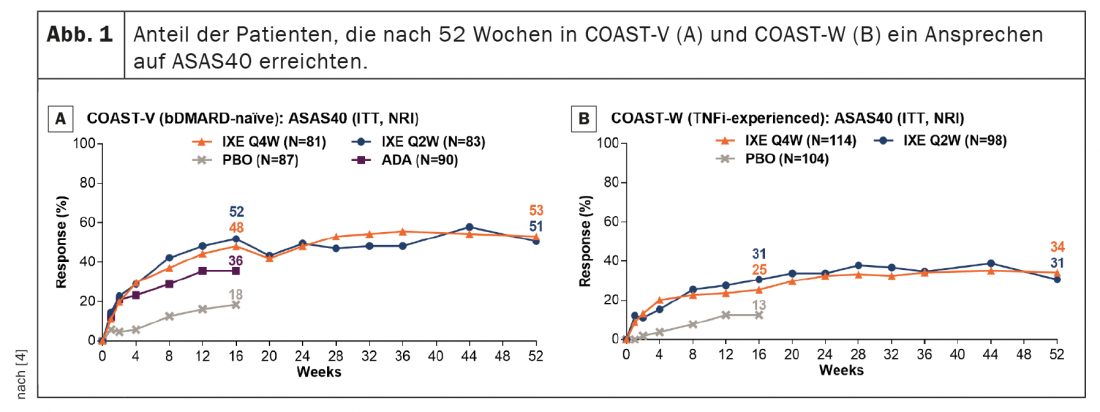
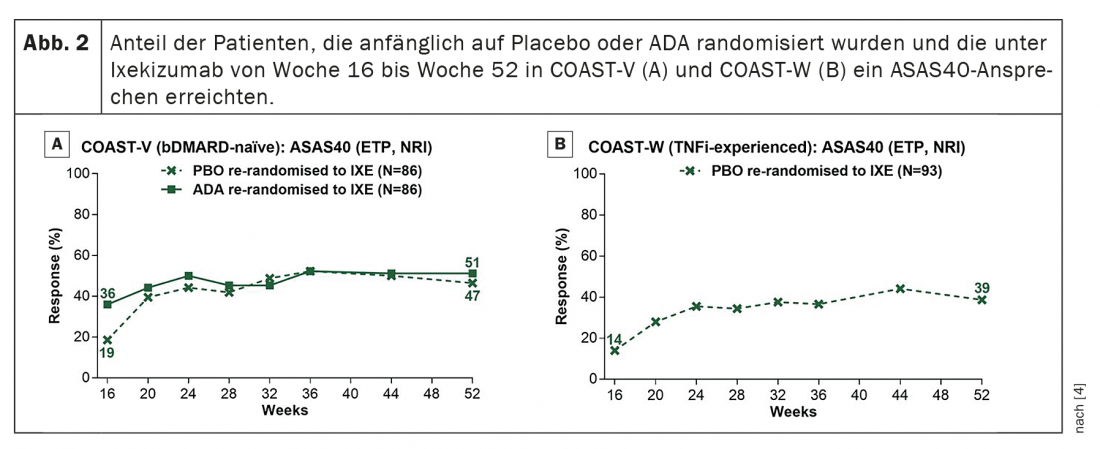
Nei pazienti trattati in modo continuativo con ixekizumab, i tassi di risposta ASAS40 sono persistiti dalla settimana 16 alla settimana 52 (Fig. 1) . I tassi di risposta ASAS40 alla settimana 52 erano del 53,1% (IXE Q4W) e del 50,6% (IXE Q2W) in COAST-V e del 34,2% (IXE Q4W) e del 30,6% (IXE Q2W) in COAST-W. I pazienti randomizzati al placebo e randomizzati nuovamente a ixekizumab alla settimana 16 hanno mostrato un rapido miglioramento dei tassi di risposta ASAS40 dopo il passaggio a ixekizumab. (Fig. 2); I tassi di risposta alla settimana 52 (46,5% in COAST-V, 38,7% in COAST-W) erano numericamente simili ai pazienti inizialmente randomizzati a ixekizumab. In COAST-V, i pazienti randomizzati ad ADA hanno mostrato ulteriori miglioramenti numerici nei tassi di risposta ASAS40 (36,0% alla settimana 16, 51,2% alla settimana 52) dopo il passaggio a ixekizumab (Figura 2A); i tassi di risposta alla settimana 52 erano numericamente simili ai pazienti inizialmente randomizzati a ixekizumab.
L’EAIR in pool per la psoriasi era 1,0. Un paziente ha avuto un grave evento avverso cerebrocardiovascolare (infarto miocardico acuto) e sono stati segnalati due tumori maligni (leucemia promielocitica acuta e cancro alla vescica). Sono state segnalate meno reazioni al sito di iniezione (ISR) con IXE Q4W (9,2%) rispetto a IXE Q2W (17,2%). Il numero di pazienti che hanno riferito ISR è diminuito nel tempo. In particolare, il 6,4%, il 3,8% e il 3,4% dei pazienti in trattamento con IXE Q4W e il 14,3%, l’8,6% e il 5,2% dei pazienti in trattamento con IXE Q2W hanno riportato ISR alle settimane 0-12, alle settimane 12-24 e alle settimane 24-36, rispettivamente. Solo pochi pazienti (IXE Q4W ≤1%; IXE Q2W circa il 3%) hanno riferito ISR oltre la settimana 36.
In generale, le risposte al trattamento sono state numericamente più basse nei pazienti con esperienza di TNFi rispetto a quelli naïve ai bDMARD, riflettendo una popolazione più difficile da trattare, con un precedente fallimento del trattamento e una malattia più duratura [4]. Le terapie biologiche attualmente approvate per l’axSpA comprendono diversi TNFi e un antagonista dell’IL-17A. Sebbene solo gli studi comparativi testa a testa possano valutare appieno l’efficacia e la sicurezza relative dei diversi trattamenti, i risultati ASAS40 qui riportati alla settimana 52 sono coerenti con quelli riportati per il TNFi nei pazienti che erano bDMARD-naïve e per il secukinumab nei sottogruppi di pazienti che erano bDMARD-naïve o che avevano precedentemente fallito il trattamento con TNFi.
Il tasso di interruzione a causa di eventi avversi (AEs) è stato <4% in entrambi gli studi, e gli eventi avversi gravi (SUEs) sono stati riportati da <6% dei pazienti. La maggior parte delle infezioni e delle ISR sono state lievi o moderate. Gli ISR erano più comuni in IXE Q2W che in IXE Q4W. Inoltre, le ISR sono state segnalate più frequentemente durante le prime 4 settimane di trattamento e sono diminuite di frequenza nel tempo. Durante i periodi di studio di 52 settimane di COAST-V e COAST-W (n=641), il tasso di incidenza aggiustato per l’esposizione per 100 anni-paziente (EAIR) di infezioni gravi è stato di 2,0 nei pazienti trattati con ixekizumab. Gli EAIR in pool dell’infezione da Candida e della neutropenia di grado 3/4 sono stati rispettivamente di 1,0 e 0,2. Gli EAIR corrispondenti per la malattia di Crohn, la colite ulcerosa e la malattia infiammatoria intestinale (IBD) (NOS) erano rispettivamente 0,8, 0,4 e 0,4 (EAIR totale IBD: 1,6). L’EAIR per l’uveite anteriore (AU) era di 3,9; 15 dei 20 pazienti (75%) avevano una storia di AU e 14 dei 20 pazienti (70%) provenivano da COAST-W. Sono stati segnalati meno eventi CED in IXE Q2W rispetto a IXE Q4W, e non c’è stata alcuna associazione apparente tra la durata dell’esposizione a ixekizumab e CED. Rapporti precedenti hanno dimostrato che l’EAIR per l’AU nei pazienti con spondilite anchilosante (AS) varia da 2,6 a 3,5 per i pazienti trattati con TNFi [11].
In sintesi, i dati COAST-V e COAST-W mostrano che ixekizumab ha ottenuto un miglioramento sostenuto e clinicamente significativo dei segni e dei sintomi della r-axSpA attiva fino a 52 settimane. I risultati sulla sicurezza erano coerenti con il profilo di sicurezza noto di ixekizumab. Questi risultati suggeriscono che ixekizumab può essere un’opzione di trattamento per l’axSpA nei pazienti che sono bDMARD-naïve o che hanno avuto in precedenza una risposta inadeguata o un’intolleranza agli inibitori del TNF.
Studio sull’effetto dopo la remissione
I risultati degli studi randomizzati sull’interruzione dell’inibitore del fattore di necrosi tumorale (TNF) nei pazienti con spondiloartrite assiale suggeriscono che l’interruzione del TNFi porta a una ricaduta nella maggior parte dei pazienti e il proseguimento del trattamento può essere importante per mantenere il controllo della malattia. Tuttavia, non sono ancora stati condotti studi incentrati sugli effetti della continuazione rispetto all’interruzione di un antagonista dell’interleuchina (IL)-17A nei pazienti con axSpA. COAST-Y è uno studio di follow-up di COAST-V e COAST-W. L’obiettivo di questo studio [12], pubblicato nel 2021, era quello di colmare questa lacuna e di esaminare la continuazione rispetto all’interruzione del trattamento con ixekizumab nei pazienti con spondiloartrite assiale che avevano raggiunto la remissione.
Nello studio di estensione di fase 3, in doppio cieco, controllato con placebo e randomizzato, i pazienti che avevano completato gli studi originali COAST-V, COAST-W o COAST-X, della durata di 52 settimane, sono entrati in una fase introduttiva di 24 settimane e hanno proseguito con 80 mg di IXE ogni 2 settimane (Q2W) o 4 settimane (Q4W). I pazienti che hanno raggiunto la remissione (cioè un punteggio di attività della malattia della spondilite anchilosante (ASDAS) <1,3 almeno una volta alla settimana 16 o alla settimana 20 e <2,1 in entrambe le visite) sono stati assegnati in modo casuale alla settimana 24 a continuare IXE Q4W, IXE Q2W o a interrompere l’assunzione di placebo in cieco. L’endpoint primario era la percentuale di pazienti senza ricadute (ASDAS ≥2,1 in due visite consecutive o ASDAS >3,5 in ogni visita) dopo il RWRP (periodo di ritiro-ritrattamento randomizzato) di 40 settimane, con il tempo alla ricaduta come importante endpoint secondario.
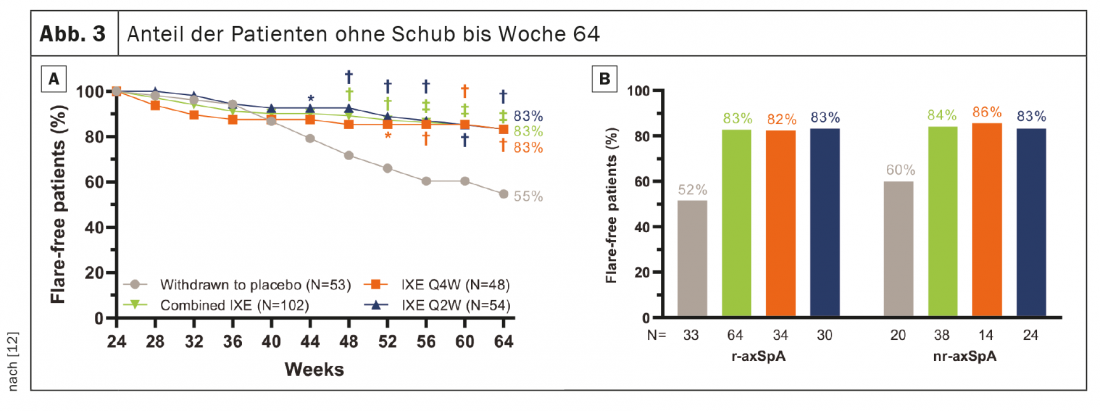
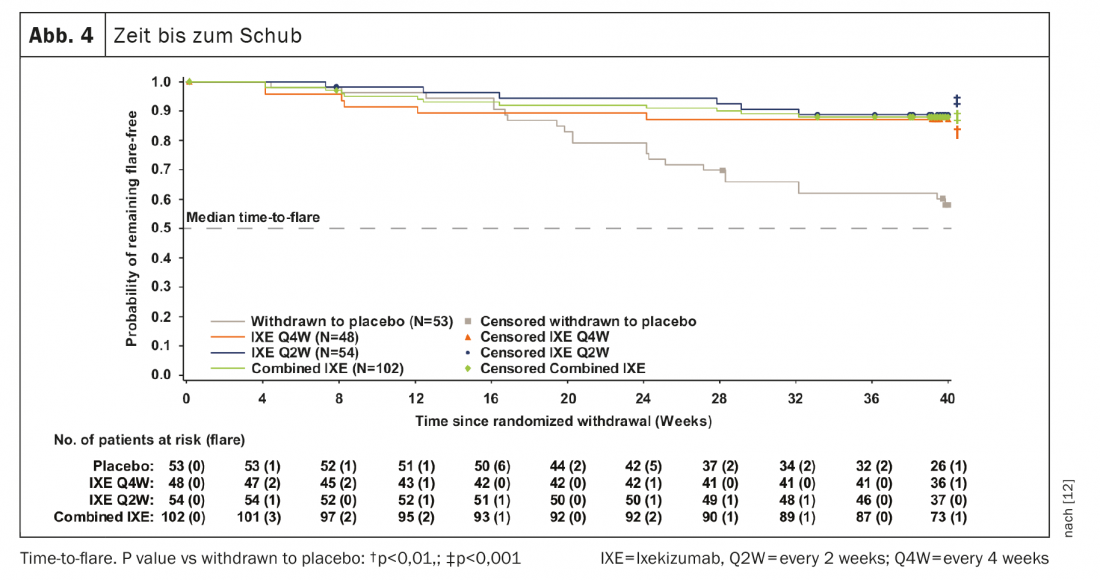
741 pazienti hanno completato la fase introduttiva di 24 settimane e 155 sono entrati nel RWRP. Gli obiettivi primari e tutti gli obiettivi secondari importanti sono stati raggiunti nella 64esima settimana. Quaranta settimane dopo il ritiro randomizzato, l’83,3% dei pazienti nei gruppi combinati è rimasto IXE (85/102, p<0,001), IXE Q4W (40/48, p=0,003) e IXE Q2W (45/54, p=0,001) senza ricadute rispetto al 54,7% del gruppo placebo (29/53). (Fig. 3A). La percentuale di pazienti senza ricadute era simile tra i sottogruppi di pazienti con r-axSpA e nr-axSpA. (Fig. 3B). La continuazione di IXE ha ritardato significativamente il tempo di ricaduta rispetto al placebo, con la maggior parte dei pazienti che sono rimasti liberi da ricadute fino a 20 settimane dopo l’interruzione di IXE. (Fig. 4). Il 54,7% dei pazienti che hanno interrotto il placebo sono rimasti liberi da ricadute durante la RWRP è stato un valore più alto rispetto a studi comparabili di interruzione di adalimumab (47%) e certolizumab pegol (20,2%). [13–16].
Predittori e sicurezza
Le analisi post-hoc hanno identificato diverse caratteristiche del paziente associate alla ricaduta, tra cui l’area ASDAS sotto la curva, suggerendo che i pazienti con una malattia meno ben controllata avevano maggiori probabilità di avere una ricaduta nel tempo rispetto a quelli il cui controllo della malattia era stabile. Inoltre, l’interruzione dell’IXE, la CRP più alta al basale e il BMI non normale (che era ≥25kg/m2 nella maggior parte dei casi) sono stati identificati come associati alla ricaduta. Un punteggio del dolore BASDAI più alto alla settimana 24 era anche associato a una ricaduta nei pazienti che hanno continuato il trattamento con IXE, ma non nei pazienti che hanno smesso con il placebo.
Il RWRP di COAST-Y comprendeva pazienti di tutto lo spettro dell’axSpA con e senza precedente fallimento del TNFi e con una durata dei sintomi compresa tra 1,9 e 44,7 anni (media 12,7 anni) [17]. Non ci sono stati problemi di sicurezza nuovi o inaspettati durante l’RWRP. Gli eventi avversi emergenti dal trattamento (TEAE) sono stati segnalati nel 42,6% (IXE Q4W), nel 44,4% (IXE Q2W) e nel 52,8% (svezzamento al placebo) dei pazienti e sono stati generalmente di gravità da lieve a moderata. Due pazienti (IXE Q2W) hanno interrotto lo studio a causa dell’UE. Le SUE sono state osservate in due (4,3%) pazienti del gruppo IXE Q4W (teratoma ovarico benigno a cellule germinali e frattura da compressione), in due (3,7%) pazienti del gruppo IXE Q2W (tonsillite cronica e mielopatia in un paziente e colite da Clostridium difficile in un altro) e in un (1,9%) paziente che aveva interrotto il trattamento con placebo (infiammazione dei tessuti molli). Solo una SUE (colite da C. difficile) ha portato all’interruzione. Non ci sono stati decessi né segnalazioni di riattivazione della tubercolosi, di malattie infiammatorie intestinali, di eventi cardiovascolari avversi gravi (MACE) o di malignità.
Nel complesso, questi risultati suggeriscono che il trattamento continuo con IXE è importante per la maggior parte dei pazienti per mantenere il controllo della malattia a lungo termine [12]. Tuttavia, la lunga durata della risposta al trattamento dopo l’interruzione dell’IXE suggerisce che l’interruzione temporanea del trattamento, ad esempio durante un’infezione o prima di un intervento chirurgico, è improbabile che porti a una ricaduta nella maggior parte dei pazienti. Questi risultati sono importanti per i medici al momento di prendere decisioni terapeutiche sull’interruzione del trattamento e sull’ottimizzazione della gestione a lungo termine dell’axSpA.

Messaggi da portare a casa
- Ixekizumab è approvato per il trattamento della psoriasi a placche da moderata a grave, dell’artrite psoriasica e della spondiloartrite assiale.
- Nella PsA, ixekizumab può portare a un miglioramento significativo delle florescenze cutanee dopo sole 6 settimane di terapia. Inoltre, è stato riportato un miglioramento del dolore nei pazienti con e senza infiammazione misurabile.
- Nei pazienti con r-axSpA attiva, naïve ai bDMARD o con esperienza di TNFi, ixekizumab è un trattamento efficace.
- Ixekizumab può migliorare l’attività della malattia, la funzione fisica, i marcatori oggettivi dell’infiammazione, la qualità della vita, lo stato di salute e la funzione generale nei pazienti con R-SPA per un periodo fino a 52 settimane.
- Nei pazienti con axSpA in remissione, il trattamento continuo con IXE è associato a una maggiore probabilità di mantenere un controllo ottimale della malattia rispetto alla sospensione dell’IXE.
Letteratura:
- Deodhar A, et al: Ixekizumab per i pazienti con spondiloartrite assiale non radiografica (COAST-X): uno studio randomizzato, controllato con placebo. Lancet 2020 4 gennaio; 395 (10217): 53-64.
- van der Heijde D, et al: Ixekizumab, un antagonista dell’interleuchina-17A nel trattamento della spondilite anchilosante o della spondiloartrite assiale radiografica in pazienti precedentemente non trattati con farmaci biologici antireumatici modificanti la malattia (COAST-V): risultati a 16 settimane di uno studio di fase 3 randomizzato, in doppio cieco, controllato attivo e con placebo. Lancet 2018 Dec 8; 392 (10163): 2441-2451.
- Deodhar A, et al: Efficacia e sicurezza di Ixekizumab nel trattamento della spondiloartrite assiale radiografica: risultati di sedici settimane di uno studio di fase III, randomizzato, in doppio cieco, controllato con placebo, in pazienti con precedente risposta inadeguata o intolleranza agli inibitori del fattore di necrosi tumorale. Arthritis Rheumatol 2019; 71 (4): 599-611.
- Dougados M, Wei JCC, Landewé R, et al: Efficacia e sicurezza di ixekizumab per 52 settimane in due studi clinici randomizzati e controllati di fase 3 su pazienti con spondiloartrite assiale radiografica attiva (COAST-V e COAST-W). Ann Rheum Dis 2020; 79: 176-185; doi: 10.1136/annrheumdis-2019-216118.
- Köhm M, Burkhardt H, Behrens F: Strategie terapeutiche dell’artrite psoriasica. DMW – Deutsche Medizinische Wochenschrift 2020; 145(11): 773-780; doi: 10.1055/a-0964-0231.
- de Vlam K, Gallo G, Mease P, et al: Ixekizumab mostra un modello di miglioramento del dolore nei pazienti con e senza infiammazione misurabile nell’artrite psoriasica. Artrite Reumatol 2021; 73 (suppl. 10).
- Mease PJ, Smolen JS, Behrens F, Il gruppo di studio SPIRIT H2H et al: Confronto testa a testa dell’efficacia e della sicurezza di ixekizumab e adalimumab in pazienti naïve ai farmaci biologici con artrite psoriasica attiva: risultati a 24 settimane di uno studio randomizzato, in aperto, con valutatore in cieco. Ann Rheum Dis 2020; 79: 123-131; doi: 10.1136/annrheumdis-2019-215386.
- Smolen JS, Sebba A, Ruderman EM, et al: Efficacia e sicurezza di Ixekizumab con o senza Metotrexato in pazienti biologici naïve con artrite psoriasica: risultati a 52 settimane dello studio SPIRIT-H2H. Rheumatol Ther 2020; 7: 1021-1035; doi: 10.1007/s40744-020-00250-3.
- Sieper J, Poddubnyy D: Spondiloartrite assiale. Lancet 2017; 390: 73-84; doi: 10.1016/S0140-6736(16)31591-4.
- Sepriano A, Regel A, van der Heijde D, et al: Efficacia e sicurezza dei DMARD biologici e sintetici mirati: una revisione sistematica della letteratura che informa l’aggiornamento 2016 delle raccomandazioni ASAS/EULAR per la gestione della spondiloartrite assiale. RMD Open 2017; 3: e000396; doi: 10.1136/rmdopen-2016-000396.
- Deodhar A, Miceli-Richard C, Baraliakos X, et al: Bassa incidenza di uveiti di nuova insorgenza e di riacutizzazioni nei pazienti con spondilite anchilosante trattati con secukinumab: studio clinico e analisi di sicurezza post-marketing. Ann Rheum Dis 2018; 77(Suppl 2): 999; doi: 10.1136/annrheumdis-2018-eular.4474.
- Landewé RBM, Gensler LS, Poddubnyy D, et al: Continuare o sospendere il trattamento con ixekizumab nei pazienti con spondiloartrite assiale che hanno raggiunto la remissione: risultati di efficacia e sicurezza di uno studio di sospensione randomizzato e controllato con placebo (COAST-Y). Ann Rheum Dis 2021; 80: 1022-1030; doi: 10.1136/annrheumdis-2020-219717.
- Landewé RB, van der Heijde D, Dougados M, et al: Mantenimento della remissione clinica nella spondiloartrite assiale precoce in seguito alla riduzione della dose di certolizumab pegol. Ann Rheum Dis 2020; 79: 920-928; doi: 10.1136/annrheumdis-2019-216839.
- Landewé R, Sieper J, Mease P, et al: Efficacia e sicurezza della prosecuzione della terapia con adalimumab rispetto alla sua sospensione nel mantenimento della remissione nei pazienti con spondiloartrite assiale non radiografica (ABILITY-3): uno studio multicentrico, randomizzato, in doppio cieco. Lancet 2018; 392: 134-144; doi: 10.1016/S0140-6736(18)31362-X.
- Haibel H, Heldmann F, Braun J, et al: Efficacia a lungo termine dell’adalimumab dopo la sospensione del farmaco e il ritiro nei pazienti con spondiloartrite assiale attiva non radiograficamente evidente che subiscono una riacutizzazione. Arthritis Rheum 2013; 65: 2211-2213; doi: 10.1002/art.38014.
- Song IH, Althoff CE, Haibel H, et al: Frequenza e durata della remissione senza farmaci dopo 1 anno di trattamento con etanercept rispetto a sulfasalazina nella spondiloartrite assiale precoce: dati a 2 anni dello studio ESTHER. Ann Rheum Dis 2012; 71: 1212-1215; doi: 10.1136/annrheumdis-2011-201010.
- Smolen JS, Schöls M, Braun J, et al.: Trattare la spondiloartrite assiale e la spondiloartrite periferica, in particolare l’artrite psoriasica, come obiettivo: aggiornamento 2017 delle raccomandazioni di una task force internazionale. Ann Rheum Dis 2018; 77: 3-17; doi: 10.1136/annrheumdis-2017-211734.
InFo PAIN & GERIATURE 2021; 3(2): 14-18