L’anemia aplastica è associata a ipocellularità del midollo osseo e pancitopenia. L’aggiunta di un agonista orale del recettore della trombopoietina alla terapia immunosoppressiva standard ha dimostrato di essere benefica nei pazienti con anemia aplastica immunomediata grave o molto grave, per i quali il trapianto di midollo osseo non è un’opzione.
Nell’anemia aplastica, c’è una mancanza completa di eritrociti, leucociti e trombociti a causa dell’insufficienza del midollo osseo. Ciò comporta un midollo osseo da ipo- ad aplastico, in quanto le cellule staminali ematopoietiche CD34-positive vengono spostate dal midollo grasso. A seconda della causa, esistono diversi meccanismi fisiopatologici sottostanti, ha spiegato il dottor Neal S. Young del National Heart, Lung and Blood Institute of the National Institutes of Health, Bethesda (USA) in occasione della Riunione annuale dell’ Associazione Europea di Ematologia (EHA) [1]. I tre meccanismi patologici più importanti sono
- Danni chimici o fisici, ad esempio a causa della chemioterapia o della radioterapia.
- Difetto costituzionale nei geni che sono importanti per mantenere l’integrità cellulare e la regolazione immunitaria.
- danno immuno-mediato alle cellule ematopoietiche.
Quest’ultima si verifica più frequentemente e viene anche definita “anemia aplastica idiopatica”. Si pensa che sia una reazione autoimmune causata dai linfociti T attivati contro le cellule staminali e progenitrici ematopoietiche. L’emocromo mostra un’anemia normocitica (MCV normale) con reticolocitopenia, trombocitopenia pronunciata e leucopenia con neutropenia. Nell’aspirato di midollo osseo sono presenti pochi o nessun precursore e la biopsia del midollo osseo è caratterizzata da una cellularità molto ridotta con proliferazione di midollo grasso. Il quadro clinico è caratterizzato da anemia (pallore, affaticamento), neutropenia (infezione) e trombocitopenia (emorragia) [2].
Le opzioni di trattamento in sintesi
Il trapianto di cellule staminali ematopoietiche è un’opzione terapeutica potenzialmente curativa. Si tratta del trattamento di scelta, soprattutto per i pazienti più giovani con un donatore adatto. Per questo motivo, i fratelli vengono analizzati per la compatibilità dell’antigene leucocitario umano non appena viene fatta la diagnosi.
Per i pazienti che non sono idonei al trapianto o che non hanno un donatore, in alternativa è disponibile un trattamento immunosoppressivo con globulina antitimocita equina (ATG) in combinazione con ciclosporina. Questa opzione terapeutica è efficace nella maggior parte dei pazienti, ma non in tutti, secondo il dottor Young [1]. Circa due terzi dei pazienti rispondono ad essa [3]. Per molti anni, sono stati tentati senza successo vari metodi per migliorare i risultati del trattamento immunosoppressivo standard (IST). Infine, una svolta è stata raggiunta quando uno studio aperto e non randomizzato di fase I/II ha dimostrato che l’aggiunta di Eltrombopag all’ATG più ciclosporina ha portato a tassi di risposta considerevoli nei pazienti non trattati con anemia aplastica grave o molto grave [4].
| L’endpoint primario dello studio era una risposta ematologica completa dopo tre mesi, definita come un livello di emoglobina superiore a 10 g per dl, una conta assoluta dei neutrofili superiore a 1000 per mm3 e una conta piastrinica di 100 000 per mm3 nei pazienti che non avevano ricevuto trasfusioni. I criteri per una risposta parziale erano l’indipendenza dalle trasfusioni (sia di globuli rossi che di piastrine), con un gruppo sanguigno che non soddisfaceva i criteri per l’anemia aplastica grave, ma era insufficiente per una risposta completa. |
Eltrombopag stimola l’ematopoiesi a livello di cellule staminali
Questo agonista orale del recettore della trombopoietina ha un effetto sul controllo della formazione delle cellule staminali ematopoietiche e delle piastrine. Il farmaco attiva la trombopoietina, che controlla la formazione dei trombociti e del sangue (ematopoiesi). Nello studio randomizzato controllato di fase III RACE (Randomized, Multicenter Trial Comparing Horse ATG plus Cyclosporine with or without Eltrombopag as First-Line), la TSI da sola (ATG più Ciclosporina) è stata confrontata con la TSI più Eltrombopag come terapia di prima linea nei pazienti con anemia aplastica grave o molto grave [3]. Il tempo mediano alla prima risposta e alla risposta completa è risultato più breve nel braccio di studio con TSI più eltrombopag (gruppo sperimentale, EG) rispetto al braccio di studio in cui è stata prescritta la sola TSI (gruppo di controllo, KG). Questi tempi di risposta più brevi spiegano perché EG era precedentemente indipendente dalle trasfusioni di globuli rossi e piastrine.
- I pazienti KG hanno ricevuto una TSI composta da ATG (40 mg per kg di peso corporeo al giorno per quattro giorni consecutivi) più ciclosporina orale (5 mg per kg di peso corporeo al giorno dal primo giorno per almeno 12 mesi). La ciclosporina è stata poi ridotta nei 12 mesi successivi e interrotta dopo 24 mesi.
- I pazienti dell’EG hanno ricevuto la terapia sperimentale composta da TSI più Eltrombopag (150 mg al giorno dal 14° giorno). Le caratteristiche demografiche e cliniche dei partecipanti ai due gruppi erano comparabili. Il periodo di follow-up mediano è stato di 24 mesi.
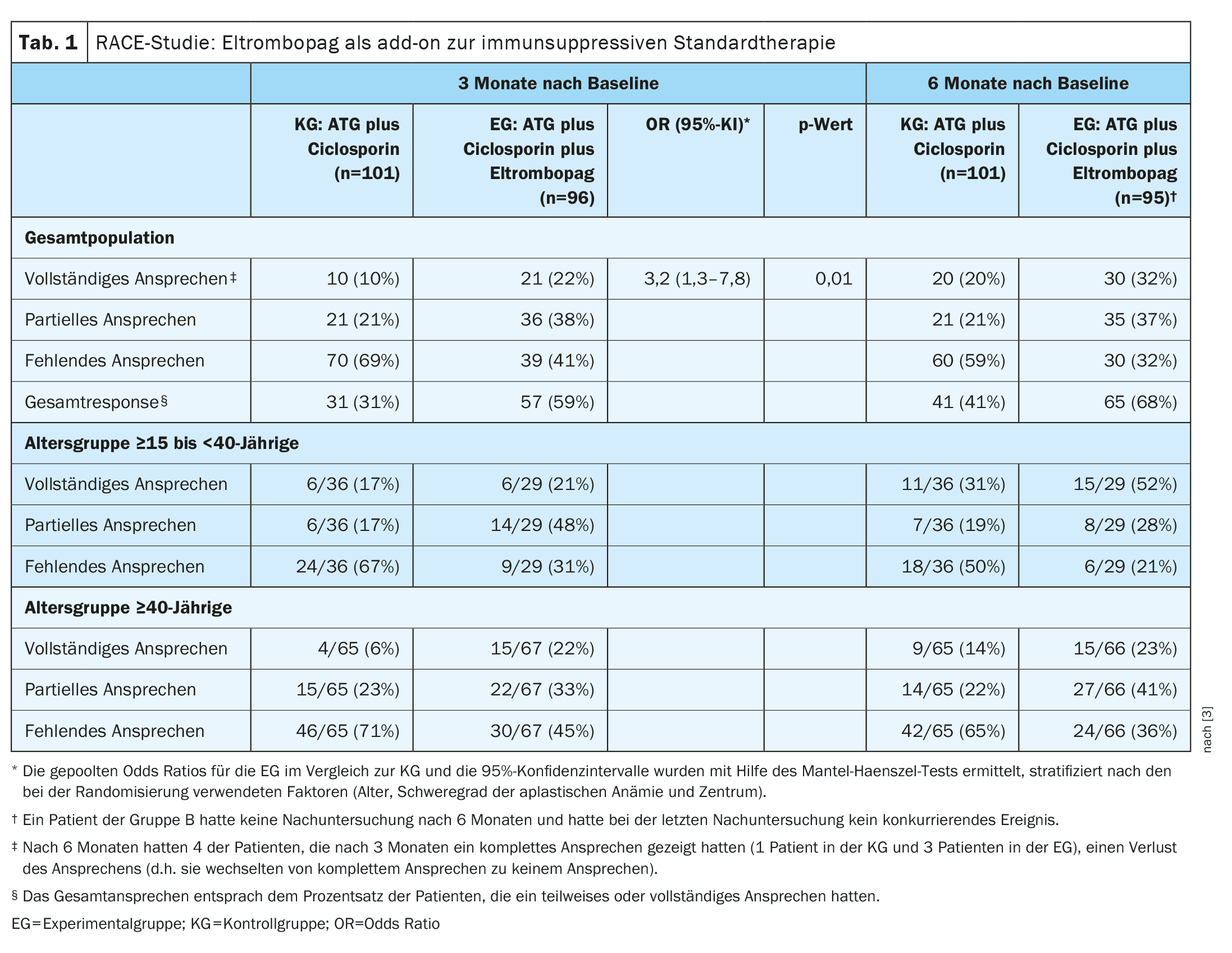
- La percentuale di pazienti che hanno risposto completamente al trattamento dopo tre mesi è stata del 10% nella CG e del 22% nella CE (odds ratio [OR] in pool, 3,2; 95% CI: 1,3-7,8; p=0,01), tab. 1).
- Il tasso di risposta globale a 3 mesi era più basso nel gruppo di controllo (31%) rispetto alla CE (59%) e il tempo mediano alla prima risposta era di 8,8 mesi nel gruppo di controllo e di 3,0 mesi nella CE. Dopo 12 mesi, il tasso di risposta completa era del 33% nel gruppo di controllo e del 52% nell’EC. Il tempo mediano alla prima risposta era di 3,0 mesi nel braccio eltrombopag e di 8,8 mesi nel braccio EC.
L’incidenza di effetti avversi gravi è stata paragonabile in entrambi i gruppi; le interruzioni del trattamento sono state rare. Le mutazioni somatiche sono state rilevate nel 31% nell’EG e nel 29% nel KG prima dell’inizio dello studio. Queste percentuali sono aumentate al 55% nell’EG e al 66% nel KG entro il mese 6 dal basale, senza alcun effetto sulla risposta ematologica e sui tassi di sopravvivenza a 2 anni (90% nell’EG vs. 85% nel KG).
Anche i trapianti di midollo osseo aploidentici sono promettenti per ampliare l’accesso al trapianto di cellule staminali ematopoietiche, ha detto il relatore [1,5].
Congresso: EHA2024
Letteratura:
- “Anemia aplastica immune: aggiornamento sulla fisiopatologia e nuovi trattamenti”, Dr Neal S. Young, EHA2024, Madrid, 13.6.-16.6.2024.
- Lauten M, Erlacher M, Knöfler R: Ematologia. Pediatria 2019: 541-570.
- Peffault de Latour R, et al: Eltrombopag aggiunto all’immunosoppressione nell’anemia aplastica grave. N Engl J Med 2022; 386(1): 11-23.
- Townsley DM, et al: Eltrombopag aggiunto all’immunosoppressione standard per l’anemia aplastica. N Engl J Med 2017; 376: 1540-1550.
- DeZern A, et al: BMT da donatore alternativo con ciclofosfamide post-trapianto come terapia iniziale per l’anemia aplastica grave acquisita [pubblicato online prima della stampa, 2023 Apr 21]. Blood 2023; blood.2023020435. doi:10.1182/blood.2023020435.
HAUSARZT PRAXIS 2024; 19(11): 34–35 (pubblicato il 25.11.24, prima della stampa)
InFo ONKOLOGIE & HÄMATOLOGIE 2024; 12(6): 26–27