Per il trattamento del diabete di tipo 2 sono disponibili classi di farmaci con diversi meccanismi d’azione. Tuttavia, la presenza di insufficienza renale o cardiaca, di malattie cardiovascolari o di carenza di insulina influenza in modo significativo la terapia.
In Svizzera, circa il 5% della popolazione ha il diabete, con una percentuale più alta negli uomini (5,5%) rispetto alle donne (3,9%) [1]. Circa il 90% delle persone colpite soffre di diabete di tipo 2 (T2D) [2]. Rispetto alla popolazione generale, la prevalenza di questa condizione è particolarmente elevata nelle persone con insufficienza cardiaca ed è di circa il 40% nelle persone ricoverate con insufficienza cardiaca [3]. Ciò è dovuto, tra l’altro, alla sovrapposizione dei fattori di rischio, della fisiopatologia e delle comorbidità [3]. Una caratteristica comune centrale di entrambe le malattie è che spesso sono accompagnate da un’alterazione della funzione renale [3]. Pertanto, la T2D e l’insufficienza cardiaca sono associate allo sviluppo e al peggioramento della malattia renale cronica, che a sua volta contribuisce a una prognosi sfavorevole [3]. A causa dell’associazione tra T2D, insufficienza cardiaca e disfunzione renale, vi è una crescente necessità di agenti anti-iperglicemici con proprietà cardio- e nefroprotettive [3].
Classi di farmaci disponibili e raccomandazioni SGED
Per il trattamento della T2D sono disponibili varie classi di farmaci con diversi meccanismi d’azione (Tab. 1) . Secondo le raccomandazioni della Società Svizzera di Endocrinologia e Diabetologia (SGED), la metformina è generalmente il farmaco di prima linea di scelta, con il quale si possono combinare precocemente gli altri farmaci disponibili, tenendo conto del loro meccanismo d’azione e degli effetti collaterali [4]. Tuttavia, vari altri fattori, come la presenza di insufficienza renale, malattie cardiovascolari, insufficienza cardiaca o carenza di insulina, possono limitare la scelta della terapia [4].
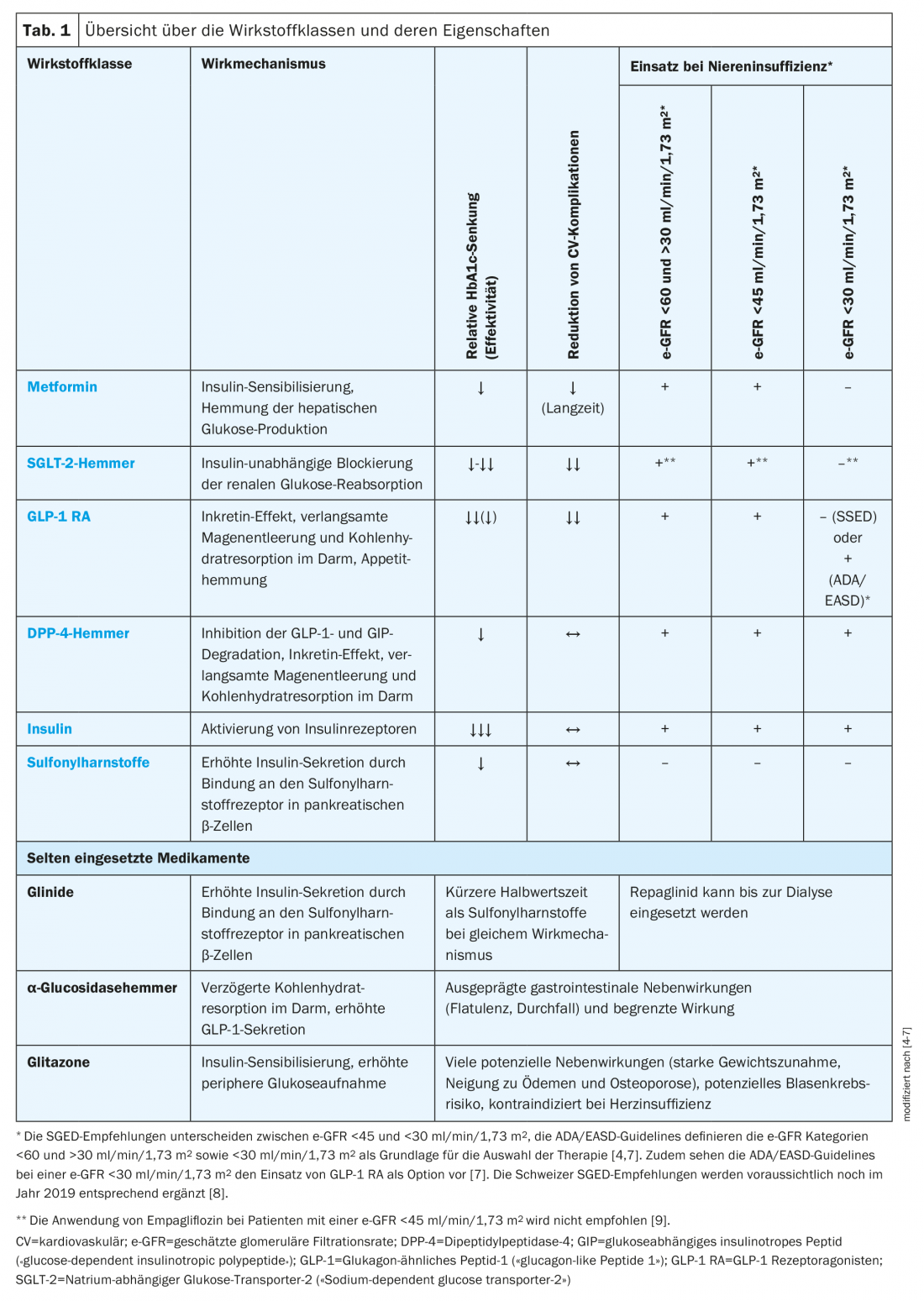
Secondo le raccomandazioni dello SGED, l’insulina basale è il trattamento di scelta per la carenza di insulina, seguita dall’insulina mista o dalle insuline coformulate, dall’insulina basale in combinazione con un agonista del recettore del peptide 1 simile al glucagone (GLP-1 RA) o da una terapia di base in bolo.
Nei pazienti con insufficienza renale, anche la gamma di farmaci utilizzabili è notevolmente limitata. Mentre le sulfoniluree a lunga durata d’azione non possono essere utilizzate nei pazienti con insufficienza renale moderata (tasso di filtrazione glomerulare stimato, e-GFR <60 ma >30 ml/min/1.73m2), Nell’insufficienza renale grave (e-GFR <30 ml/min/1,73 m2), solo gli inibitori della dipeptidil peptidasi-4 (DPP-4), gli agonisti del recettore del peptide 1 simile al glucagone (GLP-1 RA)1 e l’insulina possono essere considerati [4,7]. L’aggiustamento della dose è necessario per tutti gli inibitori della DPP-4, tranne il linagliptin, e tutti gli inibitori della DDP-4, tranne il saxagliptin, possono essere utilizzati fino alla dialisi. Se il trattamento non porta al raggiungimento dell’obiettivo individuale di HbA1c entro tre mesi, si deve somministrare l’insulina basale.
Per quanto riguarda il rischio cardiovascolare, ci sono anche differenze tra le classi di farmaci. Ad esempio, la metformina nell’uso a lungo termine e in presenza di malattie cardiovascolari, gli inibitori del trasportatore di glucosio sodio-dipendente-2 (SGLT-2) e GLP-1 RA sono associati a una riduzione delle complicanze cardiovascolari e persino della mortalità per tutte le cause [4]. Secondo le raccomandazioni dello SGED, la metformina dovrebbe quindi essere utilizzata per prima nelle persone con malattia cardiovascolare, con l’indicazione di una combinazione precoce con un inibitore SGLT-2 o un GLP-1 RA. Se l’obiettivo individuale di HbA1c non viene raggiunto, la combinazione di metformina più inibitore SGLT-2 può essere integrata con un inibitore DPP-4, gliclazide o insulina basale. Con il trattamento iniziale con metformina più inibitori della DPP-4, è possibile utilizzare gliclazide o insulina basale come farmaci aggiuntivi.
Nelle persone senza malattie cardiovascolari, è possibile il trattamento con metformina in combinazione con un inibitore SGLT-2, un GLP-1 RA o un inibitore della DPP-4. Quest’ultima può essere integrata con gliclazide o insulina basale, se necessario.
Se è presente un’insufficienza cardiaca, il trattamento con metformina più inibitore SGLT-2 è indicato per primo. Se necessario, si può utilizzare anche un inibitore della DPP-4 nel corso successivo. Se questo non porta al successo terapeutico desiderato, si deve utilizzare l’insulina basale ( Fig. 1) [4].
Cuore focalizzato
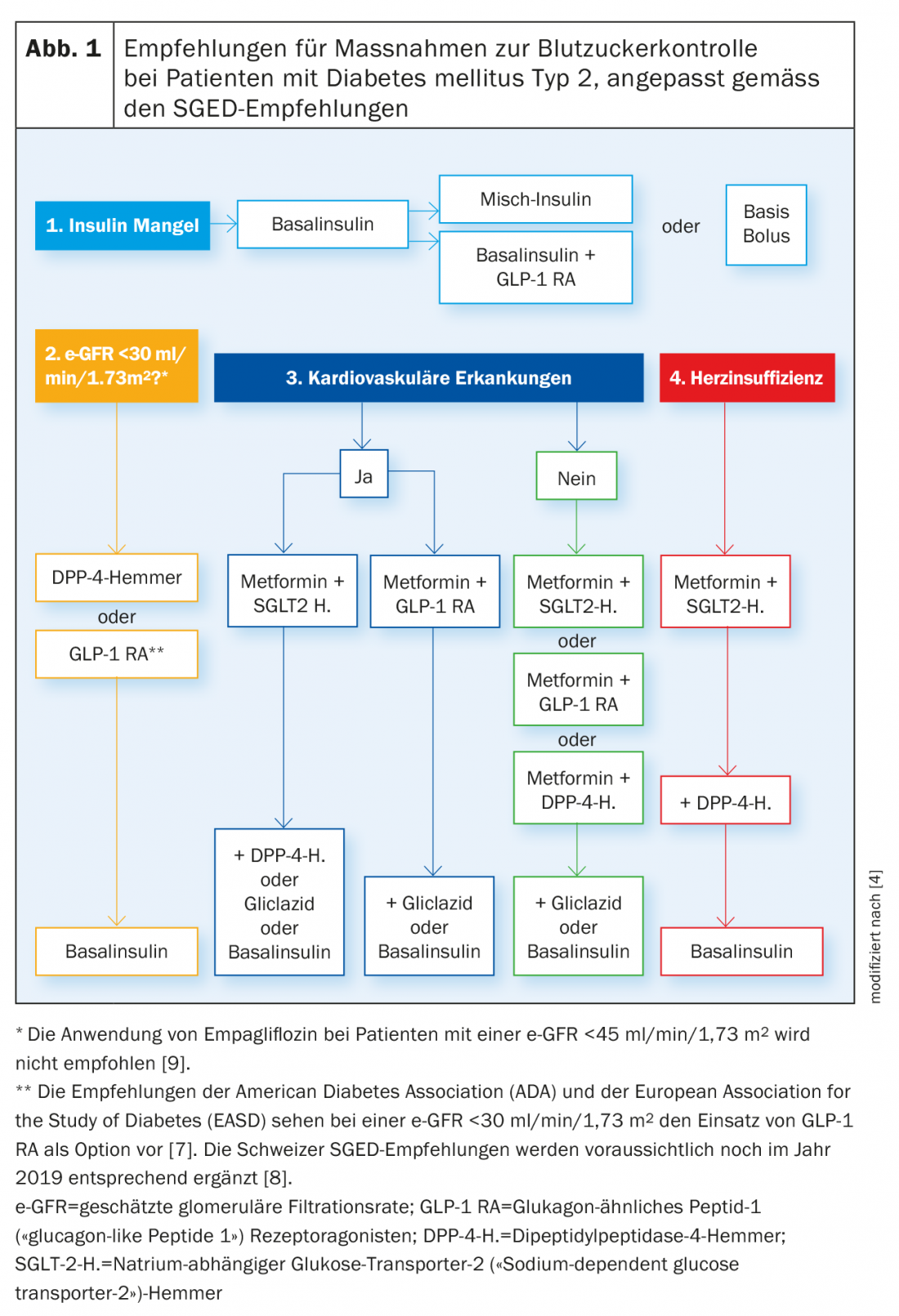
Inibitori SGLT-2: oltre al loro effetto antiiperglicemico primario, gli inibitori SGLT-2 hanno diverse proprietà che possono influenzare favorevolmente la prognosi cardiovascolare [10]. Pertanto, gli effetti positivi sugli eventi cardiovascolari sono stati dimostrati in diversi studi sull’esito cardiovascolare nei pazienti con T2D. Nello studio EMPA-REG OUTCOME nei pazienti con malattia cardiovascolare consolidata, empagliflozin è stato superiore al placebo in termini di endpoint cardiovascolare composito primario (dati raggruppati, Scheda. 2). Inoltre, empagliflozin ha ridotto la mortalità cardiovascolare, la mortalità per tutte le cause (HR 0,68; 95% CI 0,57-0,82; p<0,001) e il rischio di ospedalizzazione per insufficienza cardiaca (HR 0,65; 95% CI 0,50-0,85; p=0,002) [10,11]. Anche nell’endpoint composito di ospedalizzazione o morte per insufficienza cardiaca, empagliflozin ha mostrato un effetto positivo (HR 0,61; 95% CI 0,47-0,79; p<0,001) [12]. Sulla base di questi dati, empagliflozin è indicato da Swissmedic “per la prevenzione degli eventi cardiovascolari nei pazienti con diabete mellito di tipo 2 e malattia cardiovascolare già manifesta” [9].
Canagliflozin ha anche mostrato una riduzione dell’endpoint cardiovascolare composito primario nei pazienti con malattia cardiovascolare o fattori di rischio associati nel programma di studio CANVAS, ma non ha raggiunto la significatività in termini di mortalità cardiovascolare [10,13]. Inoltre, è stato osservato un aumento del rischio di amputazioni [13].
I dati presentati di recente dallo studio DECLARE-TIMI 58 hanno mostrato una riduzione statisticamente significativa dei ricoveri per insufficienza cardiaca nei pazienti con malattia cardiovascolare o fattori di rischio associati che assumono dapagliflozin (2,5% vs. 3,3% con placebo; p<0,005), e nell’endpoint composito di ospedalizzazione per insufficienza cardiaca o morte cardiovascolare (4,9% contro 5,8% con placebo, p=0,005). Inoltre, dapagliflozin ha raggiunto la non inferiorità ma non la superiorità rispetto al placebo in termini di eventi cardiovascolari maggiori. A differenza di canagliflozin, non è stato osservato un aumento del rischio di amputazioni con dapagliflozin [14]. Va notato anche che i pazienti dello studio DECLARE-TIMI 58 avevano valori di e-GFR significativamente migliori rispetto agli studi EMPA-REG Outcome e CANVAS, a causa dei diversi criteri di esclusione, che hanno contribuito alla minore mortalità nello studio DECLARE-TIMI 58 [11,13,14].
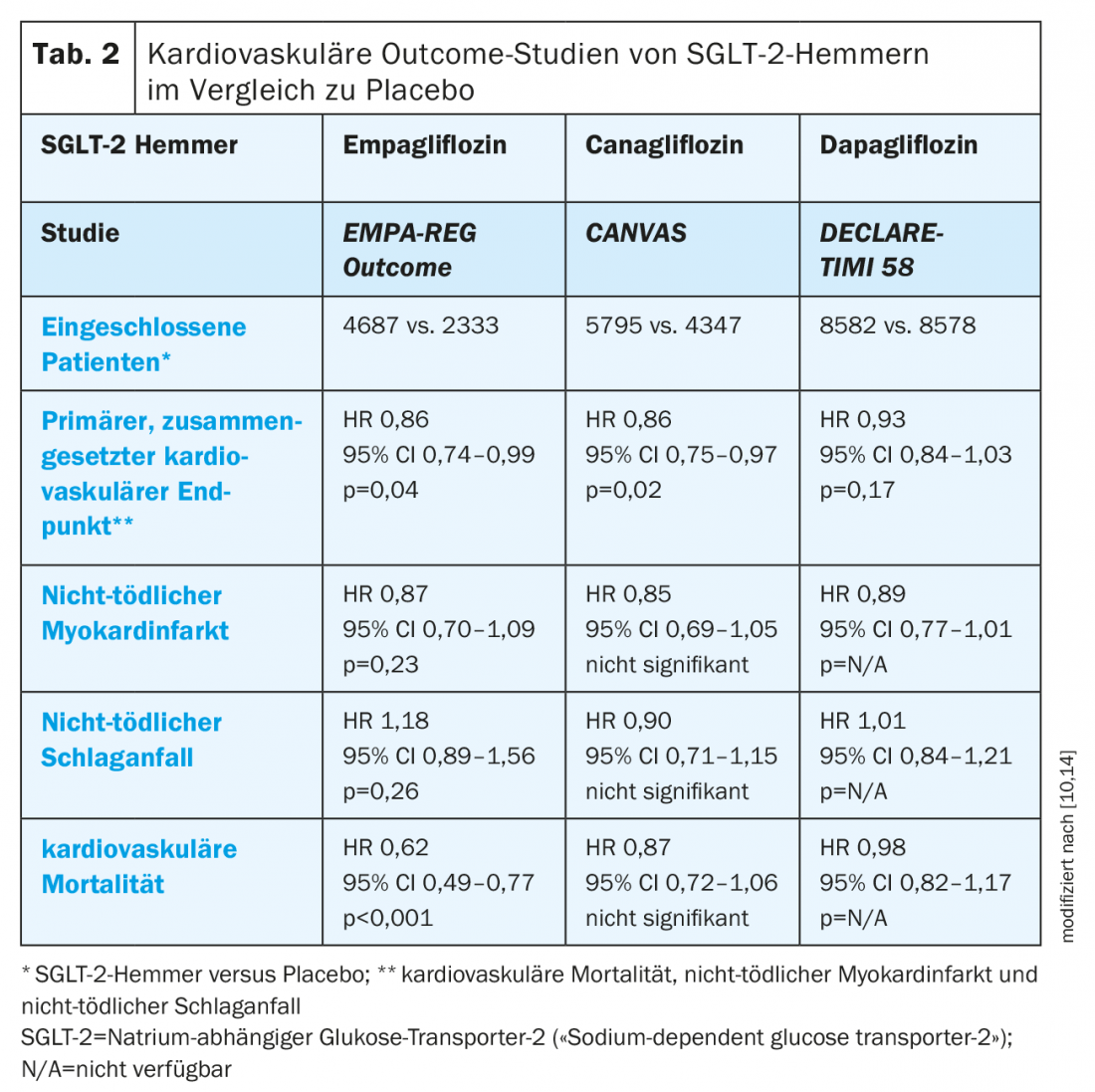
GLP-1 RA: lo studio ELIXA ha dimostrato la non inferiorità di GLP-1 RA lixisenatide rispetto al placebo rispetto all’endpoint cardiovascolare composito primario, ma nessun effetto positivo sull’esito cardiovascolare (tab. 3) [15].
Al contrario, lo studio LEADER ha dimostrato la non inferiorità di liraglutide rispetto al placebo e una riduzione significativa della mortalità cardiovascolare nei pazienti con malattia cardiovascolare o fattori di rischio associati. Anche la mortalità per tutte le cause è stata significativamente ridotta, mentre non c’è stata alcuna differenza nei ricoveri per insufficienza cardiaca [15]. Sulla base di questi dati, liraglutide è indicato da Swissmedic per la “prevenzione degli eventi cardiovascolari nei pazienti con diabete mellito di tipo 2 e malattia cardiovascolare già manifesta” [16].
La non inferiorità di semaglutide rispetto al placebo è stata confermata nel MACE a 3 punti ed è stata dimostrata una possibile superiorità (MACE a 3 punti: riduzione del 26%; p<0,001 per la non inferiorità; p=0,02 per la superiorità), sebbene lo studio non sia stato progettato per valutare la superiorità. Inoltre, è stata osservata una riduzione significativa dell’ictus non fatale e dell’infarto del miocardio, ma nessun effetto sulla mortalità cardiovascolare o per tutte le cause [17].
Il trattamento una volta alla settimana con exenatide non è stato inferiore al placebo nello studio EXSCEL, ma non ha mostrato differenze nella mortalità cardiovascolare, nel verificarsi di infarto miocardico non fatale o ictus e nell’ospedalizzazione per insufficienza cardiaca [15,17–20].
Inibitori della DPP-4: negli studi preliminari, sono stati osservati effetti cardiaci e vascolari positivi degli inibitori della DPP-4 e i primi risultati degli studi di fase II e di fase III hanno indicato una riduzione degli eventi cardiovascolari da parte di questi composti [10]. Gli studi sugli esiti cardiovascolari hanno dimostrato la non inferiorità di alogliptin, saxagliptin, sitagliptin e linagliptin rispetto al placebo (Tabella 4) . Va notato che i pazienti inclusi in questi studi ricevevano già lo standard di cura per quanto riguarda la gestione del T2D e la gestione del rischio cardiovascolare [10].
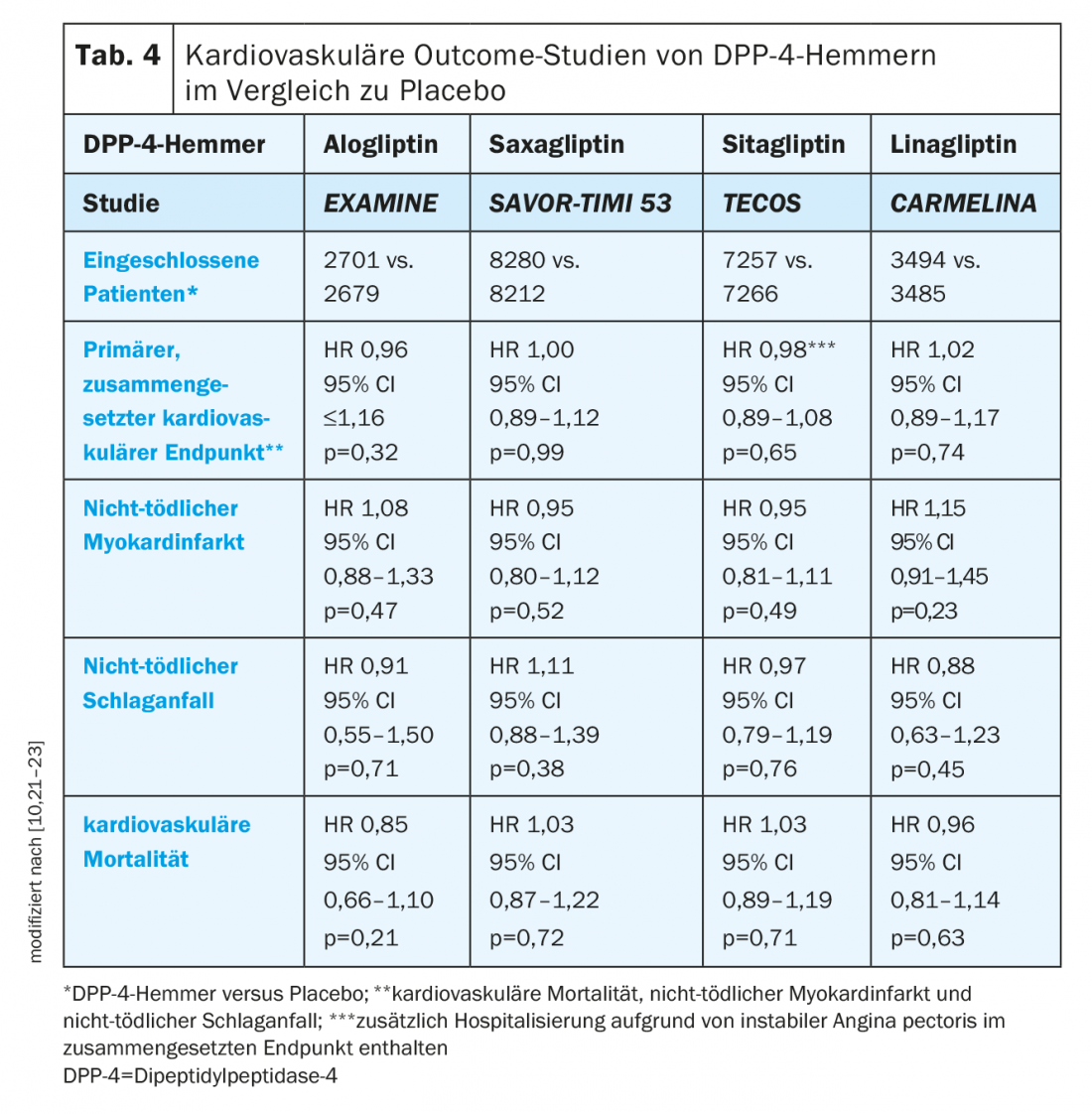
Una questione aperta riguardante l’uso degli inibitori della DPP-4 è la loro influenza sull’insorgenza dell’insufficienza cardiaca. Nello studio EXAMINE, c’è stata una tendenza non significativa per un tasso di ospedalizzazione più elevato dovuto a insufficienza cardiaca con alogliptin (1,07; 95% CI 0,79-1,46; p=0,657) [10,24]. Tuttavia, un’analisi post-hoc non ha riscontrato alcun effetto sull’endpoint composito di morte cardiovascolare e ospedalizzazione per insufficienza cardiaca (HR 1,00; 95% CI 0,82-1,21) [24].
Nello studio SAVOR-TIMI 53, un numero significativamente maggiore di pazienti nel gruppo saxagliptin è stato ricoverato con insufficienza cardiaca rispetto al placebo (3,5% vs. 2,8%; HR 1,27; 95% CI 1,07-1,51; p=0,007) [22]. Il rischio di insufficienza cardiaca era più alto nei pazienti con T2D con livelli elevati di peptide natriuretico, precedente insufficienza cardiaca o malattia renale cronica al basale [25].
A differenza di due studi precedenti, nello studio TECOS il tasso di ospedalizzazione non differiva tra i gruppi sitagliptin e placebo (HR 1,00; 95% CI 0,83-1,20; p=0,98) [10,26].
Linagliptin non ha portato ad un aumento del tasso di ospedalizzazione per insufficienza cardiaca nello studio CARMELINA (HR 0,90; 95% CI 0,74-1,08; p=0,2635) [21].
Focus rene
Inibitori SGLT-2: Empagliflozin, così come canagliflozin e dapagliflozin hanno mostrato potenziali proprietà nefroprotettive nei rispettivi studi di esito, sebbene le popolazioni di pazienti differiscano nei vari studi (Tab. 5) [3]. Mentre gli studi EMPA-REG Outcome e CANVAS hanno incluso pazienti con un e-GFR di almeno 30 ml/min/1.73 m², lo studio DECLARE-TIMI 58 ha incluso solo pazienti con un e-GFR >60 ml/min/1.73 m² [11,13,14].
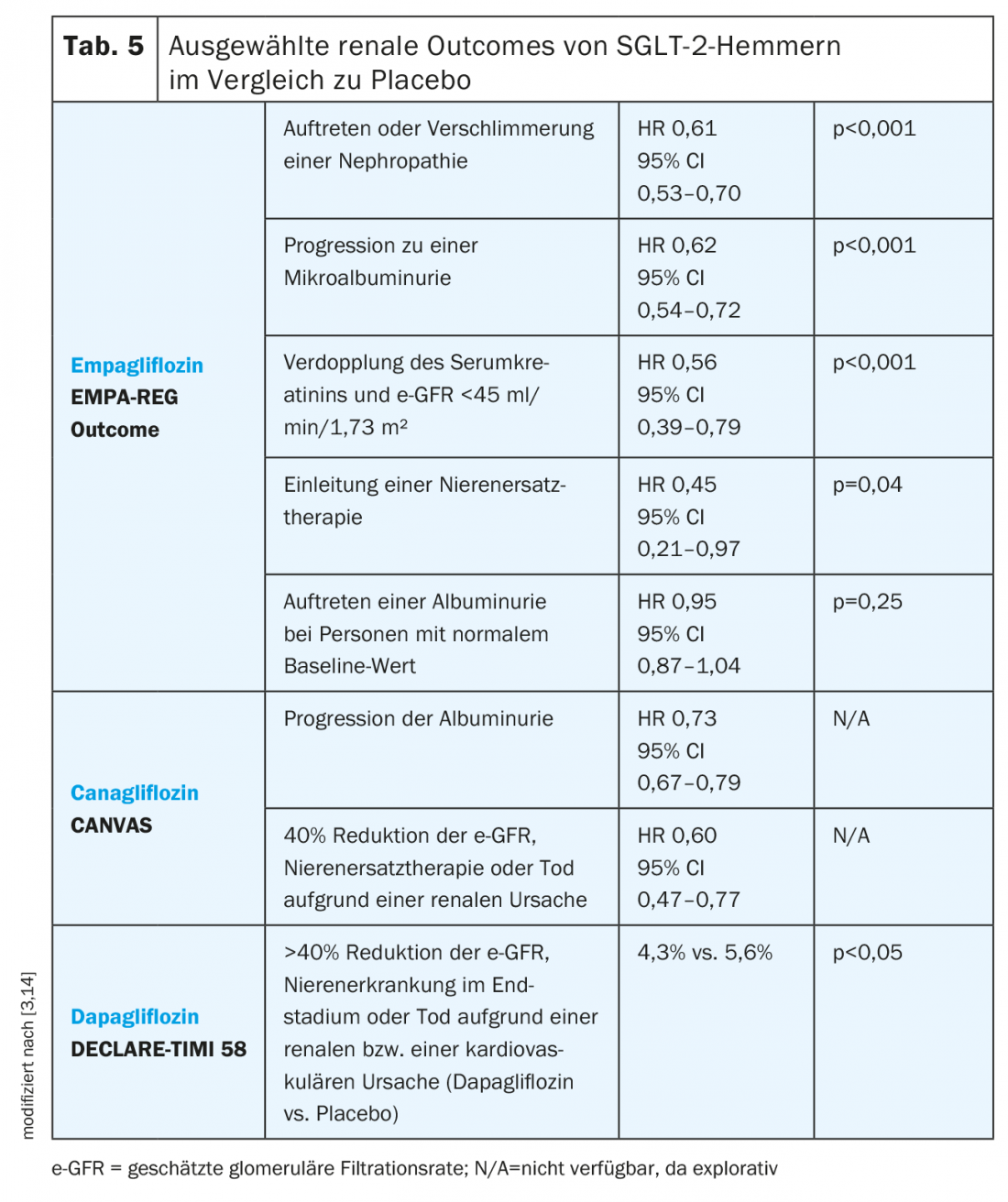
Nello studio EMPA-REG Outcome Study, empagliflozin è stato associato a una minore incidenza di peggioramento della nefropatia, definita come progressione a microalbuminuria, raddoppio della creatinina sierica con un e-GFR <45 ml/min/1.73 m², inizio di terapia sostitutiva renale o morte per malattia renale. Tutti i singoli componenti, tranne la morte per malattia renale, hanno raggiunto la significatività statistica. Nel gruppo empagliflozin, l’e-GFR è diminuito moderatamente nelle prime quattro settimane, ma poi si è stabilizzato ed è tornato al livello basale dopo la fine della terapia, mentre l’e-GFR nel gruppo placebo è diminuito continuamente per tutta la durata dello studio [3].
Nello studio CANVAS, la progressione dell’albuminuria, definita come un aumento superiore al 30% dell’albuminuria e un passaggio da normo a microalbuminuria o da micro a macroalbuminuria, è stata inferiore nel gruppo canagliflozin rispetto al placebo. Inoltre, canagliflozin ha mostrato una riduzione dell’endpoint composito di riduzione del 40% di e-GFR, terapia sostitutiva renale o morte per cause renali rispetto al placebo [3]. Anche gli esiti renali di canagliflozin sono attualmente oggetto di studio nello studio CREDENCE [27].
Come dimostrano i dati recentemente presentati dello studio DECLARE-TIMI 58, dapagliflozin ha anche un effetto positivo sugli esiti renali ed è associato a una riduzione dell’endpoint composito >40% di riduzione dell’e-GFR, della malattia renale allo stadio terminale o della morte per cause renali o cardiovascolari [14].
GLP-1 RA: nello studio ELIXA, non c’è stato un effetto significativo della GLP-1 RA lixisenatide sul rapporto albumina-creatinina urinaria dopo aver preso in considerazione l’HbA1c (Tabella 6) [3].
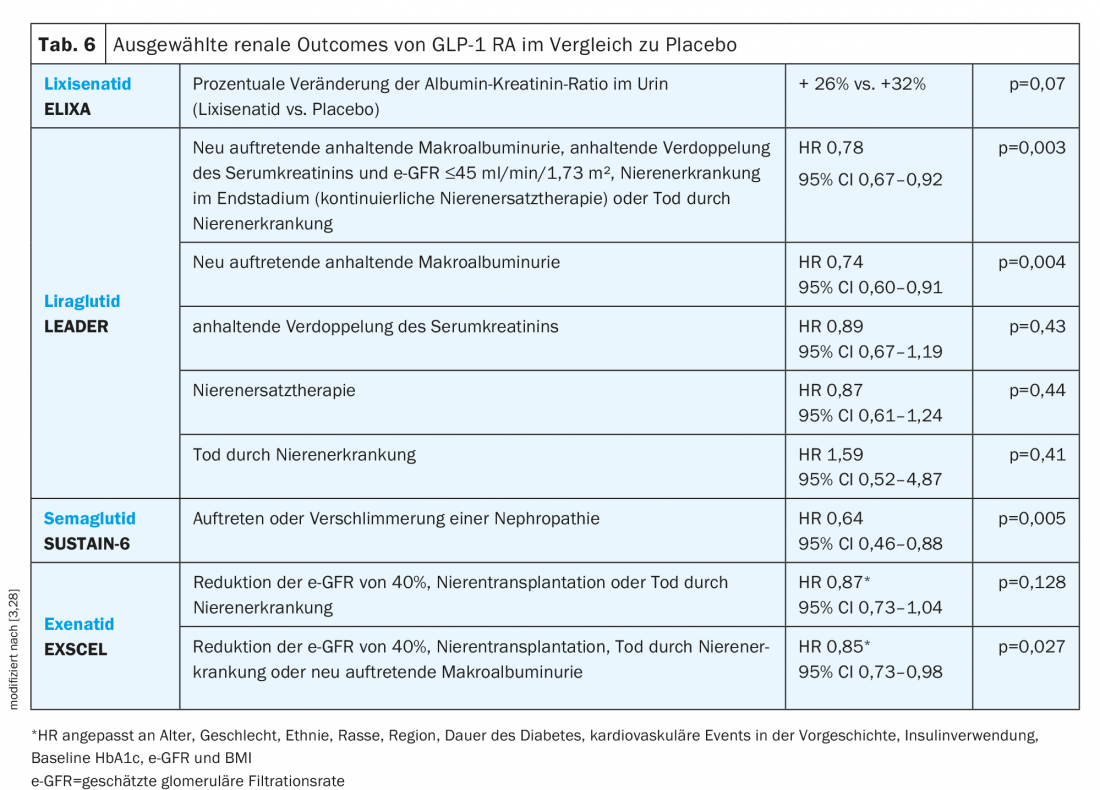
Al contrario, il trattamento con liraglutide nello studio LEADER ha comportato un rischio significativamente inferiore per l’endpoint renale composito. Inoltre, nonostante una riduzione complessiva, l’e-GFR era moderatamente migliore nel gruppo liraglutide rispetto al placebo a 36 mesi (rapporto e-GFR 1,02; 95% CI 1,00-1,03) [3].
Nello studio SUSTAIN-6, i pazienti che assumevano semaglutide hanno dimostrato di avere un rischio minore di nefropatia, definita come macroalbuminuria, raddoppio persistente della creatinina sierica e un e-GFR <45 ml/min/1,73 m² o terapia di sostituzione renale continua [3].
I dati presentati di recente dallo studio EXSCEL mostrano una riduzione significativa dell’endpoint renale composito di riduzione del 40% di e-GFR, trapianto di rene, morte per malattia renale o macroalbuminuria di nuova insorgenza con exenatide in un’analisi aggiustata. La macroalbuminuria si è verificata nel 2,2% dei pazienti nel gruppo exenatide e nel 2,5% nel gruppo placebo. Non è stata osservata alcuna differenza nell’e-GFR (“differenza media dei minimi quadrati” +0,21; 95% CI -0,27 a 0,70 ml/min/1,73 m², p=0,39) [28].
Inibitori della DPP-4: nello studio TECOS, il trattamento con l’inibitore della DPP-4 sitagliptin è stato associato a una lieve ma sostenuta diminuzione del rapporto albumina-creatinina urinaria nel corso dei 3 anni di follow-up (tab. 7) [29]. La riduzione dell’albuminuria è stata osservata anche con saxagliptin nello studio SAVOR-TIMI 53 [3]. Per quanto riguarda l’e-GFR, nello studio TECOS è stato osservato un valore leggermente ma costantemente inferiore con sitagliptin rispetto al placebo. Questo non si è verificato negli studi SAVOR-TIMI 53 o EXAMINE [24]. Questa riduzione sostenuta differisce dalla diminuzione iniziale e dalla successiva stabilizzazione di e-GFR con empagliflozin osservata nello studio sui risultati EMPA-REG [3].
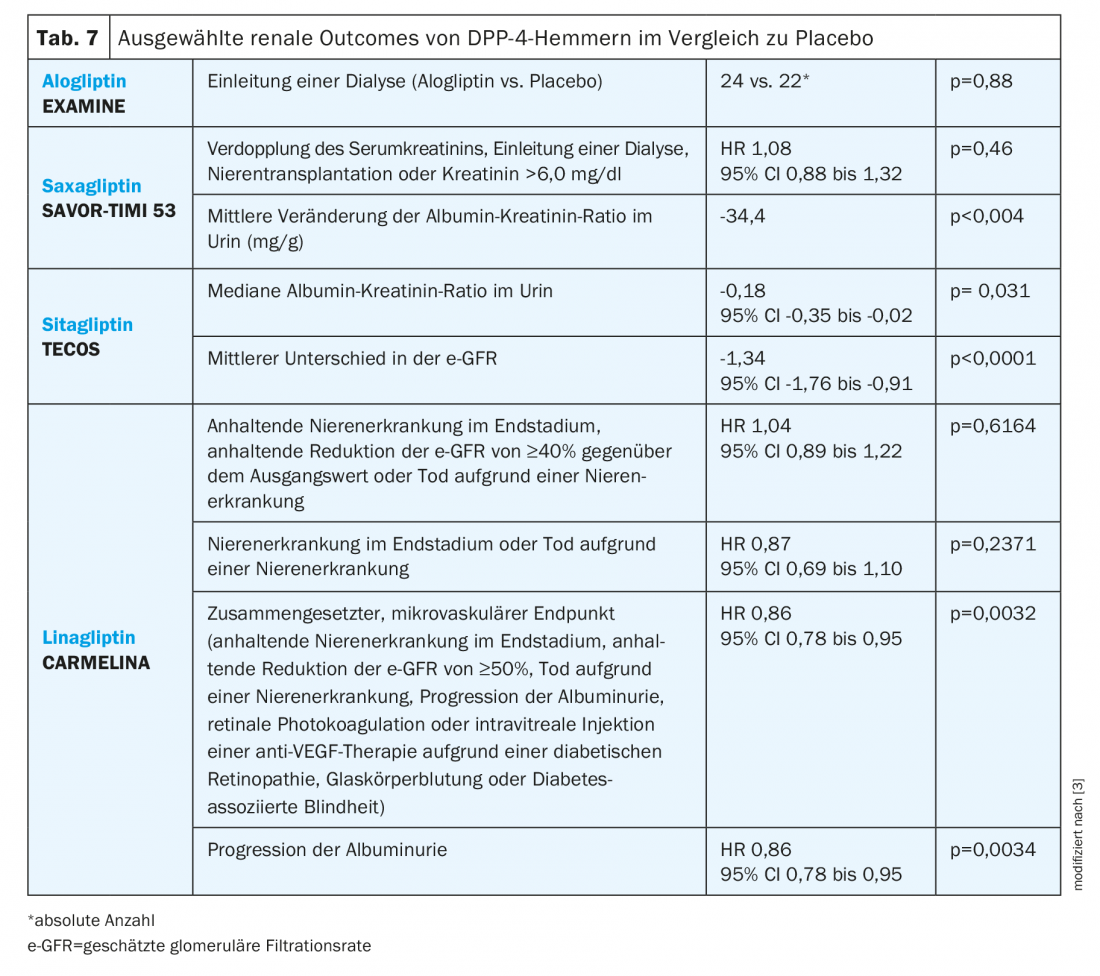
Lo studio CARMELINA ha valutato i pazienti con malattia cardiovascolare e/o malattia renale cronica, confermando la sicurezza sia cardiovascolare che renale. Inoltre, ci sono state differenze significative rispetto al placebo nell’endpoint composito, microvascolare e in termini di progressione dell’albuminuria [21].
Selezione della terapia antidiabetica
Sulla base dei dati di sicurezza cardiovascolare e delle potenziali proprietà protettive, le raccomandazioni SGED suggeriscono che gli inibitori SGLT-2 o il GLP-1 RA liraglutide, semaglutide o dulaglutide dovrebbero essere preferiti in presenza di malattie cardiovascolari. Le sulfoniluree non devono essere utilizzate nei pazienti con insufficienza renale moderata (e-GFR <45 ml/min/1.73 m2) [4]. Nell’insufficienza renale grave (e-GFR<30 ml/min/1,73 m2), la scelta degli agenti antidiabetici è limitata all’insulina, al GLP-1 RA1 e agli inibitori della DPP-4, anche se l’uso degli inibitori della DPP-4 richiede un aggiustamento della dose per quasi tutti gli agenti di questo gruppo, ad eccezione del linagliptin (Tabella 8) [4,7].

Gli inibitori SGLT-2 non devono essere utilizzati con un e-GFR <30 ml/min/1.73 m2 , poiché l’effetto di abbassamento della glicemia diminuisce anche con la diminuzione della funzione renale. Tuttavia, gli effetti positivi sulla conservazione della funzione renale e sulla riduzione degli eventi cardiovascolari e della mortalità si mantengono fino a un e-GFR di 30 ml/min/1,73m2 [4].
Una panoramica dei criteri di selezione della terapia nell’insufficienza renale o cardiaca secondo le raccomandazioni SGED è riportata nella Tabella 9 [4].
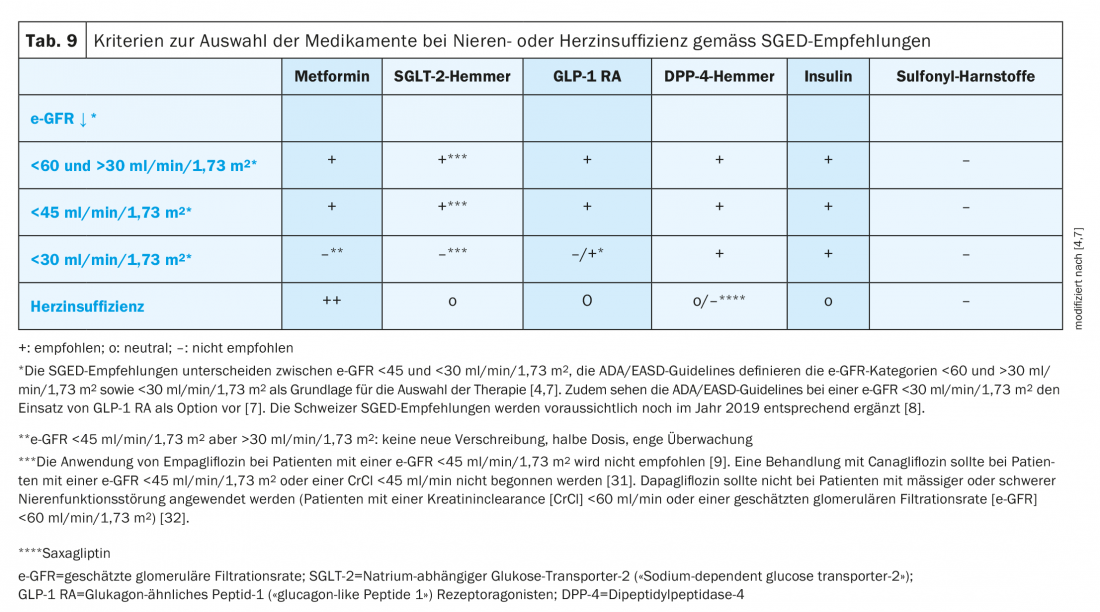
Pazienti con insufficienza cardiaca e renale
Molte osservazioni epidemiologiche hanno dimostrato un’associazione tra la morbilità e la mortalità cardiovascolare e la riduzione della funzione renale. Questo è indipendente da quale delle due malattie si presenti per prima, per cui si parla di una sindrome cardio-renale o di una sindrome reno-cardiaca a seconda del fattore scatenante iniziale. Entrambe le patologie presentano una certa sovrapposizione e possono essere favorite dal diabete [33]. La classificazione di questa patologia distingue cinque tipi diversi, con i primi quattro che descrivono sindromi cardio-renali o reno-cardiache acute o croniche. Il tipo 5, invece, si riferisce alle sindromi cardio-renali secondarie o al coinvolgimento cardio-renale nelle malattie sistemiche. Di conseguenza, si può parlare di sindrome cardio-renale di tipo 5 nel campo del diabete [34].
Indipendentemente dalla classificazione, la domanda nella pratica clinica è quale classe di farmaci debba essere utilizzata nei pazienti con T2D con insufficienza cardiaca e renale concomitante. Se la gravità dell’insufficienza renale lo consente, gli inibitori SGLT-2 sono inizialmente il trattamento di scelta. Se la funzione renale continua a diminuire, si può prendere in considerazione il GLP1-RA. Nell’insufficienza renale grave, sono indicati solo gli inibitori del DDP-4, il GLP1-RA1 e l’insulina. Nel complesso, va notato che i diuretici devono essere usati con attenzione in questi pazienti, per evitare la sovradiagnosi [4,7].
Messaggi da portare a casa
- Per il trattamento del diabete di tipo 2 sono disponibili classi di farmaci con diversi meccanismi d’azione: Metformina, inibitori SGLT-2, GLP-1 RA, inibitori DPP-4, insulina e sulfoniluree.
- Secondo le raccomandazioni dello SGED, la metformina è il farmaco di prima linea di scelta, con cui gli altri farmaci possono essere combinati precocemente.
- La presenza di insufficienza renale, malattie cardiovascolari, insufficienza cardiaca o carenza di insulina può influenzare in modo significativo la scelta della terapia.
- Nei pazienti con malattie cardiovascolari, le raccomandazioni SGED affermano che dovrebbe essere preferito un inibitore SGLT-2 (empagliflozin, dapagliflozin, canagliflozin) o un GLP-1 RA (liraglutide, semaglutide, dulaglutide).
- Nell’insufficienza renale grave (e-GFR<30 ml/min/1,73m2), la scelta degli agenti antidiabetici è limitata all’insulina, al GLP-1 RA1 e agli inibitori della DPP-4, con tutti gli inibitori della DPP-4, tranne linagliptin, che richiedono un aggiustamento della dose.
Letteratura:
- Ufficio federale di statistica: Diabete. www.bfs.admin.ch/bfs/de/home/statistiken/gesundheit/gesundheitszustand/krankheiten/diabetes.html, ultimo accesso 29.10.2018.
- Diabete Svizzera: Diabete mellito. www.diabetesschweiz.ch/diabetes/, ultimo accesso 29.10.2018.
- McHugh, KR, et al: Il ruolo emergente dei nuovi agenti anti-iperglicemici nel trattamento dell’insufficienza cardiaca e del diabete: un focus sugli esiti cardiorenali. Clin Cardiol 2018; 41(9): 1259-1267.
- Lehmann, R, et al: Raccomandazioni della SGED/SSED: Misure per il controllo della glicemia nei pazienti con diabete mellito di tipo 2. Società Svizzera di Endocrinologia e Diabetologia 2016.
- Chaudhury A, et al: Revisione clinica dei farmaci antidiabetici: implicazioni per la gestione del diabete mellito di tipo 2. Frontiers in endocrinology 2017; 8: 6. 10.3389/fendo.2017.00006
- Stein SA, Lamos EM, Davis, SN: Una revisione dell’efficacia e della sicurezza dei farmaci antidiabetici orali. Opinione di esperti sulla sicurezza dei farmaci 2013; 12(2): 153-175.
- Davies MJ, et al: Gestione dell’iperglicemia nel diabete di tipo 2, 2018. Un rapporto di consenso dell’American Diabetes Association (ADA) e dell’Associazione Europea per lo Studio del Diabete (EASD). Diabetologia 2018; 61(12): 2461-2498.
- Lehmann R: Comunicazione personale del Prof. R. Lehmann- Presidente del gruppo di lavoro SGED/SSED.
- Swissmedic: Attuale riassunto delle caratteristiche del prodotto per Jardiance®. www.swissmedicinfo.ch. Stato delle informazioni: aprile 2018.
- Scheen AJ: Effetti cardiovascolari dei nuovi agenti orali per la riduzione del glucosio: inibitori DPP-4 e SGLT-2. Circulation Research 2018; 122(10): 1439-1459.
- Zinman B, et al: Empagliflozin, esiti cardiovascolari e mortalità nel diabete di tipo 2. New England Journal of Medicine 2015; 373(22): 2117-2128.
- Fitchett D, et al: Esiti dell’insufficienza cardiaca con empagliflozin nei pazienti con diabete di tipo 2 ad alto rischio cardiovascolare: risultati dello studio EMPA-REG OUTCOME®. European Heart Journal 2016; 37(19): 1526-1534.
- Neal B, et al: Canagliflozin ed eventi cardiovascolari e renali nel diabete di tipo 2. New England Journal of Medicine 2017; 377(7): 644-657.
- Wiviott SD, et al: Dapagliflozin ed esiti cardiovascolari nel diabete di tipo 2. N. England J. Med 2019; 380: 347-357. doi: 10.1056/NEJMoa1812389. Epub 2018 Nov
- Cefalu WT, et al: Studi sugli esiti cardiovascolari nel diabete di tipo 2: dove andiamo? Riflessioni da un forum di esperti di Diabetes Care. Diabetes Care 2018; 41(1): 14-31.
- Swissmedic: Informazioni aggiornate degli esperti su Victoza®. www.swissmedicinfo.ch, a partire da informazioni: aprile 2018.
- Marso SP, et al: Semaglutide ed esiti cardiovascolari in pazienti con diabete di tipo 2. New England Journal of Medicine 2016; 375(19): 1834-1844.
- Holman RR, et al: Effetti di exenatide una volta alla settimana sugli esiti cardiovascolari nel diabete di tipo 2. New England Journal of Medicine, 2017; 377(13): 1228-1239.
- Marso SP, et al: Liraglutide ed esiti cardiovascolari nel diabete di tipo 2. New England Journal of Medicine 2016; 375(4): 311-322.
- Pfeffer MA, et al: Lixisenatide nei pazienti con diabete di tipo 2 e sindrome coronarica acuta. New England Journal of Medicine 2015; 373(23): 2247-2257.
- Rosenstock J, et al: Studio sull’esito microvascolare cardiovascolare e renale con Linagliptin nei pazienti con diabete mellito di tipo 2 (CARMELINA®). Presentazione orale al 54° Meeting annuale dell’Associazione Europea per lo Studio del Diabete (EASD), Berlino, giovedì 4 ottobre 2018. https://www.easd.org/virtualmeeting/home.html#!contentsessions/2873.
- Scirica BM, et al: Saxagliptin e gli esiti cardiovascolari nei pazienti con diabete mellito di tipo 2. New England Journal of Medicine 2013; 369(14): 1317-1326.
- White WB, et al: Alogliptin dopo una sindrome coronarica acuta nei pazienti con diabete di tipo 2. New England Journal of Medicine 2013; 369(14): 1327-1335.
- Zannad F, et al: Esiti di insufficienza cardiaca e mortalità nei pazienti con diabete di tipo 2 che assumono alogliptin rispetto al placebo in EXAMINE: uno studio multicentrico, randomizzato, in doppio cieco. The Lancet 2015; 385(9982): 2067-2076.
- Scirica BM, et al: Insufficienza cardiaca, saxagliptin e diabete mellito: osservazioni dallo studio randomizzato SAVOR-TIMI 53. Circolazione 2014; 130(18): 1579-1588.
- Green JB, et al: Effetto di sitagliptin sugli esiti cardiovascolari nel diabete di tipo 2. New England Journal of Medicine 2015; 373(3): 232-242.
- Jardine MJ, et al: Lo studio canagliflozin and renal endpoints in diabetes with established nephropathy clinical evaluation (CREDENCE) razionale, disegno e caratteristiche basali. American journal of nephrology 2017; 46(6): 462-472.
- Bethel MA, et al: Esiti renali nell’EXenatide Study of Cardiovascular Event Lowering (EXSCEL). Diabete, 2018. 67(Supplemento 1): https://doi.org/10.2337/db18-522-P
- Cornel JH, et al: Effetto di Sitagliptin sulla funzione renale e sui rispettivi esiti cardiovascolari nel diabete di tipo 2: risultati di TECOS. Diabetes Care 2016; 39(12): 2304-2310.
- Swissmedic: www.swissmedicinfo.ch.
- Swissmedic: Attuale riassunto delle caratteristiche del prodotto di Invokana®. www.swissmedicinfo.ch, a partire da informazioni: aprile 2018.
- Swissmedic: Informazioni attuali degli esperti Forxiga®. www.swissmedicinfo.ch, da informazioni: gennaio 2018.
- Schrier RW: Sindrome cardiorenale contro sindrome renocardiaca: c’è una differenza? Nat Clin Pract Nephrol 2007; 3(12): 637.
- Di Lullo L, et al.: Sindrome cardiorenale di tipo 5 (CRS-5): un aggiornamento. Nephrology@ Point of Care 2017; 3(1): p. e23-e32, https://doi.org/10.5301/napoc.5000212
PRATICA GP 2019; 14(3): 18-27
CARDIOVASC 2019; 18(2): 16-23











