Oggi i pazienti con asma possono essere trattati bene, anche nelle forme gravi, se ricevono il trattamento individuale adeguato. L’uso a lungo termine di corticosteroidi orali (OCS) è problematico a causa dei rischi e degli effetti collaterali associati. L’uso di biologici come terapia aggiuntiva è una strategia utile per ridurre l’OCS e migliorare la qualità della vita. La determinazione del fenotipo dell’asma è utile per scegliere la terapia anticorpale appropriata per l’individuo.
L’asma e la BPCO sono le malattie ostruttive delle vie aeree più comuni e svolgono un ruolo importante nell’assistenza ambulatoriale. Circa il 4-7% della popolazione svizzera soffre di asma. Le manifestazioni cliniche tipiche sono i sintomi respiratori, come respiro affannoso, oppressione toracica, tosse, fischi e respiro sibilante. I sintomi variano nel tempo, a seconda della stagionalità e delle infezioni virali, tra gli altri fattori. Soprattutto nelle forme gravi, è necessaria una gestione interdisciplinare. In occasione del Congresso Medico di Davos, il Prof. Dr. med. Jörg D. Leuppi, primario dell’Ospedale Cantonale di Basilea, ha fornito una panoramica aggiornata sulla terapia dell’asma nell’era dei biologici [1]. Circa il 5-10% di chi soffre di asma ha un’asma grave o difficile da trattare, che di solito viene trattata in collaborazione con uno pneumologo o un allergologo [2,3]. L’asma grave è definita come una scarsa funzionalità polmonare invariata, frequenti esacerbazioni che richiedono steroidi o ricoveri in ospedale e i criteri di asma parzialmente controllata o non controllata, nonostante l’aderenza ottimale al trattamento e la terapia massima con corticosteroidi per via inalatoria (ICS) alla dose più alta più almeno un altro farmaco a lungo termine e, se appropriato, la somministrazione di steroidi orali (OCS). [1,4]. Il rischio di esacerbazioni gravi aumenta nei pazienti con asma non controllata, e con esso il rischio di ospedalizzazione e mortalità. Circa un quarto dei pazienti con asma grave riferisce quattro o più esacerbazioni all’anno [12].
Il livello di eosinofilia correla con l’esito dell’asma
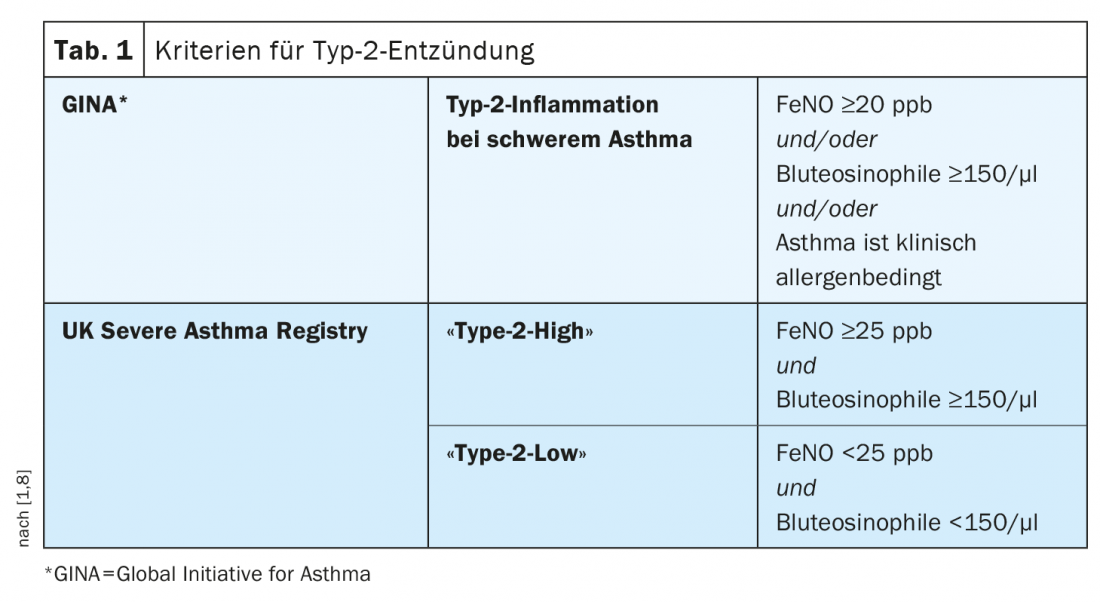
L’asma grave comprende vari fenotipi che differiscono in termini di manifestazioni cliniche, meccanismi fisiopatologici e risposta al trattamento [5]. I due fenotipi clinici più comuni sono caratterizzati dall’infiammazione eosinofila e sono definiti rispettivamente asma allergica primaria ad esordio precoce e asma eosinofila ad esordio adulto. La complessa fisiopatologia è dominata da una risposta immunitaria Th2 (Tab. 1) [1,6,8]. “Corretto per altri co-fattori, il livello di eosinofilia è un fattore di rischio per l’aumento della frequenza delle esacerbazioni e della gravità dell’asma”, spiega il Prof. Leuppi. Questo si correla con un controllo dell’asma più scarso. In uno studio epidemiologico pubblicato suLancet Respiratory Medicine da Price et al. questa correlazione potrebbe essere dimostrata statisticamente [9]. I biomarcatori clinici dell’asma eosinofila sono la conta degli eosinofili nel sangue e nell’espettorato e i livelli elevati di ossido nitrico frazionario esalato (FeNO) [7]. L’aumento dell’attivazione e del reclutamento degli eosinofili ha un effetto pro-infiammatorio. Sotto l’influenza delle chemochine, gli eosinofili migrano dal midollo osseo alle pareti bronchiali. Lì si accumulano e attivano i mediatori, che contribuiscono a danneggiare le vie aeree. Secondo la Global Initiative for Asthma (GINA), circa la metà di tutti i casi di asma grave ha un fenotipo eosinofilo [8].
Il termine “asma bassa di tipo 2” si riferisce a un fenotipo che non è ancora stato completamente caratterizzato, in cui non vi è alcuna evidenza di allergia, né di aumento del numero di granulociti eosinofili nei polmoni o nel sangue, né di infiammazione indotta da Th2. (Tab.1). L'”asma non di tipo 2″ è relativamente rara, riassume il Prof. Leuppi, e consiglia la diagnosi differenziale se un paziente con asma grave presenta bassi marcatori di tipo 2 [1].
Riduzione degli steroidi sistemici attraverso l’uso di biologici.
Il trattamento dell’asma si basa su un ciclo terapeutico in cui la terapia viene regolarmente valutata, adattata e la risposta viene successivamente monitorata [10]. Il regime terapeutico proposto dalla Global Initiative for Asthma prevede cinque fasi di trattamento dell’asma. Nello stadio 5, il trattamento aggiuntivo con un biologico specifico per il fenotipo è ora raccomandato come farmaco di mantenimento in aggiunta a ICS-LABA (Tabella 2). Gli obiettivi a lungo termine della gestione dell’asma sono il raggiungimento di un buon controllo dei sintomi e la minimizzazione del rischio di esacerbazioni e reazioni avverse ai farmaci. L’uso a lungo termine di steroidi orali sistemici (OCS) aumenta la mortalità e i tassi di complicanze, come dimostrano i dati di vari studi prospettici e retrospettivi, spiega il Prof. Leuppi. Pertanto, nell’asma grave (escalation dallo stadio 4 allo stadio 5 secondo GINA), l’inizio della terapia anticorpale deve essere preso in considerazione dopo aver controllato la tecnica inalatoria e i fattori di rischio per i pazienti che presentano biomarcatori eosinofili o allergici. Questo può ridurre l’uso a lungo termine di OCS. L’attuale linea guida GINA prevede l’OCS nell’asma grave solo in casi eccezionali, cioè quando non è possibile ottenere un controllo sufficiente nemmeno con dosi elevate di glucocorticoidi per via inalatoria in combinazione con broncodilatatori a lunga durata d’azione (LABA e/o LAMA) e con la somministrazione di un biologo [11].

Abbinare la scelta del farmaco biologico alle caratteristiche del paziente.
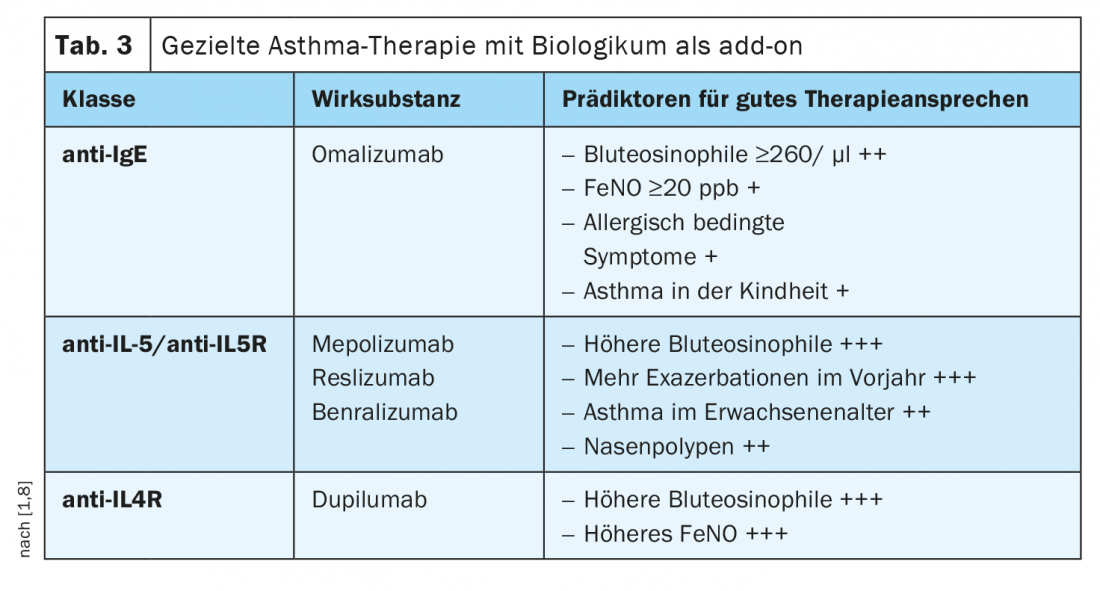
Determinando i biomarcatori o i fenotipi ad essi correlati, è possibile prevedere la risposta ad una particolare terapia anticorpale (tab. 3) [1,8]. Nel caso di allergie perenni e di concentrazioni di IgE significativamente elevate, l’uso di un anticorpo anti-IgE ha senso. Nei casi di eosinofilia ematica marcatamente aumentata (>300 cellule/µl), gli anticorpi monoclonali contro l’interleuchina-5 (IL-5) o gli anticorpi del recettore dell’IL-5 sono più adatti, e nei casi di asma eosinofila con un’eosinofilia di >150 cellule/µl e un aumento della frazione di FeNO nell’aria espirata, si può prendere in considerazione la terapia con un anticorpo del recettore dell’anti-interleuchina-4. Se si applica una strategia di trattamento personalizzata di questo tipo, in molti casi il controllo dell’asma può essere notevolmente migliorato, il che può anche riflettersi in una marcata riduzione degli steroidi sistemici. [1]. L’unico anticorpo monoclonale umanizzato contro le IgE approvato finora per l’asma è omalizumab. Questo farmaco biologico agisce legando gli anticorpi IgE liberi, determinando una riduzione dei livelli di anticorpi liberi e, in secondo luogo, la down-regulation del FcεRI sui basofili e sui mastociti. Mepolizumab, reslizumab e l’anticorpo del recettore dell’IL-5 benralizumab sono disponibili per una terapia diretta contro l’IL-5. Mentre il mepolizumab e il reslizumab bloccano la via di segnalazione della citochina legandosi in modo altamente specifico all’IL-5, riducendo così la formazione e la sopravvivenza degli eosinofili, il benralizumab interagisce sia con i recettori IL-5Rα che con quelli FcγRIII sulle cellule immunitarie effettrici. La via di segnalazione dell’IL-4 può essere inibita dall’anticorpo monoclonale IgG4 umanizzato dupilumab, che si lega ai recettori IL-4Rα e IL-13 recettore alfa (IL-13Rα).
Il relatore ha sottolineato che le raccomandazioni GINA si applicano anche durante la pandemia di Corona e che l’assunzione regolare dei farmaci per l’asma prescritti è molto importante [3]. Parallelamente al trattamento farmacologico, è importante determinare eventuali comorbidità e fattori di rischio o scatenanti modificabili (ad esempio, l’esposizione agli allergeni, il fumo) e adattarli se necessario.
Congresso: Congresso Medico Davos
Letteratura:
- Leuppi JD: Come i biologici hanno cambiato la terapia dell’asma. Prof. Dr. med. Jörg D. Leuppi, Congresso medico Davos, 11.02.2022.
- Leuppi JD, et al: Benralizumab: bersaglio del recettore IL-5 nell’asma eosinofila grave. Praxis (Bern 1994) 2019; 108 (7): 469-476.
- Leuppi J: Cosa c’è di nuovo nell’assistenza primaria all’asma: Pratica 2021; 110(16). DOI:10.1024/1661–8157/a003760.
- BÄK/KBV/AWMF: Linea guida nazionale per l’assistenza sanitaria Asma – 4a edizione, versione 1, 2020; DOI: 10.6101/ÄZQ/000469
- Bakakos A, Loukides S, Bakakos P: Asma eosinofila grave. J Clin Med 2019; 8(9): 1375.
- Kühn M, Dimitriou F, Steiner UC, et al.: Risposta immunitaria TH2: significato e influenza terapeutica. Swiss Med Forum 2021; 21(0102): 13-17.
- Pavlidis S, et al: “T2-alto” nell’asma grave in relazione agli eosinofili nel sangue, all’ossido nitrico esalato e alla periostina nel siero. Eur Respir J 2019; 53(1): 1800938.
- Iniziativa Globale per l’Asma: Strategia globale per la gestione e la prevenzione dell’asma. Aggiornato al 2020. https:// ginasthma.org, (ultimo accesso 2202.2022)
- Price DB, et al: Conta degli eosinofili nel sangue e carico annuale prospettico della malattia asmatica: uno studio di coorte del Regno Unito. Lancet Respirator Med 2015; 3(11): 849-858.
- Steurer-Stey C: Asma. Linea guida medix, aggiornamento: 11/2021, www.medix.ch (ultimo accesso 22.02.2022)
- Asma grave: i glucocorticoidi orali passano in secondo piano. Allergo J 2020; 29: 74, https://doi.org/10.1007/s15007-020-2557-7
- Wang E, et al: Caratterizzazione dell’asma grave a livello mondiale: dati del Registro Internazionale dell’Asma Grave (ISAR). Chest 2020; 157: 790-804.
- Iniziativa Globale per l’Asma: Strategia globale per la gestione e la prevenzione dell’asma. Aggiornamento 2021. https://ginasthma.org, (ultima chiamata 2202.2022)
PRATICA GP 2022; 17(3): 26-27