Le neuropatie immunomediate variano nella presentazione clinica, nel decorso e nella patogenesi. Negli ultimi anni, sono stati rilevati autoanticorpi contro le proteine nodali e paranodali dell’anello di Ranvier. Gli autoanticorpi possono causare danni assonali e portare alla demielinizzazione.
Le neuropatie immunomediate variano nella presentazione clinica, nel decorso e nella patogenesi e rappresentano circa il 9% di tutte le polineuropatie [1]. Negli ultimi anni, sono stati rilevati autoanticorpi contro le proteine nodali e paranodali dell’anello di Ranvier. Gli autoanticorpi contro la neurofascina (NF), la contactina 1 (CNTN1) o la proteina associata alla contactina 1 (CASPR1) sono stati rilevati nel 10% dei pazienti con polineuropatia demielinizzante infiammatoria cronica (CIDP) [2]. Gli autoanticorpi possono causare danni assonali e portare alla demielinizzazione [4]. I pazienti sieropositivi con CIDP differiscono dai pazienti sieronegativi nel fenotipo clinico, nei risultati elettrofisiologici e nella risposta alla terapia standard [2].
Il rilevamento di autoanticorpi nodali e paranodali specifici può aiutare a trovare terapie efficaci. Oltre alla CIDP, gli autoanticorpi associati alla malattia sono noti anche in altre neuropatie immuno-mediate, come la sindrome di Guillain-Barré (GBS) con i sottotipi polineuropatia demielinizzante infiammatoria acuta (AIDP), neuropatia assonale motoria acuta (AMAN) e neuropatia assonale motoria e sensoriale acuta (AMSAN), Sindrome di Miller-Fisher (MFS), neuropatia motoria multifocale (MMN), neuropatia anti-MAG MGUS (neuropatia paraproteinemica), neuronopatia sensibile nelle malattie immunitarie sistemiche e polineuropatie paraneoplastiche.
Fisiopatologia e cambiamenti elettrofisiologici delle nodo- e paranodopatie
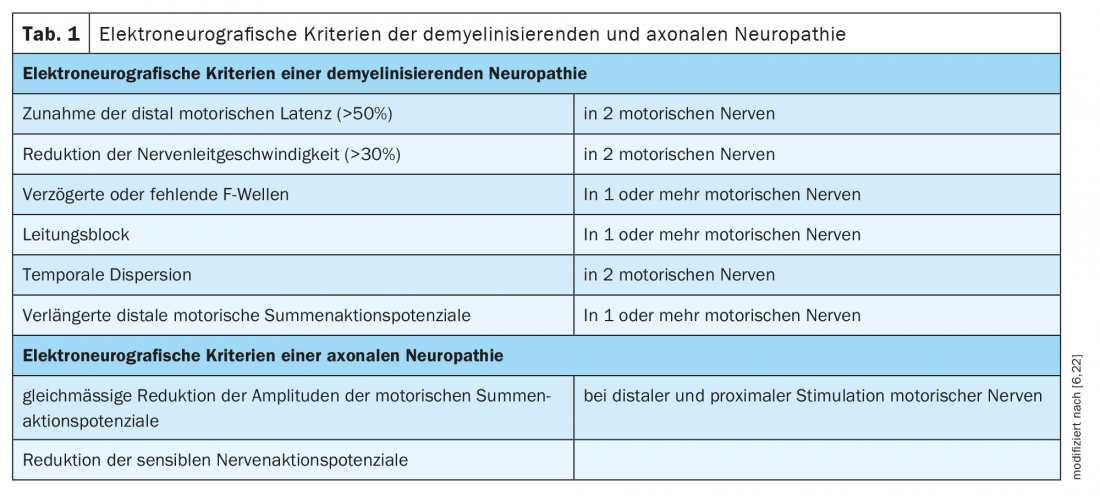
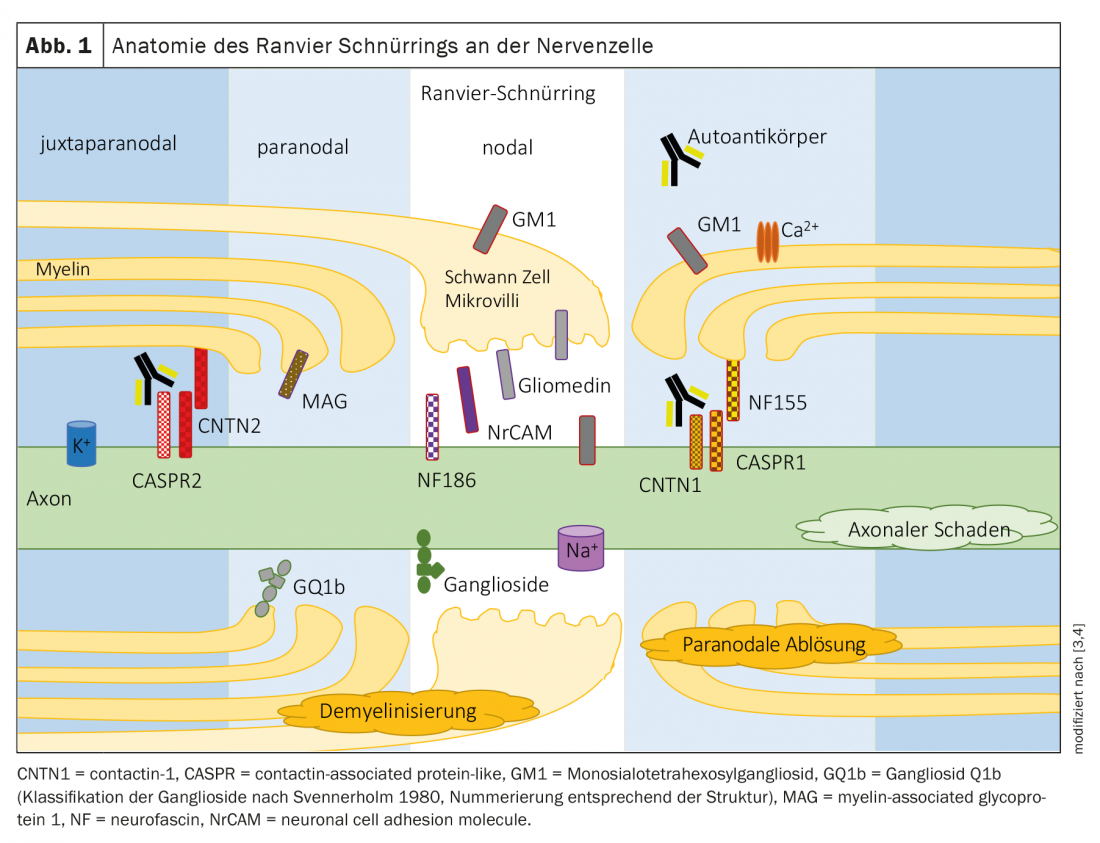
Le polineuropatie sono tradizionalmente suddivise in neuropatie demielinizzanti e assonali in base ai criteri dell’elettrofisiologia (Tab. 1). Si prevede che la patologia di base sia a livello della cellula mielinica/swan o dell’assone. Le proteine della regione nodale o paranodale dell’anello di Ranvier sono giunzioni tra la mielina/microvilli della cellula di Schwan e l’assone (Fig. 1) . Nelle neuropatie dovute ad autoanticorpi contro le proteine nodali e paranodali, non è possibile una chiara assegnazione a un modello demielinizzante o assonale, a causa del patomeccanismo sottostante. Il termine nodo- e paranodopatie è stato proposto da Uncini, Susuki e Yuki nel 2013 [8,9].
Le caratteristiche della nodo- e della paranodopatia sono
- Gli anticorpi contro le proteine nodali e paranodali hanno eziologie diverse, ma tutti portano a disfunzioni nella regione nodale dell’anello di Ranvier.
- Il continuum patologico va dal blocco di conduzione transitorio alla degenerazione assonale.
- Blocco di conduzione dovuto al distacco della mielina dall’assone, all’allargamento della regione nodale o alla disfunzione/interruzione dei canali del sodio (alta densità nella regione nodale per la conduzione saltatoria) con polarizzazione segmentaria anomala dell’assolema.
- Il blocco di conduzione può essere rapidamente reversibile senza la comparsa di una dispersione temporale significativa; il blocco di conduzione può anche persistere.
- La degenerazione assonale dipende dalla malattia specifica e dalla sua gravità, eventualmente seguita da un blocco di conduzione.
- La diagnosi può essere fatta con esami elettrofisiologici ripetuti:
- a. nella malattia acuta, nel caso di un blocco di conduzione o di una riduzione della velocità di conduzione nervosa rapidamente reversibile, senza una marcata dispersione temporale o una progressione del blocco di conduzione verso la degenerazione assonale;
- b. nelle malattie croniche con blocco di conduzione persistente e ulteriori segni di degenerazione assonale.
L’uso del termine nodo- e paranodopatie pone l’attenzione sulla localizzazione del danno nervoso primario e aiuta a classificare meglio la neuropatia demielinizzante segmentale, il paradosso del danno assonale reversibile e la buona prognosi, nonostante le anomalie assonali in elettrofisiologia [9].
Autoanticorpi nella polineuropatia demielinizzante infiammatoria cronica (CIDP)
Localizzazione: nella regione paranodale, il complesso di contattina 1 e CASPR1 sull’assone e di neurofascina 155 sulla cellula gliale della guaina mielinica consolida il contatto tra i processi mielinici e l’assone (Fig. 1) [10].
Anti Contactina 1 (CNTN1) IgG
- Sintomi: il 20 – 49% presenta un esordio subacuto della malattia. È noto un esordio dei sintomi aggressivo simile alla GBS, con paresi ad esordio subacuto (casistica). È tipica una neuropatia prevalentemente motoria e spesso si osserva un’atassia sensoriale. La comparsa di tremore è più frequente che nella CIDP sieronegativa, ma meno frequente che nella CIPD anti NF155-positiva. L’età di insorgenza è di circa 50-60 anni. Anno di vita. Complessivamente, è stata descritta un’età più alta all’esordio della malattia per i pazienti CIDP anti-CNTN1-positivi rispetto ai pazienti CIDP sieronegativi [2].
- Risultati: Gli esami elettroneurografici rivelano cambiamenti assonali all’inizio del decorso della malattia (Tab. 1) .
- Implicazioni per il trattamento: I pazienti rispondono in modo inadeguato alle immunoglobuline per via endovenosa (IVIg). I corticosteroidi hanno un buon effetto. Se la risposta alla terapia standard è insufficiente, la terapia di deplezione delle cellule B con rituximab è efficace [14]. Va notato che è importante mantenere la durata della malattia il più breve possibile, in modo da minimizzare il danno assonale [8]. In caso di immunoterapia efficace, i titoli sierici di anti CNTN1 diminuiscono [11].
Proteina 1 associata alla contattina (CASPR1) IgG
- Sintomi: Nei pazienti sieropositivi anti CASPR1 è stato descritto un dolore neuropatico pronunciato. I sintomi di solito iniziano in modo subacuto con un’espressione grave e sono inizialmente enfatizzati a livello motorio. Gli anti CASPR1 sono stati rilevati nei pazienti con CIDP e GBS. L’esordio della malattia è riportato in un caso clinico intorno ai 30 anni.
- Risultati: I blocchi di conduzione reversibili possono essere rilevati nelle indagini elettrofisiologiche [11].
- Implicazioni per il trattamento: È stata descritta la mancanza di risposta all’IVIg e al metilprednisolone. Il rituximab ha dimostrato un’ottima efficacia. Il dolore neuropatico associato migliora con una terapia efficace [2].
Anti Neurofascina 155 (NF155) IgG
- Sintomi: in genere, un’alta percentuale di pazienti CIDP NF155-positivi presenta una debolezza enfatizzata a livello distale. Altri sintomi possono includere tremore ad alta ampiezza e bassa frequenza e atassia sensoriale con segni cerebellari. L’associazione con HLA-DRB1*15 è stata descritta [12]. L’età di insorgenza è significativamente più giovane rispetto alla CIPD sieronegativa, con un’età di insorgenza intorno ai 20-30 anni.
- Risultati: L’esame elettrofisiologico mostra un modello demielinizzante con un chiaro prolungamento delle latenze distali e delle latenze delle onde F (Tab. 1). Nel liquido cerebrospinale è stato rilevato un forte aumento della proteina [13].
- Implicazioni per il trattamento: La risposta all’IVIg è scarsa. È stato descritto un miglioramento parziale con i corticosteroidi. Ci si può aspettare un buon successo terapeutico con rituximab e plasmaferesi [14]. I titoli sierici di anti NF155 diminuiscono in caso di immunoterapia efficace ed è stata dimostrata una correlazione con il miglioramento clinico [11].
Anti Neurofascina 140/186 (NF 140/186) IgG
- Sintomi: I pazienti presentano -una poli-culopatia sensomotoria simmetrica con un decorso grave. Possono verificarsi anche atassia sensoriale e coinvolgimento dei nervi cranici. Alcuni pazienti presentavano una malattia autoimmune concomitante. L’età di insorgenza è di circa 50-60 anni. descritto durante il primo anno di vita [2].
- Risultati: L’elettroneurografia ha rivelato risultati demielinizzanti con blocchi di conduzione (in 3/5 pazienti) e caratteristiche assonali (in 2/5 pazienti) [15].
- Implicazioni per il trattamento: Con IVIg e corticosteroidi, i sintomi sono parzialmente migliorati. È stata descritta una risposta potenzialmente buona al rituximab [14].
Autoanticorpi nelle polineuropatie infiammatorie acute – sindrome di Guillain-Barré (GBS) con i sottotipi AIDP, AMAN e AMSAN
Localizzazione: i canali ionici dell’anello di Ranvier sono stabilizzati dai gangliosidi, glicosfingolipidi contenuti nella membrana cellulare delle regioni nodali e paranodali [16]. I diversi sottotipi della sindrome di Guillain-Barré sono ciascuno associato ad autoanticorpi contro gangliosidi diversi e differiscono nei risultati elettrofisiologici.
La polineuropatia demielinizzante infiammatoria acuta (AIDP) è il sottotipo più comune di GBS in Europa e in Nord America. Di solito, in questo caso non si rilevano autoanticorpi specifici.
- Sintomi: La malattia è spesso preceduta da un’infezione gastrointestinale o respiratoria. All’inizio si verificano ipoestesia, parestesia, paresi e dolore alle estremità. Le paresi sono bilaterali, simmetriche e progressive. I sintomi motori si sviluppano da 12 ore a 28 giorni, fino alla tetraparesi con coinvolgimento dei muscoli respiratori. Inoltre, possono verificarsi deficit dei nervi cranici e disfunzioni autonomiche [4].
- Risultati: questo sottotipo demielinizzante di polineuropatia infiammatoria acuta è caratterizzato da una marcata riduzione della velocità di conduzione nervosa, da un aumento delle latenze motorie distali, da blocchi di conduzione, da una dispersione temporale anomala, da latenze delle onde F prolungate o dall’assenza di onde F [17].
Anti LM1 (sialosilneolactotetraosilceramide)
Gli autoanticorpi contro LM1 (sialosilneolactotetraosilceramide) causano una polineuropatia demielinizzante infiammatoria acuta (AIDP) se sono monospecifici. Sono stati descritti casi in cui gli anticorpi IgG anti LM1 causano una reazione incrociata con gangliosidi come GM1, GalNAc-GD1a, GD1b e GQ1b, per cui in questo caso si può fare la diagnosi di AMAN o AMSAN.
Anti GalC (galattocerebroside)
Autoanticorpi contro i galattocerebrosidi (GalC) sono stati rilevati nei bambini con polineuropatia demielinizzante acuta grave associata a M. pneumoniae (AIDP) [18].
Anti Neurofascina 186, Anti Gliomedina, Anti NrCAM, Anti CNTN1, Anti Neurofascina 155, Anti CASPR1 e Anti CASPR2
Negli studi sono stati rilevati gli autoanticorpi nodali anti neurofascina 186, anti gliomedina e anti NrCAM, e gli autoanticorpi paranodali anti CNTN1, anti neurofascina 155 e anti CASPR1 (vedere sopra nella sezione CIDP) nei pazienti adulti con GBS. Autoanticorpi juxtaparanodali contro CASPR2 sono stati descritti in 2 casi di GBS nei bambini.
La neuropatia assonale motoria acuta (AMAN) si verifica principalmente in Asia [19].
- Sintomi: corrispondenti all’AIDP (vedere sopra) senza disturbi sensoriali.
- Risultati: questo sottotipo assonale di polineuropatia infiammatoria acuta è caratterizzato da una marcata riduzione dell’ampiezza del potenziale d’azione cumulativo motorio (CMAP) e dal cosiddetto “fallimento reversibile della conduzione”, vale a dire che l’ampiezza ridotta del CMAP e i blocchi di conduzione possono improvvisamente riprendersi con esami elettroneurografici ripetuti, senza evidenza di dispersione temporale come segno di rimielinizzazione. [16].
Anti-GM1 IgG, Anti-GM2, Anti-GD1b IgG, Anti-GT1b, Anti- GM3, Anti-GD1a IgG e Anti-GalNac-GD1a
Gli anticorpi gangliosidi anti-GM1 IgG, anti-GM2, anti-GD1b, anti-GT1b, anti-GM3, anti-GD1a IgG e anti-GalNac-GD1a possono essere rilevati in circa l’80% dei pazienti con AMAN. Questi autoanticorpi possono presentarsi singolarmente o in combinazione.
Neuropatia assonale acuta motoria e sensoriale (AMSAN)
- Sintomi: vedere AIDP
- Risultati: stessi criteri di AMAN più riduzione dell’ampiezza del potenziale d’azione del nervo sensoriale (Unicini et al. 2018).
IgG anti-GM1, anti-GM1b, IgG anti-GD1a
Gli anticorpi ganglioside anti-GM1, anti-GM1b, anti-GD1a sono rilevabili nella neuropatia assonale acuta motoria e sensoriale (ASMAN) [19].
Autoanticorpi nella sindrome di Miller Fisher (MFS)
Localizzazione: il ganglioside GQ1b si trova principalmente nella mielina paranodale dei nervi cranici che forniscono i muscoli oculari [19].
Anti GQ1b IgG
- Sintomi: L’oftalmoplegia acuta, la neuropatia atassica acuta e l’areflessia sono i sintomi principali della sindrome di Miller-Fisher. Nell’encefalite del tronco encefalico di Bickerstaff, si verificano oftalmoplegia e atassia, alterazione della coscienza e di solito iperreflessia.
Gli autoanticorpi GQ1b possono essere rilevati nel 90% dei pazienti con sindrome di Miller Fisher (MFS). La sindrome di Miller-Fisher e l’encefalite del tronco encefalico di Bickerstaff sono associate agli anticorpi anti-GQ1b, quindi Shahrizaila e Yuki raggruppano le malattie come sindrome da anticorpi anti-GQ1b [20].
Autoanticorpi nella neuropatia motoria multifocale (MMN)
Localizzazione: il ganglioside GM1 è localizzato principalmente nella regione nodale dell’anello di Ranvier. Gli autoanticorpi si legano alla regione nodale e attivano il complemento, influenzando il raggruppamento dei canali del sodio.
IgM anti GM1 e complesso anti GM1-galattocerebroside
- Sintomi: è caratteristica una paresi delle estremità in lento aumento, per lo più asimmetrica, che spesso inizia dagli arti superiori. Non sono stati riscontrati deficit sensibili. Inoltre, possono verificarsi tremori di tenuta, fascicolazioni e crampi.
- Risultati: gli anticorpi IgM anti-GM1 sono rilevabili nel 50% di tutti i pazienti con MMN [21]. I blocchi di conduzione possono essere rilevati negli esami elettrofisiologici. L’attivazione del complemento può causare un danno assonale.
- Implicazioni per il trattamento: Buona risposta all’IVIg. Il rilevamento degli autoanticorpi può supportare la diagnosi di MMN se non sono soddisfatti tutti i criteri e aiutare a iniziare una terapia efficace con IVIg. Clinicamente, si tratta di una malattia del secondo motoneurone, che rende la MMN un’importante diagnosi differenziale della sclerosi laterale amiotrofica [11].
Autoanticorpi nella polineuropatia MGUS (MGUS-P)
Localizzazione: la glucoproteina associata alla mielina (MAG) è localizzata nella mielina della regione paranodale.
Anti MAG (glucoproteina associata alla mielina) IgM
- Sintomi: è caratteristica una polineuropatia distale atassica lentamente progressiva, prevalentemente sensibile. Le estremità distali superiori sono spesso colpite [11]. La maggior parte dei pazienti ha un’età inferiore ai 50 anni.
- Risultati: Un modello demielinizzante è rilevabile nell’esame elettrofisiologico. L’immunofissazione rivela una gammopatia monoclonale IgM. Gli anticorpi anti MAG IgM sono positivi nel 50% dei pazienti con MGUS-P. Il livello del titolo anticorpale non sembra essere correlato alla gravità della malattia e alla risposta alla terapia. Il rilevamento degli autoanticorpi anti MAG è necessario solo per la diagnosi.
- Implicazioni per il trattamento: Alcuni studi hanno dimostrato una risposta alla plasmaferesi, alla ciclofosfamide, all’IVIg e al rituximab. Ci sono prove che la deplezione precoce delle cellule B con rituximab può influenzare la progressione [11].
Autoanticorpi associati alle malattie immunitarie sistemiche
Anticorpi SSA (Ro) e SSB (La), anticorpi antineuronali, anticorpo FGFR3 (recettore 3 del fattore di crescita dei fibroblasti)
- Sintomi: Nei pazienti (più giovani) con un decorso progressivo, acuto o subacuto della neuropatia/neuronopatia sensoriale, è utile la ricerca della sindrome di Sjögren o lo screening delle malattie autoimmuni [22].
- Risultati: Nel liquor c’è un lieve aumento delle proteine con una conta cellulare normale. Elettrofisiologicamente, sono rilevabili anomalie nei nervi sensibili che non dipendono dalla lunghezza. La perdita estesa o la bassa ampiezza dei potenziali d’azione del nervo sensoriale è tipica, così come la distribuzione clinica asimmetrica (“a chiazze”). Occasionalmente, i nervi sensibili delle braccia possono essere più colpiti di quelli delle gambe [23].
- Implicazioni terapeutiche: La malattia di base deve essere trattata.
In quale presentazione clinica si dovrebbe pensare a una genesi mediata da autoanticorpi?
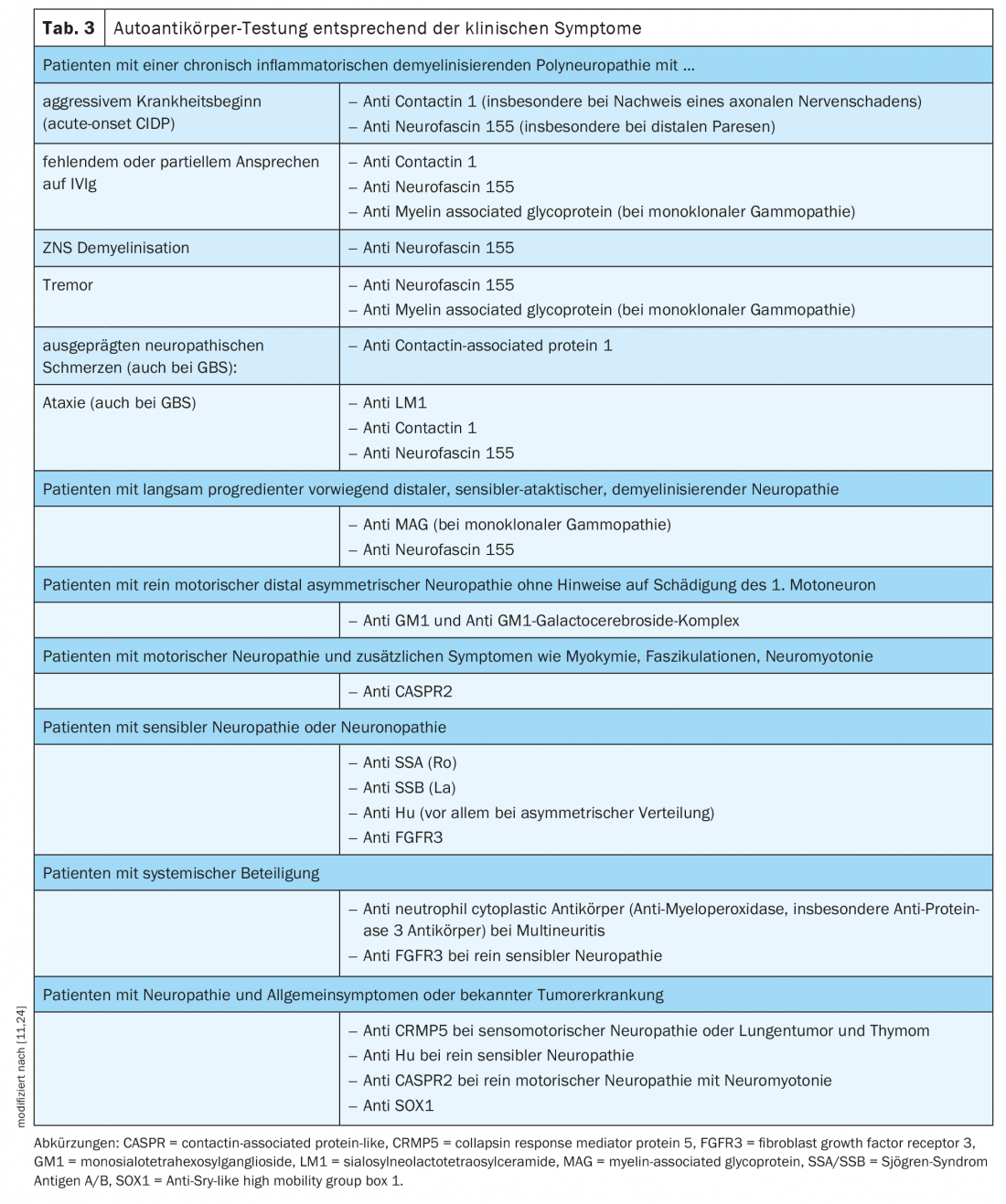
Il test per gli autoanticorpi nodali e paranodali deve essere eseguito nei pazienti con un decorso acuto, subacuto o cronico della polineuropatia demielinizzante acquisita associata a sintomi aggiuntivi come tremore, coinvolgimento distale o scarsa risposta all’IVIg [11] (Tabella 3).
Perché la terapia standard è spesso inadeguata per la polineuropatia demielinizzante infiammatoria cronica sieropositiva?
Gli studi hanno dimostrato che gli autoanticorpi nodali e paranodali appartengono a diverse sottoclassi di IgG (Tabella 4) . Le IgG2 e le IgG3 sono state riscontrate nella GBS monofasica anti CNTN1 e CASPR1 sieropositiva, le IgG4 solo nei decorsi cronici. Da Appeltshauser et al. È stato descritto che nel corso della malattia può verificarsi un cambiamento di classe da IgG3 a IgG4 nella neuropatia sieropositiva anti CNTN1 e anti CASPR1 [25]. Attualmente, le sottoclassi IgG degli autoanticorpi nodali e paranodali vengono determinate solo nei laboratori di ricerca.

Le neuropatie IgG3-mediate rispondono bene alla terapia standard con IVIg. L’IVIg è efficace nelle polineuropatie infiammatorie, in particolare attraverso l’inibizione del complemento e la neutralizzazione degli anticorpi. I pazienti con anticorpi IgG2 e IgG4 non mostrano alcun miglioramento con le infusioni di IVIg oppure la risposta diminuisce nel corso della malattia. La scarsa o assente risposta all’IVIg nelle malattie IgG4-mediate è attribuita alla bassa capacità di legare i recettori FcγIIb e alla mancanza di attivazione del complemento [14]. Nelle malattie autoimmuni neurologiche e non neurologiche mediate da IgG4, come la miastenia gravis positiva agli anti-muscoli, la pancreatite autoimmune e la colangite sclerosante, l’efficacia del rituximab è stata dimostrata in numerosi studi. L’effetto di deplezione delle cellule B del rituximab è fondamentale nella malattia IgG4-mediata. È stata riportata una risposta parziale dei pazienti con anticorpi IgG4 nodali e paranodali ai corticosteroidi [14]. Nelle neuropatie autoanticorpo-positive, è necessaria una terapia rapida ed efficace prima che si verifichi un danno irreversibile. In assenza di risposta alla terapia standard (IVIg e steroidi) per la polineuropatia demielinizzante infiammatoria cronica, si deve prendere in considerazione la terapia con rituximab.
Messaggi da portare a casa
- Nell’ambito delle neuropatie immuno-mediate, le nodo-/paranodopatie devono essere prese in considerazione per la diagnosi differenziale, poiché in questo caso esistono opzioni terapeutiche efficaci.
- La chimica di laboratorio può rilevare autoanticorpi contro le proteine nodali e paranodali dell’anello di Ranvier nelle nodo- e paranodopatie.
- Le caratteristiche elettroneurografiche sono definite per le nodo- e le paranodopatie.
- La base della diagnosi delle neuropatie associate ad autoanticorpi sono gli esami elettroneurografici (modello demielinizzante o assonale, caratteristiche delle nodo- e paranodopatie) e la diagnostica di laboratorio e del liquor (esclusione di diagnosi differenziali rilevanti, rilevamento della dissociazione della citalbumina nel liquor); è utile anche l’ecografia del nervo (modello di rigonfiamento del nervo).
- Esaminare gli autoanticorpi nodali e paranodali dal siero (nessuna produzione intratecale e titoli bassi nel liquor).
- In assenza di miglioramento con la terapia di prima linea (IVIg, steroidi) e nei pazienti con un decorso acuto o subacuto di polineuropatia demielinizzante acquisita con sintomi aggiuntivi come tremore, atassia e coinvolgimento distale (vedere Tabella 2: bandiere rosse nella CIDP), considerare la determinazione degli autoanticorpi e, se necessario, la terapia con rituximab.
- Selezione degli autoanticorpi in base ai sintomi clinici (Tab. 3).
Letteratura:
- Visser NA: Incidenza della polineuropatia a Utrecht, Paesi Bassi. Neurologia 2015, 20 gennaio; 84(3): 259-264.
- Vural A, Doppler K: Autoanticorpi contro il nodo di Ranvier nella polineuropatia demielinizzante infiammatoria cronica sieropositiva: rilevanza diagnostica, patogenetica e terapeutica. Anteriore. Immunol. 2018, 14 maggio; 9: 1029
- Stathopoulos P: Bersagli antigenici autoimmuni nel nodo di Ranvier nei disturbi demielinizzanti. Nat Rev Neurol. 2015 Mar; 11(3): 143-156.
- Kieseier BC, Mathey EK, Sommer C: Neuropatie immunomediate. Nat Rev Dis Primers 2018 4, 31.
- Svennerholm L: Designazione dei gangliosidi. Adv Exp Med Biol. 1980; 125: 11
- Grether NB, et al: Diagnostica delle polineuropatie immuno-mediate. DGNeurologia 2020; 3 (2): 147-158.
- Uncini A, Kuwabara S: Criteri elettrodiagnostici per la sindrome di Guillain-Barre: una revisione critica e la necessità di un aggiornamento. Clin Neurophysiol, 2012, 123(8), 1487-1495.
- Uncini A, Kuwabara S: Nodopatie del nervo periferico: un concetto emergente. J Neurol Neurosurg Psychiatry, 2015, 86(11), 1186-1195.
- Uncini A, Susuki K, Yuki N: Nodo-paranodopatia: oltre la classificazione demielinizzante e assonale nelle neuropatie mediate da anticorpi anti-ganglioside. Clin Neurophysiol, 2013, 124(10), 1928-1934.
- Poliak S, Peles E: La differenziazione locale degli assoni mielinizzati nei nodi di Ranvier. Nat Rev Neurosci, 2003, 4(12), 968-980.
- Querol L: Autoanticorpi nelle neuropatie infiammatorie croniche: implicazioni diagnostiche e terapeutiche, Nat Rev Neurol. Neurologia, 2017, settembre; 13(9): 533-547.
- Martinez-Martinez L: La poliradiculoneuropatia demielinizzante infiammatoria cronica anti-NF155 si associa fortemente all’HLA-DRB15. J Neuroinflammation 2017; 14: 224.
- Kadoya M: Anticorpi IgG4 anti-neurofascina155 nella poliradiculoneuropatia demielinizzante infiammatoria cronica: significato clinico e utilità diagnostica di un test convenzionale. Journal of Neuroimmunology 2016 Dec 15; 301: 16-22.
- Bunschoten C: Progressi nella diagnosi e nel trattamento della poliradiculoneuropatia demielinizzante cronica infiammatoria, Lancet Neurology 2019; 18: 784-94.
- Delmont E, Manso C, Querol L, et al: Autoanticorpi contro le isoforme nodali della neurofascina nella polineuropatia demielinizzante infiammatoria cronica. Cervello. 2017 Jul 1;140(7): 1851-1858.
- Susuki K: I gangliosidi contribuiscono alla stabilità delle giunzioni paranodali e dei cluster di canali ionici nelle fibre nervose mielinizzate. Glia, 2007a, 55(7): 746-757.
- Uncini A, Kuwabara S: L’elettrodiagnosi dei sottotipi della sindrome di Guillain-Barré: A che punto siamo? Neurofisiologia clinica. 2018 Dec; 129(12): 2586-2593.
- Meyer Sauteur PM: Mycoplasma pneumoniae che scatena la sindrome di Guillain-Barré: uno studio caso-controllo, Ann Neurol 2016 Oct; 80(4): 566-580.
- Pei S: Varianti assonali della sindrome di Guillain-Barré: un aggiornamento. Springer Nature 2020 marzo.
- Shahrizaila N, Yuki N: Encefalite del tronco encefalico di Bickerstaff e sindrome di Fisher: sindrome da anticorpi anti-GQ1b. J Neurol Neurosurg Psychiatry 2013, 84: 576-583.
- Van Asseldonk JT: Neuropatia motoria multifocale. Lancet Neurol, 2005, 4(5): 309-319.
- Heuss D: Diagnostik bei Polyneuropathien, S1-Leitlinie, 2019, in: Deutsche Gesellschaft für Neurologie (Hrsg.), Leitlinien für Diagnostik und Therapie in der Neurologie. Online: www.dgn.org/leitlinien. (recuperato il 01.04.2021).
- Sghirlanzoni A: Malattie dei neuroni sensoriali. The Lancet Neurology. 2005; 4(6): 349-361
- Sun X: Anticorpi anti-SOX1 nella sindrome neurologica paraneoplastica. J Clin Neurol. 2020 Oct;16(4):530-546.
- Appeltshauser L: Anticorpi antiparanodali e sottoclassi IgG nella neuropatia acuta autoimmune. Neurol Neuroimmunol Neuroinflamm. 2020 Jul 24; 7(5): e 817.
- Ilyas A: Distribuzione della sottoclasse di immunoglobuline G degli autoanticorpi contro i gangliosidi nei pazienti con sindrome di Giullain-Barre. Res Commun Mol Pathol Pharmacol. 2001 Jul; 109(1-2): 115-123.
- Lardone RD: Gli anticorpi IgG anti-glicosfingolipidi associati ai disturbi neurologici mostrano una distribuzione differenziata delle sottoclassi IgG. Sci Rep. 2020 Aug 4;10(1): 13074.
InFo NEUROLOGIA & PSICHIATRIA 2021; 19(3): 19-25.