Finora, i test molecolari nel carcinoma polmonare non a piccole cellule (NSCLC) sono stati riservati principalmente ai pazienti in stadio IV. Tuttavia, con l’introduzione di terapie mirate anche negli stadi tumorali più precoci, questa situazione potrebbe presto cambiare: una grande opportunità che, tuttavia, pone anche molte sfide alla pratica clinica quotidiana.
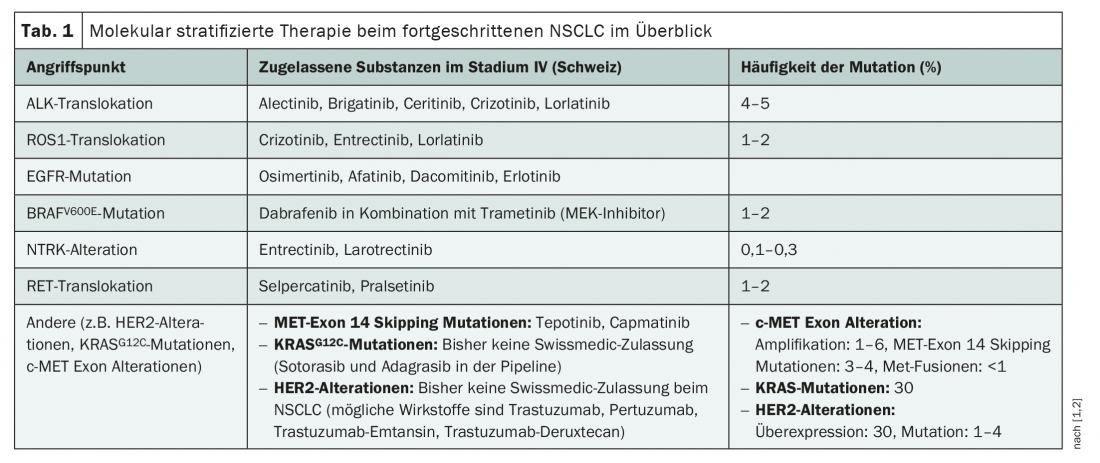
Con terapie che mirano specificamente a ROS1, ALK, EGFR, BRAF, ma anche TRK e RET, esistono già numerose opzioni di trattamento mirato per il NSCLC (tab. 1). Tuttavia, ad eccezione dell’inibitore dell’EGFR osimertinib, questi farmaci sono stati finora approvati in Svizzera solo per il trattamento dei tumori localmente avanzati e metastatici [1]. Di conseguenza, la diagnosi di mutazioni rilevanti per la terapia è raccomandata solo nello stadio IV, prima dell’inizio della terapia di prima linea [2]. In ogni caso, devono essere registrate le traslocazioni ALK, le mutazioni BRAFV600E, le mutazioni EGFR esone 18-21, le fusioni NTRK, le traslocazioni RET e le traslocazioni ROS1 [2] – perché esistono concetti terapeutici approvati per questi cambiamenti. Tuttavia, la terapia mirata nel NSCLC sta subendo un rapido cambiamento e con essa i test molecolari. Da un lato, questo potrebbe essere ampliato nel prossimo futuro con ulteriori obiettivi, dato che ci sono alcune nuove sostanze in cantiere. D’altra parte, i farmaci oncologici mirati vengono sempre più testati per l’uso neoadiuvante e adiuvante negli stadi tumorali più precoci – con successo, come dimostra la recente approvazione di osimertinib nel contesto adiuvante. La logica conseguenza: la classificazione molecolare dei tumori potrebbe essere utile già per i tumori di stadio I-III.
Altri punti di attacco in vista
Attualmente, oltre a quelle note, sono sotto i riflettori numerose altre mutazioni del conducente. Nel prossimo futuro, ad esempio, potrebbero essere approvati diversi agenti mirati diretti contro HER2 o KRAS, tra gli altri. Solo ad aprile e giugno di quest’anno, rispettivamente, sono stati lanciati sul mercato svizzero gli inibitori MET altamente specifici, capmatinib e tepotinib, per il trattamento del NSCLC metastatico con una mutazione di skipping dell’esone 14 del recettore della tirosin-chinasi MET [1]. Questa alterazione genetica colpisce il 3-4% dei pazienti con NSCLC ed è associata a una prognosi sfavorevole [2].
Nello studio pivotal VISION, che ha incluso 152 pazienti per lo più pretrattati con la mutazione di skipping dell’esone 14 di MET, tepotinib ha determinato un tasso di risposta obiettiva del 44,7% con una sopravvivenza mediana libera da progressione (PFS) di 8,9 mesi [1]. Per capmatinib, il tasso di risposta obiettiva nello studio pivotal GEOMETRY mono-1 ha raggiunto il 67,9% e la PFS mediana è stata di 9,69 mesi. Restano da vedere ulteriori dati sulla sopravvivenza globale e il confronto dell’efficacia con il trattamento immunochemioterapico standard. Quello che è già certo è che il test per le mutazioni che saltano l’esone 14 della MET probabilmente amplierà lo standard diagnostico in futuro.
Anche le mutazioni KRAS e le aberrazioni HER2 potrebbero presto essere aggiunte alla diagnostica molecolare nel NSCLC. Anche se in Svizzera non sono ancora state approvate terapie specifiche per questi obiettivi, c’è molto in cantiere. Ad esempio, soterasib e adagrasib sono stati i primi inibitori di KRASG12C ad essere sviluppati e sono attualmente in fase di sperimentazione clinica. Una domanda di autorizzazione all’immissione in commercio nell’UE per soterasib è stata depositata ed è prevista per la fine di quest’anno, mentre la Food and Drug Administration (FDA) statunitense ha già concesso un’approvazione preliminare per il trattamento di pazienti pretrattati con mutazione KRASG12C [3,4]. Circa il 13% dei pazienti affetti da NSCLC potrebbe beneficiare di un lancio sul mercato: questa è la frequenza della mutazione KRASG12C [3]. Nello studio di fase II CodeBreak 100, 124 pazienti pretrattati con mutazione KRASG12C hanno mostrato un tasso di risposta del 37,1% a suterasib, con una PFS mediana di 6,8 mesi e una OS mediana di 12,5 mesi [5]. A differenza di KRAS, esistono già agenti come trastuzumab, pertuzumab e i coniugati anticorpo-farmaco trastuzumab emtansine e trastuzumab deruxtecan per colpire HER2. Sebbene il loro uso sia stato studiato in alcuni studi clinici nel NSCLC, non ci sono stati confronti diretti con l’immunochemioterapia e non c’è stata finora alcuna approvazione di Swissmedic per il NSCLC [1,2].
Terapia adiuvante e neoadiuvante in transizione
Oltre ad ampliare la caratterizzazione molecolare del NSCLC, potrebbe aumentare anche la sua importanza negli stadi tumorali più precoci. Osimertinib è all’inizio. Quest’anno, l’inibitore dell’EGFR è stato approvato in Svizzera per il trattamento adiuvante dei pazienti con NSCLC non squamoso con delezioni dell’esone 19 dell’EGFR o mutazioni di sostituzione dell’esone 21 (L858R) dopo la resezione completa del tumore [1]. Ciò si basa sullo studio ADAURA, in cui la terapia adiuvante per tre anni negli stadi II e IIIA dopo resezione R0 ha portato a un miglioramento significativo della sopravvivenza libera da malattia rispetto al placebo (HR 0,17; p<0,001) [2]. La maggior parte dei partecipanti allo studio ha ricevuto anche una chemioterapia adiuvante. La nuova opzione del trattamento mirato adiuvante rappresenta una speranza per i pazienti affetti da NSCLC con mutazione EGFR – e richiede una selezione adeguata dei pazienti.
È probabile l’approvazione di ulteriori agenti mirati nel contesto adiuvante e neoadiuvante. Per questo motivo, diventano necessarie strategie eque e uniformi di test molecolari. Sebbene molte linee guida non includano ancora una raccomandazione per l’analisi molecolare negli stadi tumorali I-III, le linee guida del Il National Comprehensive Cancer Networks (NCCN) e l’Asian Thoracic Oncology Research Group, le Raccomandazioni di consenso canadesi, le linee guida cinesi per la diagnosi e il trattamento del tumore polmonare primario e il consenso della Society for Translational Medicine raccomandano almeno il test EGFR. Questo ha senso non solo in vista della nuova opzione terapeutica, ma anche perché le mutazioni EGFR sono le cosiddette mutazioni tronche: Sono presenti fin dall’inizio, la loro prevalenza non cambia quasi mai da una fase all’altra. Oltre agli inibitori dell’EGFR, gli inibitori di ALK, come alectinib, sono attualmente in fase di sperimentazione nella terapia neoadiuvante, adiuvante e di mantenimento del NSCLC. Le linee guida probabilmente rimarranno sempre un po’ indietro rispetto a questi sviluppi – e la loro implementazione nella pratica clinica quotidiana richiederà a sua volta un po’ di tempo. Ciò rende ancora più importante valutare ogni paziente individualmente e, in vista delle numerose nuove possibilità, pensare fuori dagli schemi delle strutture consolidate.
Fonte: Aggarwal C, et al.: Test molecolari nel carcinoma polmonare non a piccole cellule in stadio I-III: approcci e sfide. Cancro al polmone. 2021; 162: 42-53.
Letteratura:
- Informazioni sui farmaci di Swissmedic: www.swissmedicinfo.ch (ultimo accesso 25.11.2021).
- Griesinger F, et al: Linee guida dell’Oncopedia: Cancro al polmone, non a piccole cellule (NSCLC). Stato luglio 2021. www.onkopedia.com/de/onkopedia/guidelines/lungenkarzinom-nicht-kleinzellig-nsclc/@@guideline/html/index.html (ultimo accesso 25.11.2021).
- Whitlock Burton K: La FDA approva Sotorasib come prima terapia mirata per il NSCLC con mutazioni KRAS G12C. 03.06.2021. www.univadis.de (ultimo accesso il 25.11.2021).
- DGHO: Richiesta campione NUB Sotorasib 2021/2022. www.dgho.de (ultimo accesso il 25.11.2021).
- Skoulidis F, et al: Sotorasib per i tumori del polmone con mutazione KRAS p.G12C. New England Journal of Medicine. 2021; 384(25): 2371-2381.
InFo ONcOLOGIA & EMATOLOGIA