La deplezione delle cellule B e i risultati dello studio ORATORIO, recentemente pubblicati sul New England Journal of Medicine, sono stati sulla bocca di tutti al Forum ACTRIMS 2017. Anche perché il processo di approvazione negli Stati Uniti è attualmente in pieno svolgimento. Ora si tratta di classificare i dati ed esaminare la loro rilevanza clinica. Al congresso, sono stati ripresi alcuni risultati interessanti su questo tema. Dove si inserirà il nuovo anticorpo – e quindi la prima terapia diretta alle cellule B per la SM – nello spettro terapeutico?
Anche ai precedenti congressi ECTRIMS, è stato difficile evitare l’argomento della deplezione delle cellule B nella SM, tanto è stato discusso in modo prominente. Nel frattempo, ORATORIO, uno studio di fase III che testa l’anticorpo ocrelizumab nella sclerosi multipla primaria progressiva (SM), è stato pubblicato sul NEJM [1]. In questo studio, l’anticorpo, che mira in modo selettivo e specifico alle cellule B CD20-positive, ha mostrato una riduzione significativa del rischio del 24% (32,9% vs. 39,3%) nell’endpoint primario definito come progressione della disabilità nell’arco di dodici settimane (cioè aumento della Expanded Disability Status Scale, EDSS) in un totale di 732 pazienti randomizzati rispetto al placebo. 39,3%) negli endpoint secondari come la progressione in un periodo di 24 settimane, una riduzione significativa del rischio del 25% (29,6% vs. 35,7%), un deterioramento meno grave nella camminata a tempo di 25 piedi (T25-FW) del 38,9% a 120 settimane (vs. 55,1% con placebo) e una diminuzione minore del volume cerebrale.
La tolleranza è stata valutata come provvisoriamente buona – come negli studi paralleli con decorso recidivante-remittente. Con l’anticorpo somministrato per via endovenosa, si sono verificate più reazioni associate all’infusione, infezioni del tratto respiratorio superiore e herpes orale, ma non ci sono state differenze clinicamente significative nei tassi di eventi avversi gravi e infezioni. I tumori sono stati riscontrati nel 2,3% (ocrelizumab) e nello 0,8% (placebo) dei partecipanti.
Classificazione dei risultati
Al Forum ACTRIMS 2017 si è anche convenuto che i risultati sono di grande rilevanza per i pazienti con SM primariamente progressiva, in quanto l’anticorpo CD20 è la prima sostanza in grado di rallentare questa forma di SM in uno studio di fase III. La SM primariamente progressiva è caratterizzata da un accumulo costante di disabilità fin dall’esordio della malattia (con/senza plateau temporanei nella progressione). Rallentare la progressione della disabilità è quindi un obiettivo terapeutico importante, che finora non è stato quasi raggiunto negli studi clinici [2–4]. Questo dovrebbe ora cambiare con ocrelizumab. Inoltre, il composto viene studiato in due ulteriori studi di fase III nella SM recidivante-remittente (OPERA) [5], dove è stato ottenuto un effetto significativamente più favorevole rispetto al trattamento con interferone ad alte dosi. Ora si tratta di attendere i dati a lungo termine, che saranno rilevanti sia in termini di efficacia che di sicurezza.
La vera novità di ocrelizumab è l’approccio terapeutico. Invece di colpire le cellule T responsabili dell’attacco alle guaine mieliniche dei nervi del sistema nervoso centrale, come fa la maggior parte dei farmaci per la SM, l’anticorpo si lega alle proteine di superficie CD20 espresse su alcune cellule B (più precisamente, cellule B-precursori fino allo stadio di plasmablasto, ma non cellule B-stem/pro-B né plasmacellule, preservando così importanti funzioni del sistema immunitario).
Il ruolo delle cellule B è stato a lungo sottovalutato nella ricerca. Tuttavia, le cellule B che migrano nel SNC hanno il potenziale di influenzare in modo fondamentale la fisiopatologia della SM attraverso diversi meccanismi. Le loro funzioni includono la produzione di citochine e autoanticorpi, nonché la presentazione/costimolazione dell’antigene – tutti fattori che potrebbero contribuire direttamente o indirettamente al danno della guaina mielinica o dell’assone e quindi alla disabilità nei pazienti con SM.
La spinta a sviluppare ocrelizumab è stata preceduta dalla scoperta che il rituximab, che distrugge selettivamente anche le cellule B, può ottenere risultati sorprendenti nella SM. Anche nel caso della forma primaria progressiva, che finora non è stata quasi mai trattata in modo efficace, si ottiene un rallentamento della progressione – almeno nei pazienti più giovani e in quelli con lesioni arricchite di gadolinio [3]. Lo sviluppo di un anticorpo anti-CD20 più recente, questa volta completamente umanizzato (il rituximab è un anticorpo chimerico topo/umano) promette una migliore tollerabilità. La decisione di non investire ulteriormente nel “vecchio rappresentante” rituximab, ma di promuovere al suo posto ocrelizumab, è probabilmente legata anche alla scadenza della protezione brevettuale del rituximab.
In linea con i risultati per il rituximab, i partecipanti allo studio ORATORIO erano più giovani o più anziani. ha avuto la SM per meno di 10 o 15 anni (a seconda del grado di disabilità). La popolazione era quindi “arricchita”, come si direbbe in inglese, il che potrebbe aver favorito ulteriormente i risultati positivi. Resta da vedere se questa selezione si rifletterà nel testo di ammissione. Ciò che è certo è che ocrelizumab è un agente potente, soprattutto per quanto riguarda la sua attività antinfiammatoria.
NEP – un endpoint clinicamente rilevante
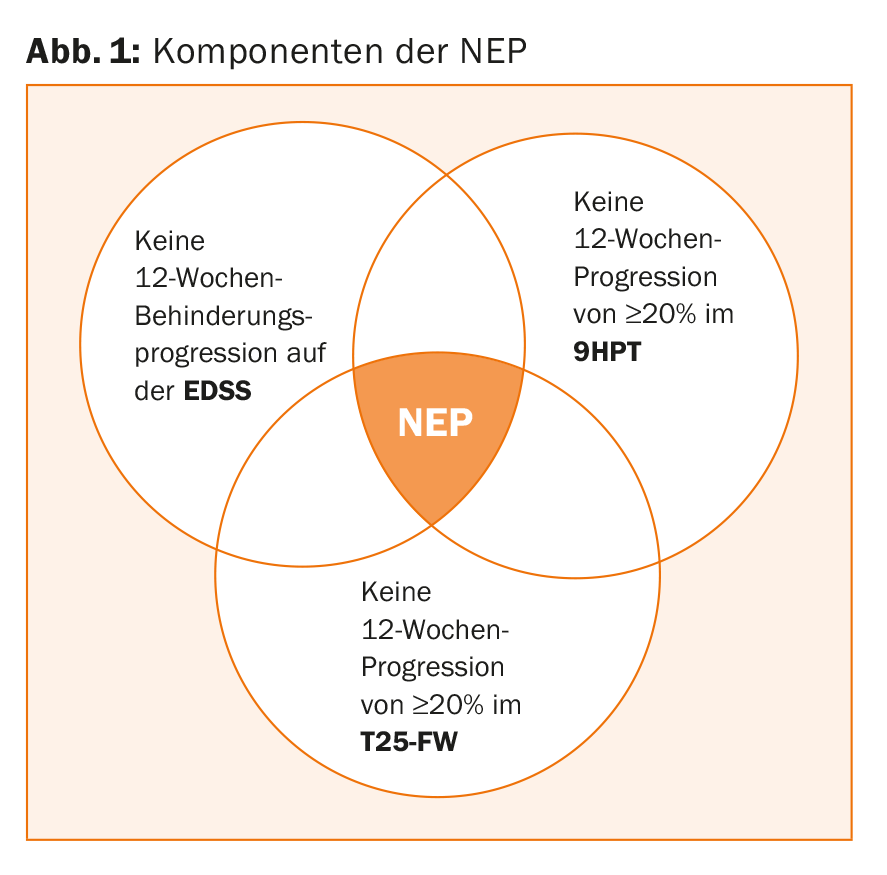
Ora, in un’ulteriore analisi dello studio ORATORIO presentata al Forum ACTRIMS 2017, i ricercatori si sono chiesti in che misura la progressione della disabilità si rifletta nella cosiddetta “non evidenza di progressione” (NEP). La NEP è un endpoint composito clinicamente rilevante che, oltre all’EDSS, comprende anche altre importanti misure di disabilità, ovvero il cosiddetto Nine-Hole Peg Test (9HPT) e il T25-FW. Questi forniscono informazioni sull’effettiva stabilizzazione clinica della malattia. Il 9HPT verifica quanto tempo impiega il paziente a posizionare nove perni nei fori designati e poi a rimuoverli di nuovo. Questo test offre una buona sensibilità per valutare la destrezza manuale nelle persone con SM. Nel T25-FW, al paziente viene chiesto di camminare per 25 piedi nel modo più veloce e sicuro possibile. Il tempo viene fermato durante il processo. In particolare, l’endpoint NEP richiesto (Fig. 1):
- Nessuna progressione della disabilità sull’EDSS
- Nessuna progressione di ≥20% negli arti superiori (9HPT)
- Nessuna progressione di ≥20% in corso (T25-FW).
Per l’analisi esplorativa, i ricercatori hanno potuto valutare i dati di 691 dei 732 pazienti totali, nel periodo compreso tra il basale e le 120 settimane. Il risultato è stato un aumento relativo della probabilità di non subire una progressione della disabilità in uno dei tre test del 47% con ocrelizumab (RR 1,47, 95% CI 1,17-1,84, p=0,0006). In particolare, il 42,7% del gruppo ocrelizumab ma solo il 29,1% del gruppo placebo ha raggiunto la NEP. Anche quando l’endpoint composito è stato sezionato, i benefici dell’anticorpo anti-CD20 sono rimasti sorprendenti (Tabella 1).

Il beneficio di ocrelizumab nella NEP integra i risultati degli endpoint primari e secondari di ORATORIO in modo coerente. Il quadro generale è quello di un rallentamento della disabilità sia negli arti superiori che in quelli inferiori. Per i pazienti con SM primariamente progressiva, si tratta di una (tanto attesa) buona notizia. Anche i risultati degli studi OPERA sulla SM recidivante-remittente sono promettenti. Resta da vedere quale sarà il testo finale dell’approvazione. La FDA prenderà la sua decisione alla fine di marzo, cioè in questi giorni. Nel frattempo, il farmaco continuerà certamente ad essere un argomento di conversazione nei congressi sulla SM.
Fonte: Forum dell’Americas Committee for Treatment and Research in Multiple Sclerosis (ACTRIMS), 23-25 febbraio 2017, Orlando.
Letteratura:
- Montalban X, et al: Ocrelizumab contro placebo nella sclerosi multipla primaria progressiva. N Engl J Med 2017; 376: 209-220.
- Wolinsky JS, et al: Glatiramer acetato nella sclerosi multipla primaria progressiva: risultati di uno studio multinazionale, multicentrico, in doppio cieco, controllato con placebo. Ann Neurol 2007; 61: 14-24.
- Hawker K, et al: Rituximab nei pazienti con sclerosi multipla primaria progressiva: risultati di uno studio multicentrico randomizzato in doppio cieco controllato con placebo. Ann Neurol 2009; 66: 460-471.
- Lublin F, et al: Fingolimod orale nella sclerosi multipla primaria progressiva (INFORMS): uno studio di fase 3, randomizzato, in doppio cieco, controllato con placebo. Lancet 2016; 387: 1075-1084.
- Hauser SL, et al: Ocrelizumab rispetto all’interferone beta-1a nella sclerosi multipla recidivante. N Engl J Med 2017; 376: 221-234.
InFo NEUROLOGIA & PSICHIATRIA 2017; 15(2): 33-36