Al meeting annuale della Società Svizzera di Cardiologia a Zurigo, una sessione principale era dedicata all’insufficienza cardiaca acuta. Sono stati presentati nuovi risultati e studi in campo farmacologico e sono state discusse le strategie terapeutiche. Nello shock cardiogeno, la forma più grave di insufficienza cardiaca acuta, l’ECMO offre un ponte verso la decisione. Il tema dell’evento è stato anche quello di come si svolge esattamente questa attività e quali risultati ci si può aspettare.
“Negli ultimi anni sono stati fatti grandi progressi nel campo dell’insufficienza cardiaca cronica. Questi sono anche urgentemente necessari nell’insufficienza cardiaca acuta, perché la mortalità è inaccettabilmente alta: dopo tre anni, circa la metà dei pazienti muore. Si tratta di un valore superiore a quello di molti tipi di cancro”, ha detto il Prof. Dr. med. Christian Müller, Cardiologia Ospedale Universitario di Basilea, a titolo di introduzione. “Perché? Spesso sottovalutiamo la gravità e l’urgenza dell’insufficienza cardiaca acuta. L’alta mortalità ha almeno in parte a che fare con il fatto che sottotrattiamo i pazienti”.
Le speranze Urodilatina e Serelaxin – a che punto sono con lo sviluppo?
Le strategie terapeutiche attualmente studiate seguono due principi: Gli obiettivi sono il trattamento più precoce possibile e la vasodilatazione. Una delle nuove sostanze oggetto di ricerca si chiama Ularitide (urodilatina). Sono stati descritti i seguenti effetti farmacologici:
- Effetto emodinamico (vasodilatazione) su vene e arterie
- Broncodilatazione
- Effetto neuroumorale: riduzione delle concentrazioni plasmatiche di renina, aldosterone e angiotensina II. Anche il livello di endotelina diminuisce.
- Effetto renale: vengono favorite la diuresi e la natriuresi.
Uno studio randomizzato e controllato di fase IIb, chiamato SIRIUS II [1], in cui 221 pazienti con insufficienza cardiaca scompensata hanno ricevuto o placebo o urodilatina a dosi di 7,5, 15 o 30 ng/kg/min ricevuto come infusione continua di 24 ore in aggiunta alla terapia standard ha mostrato non solo una riduzione significativa della pressione di occlusione capillare polmonare (PCWP) dopo sei ore e un miglioramento in termini di dispnea, ma anche una tendenza incoraggiante in termini di mortalità. Lo studio di fase III TRUE-AHF, i cui risultati sono attesi verso la fine di quest’anno, dovrebbe ora dimostrare che anche la mortalità cardiovascolare può essere influenzata positivamente a lungo termine con l’urodilatina (endpoint co-primario). Nel maggio 2015, è stato completato il reclutamento di 2152 pazienti con insufficienza cardiaca acuta. A causa del favorevole profilo beneficio-effetto, la dose di 15 ng/kg/min (infusione per 48 ore) viene utilizzata in TRUE-AHF.
La Serelaxina è una forma ricombinante di relaxina 2 umana, che provoca nelle donne in gravidanza processi renali ed emodinamici che le aiutano a far fronte alle maggiori esigenze fisiche. L’aumento della gittata cardiaca, la diminuzione della resistenza vascolare sistemica, il miglioramento del flusso plasmatico renale e l’aumento della velocità di filtrazione glomerulare possono essere utilizzati anche nell’insufficienza cardiaca acuta. In RELAX-AHF [2], è stato dimostrato in 1161 pazienti con insufficienza cardiaca acuta che la somministrazione endovenosa di 30 μg/kg/d di serelaxina, somministrata al più tardi 16 ore dopo l’esordio e poi per 48 ore, era significativamente superiore al placebo in termini di miglioramento della dispnea (ma solo secondo la scala analogica visiva, non la scala Likert della dispnea). C’è stato anche un beneficio di mortalità a lungo termine che dà speranza per gli studi futuri: il rischio di morte era quasi del 40% più basso nel gruppo Serelaxin rispetto al gruppo di controllo dopo 180 giorni (HR 0,63; 95% CI 0,42-0,93; p=0,019). I pazienti hanno anche subito meno danni agli organi finali [3]. Lo studio RELAX-AHF-II è attualmente in corso.
Uso efficace delle sostanze disponibili
Oltre allo sviluppo di nuovi farmaci, esistono anche concetti innovativi per l’utilizzo dei principi attivi già disponibili. Una possibile ipotesi è che la vasodilatazione precoce, continua e ad alto dosaggio migliori l’esito. Una simile strategia terapeutica è attualmente in fase di sperimentazione nello studio GALACTIC presso l’Ospedale Universitario di Basilea. L’obiettivo è quello di stabilire la sicurezza e l’efficacia della riduzione precoce e orientata all’obiettivo del precarico e del postcarico con una pressione arteriosa sistolica target di 90-110 mmHg. Questo si ottiene attraverso una vasodilatazione massimale aggressiva (nitrati sublinguali/transdermici, titolazione rapida degli ACE-inibitori). I partecipanti sono pazienti con insufficienza cardiaca acuta che non vengono trattati nell’unità di terapia intensiva. Nel secondo braccio, la terapia viene eseguita secondo le linee guida ESC. I pazienti sono attualmente in fase di reclutamento [4].
Ossigenazione extracorporea a membrana (ECMO)
Il PD Dr. med. Markus Wilhelm, Clinica di Chirurgia Cardiovascolare, Ospedale Universitario di Zurigo, ha parlato dell’ossigenazione extracorporea a membrana (ECMO). È indicato nello shock cardiogeno, nell’insufficienza cardiaca dopo un precedente intervento al cuore (insufficienza postcardiotomica) e nell’insufficienza respiratoria. Come “ponte verso la decisione”, l’ECMO nello shock cardiogeno comporta un miglioramento a breve termine della circolazione e un recupero o un sollievo degli organi. Consente anche una valutazione neurologica. Infine, bisogna decidere tra diverse possibilità: Nel migliore dei casi, la macchina può essere svezzata? Oppure ha bisogno di un dispositivo di assistenza ventricolare (VAD) o di un monitor cardiaco? un trapianto di cuore? Nel peggiore dei casi, bisogna lasciare che il paziente muoia.
L’ECMO veno-venosa viene utilizzata per l’insufficienza respiratoria e l’ECMO veno-arteriosa per l’insufficienza circolatoria. In quest’ultimo caso, il sangue povero di ossigeno viene pompato all’ossigenatore attraverso una grande cannula nella vena inguinale destra (V. femoralis). Da lì, il sangue ossigenato ritorna direttamente alla circolazione principale senza una deviazione attraverso il cuore, grazie a una grande cannula nell’arteria inguinale sinistra (A. femoralis). Le possibili complicazioni includono emorragie, sia nel sito di ingresso che internamente (a livello cerebrale), infezioni e sindromi da ipo/iperfusione. Per evitare l’ipoperfusione e la sindrome compartimentale con l’ECMO veno-arterioso, le cannule venose e arteriose non vengono inserite sullo stesso lato.
Sopravvivenza con ECMO nello shock cardiogeno
Il dottor Wilhelm ha presentato tre studi – due dei quali del 2015 – dedicati agli esiti dell’ECMO nei pazienti con shock cardiogeno (tab. 1).
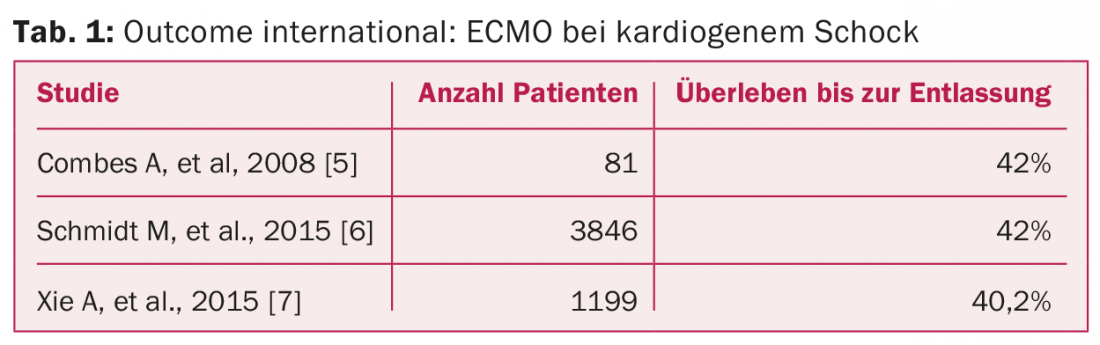
“In generale, mostra che meno della metà dei pazienti che ricevono l’ECMO sopravvive e può essere dimessa dall’ospedale. Questo è coerente con la nostra esperienza all’UniversitySpital di Zurigo: su 57 pazienti USZ, 27, ovvero il 47,4%, erano ancora vivi dopo 30 giorni. L’interruzione è stata possibile in 16, 11 hanno avuto bisogno di un VAD”, ha spiegato il dottor Wilhelm. Le caratteristiche dei pazienti sopravvissuti mostrano che tendevano ad essere più giovani e avevano livelli di lattato significativamente più bassi al basale. Dopo un anno, il 36,8% era vivo, dopo due anni il 32,2% e dopo cinque anni il 29,8% (quindi si è verificato un plateau). “Il fatto che lo shock cardiogeno non consiste solo in un’uscita profonda, ma spesso rappresenta anche uno stato infiammatorio, contribuisce in modo decisivo ai tassi di sopravvivenza”, ha concluso il relatore.
Fonte: Congresso SGK, 10-12 giugno 2015, Zurigo
Letteratura:
- Mitrovic V, et al: Eur Heart J 2006 Dec; 27(23): 2823-2832.
- Teerlink JR, et al: Lancet 2013 Jan 5; 381(9860): 29-39.
- Metra M, et al: J Am Coll Cardiol 2013 Jan 15; 61(2): 196-206.
- Goal-directed Afterload Reduction in Acute Congestive Cardiac Decompensation Study (GALACTIC). Identificatore ClinicalTrials.gov: NCT00512759.
- Combes A, et al: Crit Care Med 2008 May; 36(5): 1404-1411.
- Schmidt M, et al: Eur Heart J 2015 Jun 1. DOI: http://dx.doi.org/10.1093/eurheartj/ehv194 [Epub ahead of print].
- Xie A, et al: J Cardiothorac Vasc Anesth 2015 Jun; 29(3): 637-645.
CARDIOVASC 2015; 14(4): 32-33