La determinazione degli psicofarmaci nel sangue (monitoraggio terapeutico dei farmaci, TDM) contribuisce a una terapia ottimale e personalizzata del paziente psichiatrico. Questo documento è una breve introduzione alle rinnovate linee guida di consenso del gruppo AGNP-TDM.
La determinazione del livello ematico dei farmaci psicotropi serve a chiarire le caratteristiche farmacocinetiche nei singoli pazienti e quindi contribuisce a ottimizzare la terapia. Le linee guida per il monitoraggio terapeutico dei farmaci (TDM) pubblicate negli ultimi decenni provengono quasi esclusivamente dal gruppo TDM dell’Arbeitsgemeinschaft für Neuropsychopharmakologie und Pharmakopsychiatrie (AGNP). Seguendo le linee guida del gruppo TDM pubblicate nel 2004 [1] e nel 2011 [2], nel 2017 è stata presentata una versione aggiornata in lingua inglese, ampliata per includere un gran numero di farmaci [3], che ora è disponibile sia come versione completa [4] che come versione abbreviata [5] in tedesco. La versione abbreviata della linea guida originale qui presentata (in forma elettronica sia in tedesco che in francese) ha lo scopo di incoraggiare il lettore a tornare alla versione originale in inglese: è disponibile gratuitamente sul sito web www.agnp.de e offre il potenziale per migliorare l’efficacia e la tollerabilità della neuropsicofarmacoterapia utilizzando il TDM a beneficio diretto dei pazienti e per ridurre i costi della terapia. Per illustrare l’applicazione pratica di questa linea guida di consenso, viene presentata una situazione clinica inedita (paziente A., riquadro).

Indicazioni per il TDM
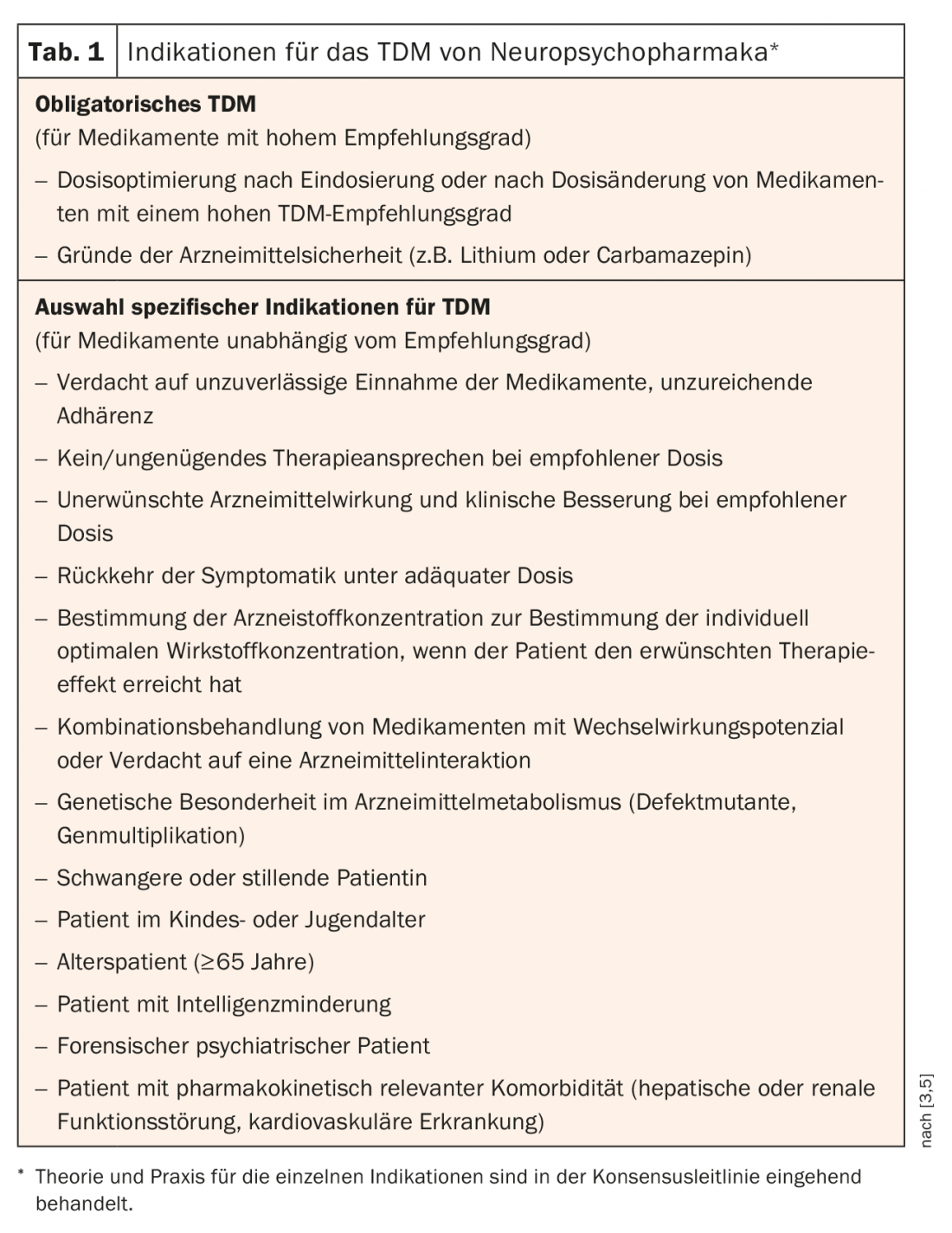
La misurazione dei livelli ematici dei farmaci non deve essere effettuata senza un’indicazione precisa. Pertanto, la Tabella 1 presenta una selezione di situazioni in cui il TDM si rivela utile.
Nel paziente A, la misurazione dei livelli ematici era indicata per diversi motivi: reazione avversa al farmaco alla dose raccomandata, infezione acuta e trattamento con substrato del CYP1A2 (qui olanzapina) e sospetta interazione farmacologica (qui cessazione del fumo). Una misurazione del livello ematico sarebbe stata indicata già prima dell’aumento della dose da 20 mg a 40 mg, a causa del ritorno dei sintomi con una dose adeguata.
Livelli di raccomandazione
C’è consenso sulla necessità di determinare il litio perché il litio ha un range terapeutico ristretto, in quanto livelli ematici troppo bassi sono associati a inefficacia terapeutica, mentre livelli ematici troppo alti sono associati a un rischio di tossicità. Il TDM non è generalmente molto utile per altri farmaci che, come l’agomelatina, hanno un’emivita di eliminazione estremamente breve. Il gruppo AGNP-TDM ha quindi definito quattro livelli di raccomandazione:
- Grado 1: fortemente raccomandato (ad es. litio)
- Grado 2: consigliato (ad esempio, risperidone)
- Grado 3: utile (ad esempio, fluoxetina)
- Grado 4: potenzialmente utile (ad es. agomelatina)
La TDM è fortemente raccomandata per 19 dei 154 farmaci studiati.
Torniamo al nostro caso di studio, il paziente A.: nel caso di olanzapina, è fortemente raccomandato il TDM con grado di raccomandazione 1 (Tab. 2), anche se in singoli casi può essere opportuno determinare non solo la sostanza madre, ma anche il metabolita non attivo N-desmetilolanzapina.
Tuttavia, non tutti i laboratori offrono questa determinazione, poiché potrebbero esserci problemi nell’ottenere le sostanze di riferimento.
Intervalli di riferimento terapeutici e legati alla dose
Per l’interpretazione dei risultati del TDM sorgono innanzitutto due domande:
- La concentrazione di farmaco misurata è all’interno o all’esterno del range terapeutico di riferimento?
- Corrisponde a quello che ci si deve aspettare in pazienti senza comedicinali e senza peculiarità genetiche al dosaggio prescritto?
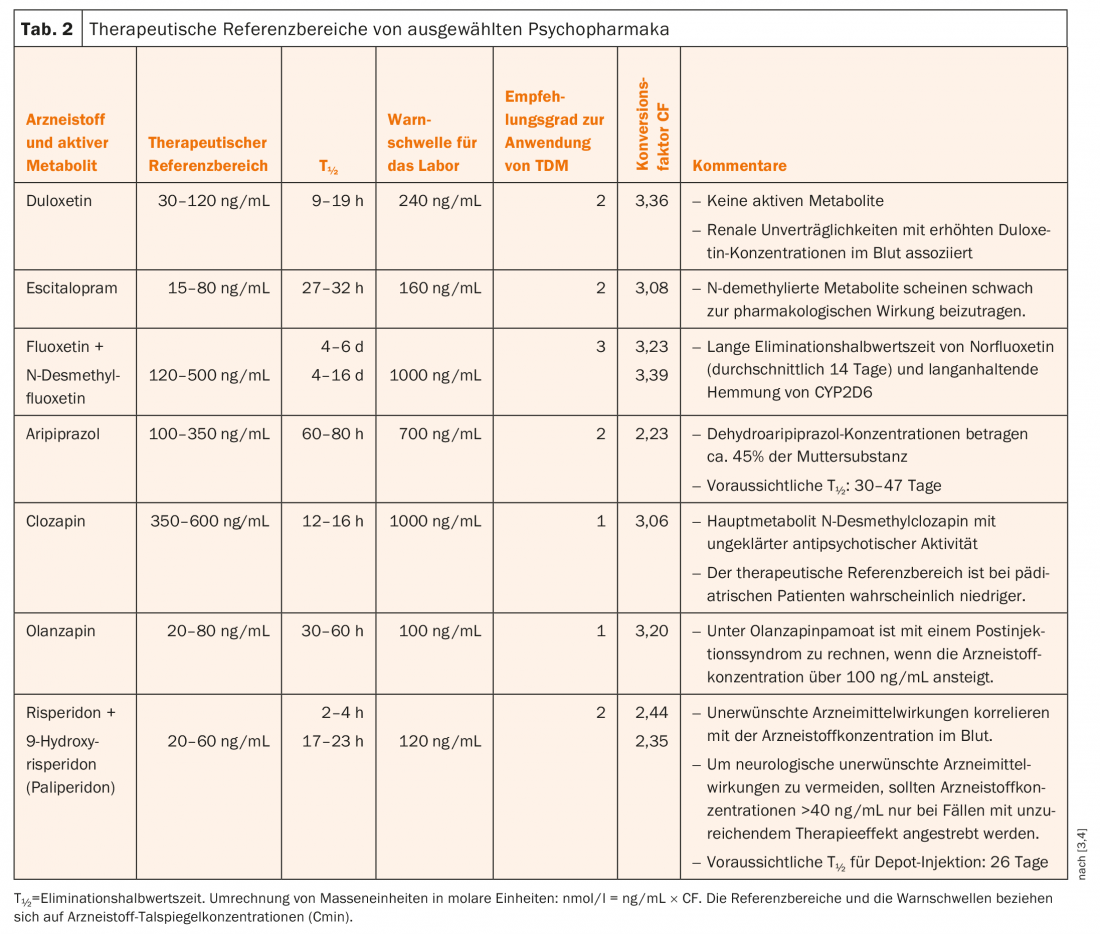
La Tabella 2 mostra gli intervalli terapeutici di riferimento delle concentrazioni ematiche di alcuni farmaci selezionati. Si tratta di concentrazioni alle quali ci si può aspettare una risposta terapeutica e una buona tollerabilità.
Nel paziente A. è stato misurato il seguente livello ematico alla dose di olanzapina di 40 mg: Olanzapina 118 ng/mL (intervallo terapeutico di riferimento 20-60 ng/mL). Il valore era superiore all’intervallo terapeutico di riferimento, addirittura superiore alla soglia di allarme del laboratorio (100 ng/mL), cioè nell’intervallo potenzialmente tossico. Pertanto, i risultati del laboratorio sono stati comunicati ai medici curanti per telefono subito dopo aver ricevuto il valore. Inoltre, il laboratorio ha calcolato e informato che il livello ematico al momento dell’incidente doveva essere superiore a 200 ng/mL.
La Tabella 3 presenta i dati farmacocinetici di una selezione di antidepressivi e antipsicotici. Dalla dose e dai cosiddetti fattori DRC (“concentrazione correlata alla dose”), si può calcolare quale intervallo di livelli ematici si può normalmente prevedere per una certa dose. I fattori DRC sono stati calcolati dai dati farmacocinetici (clearance, biodisponibilità ed emivita di eliminazione) tratti dalla letteratura corrente. Per il DRC, il valore medio (“medio”) è riportato nella Tabella 3, così come i valori limite “basso” e “alto”, che corrispondono all’intervallo della media ± una deviazione standard (SD). L’intervallo contiene quindi il 68% di una distribuzione normale dei fattori DRC. Il DRC (medio, basso, alto) deve essere moltiplicato per la dose ricevuta dal paziente per ottenere la media e i limiti superiore e inferiore, cioè il cosiddetto intervallo di riferimento legato alla dose.
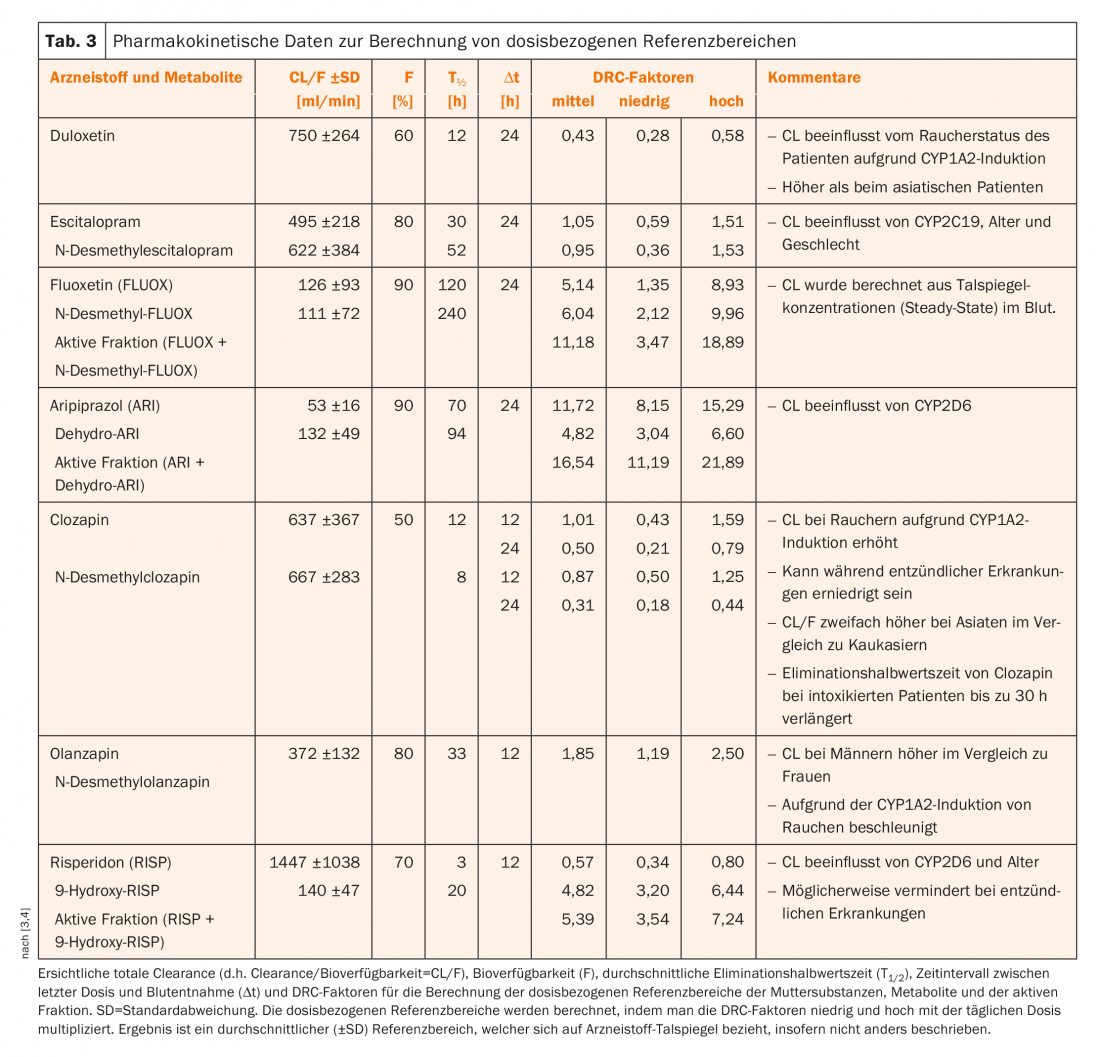
Il paziente A. è stato trattato per l’ultima volta con 40 mg/die di olanzapina. L’intervallo di riferimento legato alla dose, calcolato con i fattori DRC, è quindi compreso tra 1,19 × 40 = 48 ng/mL (basso) e 2,50 × 40 = 100 ng/mL (alto). Quindi, il livello ematico misurato di olanzapina (118 ng/mL, 48 ore dopo l’interruzione) è chiaramente al di sopra della concentrazione di farmaco normalmente prevista – soprattutto quando il laboratorio aveva calcolato che la concentrazione al momento dell’incidente doveva essere superiore a 200 ng/mL.
Interpretazione dei risultati
L’interpretazione dei risultati è una fase importante del processo di TDM, per sfruttare al meglio i benefici associati al TDM. È particolarmente impegnativo perché richiede una buona conoscenza teorica della farmacocinetica e della farmacodinamica dei farmaci, come dimostra l’esempio clinico.
Nel paziente A., ci sono diverse cause per l’aumento dei livelli di olanzapina:
- L’aumento della dose
- Il CYP1A2, che è indotto nei fumatori, è l’enzima principale nella scomposizione dell’olanzapina. Questa induzione è scomparsa in gran parte entro pochi giorni [6] dopo che il paziente ha smesso di fumare [7], per cui era prevedibile una clearance rallentata di olanzapina.
- Forse anche un’infezione, poiché un aumento dei mediatori immunitari può portare all’inibizione del CYP1A2.
Inoltre, è importante notare che un effetto inibitorio del CYP1A2 da parte delle infezioni è stato riportato per la clozapina, ma non ancora per l’olanzapina. Il TDM ha chiarito che il paziente aveva probabilmente subito l’incidente a causa del delirio indotto dall’olanzapina. Le concentrazioni erano negli intervalli riportati nella sindrome post-iniezione di olanzapina depot [8]. Non c’era alcuna indicazione di suicidalità. Il paziente è stato trasferito all’ospedale psichiatrico dopo che i livelli di droga sono scesi sotto i 100 ng/mL e poi è stato dimesso.
Sulla strada della terapia personalizzata
La linea guida TDM dell’AGNP mirava a riassumere gli intervalli di riferimento terapeutici e legati alla dose, le soglie di allarme di laboratorio, le indicazioni e i livelli di raccomandazione per l’uso del TDM per più di 154 farmaci neuropsicotropi. La Tabella 4 fornisce una panoramica incompleta di altri argomenti trattati nella linea guida. La linea guida di consenso per il TDM in neuropsicofarmacologia contiene una grande quantità di informazioni basate sulla valutazione di oltre 1350 riferimenti e sulla considerazione dell’esperienza personale degli autori. Insieme ai consigli pratici, consente un’applicazione appropriata del TDM per una terapia ottimale e personalizzata del paziente psichiatrico. Per quanto riguarda l’uso dei test farmacogenetici, si fa riferimento a una revisione critica pubblicata di recente in questa rivista [9]. È chiaro che il miglior uso possibile del TDM in neuropsichiatria richiede la collaborazione tra il medico curante, il laboratorio e uno specialista in farmacocinetica.

Messaggi da portare a casa
- La determinazione degli psicofarmaci nel sangue (monitoraggio terapeutico dei farmaci, TDM) contribuisce a una terapia ottimale e personalizzata del paziente psichiatrico.
- Le linee guida di consenso del gruppo TDM dell’AGNP sono ora disponibili in un’edizione rinnovata e notevolmente ampliata, che prende nuovamente in considerazione la combinazione di TDM e test farmacogenetici.
- Questo articolo è una breve introduzione a queste linee guida, la cui versione originale è disponibile gratuitamente su www.agn.de.
Letteratura:
- Baumann P, et al: Le linee guida di consenso del gruppo di esperti AGNP-TDM: monitoraggio terapeutico dei farmaci in psichiatria. Farmacopsichiatria 2004; 37(6): 243-265.
- Hiemke C, et al: Linee guida di consenso AGNP per il monitoraggio terapeutico dei farmaci in psichiatria: aggiornamento 2011. Farmacopsichiatria 2011; 44(6): 195-235.
- Hiemke C, et al: Linee guida di consenso per il monitoraggio terapeutico dei farmaci in neuropsicofarmacologia: Aggiornamento 2017. Farmacopsichiatria 2018; 51(1-2): 9-62.
- Hefner G, et al: Linee guida di consenso per il monitoraggio terapeutico dei farmaci in neuropsicofarmacologia: aggiornamento 2017. Psicofarmacoterapia 2017; 25(3): 92-140.
- Unterecker S, et al.: Monitoraggio terapeutico dei farmaci in neuropsicofarmacologia. Sintesi delle linee guida di consenso 2017 del gruppo di lavoro TDM dell’AGNP. Neurologo 2018.
- Faber MS, Fuhr U: Risposta temporale dell’attività del citocromo P450 1A2 alla cessazione del fumo pesante. Farmacologia clinica e terapeutica 2004; 76(2): 178-184.
- Ring BJ, et al: Identificazione dei citocromi P450 umani responsabili della formazione in vitro dei principali metaboliti ossidativi dell’agente antipsicotico olanzapina. J Pharmacol Exp Ther 1996; 276(2): 658-666.
- Sarangula SM, et al: Sindrome da delirio/sedazione post-iniezione con iniezione di olanzapina depot. Indian J Psychol Med 2016; 38(4): 366-369.
- Baumann P, et al.: Terapia personalizzata per gli psicofarmaci: principi di base e consigli pratici per i test farmacogenetici. Info Neurol Psych 2017; 15(6): 21-30. La versione francese è disponibile sul sito www.medizinonline.com/artikel/baumann_pharmacogenomique_therapie, a partire dal 18.1.19.
InFo NEUROLOGIA & PSICHIATRIA 2019; 17(1): 20-24.