Il termine intelligenza artificiale risale agli anni Cinquanta. 20° secolo e comprende un insieme di tecnologie che permettono a un computer di emulare le caratteristiche tipiche dell’intelligenza umana. Inizialmente, sono state riposte grandi speranze in queste tecnologie e sono stati fatti i primi tentativi di affermarle in medicina. All’inizio del Nel 21° secolo, la ricerca sull’IA in medicina è stata piuttosto silenziosa a causa dei risultati inizialmente sconfortanti. Tuttavia, diversi sviluppi importanti hanno spianato la strada alla svolta tecnologica.
Il termine intelligenza artificiale risale agli anni ’50 e comprende un insieme di tecnologie che consentono a un computer di emulare le caratteristiche tipiche dell’intelligenza umana [1]. Inizialmente, sono state riposte grandi speranze in queste tecnologie e sono stati fatti i primi tentativi di affermarle in medicina. Esempi degli anni ’70 sono i programmi per l’identificazione dei batteri nelle malattie infettive [2] o per la prognosi della malattia coronarica [3]. Una certa disillusione si è verificata negli anni ’90: un editoriale [4] della famosa rivista New England Journal of Medicine ha dato ai programmi di diagnosi assistita dal computer disponibili all’epoca un voto di “C”, che corrisponde all’incirca a un “3” nel sistema di classificazione svizzero. Questi programmi hanno prodotto una falsa diagnosi nel 30-50% dei casi, il che ha reso difficile il loro utilizzo e la loro accettazione in clinica. All’inizio del XXI secolo, la ricerca sull’intelligenza artificiale in medicina era piuttosto silenziosa a causa dei risultati inizialmente sconfortanti. Tuttavia, diversi sviluppi importanti hanno spianato la strada alla svolta tecnologica.
Apprendimento profondo
Da un lato, c’è stata una costante espansione dell’uso delle cartelle cliniche elettroniche. I computer hanno così avuto accesso a grandi serie di dati medici. La grande quantità di dati ha permesso di creare e sviluppare ulteriormente una nuova generazione di programmi di intelligenza artificiale. Questi programmi sono stati sviluppati negli anni 2010 e sono ora riassunti sotto il termine Deep Learning . Si tratta di algoritmi basati su reti neurali artificiali che possono riconoscere modelli in grandi quantità di dati con un’elevata precisione. In modo notevole – e con grande importanza per la medicina – questi programmi hanno una straordinaria capacità di riconoscere le strutture nelle immagini [5]. Nel confronto diretto con gli spettatori umani, è stato dimostrato che i computer hanno prestazioni di gran lunga superiori nel riconoscimento dei modelli nelle immagini, inferiori al tasso di errore umano del 5% [6]. Un gruppo di ricerca dell’Università di Stanford in California ha applicato la tecnologia Deep Learning al campo della dermatologia nel 2017. In un documento innovativo, è stato dimostrato che i computer sono alla pari con i dermatologi nel rilevamento delle lesioni cutanee maligne [6]. Da questa pubblicazione di quattro anni fa, c’è stata una proliferazione di nuovi articoli che riportano risultati simili in un’ampia gamma di campi diagnostici (ad esempio, in patologia o radiologia [7–10]). Parallelamente al riconoscimento delle immagini – e con un significato altrettanto importante per la medicina – negli ultimi anni la tecnologia di deep learningha portato a dei progressi nel riconoscimento vocale [11]. Ciò significa che i computer sono sempre più in grado di comprendere e analizzare i dati medici scritti in linguaggio naturale (rapporti di dimissione, rapporti diagnostici, ecc.) o addirittura di scrivere essi stessi dei testi [12]. In sintesi, si può dire quanto segue: Grazie alle cartelle cliniche elettroniche, il computer ha un accesso più ampio ai dati medici che sono ancora prevalentemente in forma non strutturata (immagini o testo). Una tecnologia (Deep Learning) è in grado di elaborare efficacemente questi dati non strutturati ed è quindi in grado di emulare sempre di più le attività mediche (diagnosi, decisione terapeutica o stesura di un rapporto di uscita).
In quale misura e in quale arco di tempo queste nuove tecnologie influenzeranno la medicina rimane una questione aperta. Nella prossima sezione, esploreremo queste domande e presteremo particolare attenzione alle opportunità e ai rischi dell’intelligenza artificiale nella pratica medica quotidiana (Tab. 1).

Uso dell’IA nella pratica clinica quotidiana: concorrenza per il medico?
Attualmente c’è un interesse crescente nell’utilizzo dell’intelligenza artificiale (AI) per integrare, migliorare o addirittura sostituire l’intelligenza diagnostica del medico. I sostenitori dell’IA prevedono che tali tecnologie possano migliorare l’efficienza diagnostica e l’accuratezza diagnostica (con meno sottodiagnosi e sovradiagnosi) [13].
Tuttavia, altri hanno sostenuto che questo creerà un ulteriore onere informativo durante un’ora di consultazione già sovraccarica. Potrebbe fare ben poco per migliorare i risultati dei pazienti, i livelli di stress dei medici generici o la posizione finanziaria del servizio sanitario. Queste argomentazioni si basano talvolta sull’esperienza dei sistemi esistenti che supportano i medici in attività come il rilevamento delle interazioni farmacologiche e che spesso non convincono a causa di falsi allarmi o interventi non pertinenti [14].
Con una nuova generazione di sistemi AI, tuttavia, si può prevedere che questi si affermeranno nella pratica clinica quotidiana nel lungo termine. Il motivo risiede principalmente nella capacità di questi sistemi di studiare un numero illimitato di casi e quindi di perfezionare un algoritmo diagnostico. Un radiologo, ad esempio, ha accesso a un numero elevato ma poi limitato di immagini radiologiche durante la sua formazione e anche la sua attività professionale, che può utilizzare per affinare le sue capacità diagnostiche. Al contrario, i computer hanno accesso potenzialmente a tutte le immagini radiologiche mai acquisite in uno o più ospedali. Il computer può quindi attingere alle immagini radiologiche e ai risultati di centinaia di radiologi, emulando di fatto, anche se indirettamente, la loro conoscenza collettiva. Un singolo radiologo ha quindi uno svantaggio rispetto a un computer.
Queste nuove generazioni di sistemi AI non devono necessariamente operare in modo autonomo (senza supervisione medica), in quanto sono già utilizzate in oftalmologia per la diagnosi della retinopatia diabetica [9]. Piuttosto, l’IA supporterà le attività mediche, ad esempio nei sistemi di IA radiologica che danno priorità alle immagini radiologiche ancora da valutare in base alla gravità in background o nei sistemi di assistenza basati sull’IA che avvisano il radiologo di una frattura nell’immagine a raggi X e aumentano in modo dimostrabile la precisione diagnostica [17]. Se gli specialisti accetteranno e utilizzeranno effettivamente l’aiuto dell’AI è ancora una questione aperta a questo punto. In ogni caso, i non specialisti, i medici di base, i medici in formazione e altro personale medico saranno abilitati dall’IA a eseguire autonomamente esami diagnostici complessi.
Va notato, tuttavia, che un sistema di IA non potrà mai sostituire completamente il medico, in quanto il sistema manca di empatia e compassione per il paziente, per il momento. Un medico deve comprendere il contesto del paziente e prendere in considerazione le circostanze sociali e psicologiche con empatia, attenzione e compassione. La conoscenza esplicita del valore predittivo dei sintomi può essere insegnata a un sistema AI, ma che impari come ottenere la fiducia di una persona è improbabile in questa fase.
Migliorare la qualità della medicina
Se applicati correttamente, tuttavia, i sistemi di AI potrebbero portare a un aumento della qualità dell’assistenza medica. I sistemi AI non si affaticano e garantiscono prestazioni diagnostiche costanti, indipendentemente dall’ora del giorno o dal volume dei pazienti. L’AI può monitorare i processi medici in background e intraprendere azioni correttive. In modo ottimistico, l’AI potrebbe portare a un significativo risparmio di tempo e quindi migliorare la qualità del rapporto paziente-medico. In concreto, i medici potrebbero lasciare gli esami di routine all’IA e dedicare più tempo a parlare con i pazienti. Un esempio dalla pratica del medico di famiglia potrebbe essere la consultazione di un paziente con diabete mellito di tipo 2. Attualmente, i medici di famiglia passano molto tempo a raccogliere informazioni da varie fonti, ad esempio leggendo i rapporti di dimissione di pazienti ambulatoriali o ricoverati, analizzando gli esami del sangue degli ultimi mesi e consultando le linee guida cliniche. Al contrario, i sistemi di assistenza AI potrebbero preparare automaticamente le cose più importanti e indicare rischi e misure in base al profilo di rischio individuale del paziente. Pertanto, i sistemi di intelligenza artificiale potrebbero svolgere un ruolo importante anche nella prevenzione. Questi sistemi potrebbero suggerire proattivamente delle consultazioni se determinano che un paziente con diabete mellito di tipo 2 è a maggior rischio di sviluppare una particolare complicanza diabetica e merita un intervento.
L’AI al GP
I sistemi basati sull’AI apportano anche competenze diagnostiche di supporto all’assistenza primaria. Un’immagine di una lesione cutanea è sufficiente per diagnosticarne l’eziologia mediante un sistema di intelligenza artificiale. Le immagini potrebbero essere acquisite in uno studio medico di base e inviate a un sistema AI specializzato in dermatologia per un’analisi tempestiva [6]. I pazienti a basso rischio riceverebbero una rassicurazione immediata, mentre i pazienti a maggior rischio di melanoma potrebbero essere indirizzati immediatamente a un dermatologo e non dovrebbero aspettare a lungo, poiché gli specialisti vedono solo casi selezionati. Questo concetto non è limitato al campo della dermatologia, ma anche all’interpretazione di molti altri dati complessi del paziente, ad esempio scansioni della retina, raggi X o immagini a ultrasuoni. Molte di queste immagini possono essere presto raccolte e analizzate con apparecchiature e AI relativamente poco costose. Un buon esempio è la nuova generazione di piccoli dispositivi a ultrasuoni che si collegano direttamente allo smartphone e possono analizzare un’ampia varietà di sistemi di organi tramite l’AI [18].
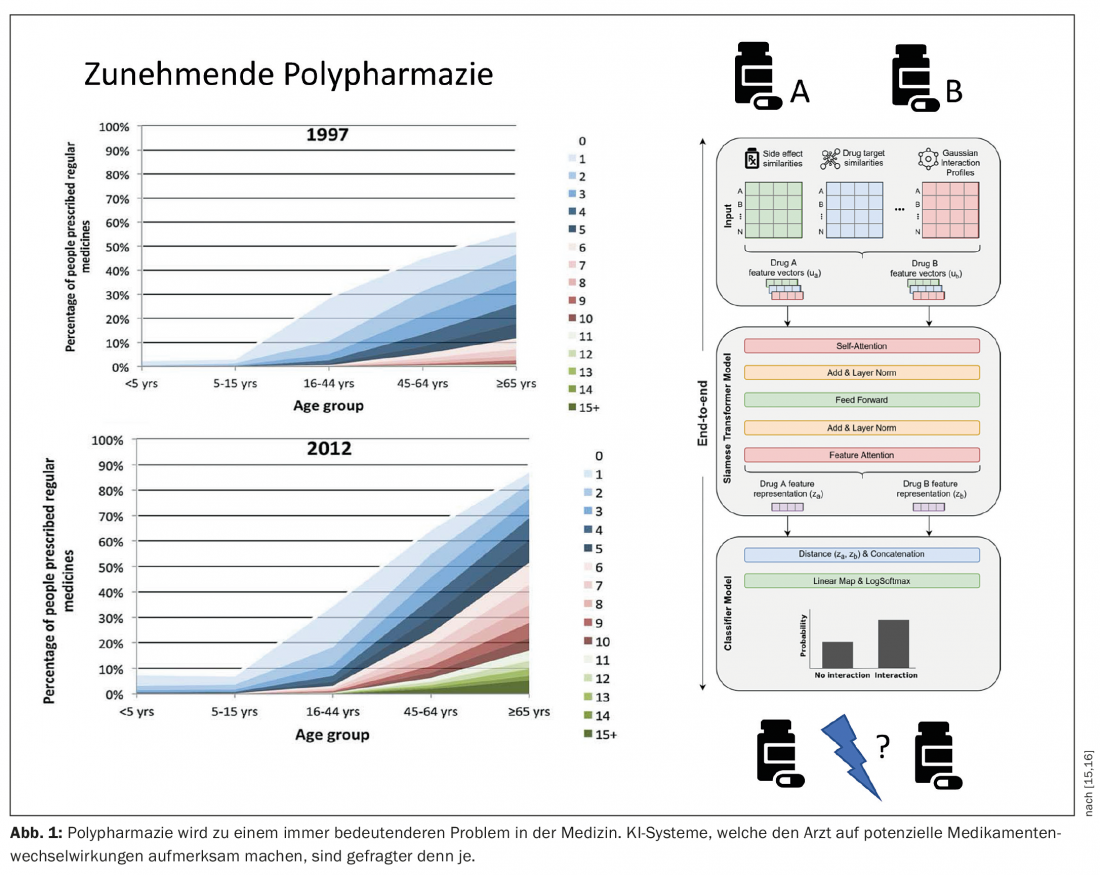
Anche altre applicazioni sono rilevanti. Ad esempio, i nuovi approcci per il rilevamento delle interazioni farmacologiche basati su algoritmi di apprendimento profondo mostrano un potenziale. La politerapia è un problema crescente nella medicina di famiglia, con un alto rischio di interazioni farmacologiche avverse. I sistemi di intelligenza artificiale che supportano il medico possono svolgere un ruolo importante nel rilevamento e anche nella prevenzione (Fig. 1) [15,16].
Tuttavia, un ostacolo all’implementazione sicura e diffusa dei sistemi di IA negli studi medici di base e in molti altri settori della medicina è l’inserimento dei dati, spesso inadeguato. Nel settore sanitario, il processo è raramente automatizzato e spesso dipende dai medici che non hanno il tempo di inserire i dati. Senza dati corretti e aggiornati, i sistemi di AI non dispongono delle informazioni necessarie per generare un algoritmo funzionante per un corretto processo decisionale [19]. Soprattutto nella medicina generale, sono ancora necessari molti sforzi per migliorare di conseguenza la situazione dei dati.
Natura della scatola nera e pregiudizio sistematico dell’IA
Lo sviluppo di algoritmi di apprendimento profondooffre ai computer la capacità di esplorare associazioni sempre più complesse. Gli algoritmi di apprendimento profondosi basano sull’idea di un cervello “computerizzato”. Tuttavia, i processi neurali che avvengono nel sistema non sono sempre comprensibili agli esseri umani (l’IA è una “scatola nera”). Questo rende più difficile l’interpretazione dei risultati. Questo a sua volta può portare a una riduzione della fiducia nei confronti del sistema e quindi rendere più difficile l’integrazione nella pratica clinica [19]. Inoltre, un sistema di intelligenza artificiale è buono solo quanto i dati che gli vengono forniti; se i dati sono difettosi o distorti, possono contenere pregiudizi sistematici. Il rischio di un’inesattezza sistematica del sistema di AI diventa quindi maggiore. Per esempio, i pazienti con uno status socioeconomico basso possono ricevere meno esami diagnostici e farmaci per le malattie croniche e avere un accesso limitato all’assistenza sanitaria. Un sistema di intelligenza artificiale ha quindi solo una quantità limitata di informazioni su questa popolazione di pazienti e può suggerire un intervento necessario più tardi rispetto ai pazienti che si recano regolarmente dal medico [20].
D’altra parte, i medici professionisti non sono immuni da pregiudizi. Il processo decisionale clinico spesso dipende in parte da una serie di “regole empiriche” e di algoritmi. Sheringham et al. [21] ha mostrato, ad esempio, che i medici di base britannici non avevano maggiori probabilità di diagnosticare i pazienti con sintomi di cancro ad alto rischio rispetto ai pazienti con sintomi a basso rischio. È stato anche dimostrato che i pazienti con gli stessi sintomi vengono trattati o chiariti in modo diverso [21].
Un sistema di AI può potenzialmente sintetizzare e interpretare in modo oggettivo tutti i dati disponibili nella cartella clinica elettronica, cosa impossibile per il medico a causa della grande quantità di dati. L’interazione medico/AI è sinergica e offre l’opportunità di mitigare i pregiudizi e di ottenere una migliore assistenza al paziente.
Open Data – implicazioni per l’AI, la protezione dei dati e la sicurezza
I dati aperti sono una tendenza che sta diventando sempre più importante anche nell’assistenza sanitaria. Uno dei principali vantaggi degli Open Data è che i dati degli studi clinici e di altre fonti possono essere utilizzati, rianalizzati, condivisi e combinati con altri dati. Gli Open Data facilitano la collaborazione scientifica, arricchiscono la ricerca, migliorano la capacità analitica di prendere decisioni e garantiscono progressi molto più rapidi nella medicina. Ad esempio, MIMIC-IV è un set di dati che contiene dati sanitari non identificabili su oltre 60.000 pazienti di terapia intensiva presso il Beth Israel Deaconess Medical Centre dal 2008 al 2019 ed è disponibile pubblicamente [22].
I dati aperti stanno alimentando l’AI, che dipende da serie di dati di pazienti molto grandi. Questo aspetto porterà inevitabilmente a una convergenza dei sistemi sanitari, almeno a livello di dati, in modo che nella rete di ospedali vengano raccolti dati sufficienti per l’IA. Questa “trasparenza dei dati” potrebbe portare a ulteriori effetti positivi a lungo termine, come un migliore controllo dei costi nel sistema sanitario.
La dipendenza dai dati ha anche i suoi lati negativi. I dati medici contengono informazioni altamente sensibili che devono essere protette per motivi di protezione dei dati e, a prima vista, rappresentano una barriera importante per gli Open Data. Pertanto, l’uso degli Open Data richiede un attento equilibrio tra il libero accesso e la privacy del paziente. Per rispondere a queste sfide di sicurezza e protezione dei dati, è necessario porre grande enfasi sulle garanzie legali (“accordi sull’uso dei dati”), sugli algoritmi di crittografia avanzati e sulla pseudo-anonimizzazione dei dati personali. I sistemi di IA in generale dovrebbero garantire la protezione e la sicurezza dei dati e stabilire standard di buona governance [23].
Conclusione
L’uso dei sistemi di intelligenza artificiale nella pratica medica per una diagnosi e una terapia più efficienti richiede l’accettazione e il sostegno dei medici. Prima dell’uso, bisogna assicurarsi che la combinazione AI-medico apporti un beneficio alla cura del paziente, anche riducendo il carico sui medici e senza creare incertezza per i pazienti. Ciò che serve ora è una ricerca sull’IA che esamini in modo olistico e sistematico le conseguenze per la pratica clinica quotidiana.
Messaggi da portare a casa
- L’intelligenza artificiale è un campo in crescita che avrà un impatto importante sulla medicina di domani.
- Una comprensione di base dell’intelligenza artificiale è fondamentale per la sua corretta implementazione nella pratica clinica.
- Il supporto dell’attività medica da parte dell’intelligenza artificiale porta a un potenziale miglioramento della qualità e a un risparmio di tempo.
- L’intelligenza artificiale non è infallibile. Nuovi sistemi promettenti sono oggetto della ricerca attuale, ma presentano ancora difficoltà di implementazione in un’ampia applicazione clinica.
Riconoscimento
Ringraziamo Lukas Bachmann, MD, per la sua revisione costruttiva dell’articolo.
Letteratura:
- McCarthy J, Minsky ML, Rochester N, Shannon CE: Una proposta per il Progetto di Ricerca Estiva Dartmouth sull’Intelligenza Artificiale, 31 agosto 1955. Rivista AI 1955; 27(4): 12.
- Shortliffe EH, Buchanan BG: Un modello di ragionamento inesatto in medicina. Bioscienze matematiche 1975; 23(3): 351-379.
- Rosati RA, McNeer JF, Starmer CF, et al: Un nuovo sistema informativo per la pratica medica. Arch Intern Med 1975; 135(8): 1017-1024.
- Kassirer JP: Una pagella sulla diagnosi assistita da computer: voto: C. N Engl J Med 1994; 330(25): 1824-1825.
- Langlotz CP, Allen B, Erickson BJ, et al: Una tabella di marcia per la ricerca fondamentale sull’intelligenza artificiale nell’imaging medico: Dal Workshop 2018 NIH/RSNA/ACR/The Academy. Radiologia 2019; 291(3): 781-791.
- Esteva A, Kuprel B, Novoa RA, et al: Classificazione del cancro della pelle a livello di dermatologo con reti neurali profonde. Natura 2017; 542(7639): 115-118.
- Kooi T, Litjens G, van Ginneken B, et al: Apprendimento profondo su larga scala per il rilevamento computerizzato delle lesioni mammografiche. Med Image Anal 2017; 35: 303-312.
- Gulshan V, Peng L, Coram M, et al: Sviluppo e convalida di un algoritmo di apprendimento profondo per il rilevamento della retinopatia diabetica nelle fotografie del fondo retinico. JAMA 2016; 316(22): 2402-2410.
- De Fauw J, Ledsam JR, Romera-Paredes B, et al: Apprendimento profondo clinicamente applicabile per la diagnosi e il referral nelle malattie della retina. Nat Med 2018; 24(9): 1342-1350.
- van der Laak J, Litjens G, Ciompi F: Apprendimento profondo in istopatologia: il percorso verso la clinica. Nat Med 2021; 27(5): 775-784.
- Li Y, Rao S, Solares JRA e altri: BEHRT: Transformer for Electronic Health Records. Sci Rep 2020; 10(1): 7155.
- Nooralahzadeh F, Gonzalez NP, Frauenfelder T, et al: Generazione progressiva di referti radiologici basata su trasformatori. arXiv preprint arXiv:210209777; 2021.
- Summerton N, Cansdale M.: Intelligenza artificiale e diagnosi nella medicina generale. Br J Gen Pract 2019; 69(684): 324-325.
- Embi PJ, Leonard AC: Valutazione dell’affaticamento nel tempo agli avvisi di sperimentazione clinica basati su EHR: risultati di uno studio controllato randomizzato. J Am Med Inform Assoc 2012; 19(e1): e145-148.
- Schwarz K, Allam A, Gonzalez NAP, Krauthammer M: AttentionDDI: metodo di apprendimento profondo basato sull’attenzione siamese per le previsioni di interazione farmaco-farmaco. ArXiv. 2020; abs/2012.13248.
- Moriarty F, Hardy C, Bennett K, et al: Tendenze e interazione della polifarmacia e della prescrizione potenzialmente inappropriata nell’assistenza primaria in 15 anni in Irlanda: uno studio trasversale ripetuto. BMJ Open 2015; 5(9): e008656.
- Rainey C, McConnell J, Hughes C, et al: Intelligenza artificiale per la diagnosi di fratture su radiografie semplici: una revisione approfondita della letteratura attuale. Medicina basata sull’intelligenza 2021; 5: 100033.
- Buonsenso D, Pata D, Chiaretti A: Epidemia COVID-19: meno stetoscopio, più ultrasuoni. Lancet Respir Med 2020; 8(5): e27.
- Liaw W, Kakadiaris IA: Intelligenza artificiale delle cure primarie: un ramo che si nasconde in piena vista. Ann Fam Med 2020; 18(3): 194-195.
- Obermeyer Z, Powers B, Vogeli C, Mullainathan S.: Dissezione dei pregiudizi razziali in un algoritmo utilizzato per gestire la salute delle popolazioni. Scienza 2019; 366(6464): 447-453.
- Sheringham J, Sequeira R, Myles J, et al: Variazioni nelle decisioni dei medici di base di indagare su un sospetto tumore al polmone: un esperimento fattoriale con vignette multimediali. BMJ Qual Saf 2017; 26(6): 449-459.
- Johnson ABL, Pollard T, Horng S, et al: MIMIC-IV (versione 1.0). PhysioNet0 2021; doi: 10.13026/s6n6-xd98.
- Kobayashi S, Kane TB, Paton C: Le implicazioni sulla privacy e sulla sicurezza dei dati aperti nell’assistenza sanitaria. Yearb Med Inform 2018; 27(1): 41-47.
PRATICA GP 2021; 16(11): 6-10