Non esistono screening consolidati per il cancro dell’endometrio e dell’ovaio. Pertanto: ogni donna con sanguinamento in postmenopausa o atipico in premenopausa deve essere esaminata e, se necessario, chiarita ulteriormente. Il cancro ovarico precoce viene spesso scoperto per caso. Solo il carcinoma del collo dell’utero può essere sottoposto a screening efficace con lo striscio PAP.
Mentre il carcinoma mammario è il tumore più comune nelle donne in Svizzera, con il 32,5% di tutte le nuove diagnosi di cancro, il carcinoma endometriale è al quinto posto in termini di incidenza. Il carcinoma ovarico è un po’ meno comune, ma ha una mortalità maggiore o una prognosi peggiore. Solo al 15° posto si trova il carcinoma cervicale, la cui incidenza è diminuita negli ultimi due decenni grazie allo screening della displasia cervicale. Il carcinoma vulvare è ancora più raro e rappresenta poco meno dell’1% di tutte le nuove diagnosi di cancro nelle donne [1].
Il carcinoma endometriale [2–4]
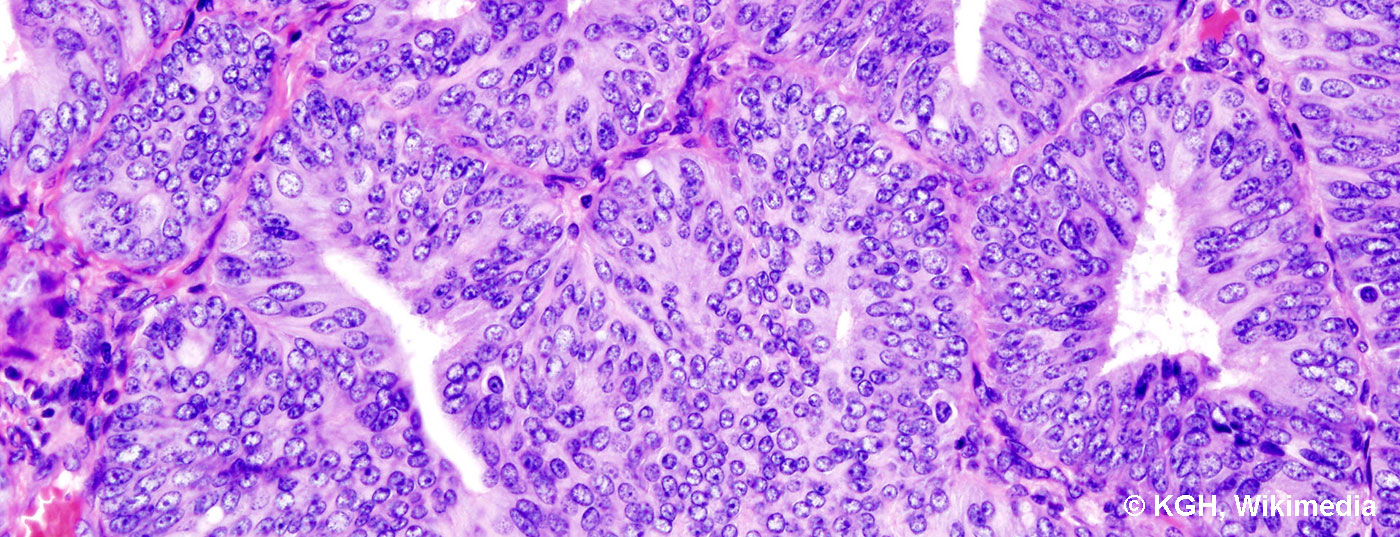
Il carcinoma endometriale è considerato un carcinoma delle donne anziane. Tuttavia, si verifica anche in età più giovane, soprattutto in presenza di sindromi tumorali familiari come il cancro al colon ereditario non poliposico (HNPCC o sindrome di Lynch). Si distingue tra due tipi di carcinoma endometriale. Il carcinoma endometriale di tipo I corrisponde istologicamente al carcinoma endometriale endometrioide, che è associato agli estrogeni e piuttosto ben differenziato e di conseguenza ha una prognosi più favorevole. Il fattore di rischio influenzabile per questo carcinoma è la sindrome metabolica, in particolare l’obesità e l’ipertensione. Il carcinoma endometriale di tipo II istologicamente corrisponde solitamente a un tipo sieroso o a cellule chiare. Non è associato agli estrogeni ed è paragonabile al carcinoma ovarico in termini di prognosi e di terapia da effettuare, cioè è associato a una prognosi significativamente meno favorevole. Non ci sono fattori di rischio tipici per il carcinoma di tipo II.
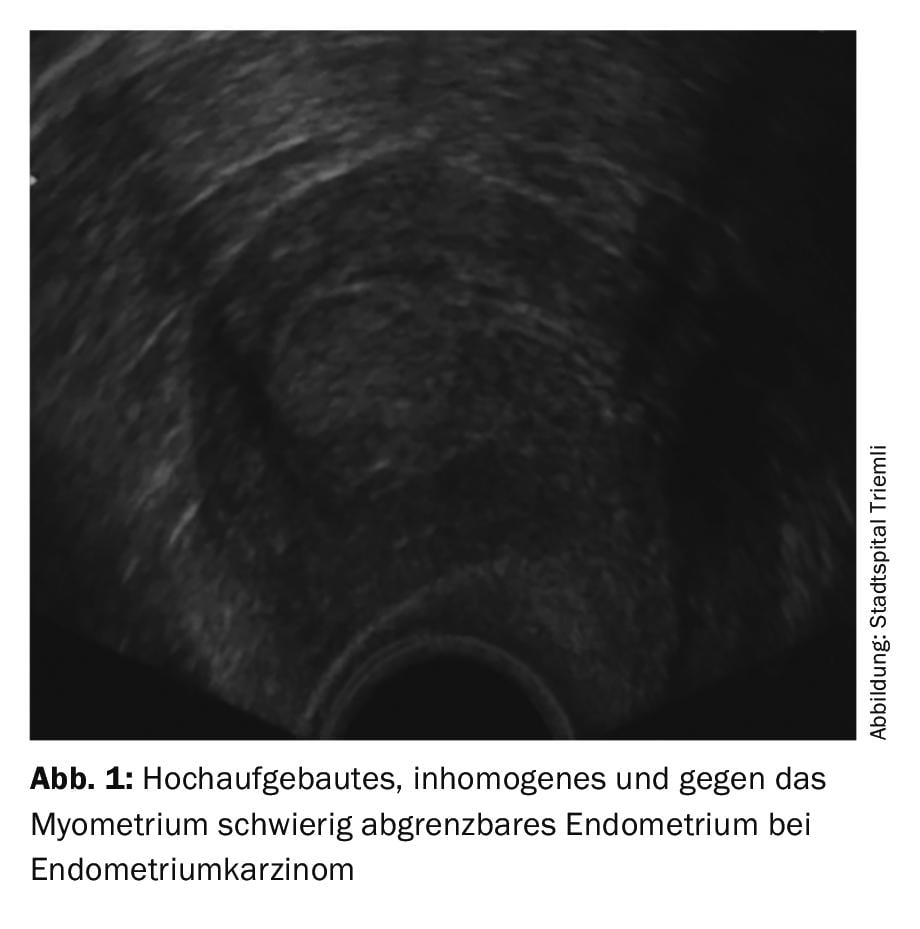
Lo screening generale per il carcinoma endometriale o i suoi precursori con l’ecografia transvaginale non è raccomandato per le donne asintomatiche, in quanto ad oggi non è stato dimostrato alcun beneficio. Questo vale anche per le donne in terapia con tamoxifene per il cancro al seno. Tuttavia, ogni donna che presenta un’emorragia in postmenopausa o un’emorragia atipica in premenopausa deve essere esaminata ginecologicamente e mediante ecografia transvaginale e, se necessario, chiarita ulteriormente. Va notato che i carcinomi di tipo II, in particolare, non sempre mostrano la tipica immagine ecografica con endometrio altamente costruito e disomogeneo (fig. 1).
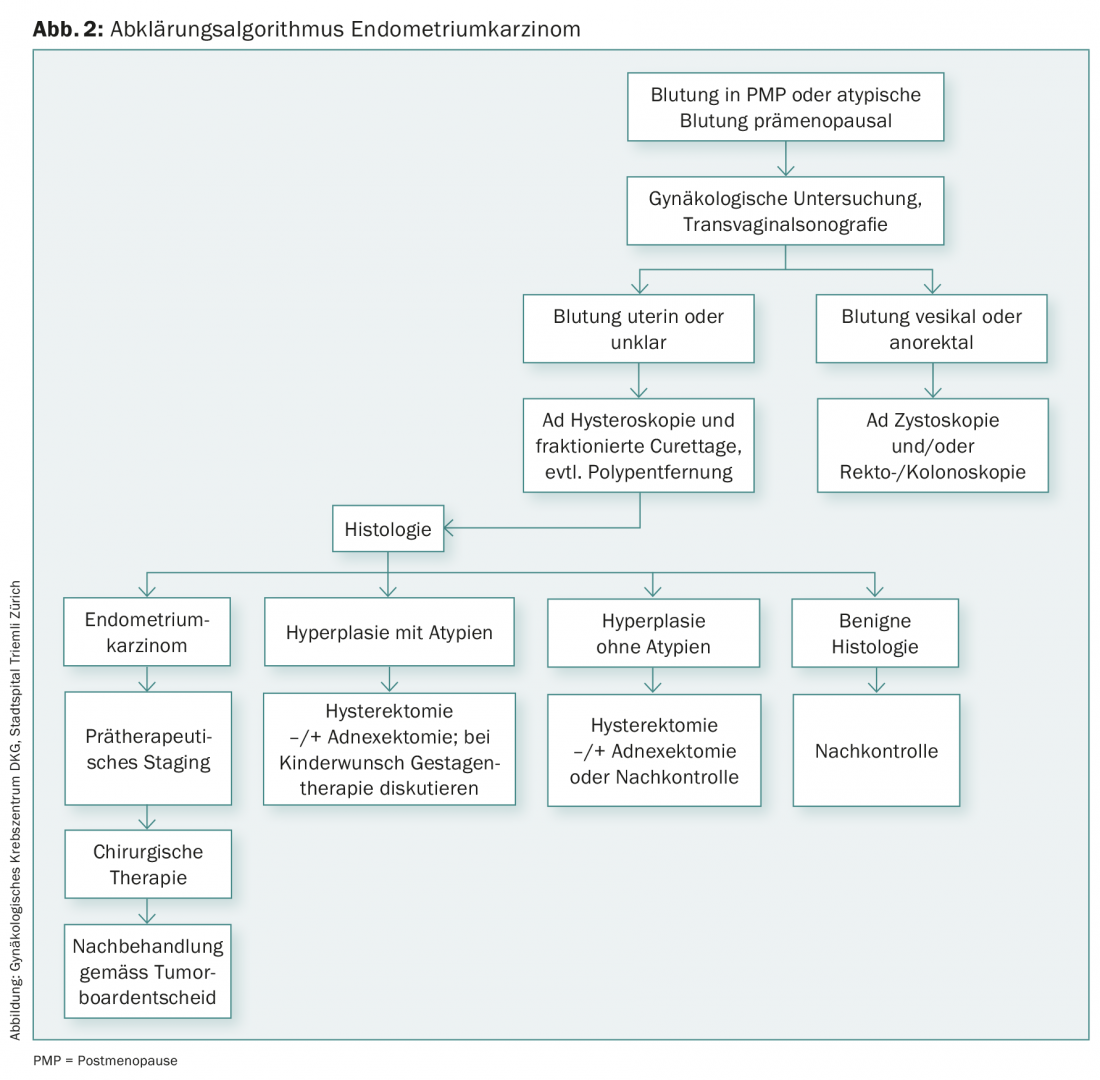
Il chiarimento istologico, che di solito viene effettuato mediante isteroscopia e curettage, è particolarmente necessario in caso di emorragie ripetute in postmenopausa e in presenza di fattori di rischio come obesità, ipertensione, diabete mellito, ma anche in caso di PCO (ovaie policistiche), sindrome HNPCC o terapia con tamoxifene (Fig. 2).
Una volta effettuata la diagnosi istologica, si raccomanda una stadiazione radiologica, ad esempio mediante tomografia computerizzata dell’addome e del torace, prima di effettuare una terapia definitiva. Il trattamento del carcinoma endometriale consiste principalmente nell’isterectomia con annessiectomia. Nel caso di carcinomi di tipo I ben differenziati o moderatamente differenziati, senza un’estesa infiltrazione miometriale e con linfonodi retroperitoneali poco evidenti alla diagnostica per immagini, questa terapia chirurgica è solitamente sufficiente. Inoltre, la radioterapia intravaginale deve essere valutata nel post-operatorio.
Nei carcinomi endometrioidi G3 e in tutti i carcinomi di tipo II, secondo le attuali linee guida, è indicata una linfonodectomia pelvica e para-aortica in aggiunta all’isterectomia, nonché il debulking del tumore in analogia al carcinoma ovarico in caso di coinvolgimento peritoneale. Inoltre, nella maggior parte dei casi si raccomanda la chemioterapia (carboplatino e paclitaxel) e, se necessario, la radioterapia percutanea della pelvi. Il valore di una linfonodectomia retroperitoneale sistematica è controverso e attualmente è oggetto di diversi studi. Soprattutto in combinazione con la successiva radioterapia, il linfedema delle gambe può verificarsi fino al 40% dei pazienti. Attualmente si sta valutando se la linfonodectomia sentinella possa avere un posto nell’algoritmo di trattamento del carcinoma endometriale.
Da un lato, il follow-up è orientato ai sintomi, ma dall’altro è anche importante individuare il più precocemente possibile la recidiva centrale sul moncone vaginale, che può ancora essere trattata sotto l’aspetto curativo. Per questo motivo, gli strisci citologici dalla colpotomia vengono prelevati ogni sei mesi e un’ecografia transvaginale viene eseguita ad ogni controllo. Gli intervalli di controllo sono fissati ogni tre o quattro mesi per i primi tre anni dopo la terapia, poi ogni sei mesi. I controlli annuali possono essere effettuati a partire da cinque anni dopo la terapia. La diagnostica per immagini di routine, come la tomografia computerizzata o la risonanza magnetica, nonché i controlli di laboratorio non sono raccomandati e devono essere eseguiti in presenza di sintomi specifici [5].
Il carcinoma ovarico [6–8]
Si distingue tra il carcinoma ovarico precoce, che è limitato agli annessi e all’utero (fino allo stadio FIGO IIA), e il carcinoma ovarico avanzato, che si diffonde a livello peritoneale e spesso comporta un coinvolgimento esteso del Douglas, dell’omento e degli organi addominali superiori, compresa la cavità addominale. Le cupole del diaframma e la capsula del fegato sono visibili. Il 10% di tutti i tumori ovarici è di origine genetica, principalmente a causa di una mutazione BRCA (“sindrome ereditaria del cancro al seno-ovarico”). Il rischio di sviluppare un cancro ovarico nel corso della vita con una mutazione genetica accertata è fino al 60%.
Nel caso del cancro ovarico, non ci sono nemmeno prove di uno screening efficace, soprattutto nelle donne con una mutazione BRCA nota.
Il carcinoma ovarico precoce è spesso un reperto incidentale, nel senso di un reperto annessiale poco chiaro con sintomi assenti o non specifici. Nel carcinoma ovarico avanzato, di solito sono presenti sintomi aspecifici dovuti alla carcinomatosi peritoneale – sensazione di pienezza, aumento della circonferenza addominale, malessere, fastidio addominale diffuso, ecc.
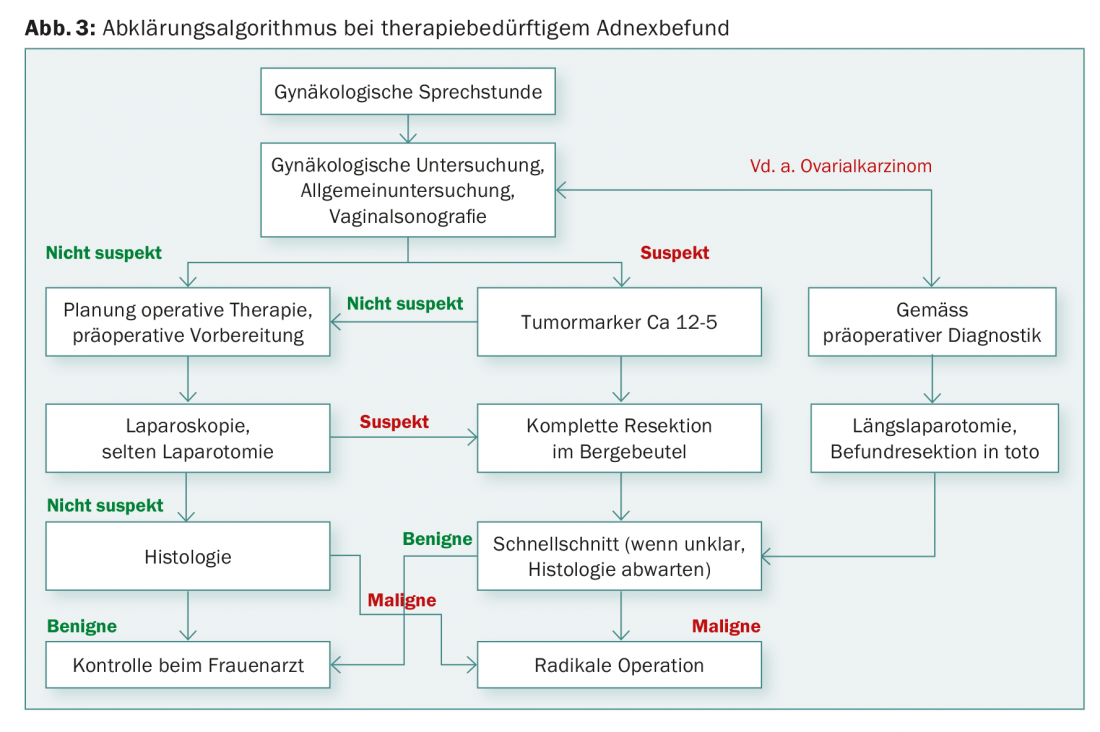
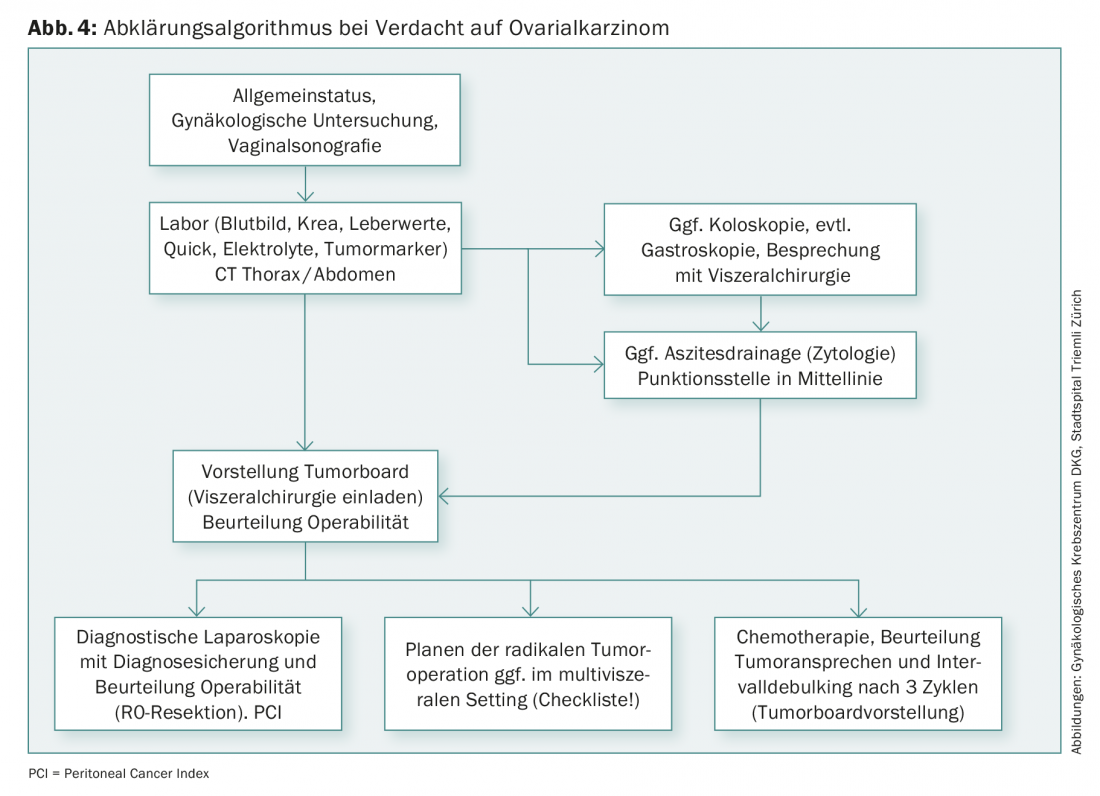
La terapia per il cancro ovarico consiste in un intervento chirurgico seguito da chemioterapia (di solito sei cicli di carboplatino/Taxol®). Chirurgicamente, l’isterectomia viene eseguita con annessiectomia bilaterale, omentectomia, biopsie peritoneali e linfonodectomia pelvica e para-aortica e in alcuni casi appendicectomia. In caso di coinvolgimento peritoneale, l’asportazione completa di tutte le aree coinvolte dal tumore è associata a una prognosi migliore rispetto alla chirurgia incompleta del tumore. Ciò significa che spesso è necessario eseguire una resezione multiviscerale con, ad esempio, resezione rettosigmoidea, ulteriori resezioni intestinali parziali, mastripping del diaframma, resezione della capsula epatica e/o splenectomia, se le condizioni generali sono adeguate. Di conseguenza, il setting chirurgico deve essere pianificato su base interdisciplinare, con adeguati requisiti anestesiologici e di terapia intensiva. Se, sulla base dei chiarimenti, la diagnosi non è ancora chiara o l’asportazione chirurgica completa è solo discutibile, si esegue principalmente una laparoscopia diagnostica o, se necessario, si inizia direttamente la chemioterapia. Se la risposta è buona, la terapia chirurgica può essere eseguita come debulking di intervallo dopo tre cicli di chemioterapia. Se non è stato possibile eseguire una resezione completa nello stadio FIGO III, la chemioterapia viene combinata con bevacizumab, seguita da una terapia di mantenimento.
Il follow-up del carcinoma ovarico è principalmente orientato ai sintomi, con gli stessi intervalli di controllo del carcinoma endometriale. Ad ogni visita di controllo, oltre all’esame ginecologico, viene effettuata un’ecografia transvaginale e una volta all’anno viene prelevato uno striscio citologico dalla colpotomia. La tomografia computerizzata e i marcatori tumorali devono essere eseguiti solo se sono presenti sintomi e si sospetta una recidiva, in quanto il rilevamento precoce della recidiva senza sintomi comporta una peggiore qualità di vita con l’avanzamento della fase palliativa e degli effetti collaterali della terapia, senza influire sulla sopravvivenza complessiva.
Il carcinoma cervicale [9,10]
Praticamente tutti i carcinomi cervicali sono associati all’HPV (Fig. 5), con i tipi di HPV 16 e 18 responsabili del 70-80% di tutti i carcinomi cervicali. Questi due tipi sono coperti dalla vaccinazione HPV come parte del programma nazionale di vaccinazione dal 2008. Lo screening per le lesioni precancerose del collo dell’utero viene effettuato con strisci citologici annuali (strisci PAP) ed è raccomandato per la prima volta all’età di 21 anni. Se gli ultimi tre strisci non hanno dato risultati significativi e non ci sono altri fattori di rischio, gli intervalli possono essere estesi a due o tre anni. Inoltre, attualmente si parla di screening dell’HPV al posto dell’esame citologico [11].
Dopo la diagnosi istologica di carcinoma cervicale, si esegue una valutazione clinica e di imaging dello stadio del tumore. Nei carcinomi cervicali precoci fino allo stadio FIGO Ib1 (dimensioni del tumore <4 cm), la terapia chirurgica viene solitamente effettuata mediante isterectomia estesa e linfonodectomia pelvica e paraaortica profonda; negli stadi più avanzati, radio-chemioterapia combinata primaria. Il valore della linfonodectomia sentinella è attualmente in fase di valutazione anche nel carcinoma cervicale.
Nel follow-up, è importante individuare la recidiva centrale o la recidiva della parete pelvica in una fase precoce. Pertanto, in occasione di tutti i controlli, è necessario eseguire uno striscio citologico della colpotomia, un’ecografia transvaginale e un’ecografia del sistema pelvico renale.
Messaggi da portare a casa
- Non esiste uno screening stabilito ed efficace per il cancro dell’endometrio e dell’ovaio.
- Praticamente tutti i carcinomi cervicali sono associati all’HPV. Per il carcinoma del collo dell’utero, esiste uno screening efficace con gli strisci citologici del collo dell’utero (strisci PAP). In futuro, questo sarà probabilmente fatto con lo screening HPV.
- Ogni donna che presenta un’emorragia in postmenopausa o un’emorragia atipica in premenopausa deve essere esaminata ginecologicamente e con un esame transvaginale.
- ecografia e, se necessario, chiarita mediante isteroscopia e curettage.
- La terapia chirurgica del cancro ovarico avanzato richiede un team interdisciplinare ben coordinato. L’attenta
- La pianificazione pre-terapeutica e la discussione interdisciplinare del concetto di terapia sono fondamentali per il risultato.
Letteratura:
- Ufficio federale di statistica (UST), Istituto nazionale di epidemiologia e registrazione del cancro (NICER): Krebs in der Schweiz, Stand und Entwicklung von 1983 bis 2007.
- Emons G, et al: Versione di consultazione. Rapporto di linea guida. Linea guida S3 Diagnostica, terapia e follow-up delle pazienti con carcinoma endometriale. Numero di registro AWMF 032/034OL. 2017.
- Colombo N, et al: Tumore dell’endometrio: Linee guida di pratica clinica ESMO per la diagnosi, il trattamento e il follow-up. Ann Oncol 2013; 24(Suppl 6): vi33-8.
- Linee guida NCCN: Neoplasie uterine. 2017.
- Gruppo di lavoro sull’oncologia ginecologica dell’SGGG: Raccomandazioni per l’assistenza post-ospedaliera oncologica ginecologica. 2009.
- DGGG: S3-Leitlinie Diagnostik, Therapie und Nachsorge maligner Ovarialtumoren. Numero di registro AWMF 032/035OL. 2017.
- Ledermann JA, et al: Carcinoma ovarico epiteliale di nuova diagnosi e recidiva: Linee guida di pratica clinica ESMO per la diagnosi, il trattamento e il follow-up. Ann Oncol 2013; 24(Suppl 6): vi24-32.
- Linee guida NCCN: Cancro ovarico. 2017.
- DGGG, AGO: S3-Leitlinie Diagnostik, Therapie und Nachsorge der Patientin mit Zervixkarzinom. Numero di registro AWMF 032/033OL. 2014.
- Linee guida NCCN: Cancro della cervice uterina. 2017.
- Gerber S, et al: Aggiornamento dello screening per il cancro al collo dell’utero e del follow-up mediante colposcopia. Lettera di esperti SGGG n. 40. 2012.
InFo ONCOLOGIA & EMATOLOGIA 2018; 6(1): 6-10.