L’herpes zoster è una malattia onerosa e potenzialmente pericolosa, ma oggi è efficacemente e facilmente prevenibile attraverso la vaccinazione. Il vaccino ricombinante adiuvato contro lo zoster fornisce una profilassi efficace ai pazienti. L’assistenza sanitaria preventiva per i pazienti è quindi una priorità assoluta per i medici. per i pazienti in cima alla lista delle priorità.
Spesso liquidata come una malattia infantile innocua, la varicella è spesso e regolarmente associata a infezioni batteriche secondarie. Sono note anche le efflorescenze emorragiche gravi, a volte pericolose per la vita, e il coinvolgimento degli organi nell’immunodeficienza. Già nell’infanzia, esiste un rischio di riattivazione endogena del VZV (herpes zoster), in genere quando un bambino contrae la varicella nei primi mesi di vita. Tuttavia, la varicella non è una malattia esclusivamente infantile. Chi non si infetta durante l’infanzia, lo farà prima o poi in età adulta, con conseguenze spiacevoli. Questo perché una malattia in età adulta è solitamente più grave ed è spesso accompagnata da complicazioni. Soprattutto durante la gravidanza, è necessario evitare di contrarre la varicella, in quanto può danneggiare il feto e, nel peggiore dei casi, provocare un parto morto.
Patogenesi
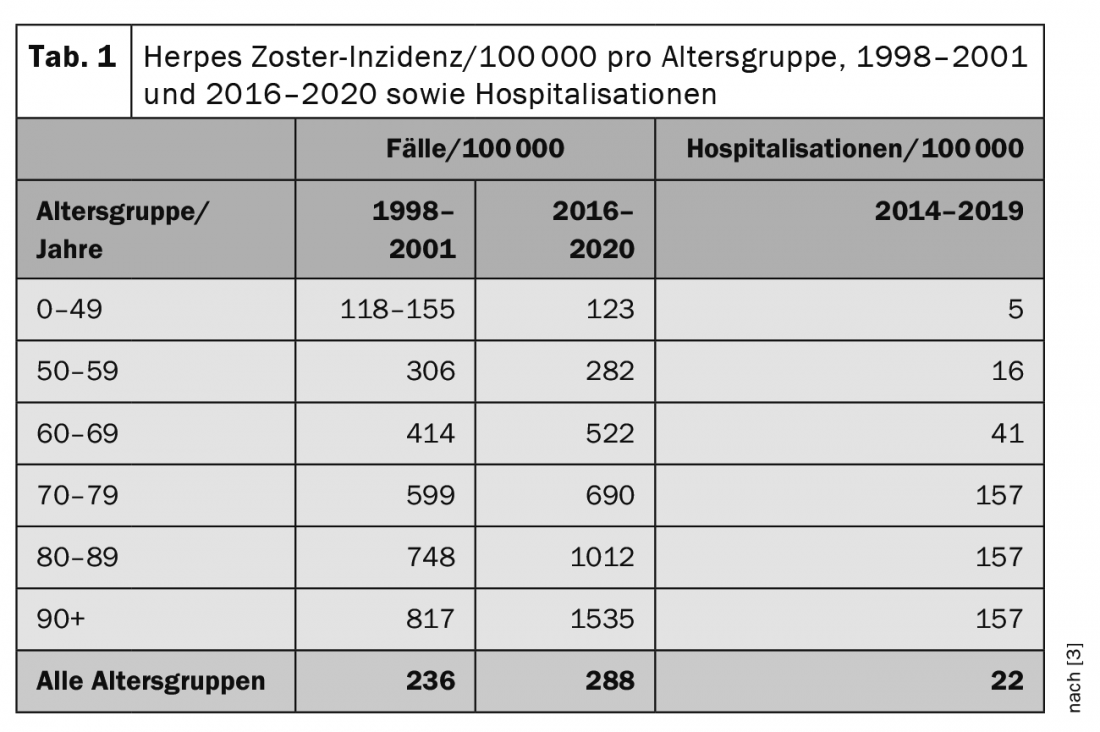
L’infezione iniziale con il virus della varicella-zoster porta, da un lato, all’immunità dalla reinfezione attraverso l’esposizione esogena e, dall’altro, alla protezione dalla riattivazione endogena. Presumibilmente, c’è un rafforzamento del sistema immunitario in caso di nuovo contatto con il virus o in caso di herpes zoster stesso. Tuttavia, questo potenziamento naturale non è molto efficiente, motivo per cui si osservano sempre più riattivazioni con l’aumentare dell’età (Fig. 1) [1].

Il motivo della comparsa dell’herpes zoster è la persistenza del virus della varicella zoster. Si presume che dopo la guarigione delle lesioni dell’eruzione cutanea originale, dove i virus si diffondono in modo ematogeno e sono presenti al massimo in centinaia di efflorescenze sulla pelle, migrino di nuovo lungo i nervi sensoriali nel midollo spinale, dove risiedono nel corno posteriore in una fase di latenza e rimangono per tutta la vita. Se poi l’immunità diminuisce, ad esempio a causa di farmaci, immunosoppressione o invecchiamento naturale del sistema immunitario, il virus ritorna sulla pelle lungo questi nervi e porta alla classica immagine a metà dell’herpes zoster.
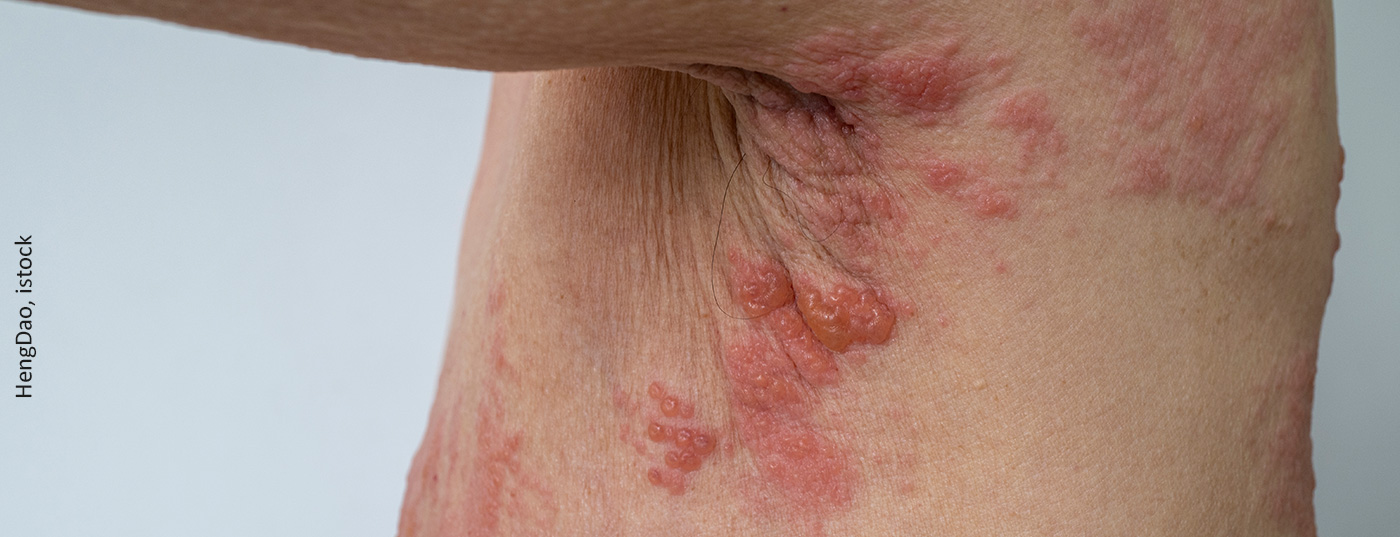
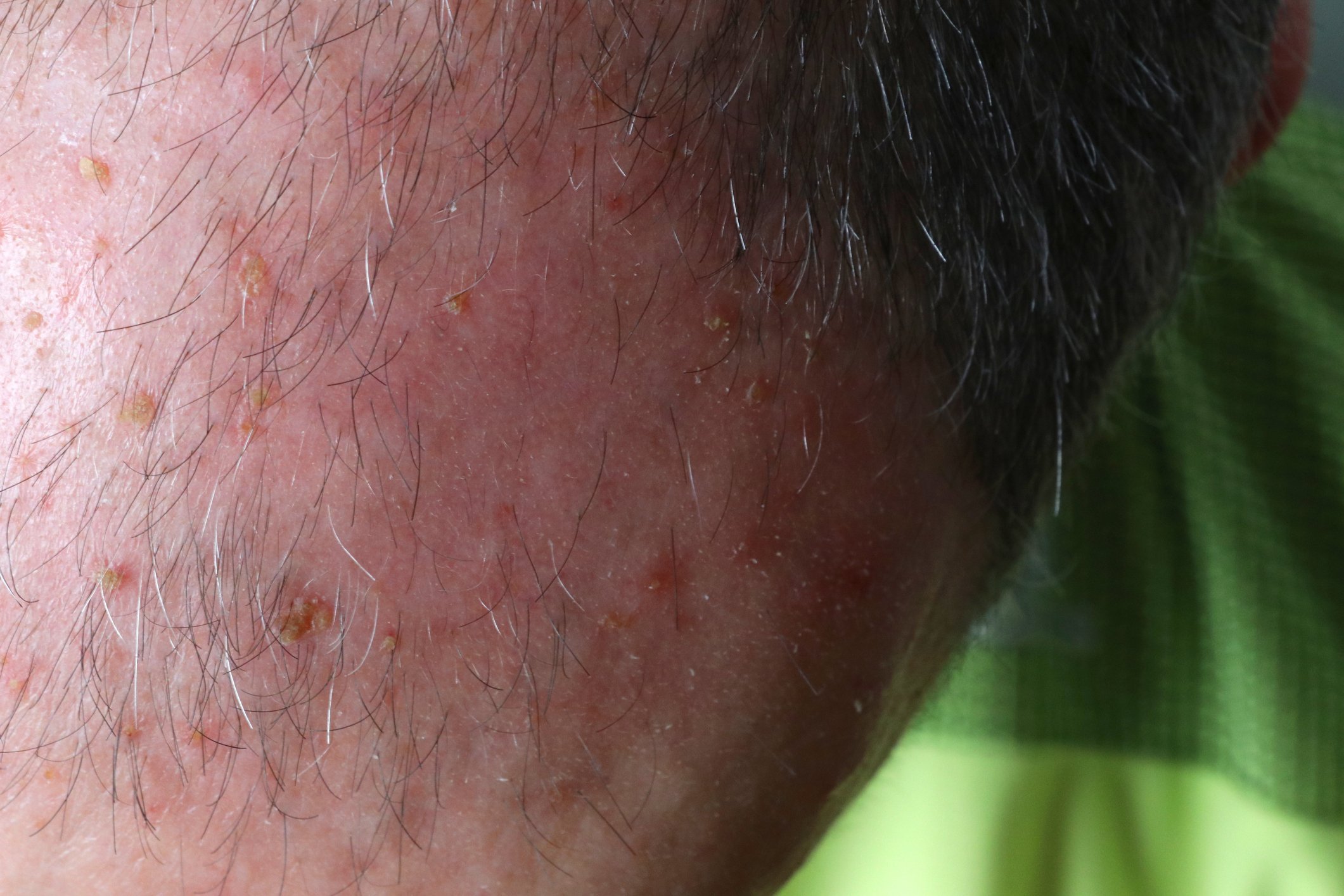
Presentazione clinica dell’herpes zoster
Il quadro clinico dell’herpes zoster si manifesta con efflorescenze dolorose, raggruppate nel rispettivo dermatoma che subisce la riattivazione. L’herpes zoster è temuto anche per la nevralgia post-erpetica. La probabilità di convivere con un dolore intenso per settimane o mesi dopo aver superato la malattia è correlata all’età. Se la malattia viene diagnosticata all’età di 30 anni, colpisce il 7% dei pazienti, a 50 anni il 12% e a 70 anni il 18%. Si temono anche complicazioni oftalmologiche nel viso, soprattutto nella parte superiore del trigemino, dove viene colpito l’occhio. Queste possono portare alla formazione di cicatrici nella cornea e danneggiare la vista [2].
Epidemiologia
In Svizzera, il sistema di sorveglianza Swiss Sentinella ha stimato l’incidenza annuale delle visite del medico di famiglia dovute all’herpes zoster nei quattro anni dal 1998 al 2001. I risultati hanno mostrato una media stabile di circa 17.000 casi all’anno. Nel gruppo di età compreso tra 60 e 69 anni, sono stati segnalati circa 2700 casi all’anno, nel gruppo di età compreso tra 70 e 79 anni circa 3000 casi all’anno e nel gruppo di età di 80 anni e oltre circa 2200 casi all’anno. Dal 2016, l’herpes zoster è stato nuovamente segnalato nel sistema di sorveglianza Sentinella. (Tab. 1) [3] mostra le incidenze annuali estrapolate per i due periodi di indagine (valori medi) per gruppo di età. Nel corso della vita, il rischio di contrarre l’herpes zoster è cumulativo. Si stima che circa il 10-20% di tutte le persone si ammali almeno una volta nel corso della vita. Inoltre, negli ultimi 10-20 anni si può osservare un aumento significativo del numero di casi di herpes zoster, soprattutto nelle persone anziane. La ragione di ciò è probabilmente che negli ultimi anni sono state introdotte in questa fascia d’età diverse opzioni terapeutiche di natura medicinale (“biologici”). Sebbene questi consentano un trattamento più efficace, ad esempio, del lupus eritematoso sistemico (LES) o dell’artrite reumatoide (RA), come effetto collaterale possono portare a un’immunodeficienza parziale e quindi aumentare il rischio di herpes zoster. Il rischio di dover essere ricoverati in ospedale a causa di un decorso grave dell’herpes zoster è quindi correlato anche all’età. Ogni anno in Svizzera si registrano circa 30.000 nuovi casi di herpes zoster [3,4].
Prevenzione vaccinale – “La regina della medicina
Già nel 2018, l’Ufficio federale della sanità pubblica (UFSP) e la Commissione federale per le domande di immunizzazione (EKIF) hanno raccomandato per la prima volta la vaccinazione contro l’herpes zoster con un nuovo vaccino vivo attenuato (Zostavax).®) per i seguenti due gruppi di persone: Persone immunocompetenti di età compresa tra 65 e 79 anni e persone immunocompromesse di età compresa tra 50 e 79 anni, a condizione che non siano ancora immunocompromesse o lo siano solo leggermente al momento della vaccinazione. La vaccinazione viene somministrata indipendentemente dal fatto che la persona abbia già avuto la varicella e/o l’herpes zoster. Questo vaccino vivo contiene 14 volte più virus della varicella zoster rispetto a Varivax® ed è quindi altamente concentrato per potenziare l’immunità primaria naturale della persona vaccinata. Il programma di vaccinazione raccomandato corrisponde a una dose (0,65 ml s.c.) ed è indicato per la prevenzione dell’herpes zoster e della nevralgia post-erpetica (PHN) causata dall’herpes zoster [5].
Vaccino vivo Zostavax®
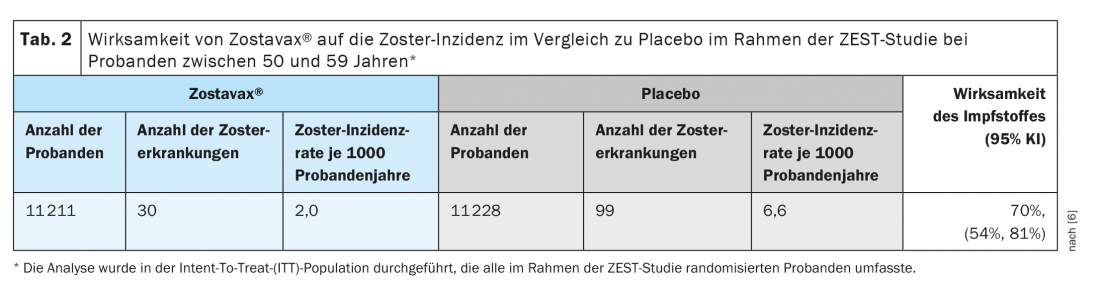
L’efficacia clinica protettiva del vaccino vivo è stata dimostrata in due ampi studi clinici randomizzati e controllati con placebo, in cui i soggetti hanno ricevuto il vaccino per via sottocutanea. Lo studio ZEST è stato un trial clinico in doppio cieco, controllato con placebo, in cui 22.439 soggetti di età compresa tra 50 e 59 anni sono stati randomizzati a ricevere una singola dose di vaccino o placebo e sono stati seguiti per una mediana di 1,3 anni (da 0 a 2 anni) per lo sviluppo dello zoster. La determinazione finale dei casi di zoster è stata effettuata mediante la reazione a catena della polimerasi (PCR) (86%) o da un gruppo di valutazione clinica (14%). Zostavax® ha provocato una diminuzione significativa dei casi di zoster con un’efficacia del 70% rispetto al placebo (Tab. 2) [6].
Anche lo studio SP era uno studio clinico in doppio cieco, controllato con placebo, in cui 38 546 soggetti di età pari o superiore a 60 anni sono stati randomizzati a ricevere una singola dose di vaccino o placebo e sono stati seguiti per una mediana di 3,1 anni (da 31 giorni a 4,9 anni) per lo sviluppo dello zoster. Nello studio SP, sebbene lo zoster sia diminuito in quasi tutti i dermatomi, l’efficacia del vaccino è diminuita. Questo era dell’ordine del 50-60% per i soggetti di età compresa tra 60 e 69 anni o addirittura ben al di sotto del 50% a partire dai 70 anni (Tabella 3) [6].

Vaccino morto Shingrix®
Recentemente, in Svizzera è stato introdotto un ulteriore sviluppo del vaccino contro l’herpes zoster, che viene somministrato da tempo a livello internazionale. Si tratta del vaccino inattivato Shingrix®, che contiene 50 µg di glicoproteina E del virus della varicella-zoster (antigene gE) + adiuvante AS01B. Il coadiuvante AS01B è composto dall’estratto vegetale Quillaja saponaria Molina, frazione 21 (QS-21) (50 µg) e dal 3-O-desacil-4′-monofosforil lipide A (MPL) di Salmonella minnesota (50 µg). Il programma di vaccinazione raccomandato corrisponde a due dosi (0,5 ml i.m.) a intervalli di due mesi ed è indicato per la prevenzione dell’herpes zoster a partire dai 18 anni di età.
Come per tutte le infezioni virali, l’immunità umana è diretta contro i componenti della superficie del virus varicella-zoster, presentati dalle cellule immunodominanti dopo l’infezione. La glicoproteina E è una proteina simile al processo spinoso sulla superficie del virus della varicella-zoster ed è il bersaglio principale della risposta immunitaria umorale e cellulare contro il virus [7].
In uno studio di ricerca della dose, i soggetti hanno ricevuto 25, 50 o 100 µg di un candidato vaccino contro l’herpes zoster contenente la glicoproteina E (gE) del virus della varicella zoster con o senza il sistema adiuvante AS01B. La frequenza delle cellule T CD4+ gE-specifiche era >3 volte superiore dopo due dosi di tutte le formulazioni gE/AS01B rispetto a una dose di 100 µg gE/AS01B o a due dosi di 100 µg gE/sale. Le frequenze erano comparabili dopo due dosi di 25, 50 o 100 µg gE/AS01B. Le concentrazioni sieriche di anticorpi anti-GE erano comparabili e più elevate rispetto agli altri gruppi dopo due dosi di 50 o 100 µg di gE/AS01B. Le risposte immunitarie sono durate per almeno 36 mesi. La reattività di tutte le formulazioni gE/AS01B era simile ma superiore a quella di gE/sale. I risultati hanno mostrato che le tre formulazioni di gE/AS01B erano immunogene e ben tollerate dagli adulti di età ≥60 anni. Inoltre, due vaccinazioni con gE/AS01B hanno indotto risposte immunitarie più elevate rispetto a una sola e la dose di gE ha influenzato la risposta immunitaria umorale ma non quella cellulare [8].
Efficacia e tollerabilità
Lo studio ZOE-50, condotto su un totale di 15.411 adulti di età pari o superiore a 50 anni, ha dimostrato che il vaccino a subunità per l’herpes zoster (HZ/su), contenente la glicoproteina E ricombinante del virus della varicella zoster e il sistema adiuvante AS01B, è stato associato a un rischio di herpes zoster inferiore del 97,2% (intervallo di confidenza del 95%, da 93,7 a 99,0; p<0,001) rispetto al placebo. L’efficacia del vaccino era compresa tra il 96,6% e il 97,9% per tutti i gruppi di età (Tab. 4) [9].
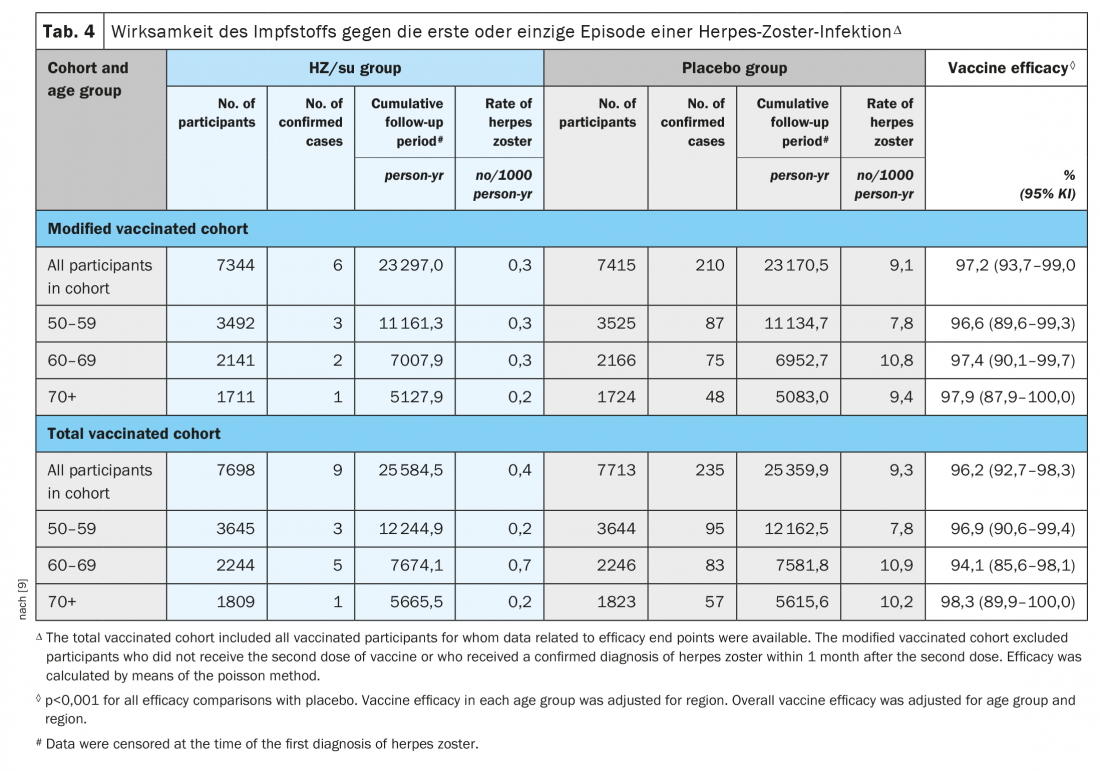
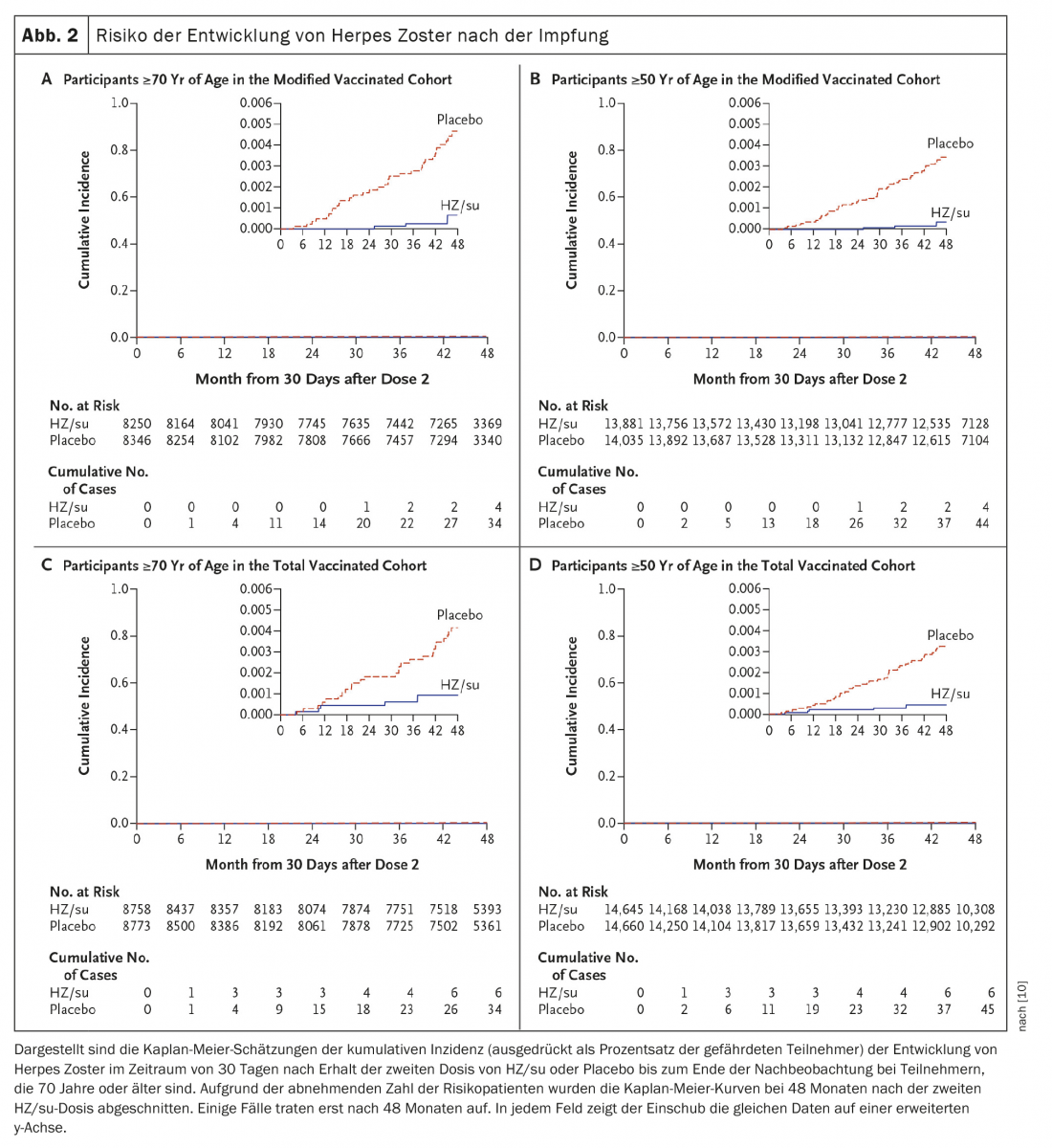
Un secondo studio è stato condotto contemporaneamente negli stessi siti e ha analizzato la sicurezza e l’efficacia di HZ/su negli adulti di età pari o superiore a 70 anni (ZOE-70). Nello ZOE-70, 13 900 partecipanti valutabili (età media 75,6 anni) hanno ricevuto HZ/su (6950 partecipanti) o placebo (6950 partecipanti). Durante un follow-up mediano di 3,7 anni, l’herpes zoster si è verificato in 23 riceventi HZ/su e in 223 riceventi placebo (0,9 vs. 9,2 per 1000 anni-persona). L’efficacia del vaccino contro l’herpes zoster è stata dell’89,8% (intervallo di confidenza al 95%, da 84,2 a 93,7; p<0,001) ed è stata simile nei partecipanti di età compresa tra 70 e 79 anni (90,0%) e nei partecipanti di età pari o superiore a 80 anni (89,1%). Nelle analisi in pool dei dati dei partecipanti di età pari o superiore a 70 anni a ZOE-50 e ZOE-70 (16 596 partecipanti), l’efficacia del vaccino contro l’herpes zoster è stata del 91,3% (95% CI, da 86,8 a 94,5; p<0,001) e l’efficacia del vaccino contro la nevralgia post-erpetica dell’88,8% (95% CI, da 68,7 a 97,1; p<0,001) (Fig. 2) [10].
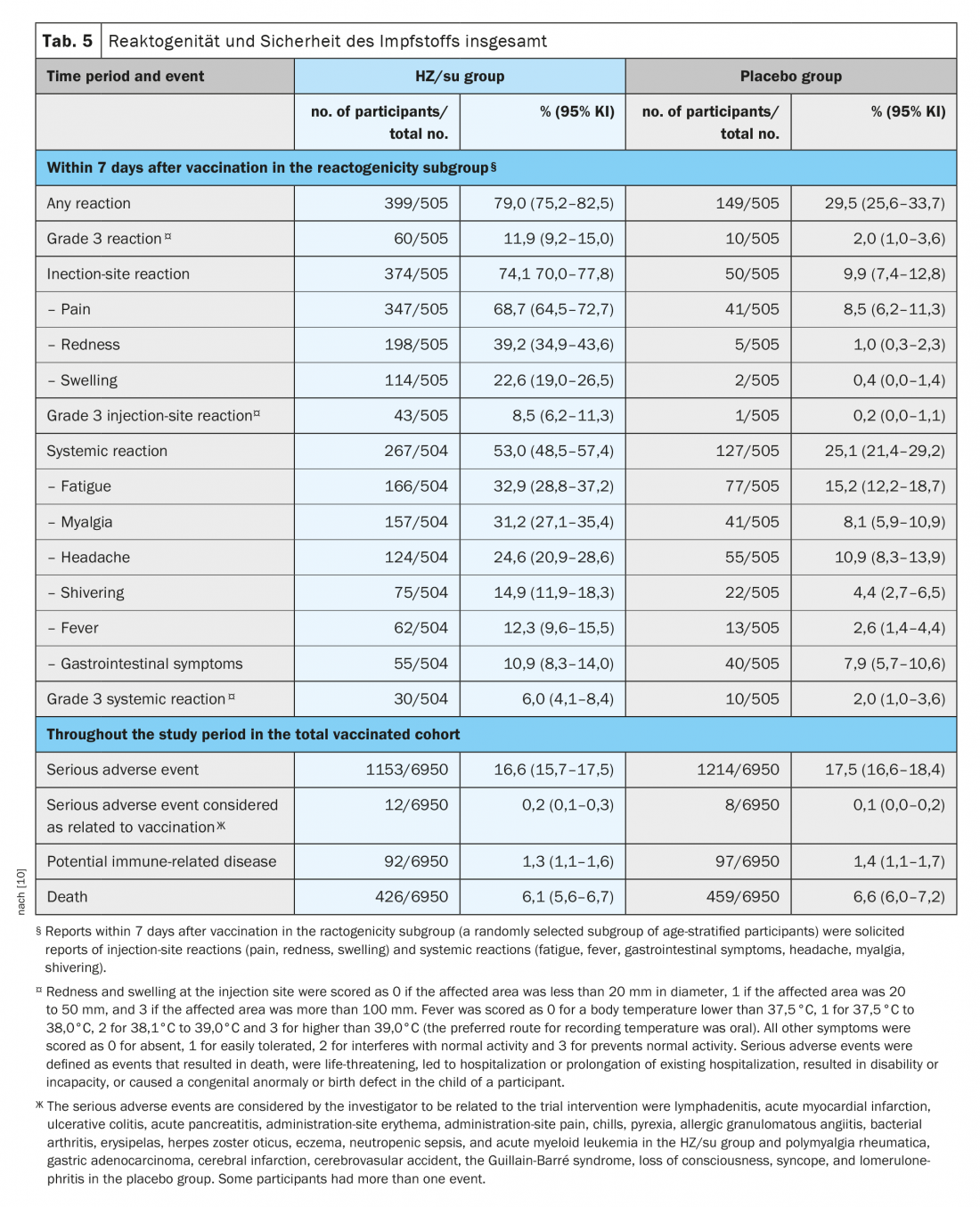
Nello studio ZOE-70, un totale di 1025 partecipanti (7,4%) sono stati assegnati in modo casuale al sottogruppo di reattogenicità (512 riceventi HZ/su e 513 riceventi placebo). In questo sottogruppo, le segnalazioni di reazioni richieste si sono verificate entro sette giorni da ciascuna vaccinazione nel 79,0% dei riceventi HZ/su e nel 29,5% dei riceventi placebo (Tabella 5) [10]. Mentre le reazioni al sito di iniezione si sono verificate nel 74,1% dei riceventi HZ/su e nel 9,9% dei riceventi placebo; la maggior parte delle reazioni erano di intensità lieve o moderata. Reazioni di grado 3 al sito di iniezione sono state segnalate nell’8,5% dei riceventi HZ/su e nello 0,2% dei riceventi placebo. Le reazioni sistemiche si sono verificate nel 53,0% dei riceventi HZ/su e nel 25,1% dei riceventi placebo (le reazioni di grado 3 sono state riportate nel 6,0% e nel 2,0%, rispettivamente). Nel gruppo HZ/su, la reazione più comune al sito di iniezione è stata il dolore (nel 68,7% dei riceventi HZ/su) e la reazione sistemica più comune è stata l’affaticamento (nel 32,9%). Le reazioni sono state transitorie, con una durata mediana di due o tre giorni per le reazioni al sito di iniezione, di uno o due giorni per le reazioni sistemiche e di uno o due giorni per le reazioni di grado 3. La frequenza complessiva e la gravità delle reazioni innescate non sono aumentate in modo significativo dopo la seconda dose. [10].
Nuova raccomandazione per la vaccinazione contro l’herpes zoster
Sulla base di questi risultati, chiaramente positivi rispetto al vaccino vivo, l’UFSP e l’EKIF raccomandano la vaccinazione contro l’herpes zoster con il vaccino a subunità adiuvato Shingrix® dal 2021. Questo vale sia per le persone sane di età pari o superiore a 65 anni, sia per i pazienti con immunodeficienza di età pari o superiore a 50 anni o con immunodeficienza grave di età pari o superiore a 18 anni. Le precedenti raccomandazioni del novembre 2017 per il vaccino vivo Zostavax® si applicano ora solo alle persone di età compresa tra 65 e 79 anni senza immunodeficienza, che preferiscono Zostavax® a Shingrix® [3].
Shingrix® è raccomandato come vaccinazione supplementare per tutti gli individui immunocompetenti di età ≥65 anni, indipendentemente dalla loro storia individuale di varicella e herpes zoster. I medici sono tenuti a informare i loro pazienti su questa opzione di vaccinazione. Inoltre, Shingrix® è raccomandato per tutti i pazienti di età ≥50 anni con immunodeficienza attuale o futura (soprattutto cellulare) associata a un aumento del rischio di herpes zoster. Questo riguarda, ad esempio, le persone sieropositive o i pazienti prima, durante o dopo una terapia oncologica attiva. In questi pazienti, la prima dose dovrebbe essere somministrata idealmente ≥2 settimane prima dell’inizio della chemioterapia. La seconda dose con un intervallo minimo di uno o due mesi dopo la prima dose o il prima possibile durante o dopo la chemioterapia. Sono colpiti anche i pazienti con malattia renale in fase terminale o in dialisi, in terapia con biologici, azatioprina, metotrexato a basso dosaggio o corticosteroidi di mantenimento a basso dosaggio, e i pazienti con altre malattie di base che compromettono l’immunità (soprattutto quella cellulare). Questo include anche, ad esempio, i pazienti con artrite reumatoide, asma/COPD grave, diabete mellito di tipo 1 non adeguatamente controllato e altre malattie autoimmuni. In questi soggetti, si raccomandano due dosi di Shingrix® con un intervallo minimo di due mesi.
Inoltre, Shingrix® è raccomandato per i pazienti di età ≥18 anni che soffrono attualmente di immunodeficienza grave o che stanno ricevendo un trattamento immunosoppressivo o che lo riceveranno nel prossimo futuro. In questo caso, la prima dose dovrebbe essere somministrata idealmente ≥4 settimane prima di un’insorgenza presunta, prevista o programmata di immunosoppressione grave. La seconda dose con un intervallo minimo di uno o due mesi dopo la prima dose o il prima possibile in un momento successivo favorevole dal punto di vista medico durante o dopo la terapia. Questi includono, ad esempio, i pazienti con neoplasie ematologiche, i riceventi di cellule staminali ematopoietiche e di trapianti d’organo, le persone in trattamento con inibitori JAK o con immunosoppressione intensiva (ad esempio, combinazioni di immunosoppressori, corticosteroidi ad alte dosi) a causa di una malattia immuno-mediata, come l’artrite reumatoide o la malattia infiammatoria intestinale, e le persone HIV-positive con <200 cellule T CD4+/l o <5% di percentuale di linfociti.
Nelle donne in gravidanza o in fase di allattamento, è necessario effettuare un’attenta valutazione individuale del rapporto rischio/beneficio. La sierologia VZV (test degli anticorpi) non è raccomandata prima della vaccinazione con Shingrix®. Né Shingrix® né Zostavax® devono essere utilizzati per prevenire l’infezione iniziale da VZV (varicella = varicella).
Raccomandazioni per il vaccino vivo Zostavax
Il vaccino vivo Zostavax® attualmente disponibile è controindicato nelle persone con immunodeficienza e non dovrebbe più essere utilizzato nelle persone che ricevono terapie immunosoppressive nel prossimo futuro. Zostavax® rimane un’opzione per le persone immunocompetenti di età compresa tra 65 e 79 anni che preferiscono Zostavax® a Shingrix®. Zostavax® non è rimborsato dall’OKP.
Messaggi da portare a casa
- L’herpes zoster è una malattia onerosa e potenzialmente pericolosa, ma oggi è efficacemente e facilmente prevenibile attraverso la vaccinazione.
- Il vaccino ricombinante adiuvato contro lo zoster fornisce una profilassi efficace ai pazienti.
- Uno dei compiti dei medici professionisti è quindi quello di mettere l’assistenza sanitaria preventiva per i pazienti in cima alla lista delle priorità.
Letteratura:
- Arvin A: L’immunità e il virus Varicella-Zoster. N Engl J Med 2005; doi: 10.1056/NEJMp058091.
- Eidgenössische Kommission für Impffragen (EKIF): Valutazione dei vaccini e della vaccinazione contro l’herpes zoster (ZOSTAVAX® e SHINGRIX®), 2021.
- Ufficio federale della sanità pubblica UFSP: Bollettino UFSP 47/2021, edizione del 27 novembre 2021.
- Bundesamt für Gesundheit = Ufficio federale della sanità pubblica. Vaccinazione contro l’herpes zoster: non inclusa nel calendario vaccinale svizzero. Bollettino BAG – OFSP 2010(6): 97.
- Ufficio federale della sanità pubblica, Commissione federale per le questioni di immunizzazione (EKIF): Schweizerischer Impfplan 2018. Linee guida e raccomandazioni. Berna: Ufficio federale della sanità pubblica, 2018.
- Informazioni specialistiche Zostavax®, disponibili su: www.ema.europa.eu/en/documents/product-information/zostavax-epar-product-information_de.pdf.
- Zerboni L, et al: Meccanismi molecolari della patogenesi del virus varicella zoster. Nat Rev Microbiol 2014; doi: 10.1038/nrmicro3215.
- Chlibek R, et al: Sicurezza e immunogenicità di tre diverse formulazioni di un candidato vaccino a subunità di virus varicella-zoster adiuvato negli adulti più anziani: uno studio di fase II, randomizzato e controllato. Vaccino 2014; doi: 10.1016/j.vaccine.2014.01.019.
- Lal H, et al: Efficacia di un vaccino adiuvato con subunità di Herpes Zoster negli anziani. N Engl J Med 2015; doi: 10.1056/NEJMoa1501184.
- Cunningham AL, et al: Efficacia del vaccino a subunità dell’Herpes Zoster negli adulti di 70 anni o più. N Engl J Med 2016; doi: 10.1056/NEJMoa1603800.
PRATICA GP 2022; 17(10): 6-12