Non tutti i pazienti depressi in remissione traggono beneficio dagli antidepressivi in termini di prevenzione delle ricadute. Molti pazienti vogliono interrompere l’assunzione di antidepressivi, in parte a causa degli effetti collaterali indesiderati. Attualmente non ci sono predittori di quali pazienti avranno una ricaduta e quali no. È possibile che i biomarcatori neurobiologici possano servire come predittori. L’Antidepressant Discontinuation Trial (AIDA) sta studiando i predittori di un’interruzione sicura, continuando a cercare i pazienti che sono in remissione e vogliono interrompere il loro antidepressivo.
La ricaduta è un problema clinicamente molto rilevante nel trattamento della depressione. La prevalenza nell’arco della vita di una ricaduta è molto alta, pari al 60% dopo il primo episodio, e il rischio aumenta con l’aumentare del numero di episodi [1]. Senza farmaci antidepressivi (ADM), due terzi dei pazienti hanno una ricaduta entro due anni, mentre con l’ADM solo un terzo circa lo fa [2]. Da un lato, questo dimostra che il rischio di ricaduta può essere ridotto del 50% (dal 60% al 30%) continuando il trattamento con ADM. D’altra parte, due terzi dei pazienti non traggono sufficiente beneficio dall’ADM, perché hanno avuto una ricaduta nonostante l’ADM o perché non avrebbero avuto una ricaduta anche senza ADM. Un terzo dei pazienti probabilmente trae beneficio e non ha una ricaduta grazie all’ADM.
Aumenta la motivazione a continuare a prendere gli antidepressivi
Gli antidepressivi sono noti per avere effetti collaterali come disfunzioni sessuali o aumento di peso. A causa di questi effetti collaterali, molti pazienti interrompono il farmaco su loro richiesta e spesso contro il parere del medico [3,4] – compreso il terzo che molto probabilmente trarrebbe beneficio dalla continuazione dell’ADM. Inoltre, è dimostrato che l’uso prolungato di ADM porta allo sviluppo della tolleranza e potrebbe aumentare artificialmente il rischio di ricaduta dopo l’interruzione, inducendo processi controregolatori [5]. Il trattamento individualizzato con una raccomandazione di trattamento personalizzata potrebbe quindi avere un elevato valore clinico a lungo termine. Se i pazienti sanno che il trattamento continuo con un ADM è necessario per loro personalmente per prevenire le ricadute, questo potrebbe anche aumentare la motivazione ad assumere il farmaco.
Come si può prevedere il rischio di ricaduta?
Per decidere se un determinato paziente beneficerà o meno di un ulteriore trattamento con ADM, abbiamo bisogno di predittori che prevedano il decorso della malattia depressiva e distinguano tra i diversi gruppi di pazienti. I predittori possono essere, ad esempio, informazioni cliniche, variabili genetiche, biomarcatori o una combinazione di queste variabili. In realtà, però, la letteratura e la ricerca su questo tema sono molto scarse. Un fattore predittivo del rischio di ricaduta dopo l’interruzione potrebbe essere il tipo di risposta all’ADM. Un rischio maggiore sembra essere presente nei pazienti che rispondono lentamente ma in modo persistente all’ADM, mentre i pazienti che rispondono rapidamente ma non in modo persistente (i cosiddetti “responder al placebo”) non presentano un rischio maggiore di ricaduta dopo l’interruzione [6,7]. La durata del trattamento è un altro possibile fattore predittivo, a cui si fa riferimento anche nelle linee guida sulla terapia di mantenimento [8]. Le raccomandazioni si basano sull’osservazione del decorso naturale degli episodi depressivi. Poiché un episodio depressivo di solito dura da sei a nove mesi, questa è anche approssimativamente la durata raccomandata della terapia di mantenimento [9]. Sorprendentemente, però, gli studi non hanno ancora dimostrato chiaramente che il rischio di ricaduta dopo l’interruzione diminuisce con la durata del trattamento [2,10–12].
Un altro potenziale predittore è il numero di episodi precedenti. Sebbene si presuma che un maggior numero di episodi aumenti il rischio di ricaduta dopo l’interruzione, ad esempio a causa del fatto che il rischio complessivo di ricaduta aumenta con il numero di episodi precedenti, due meta-analisi su questo argomento sono giunte a conclusioni opposte [11,12].
I biomarcatori come predittori del rischio di ricaduta
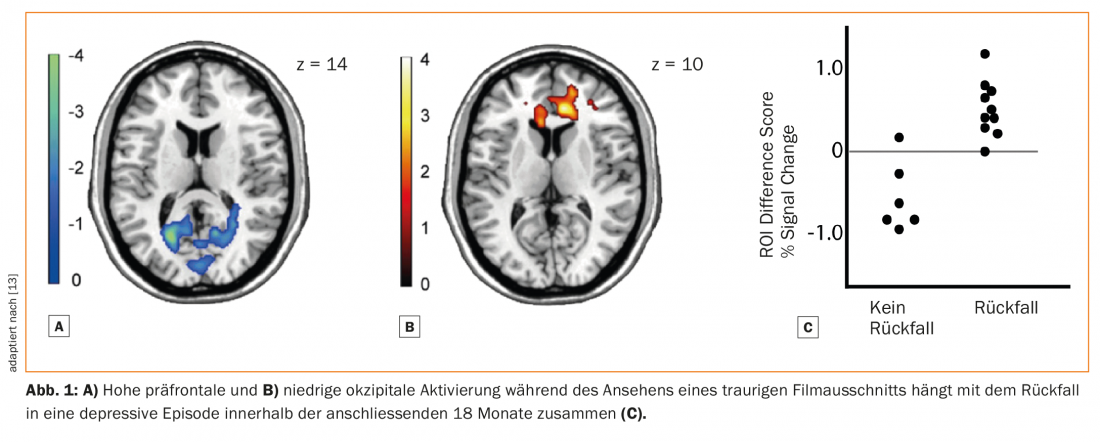
A nostra conoscenza, nessuno studio ha ancora esaminato il potenziale dei biomarcatori come predittori del rischio di ricaduta dopo l’interruzione dell’ADM. I biomarcatori neurobiologici sono stati studiati finora solo in relazione al rischio generale di ricaduta, indipendentemente dall’uso di ADM. Per esempio, uno studio ha utilizzato la risonanza magnetica funzionale (fMRI) per esaminare l’attività cerebrale mentre i soggetti guardavano film tristi. Una diminuzione dell’attività occipitale, rispetto a quella prefrontale mediale, ha predetto la ricaduta (Fig. 1) [13]. Un altro studio ha utilizzato stimoli che hanno innescato i sensi di colpa. In questo caso, una maggiore connettività tra la corteccia prefrontale mediale e il lobo temporale anteriore ha predetto la ricaduta [14].
Il ruolo rilevante della corteccia prefrontale mediale nell’anedonia, uno dei sintomi principali della depressione, è stato confermato anche nei modelli animali. Nei roditori, la corteccia prefrontale mediale controlla l’interazione dopaminergica del mesencefalo con lo striato [15]. L’aumento dell’attività della corteccia prefrontale mediale porta a una riduzione della ricerca della ricompensa, che spesso si riflette nelle persone come un disturbo pulsionale.
In sintesi, sarebbe clinicamente utile identificare i pazienti che beneficerebbero di un ulteriore trattamento con ADM. Sebbene non esistano ancora predittori per questo, le caratteristiche neurobiologiche hanno un grande potenziale. Per questo, è importante studiare gli effetti neurobiologici dello svezzamento stesso, che sono ancora poco conosciuti.

Lo studio sullo svezzamento AIDA
L’obiettivo dello Studio sulla Discontinuazione degli Antidepressivi (AIDA, www.absetzstudie.ch), finanziato dalla Fondazione Nazionale Svizzera per la Scienza e dalla Fondazione Tedesca per la Ricerca, è quello di trovare, da un lato, i predittori per una sospensione sicura dell’ADM e, dall’altro, di indagare l’effetto della sospensione dei farmaci sulla neurobiologia e sul comportamento dei pazienti. Lo studio viene condotto presso l’Unità di Neuromodellismo Traslazionale in collaborazione con l’Ospedale Psichiatrico Universitario di Zurigo e la Charité di Berlino. La reattività emotiva, la pianificazione del comportamento e la regolazione delle emozioni sono registrate con l’imaging funzionale (fMRI ed EEG). In combinazione con i nuovi approcci della cosiddetta “psichiatria computazionale” [16], questi vengono modellati matematicamente e quantificati [17]. Inoltre, si stanno studiando anche le misure che hanno dimostrato di essere buoni predittori della risposta all’ADM. L’obiettivo a lungo termine è identificare parametri clinicamente rilevanti e misurabili per rendere lo svezzamento più sicuro.
Conclusione
La prevenzione delle ricadute è una componente importante del trattamento di successo della depressione a lungo termine. Sebbene gli antidepressivi siano complessivamente efficaci nel prevenire le ricadute, non tutti i pazienti rispondono. Gli effetti collaterali possono creare difficoltà significative per i trattamenti a lungo termine e molti pazienti optano per un trattamento farmacologico a lungo termine. Per ridurre al minimo le ricadute, sarebbe importante identificare i pazienti che possono sospendere i farmaci in modo sicuro. Tuttavia, finora non sono stati trovati predittori di interruzione sicura. I biomarcatori neurobiologici potrebbero servire come buoni predittori. Ecco perché stiamo attualmente conducendo l’Antidepressant Discontinuation Study (AIDA) a Zurigo e Berlino, uno studio osservazionale con l’obiettivo di identificare i predittori di un’interruzione sicura.
Letteratura:
- Associazione Psicologica Americana: Manuale diagnostico e statistico – revisione del testo (DSM-IV-TR). APA 2000.
- Geddes JR, et al: Prevenzione delle ricadute con il trattamento farmacologico antidepressivo nei disturbi depressivi. Una revisione sistematica. Lancet 2003; 361(9358): 653-661.
- Olfson M, et al: Continuità del trattamento antidepressivo per gli adulti con depressione negli Stati Uniti. Am J Psychiatry 2006; 163(1): 101-108.
- Hunot VM, et al: Uno studio di coorte sull’aderenza agli antidepressivi nelle cure primarie. L’influenza delle preoccupazioni antidepressive e delle preferenze di trattamento. Prim Care Companion J Clin Psychiatry 2007; 9(2): 91-99.
- Andrews PW, et al: Ancora blu. Gli effetti perturbatori degli antidepressivi suggeriscono l’omeostasi monoaminergica nella depressione maggiore. Front Psychol 2011; 2.
- Nierenberg AA, et al: Trattamento di continuazione controllato con placebo con mirtazapina. Il modello di risposta acuta predice la ricaduta. Neuropsicofarmacologia 2004; 29(5): 1012-1018.
- Stewart JW, et al: Uso dell’analisi dei modelli per prevedere la ricaduta differenziale dei pazienti con depressione maggiore rimessi durante 1 anno di trattamento con fluoxetina o placebo. Arch Gen Psychiatry 1998; 55(4): 334-343.
- DGPPN, et al.: per il gruppo di linee guida Depressione unipolare. S3-Leitlinie/Nationale Versorgungsleitlinie Unipolare Depression – Langfassung, 2. Auflage. 2015.
- Spijker J, et al: Durata degli episodi depressivi maggiori nella popolazione generale. Risultati del Netherlands Mental Health Survey and Incidence Study (NEMESIS). Br J Psychiatry J Ment Sci 2002; 181: 208-213.
- Glue P, et al: Meta-analisi degli studi antidepressivi di prevenzione delle ricadute nei disturbi depressivi. Aust N Z J Psychiatry 2010; 44(8): 697-705.
- Kaymaz N, et al.: Evidenza che i pazienti con episodi depressivi singoli o ricorrenti sono sensibili in modo diverso all’interruzione del trattamento. Una meta-analisi di studi randomizzati controllati con placebo. J Clin Psychiatry 2008; 69(9): 1423-1436.
- Viguera AC, et al: Interruzione del trattamento antidepressivo nella depressione maggiore. Harv Rev Psychiatry 1998; 5(6): 293-306.
- Farb NAS, et al: Le risposte legate all’umore nella corteccia prefrontale mediale predicono la ricaduta nei pazienti con depressione unipolare ricorrente. Biol Psychiatry 2011; 70(4): 366-372.
- Lythe KE, et al: Iperconnettività selettiva di auto-colpevolezza tra corteccia temporale anteriore e corteccia subgenuale e previsione di episodi depressivi ricorrenti. JAMA Psychiatry 2015; 72(11): 1119-1126.
- Ferenczi EA, et al.: Regolazione corticale prefrontale delle dinamiche dei circuiti cerebrali e del comportamento legato alla ricompensa. Science 2016; 351(6268): aac9698.
- Huys QJM, et al.: La psichiatria computazionale come ponte dalle neuroscienze alle applicazioni cliniche. Nature Neurosci [accettato, pubblicazione anticipata].
- Huys QJM, et al: Interazione di strategie di pianificazione approssimative. Proc Natl Acad Sci USA 2015; 112(10): 3098-3103.
InFo NEUROLOGIA & PSICHIATRIA 2016; 14(2): 16-19.