Con l’approvazione di Dupilumab come primo biologico per il trattamento della dermatite atopica, sono stati compiuti progressi significativi. Come dimostra un’occhiata agli studi clinici in corso, la ricerca ha altre frecce nella sua faretra. Tra i biologici, i programmi di studio per l’anticorpo IL13 tralokinumab sono i più avanzati. Tra gli inibitori JAK, baricitinib è un candidato promettente che ha già ricevuto un’estensione dell’indicazione per la dermatite atopica nell’UE.
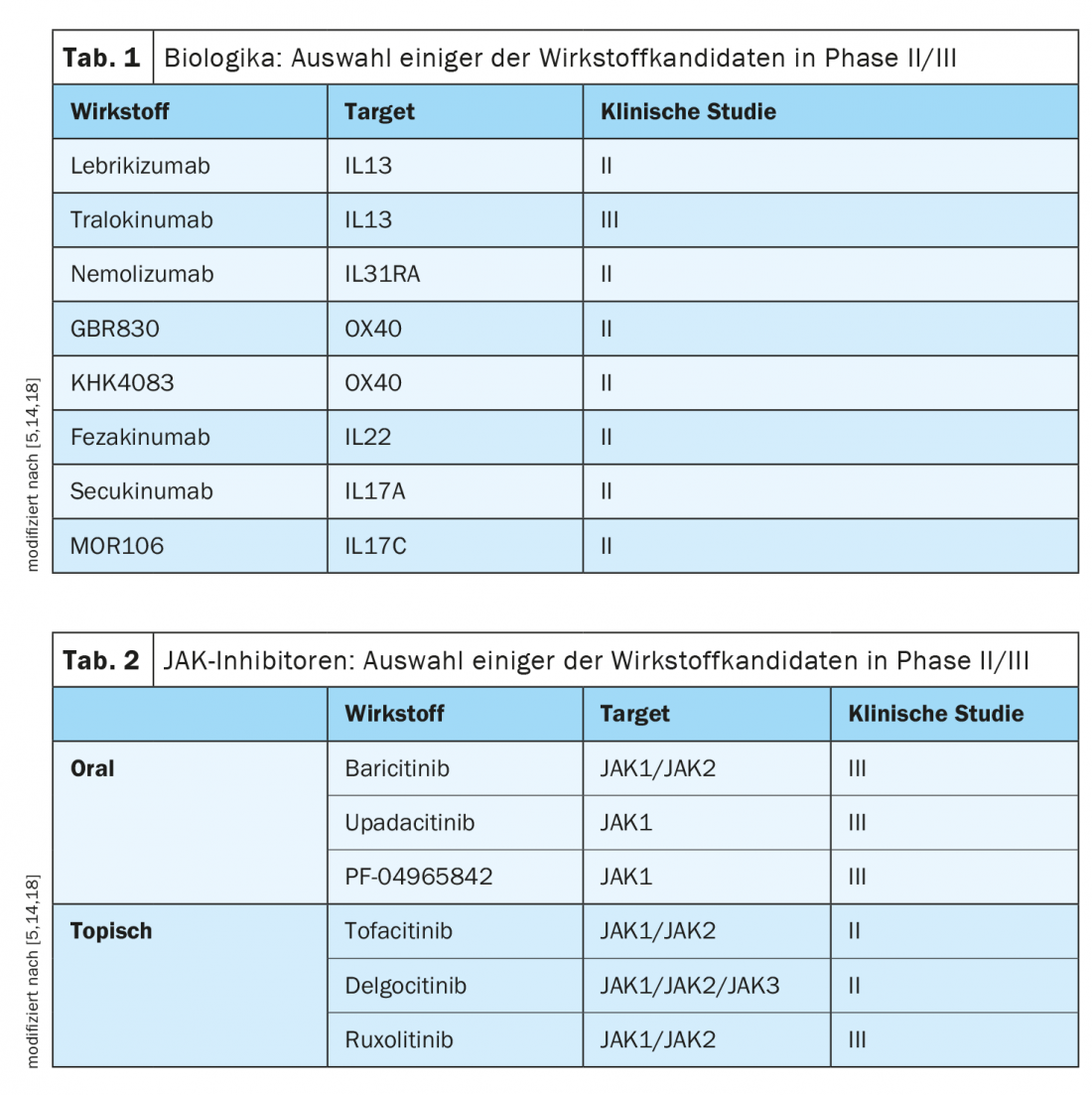
L’ulteriore sviluppo di approcci terapeutici mirati si basa, tra l’altro, sui progressi nella comprensione della complessa ed eterogenea base immunopatologica della dermatite atopica [1]. Secondo gli esperti, il panorama terapeutico di questa complessa malattia infiammatoria cambierà rapidamente nei prossimi anni. C’è una buona probabilità che, oltre a Dupilumab, altri rappresentanti della classe dei biologici amplieranno lo spettro di trattamento delle forme moderate e gravi della malattia in un futuro non troppo lontano. (Tab.1). Anche nel campo degli inibitori della JAK, ci sono diversi composti promettenti che sono in fase di sperimentazione clinica. (Tab.2). A differenza del cortisone o della ciclosporina, i biologici e gli inibitori della JAK influenzano selettivamente le singole cascate di attivazione del sistema immunitario. Di conseguenza, questi approcci terapeutici moderni non solo hanno un alto grado di efficacia, ma anche un profilo di effetti collaterali favorevole, che offre grandi vantaggi, soprattutto in considerazione del fatto che la dermatite atopica è un quadro clinico cronico e recidivante.
Il biologico Dupilumab (Dupixent®), approvato in Svizzera dal 2019 per la dermatite atopica da moderata a grave, ha dimostrato di essere estremamente efficace e ha un eccellente profilo beneficio-rischio. È il primo rappresentante degli anticorpi monoclonali per questa indicazione. Dupilumab inibisce le vie di segnalazione delle due citochine chiave IL4 e IL13, che sono considerate importanti motori del processo infiammatorio in corso nella dermatite atopica [2,3]. Che i risultati di grandi studi clinici come SOLO1/2, CHRONOS o CAFE siano confermati anche nella pratica, è dimostrato dai dati sulla valutazione di questa opzione terapeutica nel “mondo reale” [2,4,5]. I pazienti traggono un grande beneficio da questo trattamento, che si riflette anche in una buona aderenza [5]. Uno sguardo agli studi clinici in corso mostra che, oltre a dupilumab, altre terapie mirate potrebbero fare un passo avanti nei prossimi anni (Tab. 1 e 2).
Oltre a tralokinumab, anche lebrikizumab, con risultati promettenti.
Gli studi sui meccanismi immunopatologici nella dermatite atopica hanno dimostrato che le citochine IL4, IL13 e IL31 prodotte dalle cellule Th2 sono di importanza fisiopatologica centrale [6]. Tra gli agenti attualmente testati clinicamente, gli studi sull’inibitore dell’IL13 tralokinumab sono i più avanzati [5]. Negli studi di fase III ECZTRA 1 e 2, la condizione tralokinumab (300 mg ogni 2 settimane) ha mostrato un miglioramento significativo dell’IGA* rispetto al placebo (p<0,001) dopo solo 16 settimane [19]. Ciò ha confermato i buoni risultati dello studio di fase IIb, in cui sono stati raggiunti tassi di risposta fino al 70% per EASI50 e fino al 40% per EASI75 nei pazienti con dermatite atopica da moderata a grave [7].
* IGA = Valutazione Globale degli Investigatori
|
La dermatite atopica può portare a livelli elevati di sofferenza. Diversi studi empirici dimostrano che la dermatite atopica è spesso accompagnata da una notevole compromissione della qualità della vita. In uno studio basato sulla popolazione adulta, oltre la metà delle persone colpite ha riferito che la condizione della pelle era associata a limitazioni nella vita quotidiana, e per oltre un terzo l’aspetto ha portato a evitare i contatti sociali [15]. Inoltre, queste conseguenze negative sono risultate significativamente più pronunciate nei pazienti con dermatite atopica da moderata a grave, rispetto alle forme lievi della malattia. Secondo i dati attuali della ricerca sui servizi sanitari, circa un paziente di neurodermite su dieci è affetto da sintomi da moderati a gravi [16,17]. |
Anche per lebrikizumab sono disponibili buoni dati di efficacia. Anche questo è un inibitore dell’IL13. A differenza di tralokinumab, lebrikizumab impedisce il legame del complesso di segnalazione del recettore IL13R-α1 e dell’eterodimero IL4R-α, ma non il legame dell’IL13 al “recettore decoy IL13R-α2”, che può assorbire l’IL13 in eccesso [8]. I risultati degli studi di fase III in corso sono ancora in attesa. Nei due studi randomizzati di fase II controllati con placebo condotti finora, i pazienti trattati con lebrikizumab hanno mostrato una riduzione rapida e dose-dipendente del prurito, nonché un miglioramento significativo dell’EASI 50/75 e della BSA [9,10]. I pazienti sono stati randomizzati ai bracci di trattamento di 125 mg ogni quattro settimane, 250 mg ogni quattro settimane o 250 mg ogni due settimane per 16 settimane [11].
Un candidato farmaco interessante che ha come bersaglio l’IL31 è il nemolizumab. Sia gli studi proof-of-concept che le osservazioni più lunghe nella fase IIb hanno dimostrato un valore aggiunto nell’area del controllo del prurito [12]. Ulteriori studi mostreranno quale sia il potenziale di effetto rispetto ad altri parametri. Sono in fase di sperimentazione clinica anche i rappresentanti degli anticorpi anti-OX40, anti-IL22 e anti-IL17 [5].
Baricitinib presto approvato anche in Svizzera?
A differenza delle terapie basate sugli anticorpi, che di solito hanno come bersaglio le citochine o i recettori delle citochine, le piccole molecole interferiscono con le vie di segnalazione intracellulare. Il gruppo più numeroso di queste sostanze a piccole molecole è costituito dagli inibitori della Janus chinasi (JAK). Le JAK sono enzimi intracellulari che mediano la cascata di segnalazione da un recettore di citochina alla cellula. Finora sono stati sviluppati vari inibitori JAK con diverse capacità di legame con le singole sottoforme delle Janus chinasi (JAK1-3). Il baricitinib, una sostanza diretta contro JAK1/2, è uno degli inibitori orali di JAK più promettenti [5]. Nelle valutazioni dei primi studi clinici di fase II, è stata riportata un’efficacia dell’ordine del 60-82% per quanto riguarda i tassi EASI50, a seconda dei periodi di terapia e dei protocolli di studio [13]. Nell’UE, è già stata concessa un’estensione dell’indicazione per la dermatite atopica per il baricitinib [20]. In Svizzera, tuttavia, questa opzione terapeutica è attualmente approvata solo per l’indicazione dell’artrite reumatoide attiva. Sono disponibili anche dati promettenti sull’inibitore JAK1 upadacitinib. I risultati delle analisi intermedie di uno studio di fase IIb mostrano una buona efficacia e tollerabilità alla dose di 30 mg/d nei pazienti adulti con dermatite atopica da moderata a grave [10].
In sintesi, gli inibitori di JAK si sono dimostrati efficaci nel trattamento della dermatite atopica negli studi condotti finora, e la loro rapida insorgenza d’azione è particolarmente interessante [5]. Per quanto riguarda il profilo degli effetti collaterali, è stato dimostrato che è necessario un monitoraggio intensivo dei pazienti per controllare il rischio di infezione e le possibili alterazioni dell’emocromo. Gli inibitori della JAK potrebbero essere utili in futuro, soprattutto per le terapie di intervallo a breve termine [5]. Il profilo degli effetti collaterali varia a seconda della sostanza e della dose e può essere ridotto con l’applicazione topica; diversi studi sono attualmente in corso (ad esempio su tofacitinib, delgocitinib, ruxolitinib). Grazie alle piccole dimensioni molecolari degli inibitori JAK, è possibile la penetrazione attraverso la pelle, che è un buon prerequisito per l’applicazione topica.
Fonte: Riunione annuale EADV 2020
Letteratura:
- Langley RGB: Biologici emergenti per la dermatite atopica negli adulti e nei bambini, Professor Richard GB Langley MD, Halifax (Canada), EADV (virtuale) 31.10.2020.
- Simpson EL, et al: Due studi di fase 3 su dupilumab rispetto al placebo nella dermatite atopica. N Engl J Med 2016; 375: 2335-2348.
- Compendio svizzero dei farmaci, www.compendium.ch (ultimo accesso 17.2.2021)
- Thaci: Efficacia e sicurezza della monoterapia con dupilumab negli adulti con dermatite atopica da moderata a grave: un’analisi congiunta di due studi randomizzati di fase 3 (LIBERTY AD SOLO 1 e LIBERTY AD SOLO 2). J Dermatol Sci 2019 266-275.
- Worm M, et al: La terapia moderna della dermatite atopica: biologici e farmaci a piccole molecole. JDDG 2020; 18: 10: 1085-1093.
- Bieber T, et al: Nuove terapie basate sulla fisiopatologia della dermatite atopica. JDDG 2019 17; 11: 1150-1163.
- Wollenberg A, et al: Trattamento della dermatite atopica con tralokinumab, un anti-IL 13mAb. J Allergy Clin Immunol 2019; 143(1): 135-141.
- Maul JT: Novità 2019/2020: Dermatosi infiammatorie. Julia-Tatjana Maul, MD, Zürcher Dermatologische Fortbildungstage (ZDFT), 14/15.05.2020.
- Simpson EL, Flohr C, Eichenfield LF, et al: Efficacia e sicurezza di lebrikizumab (un anticorpo monoclonale anti-IL-13) negli adulti con dermatite atopica da moderata a grave non adeguatamente controllata dai corticosteroidi topici: uno studio di fase II randomizzato, controllato con placebo (TREBLE). J Am Acad Dermatol 2018; 78(5): 863-871.e811
- Guttman-Yassky E, et al: Efficacia e sicurezza di Lebrikizumab, un inibitore dell’Interleuchina 13 ad alta affinità, negli adulti con dermatite atopica da moderata a grave: uno studio clinico randomizzato di fase 2b. JAMA Dermatol 2020: 156(4): 411-420.
- Loh TY, et al: Potenziale terapeutico di Lebrikizumab nel trattamento della dermatite atopica. J Asthma Allergy 2020; 13: 109-114.
- Ruzicka T, et al. Anticorpo anti-interleuchina-31 recettore A per la dermatite atopica. N Engl J Med 2017; 376: 826-835.
- Fragoulis GE, McInnes IB, Siebert S: Inibitori della JAK. Nuovi attori nel campo delle malattie immuno-mediate, oltre l’artrite reumatoide. Reumatologia 2019; 58: i43-i54.
- Clinicaltrial.gov, www.clinicaltrial.gov (ultimo accesso 17.2.2021).
- Silverberg JI, et al: Carico del paziente e qualità della vita nella dermatite atopica negli adulti statunitensi Uno studio trasversale basato sulla popolazione. Annals of Allergy, Asthma and Immunology 2018, DOI: https://doi.org/10.1016/j.anai.2018.07.006
- Augustin, et al.: Datenanalyse CVderm 2020. Versorgungsexpertise Neurodermitis in Deutschland, dati in archivio.
- Kirsten N: Terapia della neurodermite durante la Corona: concetti attuali messi alla prova e cosa è importante per lei ora. Evento per i pazienti, Dott.ssa Natalia Kirsten, Hautnetz Hamburg, 17.09.20
- Li R, Hadi S, Guttman-Yassky E: Terapie biologiche e di piccole molecole attuali ed emergenti per la dermatite atopica. Expert Opin Biol Ther 2019; 4: 367-380.
- Wollenberg A: Tralokinumab per la dermatite atopica da moderata a grave: risultati di due studi di fase III, randomizzati, in doppio cieco, multicentrici, controllati con placebo, della durata di 52 settimane (ECZTRA 1 e ECZTRA 2), https://doi.org/10.1111/bjd.19574
- Hüttemann D: Inibitori della JAK: Nuova modalità d’azione approvata per la dermatite atopica. Giornale farmaceutico (Online), 03.11.2020
DERMATOLOGIE PRAXIS 2021; 31(1): 33-34 (pubblicato il 22.2.21, prima della stampa).











