La gestione del dolore dei pazienti con malattia renale cronica grave non è una questione banale, a causa dei fattori limitanti. Non solo i potenziali effetti collaterali possono far sì che l’uso di antidolorifici Deve essere preso in considerazione anche il potenziale di interazione con altri farmaci.
Se si pensa ai reni e agli antidolorifici, la prima cosa che viene in mente è la famosa nefropatia da analgesici (nota anche come rene da fenacetina). Questa nefrite tubulointerstiziale cronica con necrosi papillare, che è stata descritta per la prima volta in Svizzera [1], ha spesso portato a un’insufficienza renale terminale. Tuttavia, a causa del divieto in tutta Europa, negli anni ’90, degli antidolorifici combinati contenenti fenacetina e sostanze che creano dipendenza come la codeina, questa malattia è praticamente scomparsa e non è quindi oggetto di questo articolo.
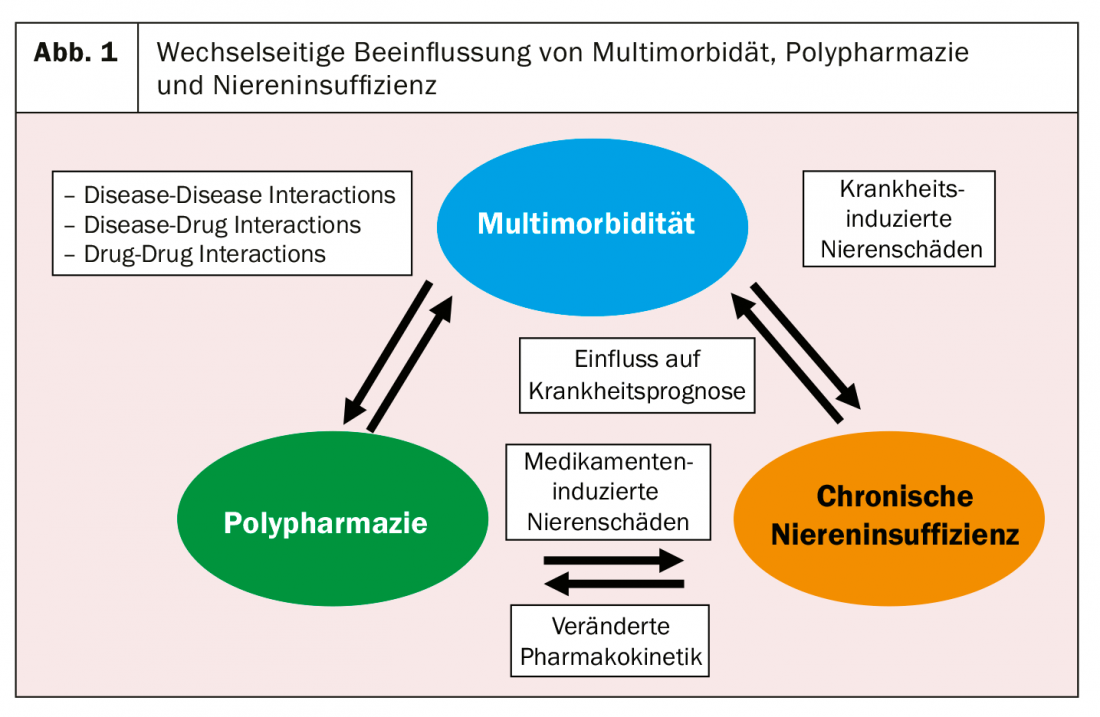
L’interdipendenza tra il rene (o la funzione renale) e gli antidolorifici è complessa (Fig. 1). Da un lato, comprende l’effetto nefrotossico diretto di alcune classi di analgesici (ad esempio, i farmaci antinfiammatori non steroidei, FANS) e, dall’altro, l’influenza di una funzione renale significativamente compromessa (ad esempio, molti oppioidi) sulla farmacocinetica di alcuni analgesici. Infine, ma non meno importante, il dolore e l’insufficienza renale sono strettamente legati alla questione della multimorbilità/poli-farmacia. In uno studio condotto su oltre 400 pazienti internisti generali di un centro terziario, la combinazione di insufficienza renale cronica, dolore cronico (alla schiena e/o alle grandi articolazioni) e ipertensione arteriosa è stata il principale cluster di multimorbilità [2]. D’altra parte, un recente studio americano ha dimostrato che i pazienti con insufficienza renale cronica soffrono maggiormente di multimorbilità e polifarmacia [3].
In questo articolo, vorremmo innanzitutto fornire una panoramica dell’influenza reciproca del rene e degli antidolorifici, poi approfondire i temi della nefrotossicità e della farmacocinetica, e infine fornire una raccomandazione pratica per la terapia del dolore nei pazienti con insufficienza renale cronica.
Terapia del dolore secondo l’OMS – Influenza del rene
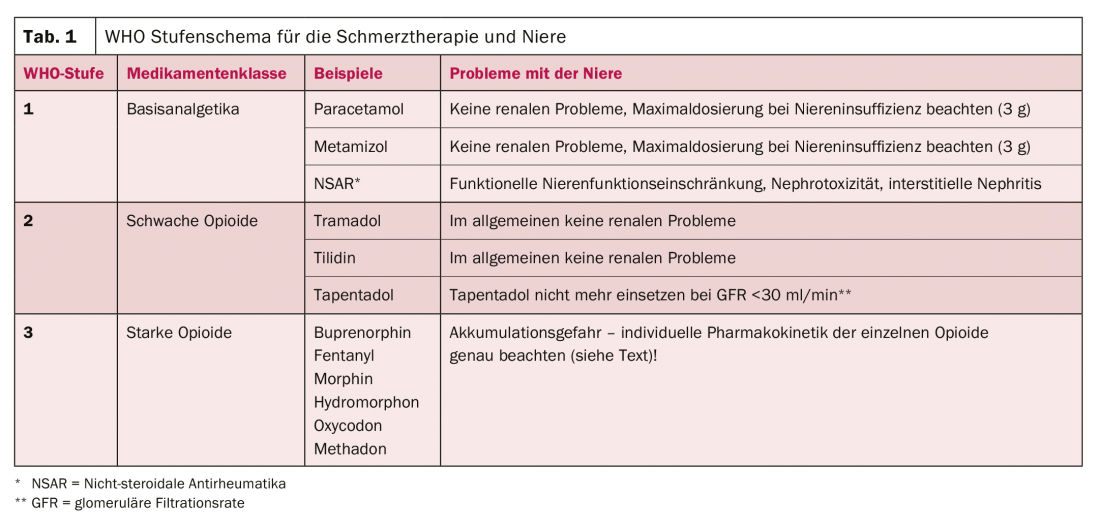
La terapia del dolore viene solitamente pianificata secondo lo schema a tappe dell’OMS, che deve sempre essere adattato alla situazione patologica individuale [4]. Se osserviamo questo schema con l'”ottica del rene”, si possono fare le seguenti affermazioni (Tab. 1, [5]):
- Livello 1 dell’OMS: gli analgesici di base, il paracetamolo e il metamizolo, non comportano quasi alcun problema renale; i FANS, invece, sono potenzialmente dannosi per i reni sotto diversi aspetti, che verranno discussi in dettaglio nella prossima sezione.
- OMS stadio 2: Gli oppioidi deboli offrono anche pochi problemi renali, anche se il tapentadolo non dovrebbe essere utilizzato al di sopra di un tasso di filtrazione glomerulare (GFR) inferiore a 30 ml/min.
- Livello 3 dell’OMS: come gli oppioidi deboli, gli oppioidi forti non sono nefrotossici. D’altra parte, la funzione renale ha un’influenza molto diversa sulla loro farmacocinetica, motivo per cui questa deve essere osservata attentamente nell’insufficienza renale avanzata. La sezione successiva è dedicata a questo argomento.
FANS e reni
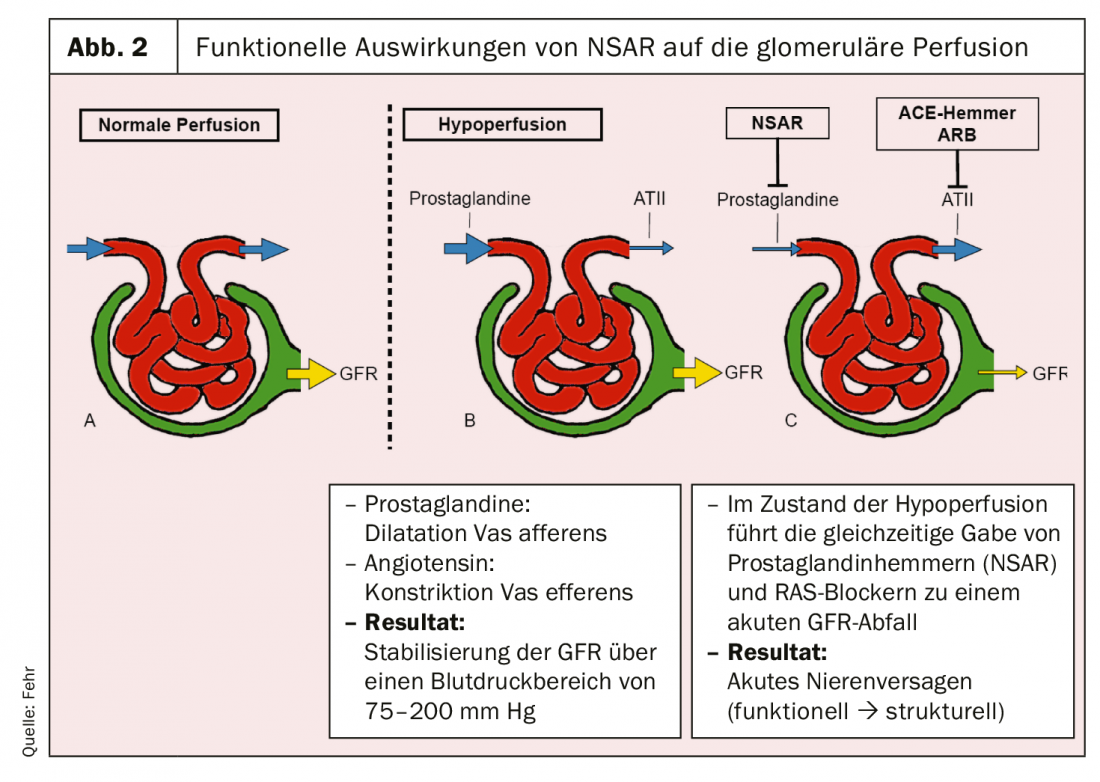
I FANS influenzano il rene in molti modi. Possono portare a una restrizione funzionale del tasso di filtrazione glomerulare, ma anche a un danno strutturale. La diminuzione funzionale può essere spiegata dall’inibizione della sintesi di prostaglandine (Fig. 2). Le prostaglandine provocano la vasodilatazione dell’arteriola afferente nel glomerulo. La loro inibizione riduce la perfusione glomerulare. Al contrario, i bloccanti del sistema renina-angiotensina (RAS) provocano una vasodilatazione nell’arteriola efferente, che porta anche a una riduzione della pressione di perfusione nel glomerulo. Se la disidratazione con RAS attivato è clinicamente presente e i FANS vengono utilizzati in combinazione con i bloccanti RAS, può verificarsi una grave insufficienza renale acuta oligurica [6]. Questo è fondamentalmente reversibile, ma può trasformarsi in necrosi tubulare acuta ischemica se persiste a lungo.
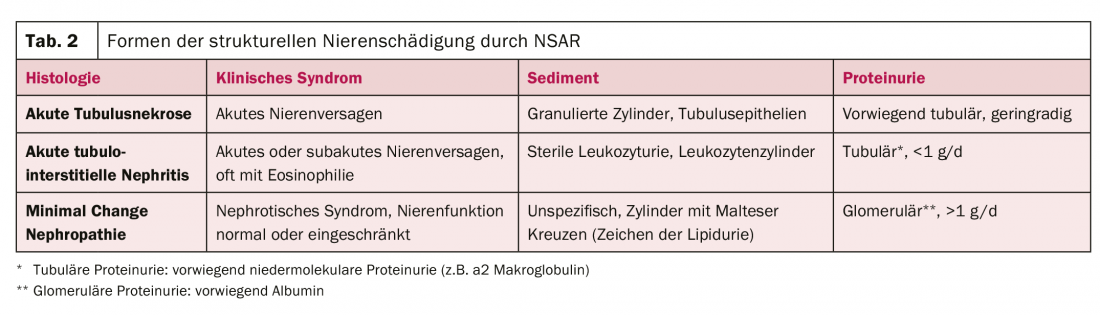
Questo ci porta ai tre modelli strutturali di danno che i FANS possono causare al rene (Tabella 2):
- Necrosi tubulare acuta: il suo sviluppo è principalmente ischemico, come fase finale nel continuum dell’insufficienza renale funzionale descritta sopra. Ha un decorso tipico e si riprende nell’arco di alcuni giorni o settimane. Per ora non esiste una terapia specifica.
- Nefrite tubulointerstiziale acuta: la nefrite tubulointerstiziale acuta è una reazione allergica ai farmaci [7]. La biopsia mostra in genere un esteso infiltrato tubulo-interstiziale con formazione di edema. I tubuli renali vengono distrutti nel processo. La terapia consiste principalmente nell’interrompere l’agente scatenante. Vengono utilizzati anche i corticosteroidi, ma con un’evidenza solo moderata in letteratura.
- Nefropatia a cambiamento minimo: se dopo la somministrazione di FANS si verifica una grave proteinuria con segni di sindrome nefrosica (edema, versamenti, ipoalbuminemia, iperlipidemia), la diagnosi più probabile è la nefropatia a cambiamento minimo [8]. La diagnosi viene fatta biopticamente e la terapia consiste in corticosteroidi – oltre all’interruzione dell’agente scatenante.
In sintesi, i FANS sono eccellenti antidolorifici antinfiammatori. Tuttavia, dal punto di vista renale, si consiglia cautela nei pazienti con insufficienza renale cronica preesistente e nei pazienti in uno stato di carenza di volume intravascolare (disidratazione, insufficienza cardiaca, cirrosi epatica).
Gli oppioidi e i reni
Gli oppioidi non sono generalmente nefrotossici. Il loro uso nei pazienti con insufficienza renale cronica è limitato principalmente dalla farmacocinetica. Molti oppioidi o i loro metaboliti attivi si accumulano nell’insufficienza renale avanzata. Il prototipo è la morfina, i cui metaboliti attivi morfina-3-glucuronide, morfina-6-glucuronide e normorfina vengono escreti per via renale. Per questo motivo, è necessario un aggiustamento della dose anche nel caso di una lieve restrizione della funzione renale. Nell’insufficienza renale grave (GFR <30 ml/min), la morfina non deve più essere utilizzata [9].
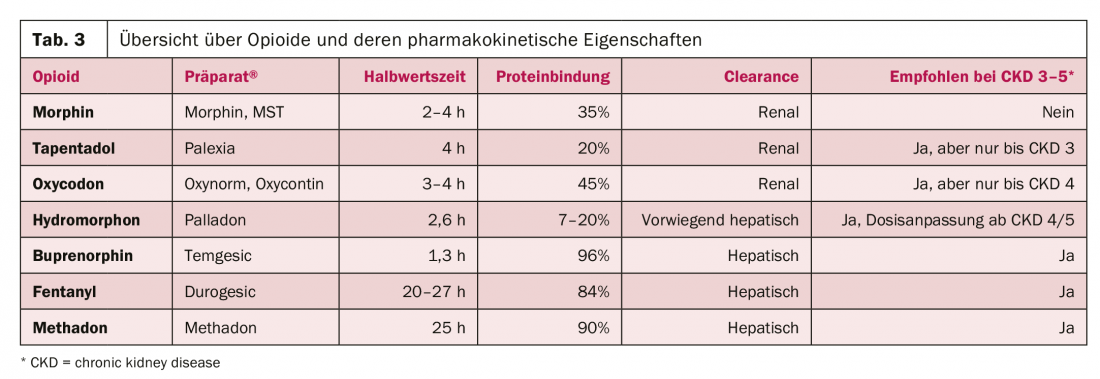
La Tabella 3 fornisce una panoramica dei principali oppioidi e delle loro proprietà farmacocinetiche, nonché le raccomandazioni per l’uso nella disfunzione renale. Si possono distinguere tre gruppi:
Oppioidi con eliminazione prevalentemente renale, che non dovrebbero più essere utilizzati nei pazienti con CKD 3-5 (morfina).
- Oppioidi a parziale escrezione renale, che devono essere utilizzati con cautela e con una dose adattata nei pazienti con CKD 4/5 (idromorfone, ossicodone, tapentadolo).
- Oppioidi con elevato legame proteico ed eliminazione epatica, che possono essere utilizzati con relativa facilità nei pazienti con CKD 4/5 (buprenorfina, fentanil, metadone).
Raccomandazioni pratiche per l’uso di analgesici nei pazienti con insufficienza renale cronica grave (CKD 4/5, GFR <30 ml/min)
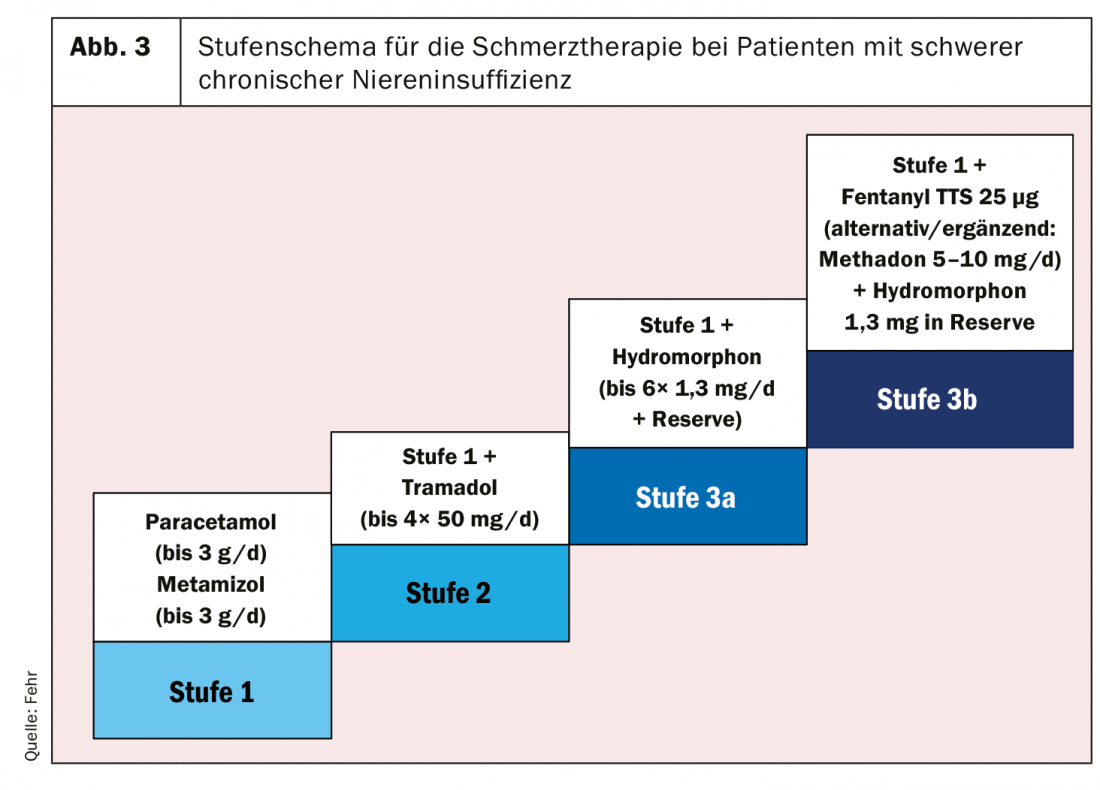
Sulla base di quanto sopra, vorremmo proporre qui uno schema graduato per la pratica della gestione del dolore nei pazienti con CKD 4/5 (Fig. 3) [5].
- Nella fase 1 dell’OMS, i FANS dovrebbero essere evitati quando possibile. L’uso di paracetamolo e metamizolo è in gran parte privo di problemi, sebbene la dose massima debba essere limitata a 3 (anziché 4) g/d.
- Nella fase 2 dell’OMS, si consiglia di utilizzare il tramadolo in prima istanza. Il suo impiego nell’insufficienza renale grave è in gran parte privo di problemi, ma il restante profilo di effetti collaterali (nausea, vertigini, allucinazioni, ecc.) spesso ne limita l’uso. Si noti il potenziale di interazione con i farmaci che inibiscono i citocromi CYP2D6 e CYP3A4.
- Al livello 3 dell’OMS, si consiglia di utilizzare principalmente l’idromorfone, che può essere somministrato per via orale e sottocutanea (se necessario, anche in una pompa sottocutanea). Un’alternativa è il fentanil nell’applicazione di cerotti. Entrambi i preparati possono essere combinati con il metadone (soprattutto per il dolore neuropatico).
- Quando si utilizzano gli oppioidi, in genere si deve associare anche un farmaco di livello 1 dell’OMS, per ottenere un effetto sinergico nella soppressione del dolore. Per il dolore neuropatico, oltre al metadone, si consiglia di utilizzare principalmente il gabapentin (iniziare con 50-100 mg/d, aumentare fino a un massimo di 300 mg/d) [10].
Letteratura:
- Zollinger HU. [Chronic interstitial nephritis caused by the abuse of anal getics containing phenacetin (Saridon etc.)]. Schweiz Med Wochenschr 1955; 85: 746.
- Siebenhuener K, Eschmann E, Kienast A, et al: Dolore cronico: quanto sono impegnative le DDI nel trattamento analgesico dei pazienti ricoverati con patologie croniche multiple? PLoS One 2017; 12:e0168987.
- Tonelli M, Wiebe N, Manns BJ, et al: Confronto della complessità dei pazienti visitati da diversi medici subspecialisti in un sistema di assistenza sanitaria universale. JAMA Netw Open 2018; 1:e184852.
- Caraceni A, Hanks G, Kaasa S, et al: Uso di analgesici oppioidi nel trattamento del dolore da cancro: raccomandazioni basate sulle evidenze dell’EAPC. Lancet Oncol 2012; 13:e58-68.
- Davison SN: Considerazioni di farmacologia clinica sulla gestione del dolore nei pazienti con insufficienza renale avanzata. Clin J Am Soc Nephrol 2019; 14: 917-931.
- Cippa PE, Fehr T: Farmaci che vanno ai reni. GP Practice 2010: 3.
- Nast CC: Nefrite interstiziale indotta da farmaci nel 21° secolo. Adv Chronic Kidney Dis 2017; 24: 72-79.
- Fogo AB: Pagina dei quiz. Nefrite interstiziale acuta e lesione da malattia a cambiamento minimo, causata da lesioni da FANS. Am J Kidney Dis 2003; 42:A41, e1.
- Dean M: Gli oppioidi nell’insufficienza renale e nei pazienti in dialisi. J Pain Symptom Manage 2004; 28: 497-504.
- Finnerup NB, Attal N, Haroutounian S, et al: Farmacoterapia per il dolore neuropatico negli adulti: revisione sistematica e meta-analisi. Lancet Neurol 2015; 14: 162-173.
CARDIOVASC 2019; 18(6): 18-20