In caso di mal di testa frequenti, può essere utile una profilassi farmacologica. Quali sono i farmaci disponibili e quali sono le prove della loro efficacia?
Circa il 15% della popolazione europea soffre di attacchi di emicrania [1]. Le persone colpite non solo devono affrontare il dolore, ma anche gli effetti della malattia sulla loro vita professionale e privata [2]. Tuttavia, il peso della malattia non è uguale per tutti, ma aumenta con il numero di giorni di cefalea.
Sebbene siano disponibili numerosi farmaci, spesso molto efficaci, per il trattamento acuto dell’emicrania, questo approccio terapeutico non è sempre sufficiente. Se corre dietro al dolore invece di prevenirlo, riduce la durata degli attacchi, ma non aumenta necessariamente la prevedibilità della sua vita. Inoltre, l’uso frequente di farmaci acuti comporta il rischio di cefalea da uso eccessivo di farmaci (MÜKS) [3]. Questo minaccia se vengono assunti analgesici semplici per ≥15 giorni o triptani, oppiacei o analgesici combinati su più di dieci giorni al mese per un periodo più lungo (almeno tre mesi). È molto più costoso per la società rispetto all’emicrania stessa, ed è associato a oneri aggiuntivi per l’individuo [4,5].
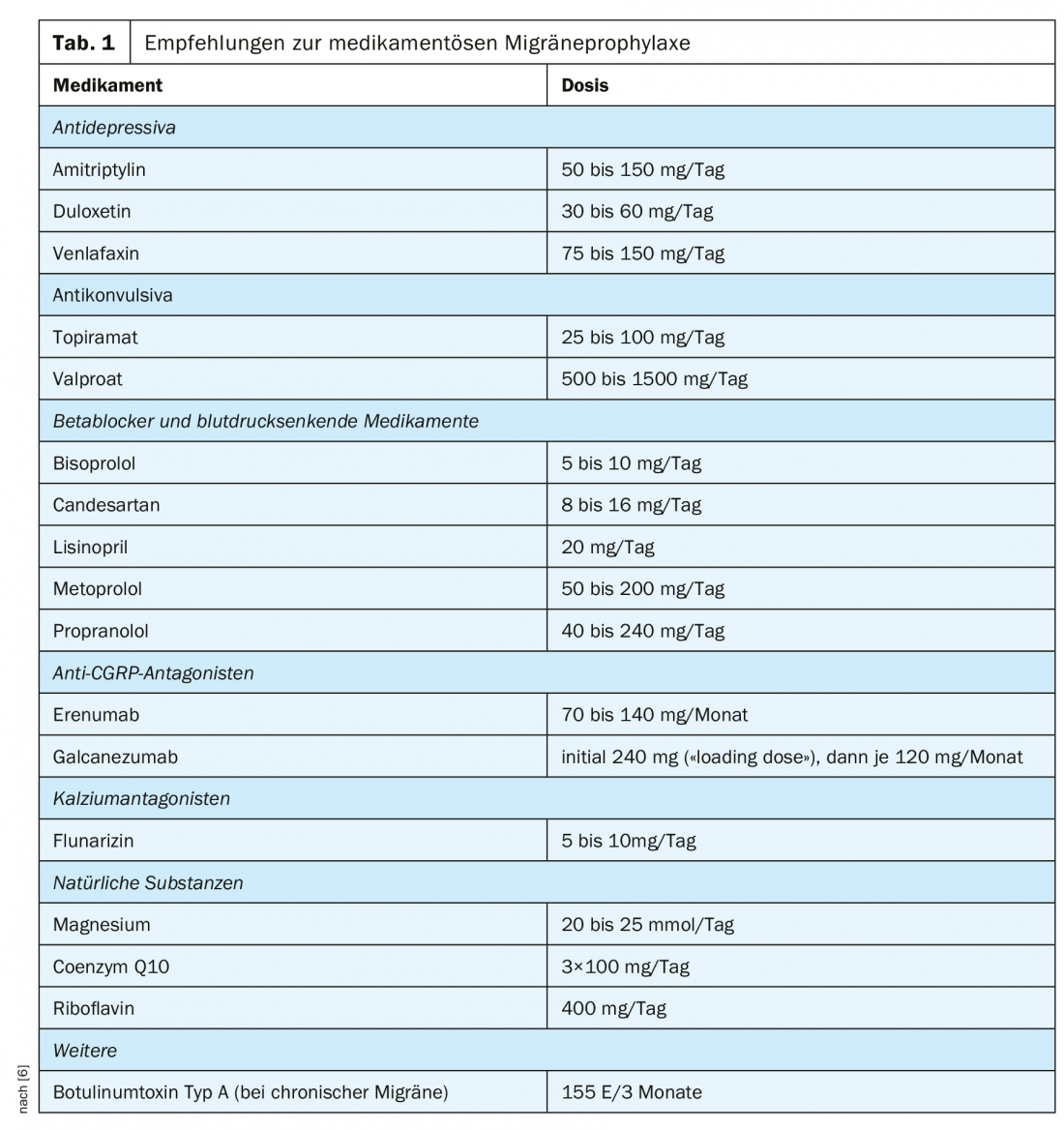
Quindi l’obiettivo è quello di evitare che le crisi si verifichino in primo luogo, o almeno di ridurne il numero il più possibile. Diversi principi attivi si sono dimostrati utili a questo proposito (Tab. 1) [6]. Tuttavia, la scelta del momento giusto per la profilassi e la scelta del farmaco giusto possono essere impegnative. D’altra parte, questo approccio terapeutico offre la possibilità di alleviare in modo significativo i sintomi delle persone colpite.
Principi della terapia
Fondamentalmente, si fa una distinzione tra approcci terapeutici farmacologici e non farmacologici. Di solito si presume che il trattamento profilattico debba essere iniziato quando si verificano cinque o più giorni di mal di testa o almeno tre attacchi di emicrania al mese [6]. È consigliabile decidere una terapia individuale, poiché non tutti i pazienti sono limitati dal mal di testa nella stessa misura. Se il carico dei singoli attacchi è già molto elevato (ad esempio, nel caso di emicrania emiplegica o di attacchi di lunga durata), la profilassi può essere presa in considerazione anche se il numero di giorni di cefalea è basso.
Prima di iniziare la terapia, i pazienti devono essere informati dettagliatamente sulle possibilità e sui rischi del trattamento. Il successo della terapia spesso diventa evidente solo dopo alcune settimane, mentre gli effetti collaterali si notano molto prima.
I metodi non farmacologici come la neuromodulazione, la stimolazione non invasiva del nervo vago, le tecniche di rilassamento, il biofeedback e la stimolazione magnetica transcranica sono spesso efficaci, ma non sempre sufficienti. In questo articolo, ci limiteremo alle opzioni di profilassi dell’emicrania con i farmaci.
I farmaci orali per la profilassi dell’emicrania devono essere utilizzati quotidianamente, indipendentemente dalla presenza del dolore. La valutazione del successo del trattamento è difficile perché il numero di giorni di cefalea è retrospettivamente sottostimato [7]. Pertanto, i pazienti in profilassi delle crisi epilettiche devono assicurarsi di tenere un diario della cefalea (3-6 mesi). Anche l’aderenza alla terapia, che spesso è molto bassa, dovrebbe essere promossa e messa in discussione [8].
Per raggiungere comunque il successo terapeutico, riteniamo che siano essenziali una consulenza dettagliata, una scelta individuale dei farmaci e una valutazione dei cambiamenti avvenuti che sia il più obiettiva possibile (panoramica 1).

Farmaci
Fondamentalmente, si consiglia di iniziare con una dose bassa e di aumentarla lentamente secondo le necessità. Se il trattamento ha successo, si può prendere in considerazione una riduzione graduale della dose dopo sei-dodici mesi.
Beta-bloccanti e altri farmaci che abbassano la pressione sanguigna: Il fatto che i beta-bloccanti siano utili nella profilassi dell’emicrania è stato scoperto per caso [9]. Riducono l’ampiezza dei potenziali evocati visivi, che sono spesso aumentati nei pazienti con emicrania, il che potrebbe indicare un miglioramento della funzione delle connessioni talamo-corticali [9–13]. Tuttavia, se questo sia responsabile della riduzione della frequenza dell’emicrania non è ancora stato chiarito in modo definitivo [9,12].
L’effetto del propranololo [14] e del metoprololo [15,16], entrambi approvati in Svizzera per la profilassi dell’emicrania [17], è stato confermato in diversi studi.
Il candesartan ha un’efficacia simile al propranololo e anche gli effetti collaterali dei due farmaci sono simili. Mentre le vertigini e le parestesie sono state riportate più frequentemente con il candesartan, gli episodi di bradicardia sono più comuni con il propranololo [18].
Il lisinopril è stato analizzato in due studi più piccoli e ha mostrato anche un effetto profilattico; tuttavia, alcuni pazienti hanno dovuto interrompere il trattamento a causa della tosse [19,20].
Calcio antagonisti: il calcio antagonista flunarizina è approvato anche per la profilassi dell’emicrania [17]. La sua efficacia può essere considerata assicurata, anche se alcuni studi hanno mostrato una potenza troppo bassa [21]. Il meccanismo d’azione non è noto, ma è stato discusso un blocco dei canali del sodio e del calcio dipendenti dal voltaggio corticale [22]. Gli effetti collaterali più comuni sono l’affaticamento e l’aumento di peso, mentre l’umore depresso o la sindrome extrapiramidale sono riportati molto raramente [21].
Antidepressivi: in Svizzera, nessun antidepressivo è attualmente approvato per la profilassi dell’emicrania, ma il loro uso è comunque supportato dalle attuali raccomandazioni terapeutiche [6]. Tuttavia, nella nostra esperienza, molti pazienti hanno chiare riserve su questi farmaci.
Il più studiato è l’amitriptilina, che riduce il numero di giorni di emicrania più di un placebo [23]. I triciclici potenziano l’effetto anti-nocicettivo delle vie discendenti e riducono la depressione da diffusione negli studi sugli animali, il che può spiegare il loro effetto nella profilassi dell’emicrania [24–26].
Le prove di efficacia degli inibitori selettivi della ricaptazione della serotonina sono significativamente peggiori [24]. La fluoxetina ha mostrato pochi [27] o nessun effetto negli studi [28]; la sertralina non ha avuto alcun effetto sulla gravità della cefalea [29]. L’SNRI venlafaxina, invece, ha ridotto significativamente il numero di giorni di mal di testa in uno studio controllato con placebo [30]. Per quanto ne sappiamo, l’effetto della duloxetina – anch’essa un SNRI – non è ancora stato testato in nessuno studio randomizzato controllato. Tuttavia, uno studio retrospettivo [31] e uno studio prospettico open-label [32] hanno mostrato prove di buona efficacia in alcuni pazienti.
Anticonvulsivanti: del gruppo degli anticonvulsivanti, solo il topiramato è attualmente approvato in Svizzera per la profilassi dell’emicrania [17]. Numerosi studi hanno confermato la buona efficacia del farmaco [33–37]. Tuttavia, gli effetti collaterali come affaticamento, parestesia, nausea e problemi di concentrazione ne limitano l’utilità [35,38].
Anche l’effetto del valproato è ben documentato [39–41]. Tuttavia, con entrambi i farmaci, è necessario notare che il rischio di malformazione aumenta in modo significativo quando vengono utilizzati durante la gravidanza e quindi è necessaria una contraccezione efficace nelle donne in età fertile [42].
In generale, si ritiene che gli anticonvulsivi impediscano la polarizzazione di dispersione e la sensibilizzazione centrale, riducendo così la frequenza degli attacchi di emicrania [43]. Tuttavia, altri anticonvulsivanti come l’acetazolamide, il clonazepam, la lamotrigina, l’oxcarbazepina, il vigabatrin e il gabapentin non hanno dimostrato di avere alcun effetto [44,45].
Anticorpi anti-CGRP: Dopo la prima descrizione del peptide legato al gene della calcitonina (CGRP) nel 1983 [46], negli anni successivi sono stati riconosciuti il suo effetto vasodilatatore [47] e il suo significato per i disturbi della cefalea [48]. I primi antagonisti sono stati presto sviluppati e testati [49–51]. Infine, gli anticorpi monoclonali diretti contro la molecola CGRP stessa o il suo recettore hanno raggiunto la maturità del mercato [52–58]; tutti riducono significativamente il numero di giorni di mal di testa.
Attualmente in Svizzera sono disponibili erenumab e galcanezumab, che possono essere iniettati per via sottocutanea a domicilio [59,60]. Finora, i farmaci sembrano essere ben tollerati; la frequenza e il tipo di eventi avversi differiscono solo leggermente dal gruppo placebo – solo il dolore e il prurito nel sito di iniezione si sono verificati più frequentemente nel gruppo verum in uno studio [52, 54, 56, 58]. Tuttavia, non sono ancora disponibili dati a lungo termine sulla tollerabilità e sugli effetti, nonché informazioni sulla possibile embriotossicità.
Magnesio: si ritiene che gli attacchi di emicrania siano associati a bassi livelli di magnesio nel siero [61,62]. Il motivo potrebbe essere che il magnesio normalmente inibisce sia i recettori NMDA [63,64] che la produzione di ossido nitrico [65,66] e questo effetto è ridotto nell’ipomagnesemia.
In singoli studi – ma non in tutti [67,68] – l’integrazione di magnesio ha abbreviato la durata delle crisi [69] o ridotto la frequenza [70]. Tuttavia, una meta-analisi non ha confermato il beneficio nel trattamento acuto [71]. Con un dosaggio e una tempistica regolati individualmente, il trattamento è solitamente ben tollerato [67]. Tuttavia, si consiglia cautela nell’utilizzo durante la gravidanza.
Riboflavina: l’effetto della riboflavina sull’emicrania è stato analizzato in diversi studi. Ciò si basava sull’idea che la disfunzione mitocondriale potesse svolgere un ruolo nella fisiopatologia dell’emicrania [72] e che la riboflavina in dosi elevate aumentasse l’attività dei complessi I e II della catena respiratoria in alcune malattie [73,74].
È stato dimostrato che negli adulti, dosi elevate (400 mg/die) possono portare a una riduzione della frequenza delle crisi [74,75], mentre questo effetto non è stato riprodotto nei bambini [76]. Gli effetti collaterali più comuni riportati sono diarrea e poliuria [74].
Coenzima Q10: l’idea alla base dell’uso del coenzima Q10 è anche che la disfunzione mitocondriale potrebbe essere una causa dell’emicrania [77]. Assume gli elettroni generati nei complessi I e II della catena respiratoria e li trasporta ulteriormente al complesso III [78].
Negli adulti, il trattamento ha dimostrato un’efficacia significativa nella profilassi dell’emicrania in uno studio randomizzato controllato [77] e in due studi in aperto [79,80]. Questo effetto non è stato riprodotto nei bambini [81]. Non sono stati segnalati effetti collaterali.
Gravidanza
Durante la gravidanza, il numero di giorni di emicrania diminuisce temporaneamente in un’ampia percentuale di pazienti [82,83], mentre gli attacchi di emicrania sono comuni subito dopo il parto [84]. Spesso, non è necessaria alcuna profilassi farmacologica durante la gravidanza. Si consigliano invece metodi non farmacologici (agopuntura, neuromodulazione, biofeedback e igiene del sonno, ecc. [85,86]. Se la rinuncia ai farmaci non è un’opzione, si può prendere in considerazione l’uso di propranololo e metoprololo e di amitriptilina [85]. Tuttavia, i due beta-bloccanti sono stati associati a una riduzione del peso alla nascita e l’amitriptilina a disturbi dell’adattamento del bambino [42]. Anche se questi farmaci non sono stati valutati come teratogeni, è comunque necessaria un’attenta valutazione dei rischi e dei benefici.
Le raccomandazioni per la sostituzione del magnesio durante la gravidanza devono essere considerate con cautela [85]. Da allora si sa che l’uso del solfato di magnesio può portare all’osteopenia nel neonato [87], motivo per cui la FDA ne sconsiglia l’uso per la tocolisi per un periodo superiore a cinque-sette giorni [88].
Poiché non è noto a quale dose si verifichi l’osteopenia e il rischio non può quindi essere quantificato, anche l’uso del magnesio per la profilassi dell’emicrania durante la gravidanza è stato sconsigliato [89].
Emicrania mestruale
Circa il 50% delle donne con emicrania descrive un aumento della frequenza degli attacchi durante il periodo mestruale; tuttavia, è raro che si verifichi esclusivamente durante le mestruazioni [82]. Soprattutto nelle donne con attacchi frequenti, bisogna tenere presente che questi possono verificarsi anche in coincidenza del ciclo mestruale [90]; una delimitazione esatta è spesso possibile solo con un diario dell’emicrania tenuto per un periodo di tempo più lungo [91]. Gli attacchi associati alle mestruazioni spesso durano più a lungo ed è più probabile che siano associati a nausea [92].
Si raccomanda alle donne con attacchi di emicrania che non si verificano sempre in concomitanza con le mestruazioni di adottare la profilassi “normale”, come discusso sopra [90]. Tuttavia, se gli attacchi sono strettamente associati alle mestruazioni e la persona colpita ha un ciclo regolare, questo può essere utile per pianificare la terapia, in quanto la comparsa dei sintomi è prevedibile. In questi casi, i FANS e i triptani possono essere assunti (tenendo conto delle controindicazioni e delle avvertenze) come “profilassi a breve termine” per quattro-sette giorni [90]. Inoltre, mentre in passato il gel estrogenico era raccomandato per la profilassi a breve termine [93] e la contraccezione contenente estrogeni era raccomandata per prolungare i cicli [94], da allora le linee guida sono cambiate per quanto riguarda il rischio cardiovascolare [6,95]. Attualmente si raccomandano contraccettivi contenenti progestinici [6]. In ogni caso, il trattamento dell’emicrania mestruale deve essere effettuato in consultazione con un ginecologo.
Emicrania cronica
L’emicrania cronica si ha quando un paziente ha mal di testa ≥15 giorni al mese per almeno tre mesi, con almeno otto giorni che soddisfano i criteri per un attacco di emicrania [3]. La loro prevalenza varia dall’1,4 al 2,2% nella popolazione generale [96]. Un’ampia percentuale di persone colpite presenta anche un’FMD [97], per la quale si applicano altre raccomandazioni di trattamento (veda sotto).
Negli studi controllati con placebo, è stato confermato che il topiramato [38,98,99]Tossina botulinica [100–103]Valproato [104] ed erenumab [54]Galcanezumab [58] e fremanezumab (non ancora in commercio in Svizzera). [57] può ridurre significativamente il numero di giorni di mal di testa. Raccomandiamo pertanto di preferire questi farmaci nel trattamento dell’emicrania cronica.
Cefalea da uso eccessivo di farmaci
La cefalea da uso eccessivo di farmaci (MTNH) è comune – si stima una prevalenza dall’1 al 2% [105] – e deve essere sempre sospettata nei pazienti con molti giorni di cefalea. Il trattamento consiste nel non assumere farmaci acuti [106]. Si dubita che la profilassi aggiuntiva con farmaci sia utile [106], ma non è ancora possibile fare affermazioni definitive. Prima di iniziare la pausa farmacologica, è di grande importanza informare bene i pazienti sulla durata e sui benefici attesi. Inizialmente (per circa quattro settimane), può verificarsi un aumento temporaneo della frequenza del mal di testa e anche in seguito non ci si può aspettare la liberazione dal dolore. L’obiettivo del trattamento è quello di ridurre la frequenza degli attacchi al livello precedente all’uso eccessivo di farmaci.
Messaggi da portare a casa
- Se il numero di giorni di cefalea aumenta o la necessità di assumere farmaci acuti diventa più frequente, si dovrebbe discutere la profilassi.
- Quando si sceglie un farmaco, si devono sempre prendere in considerazione gli effetti collaterali, le condizioni di vita del paziente e l’accettazione della terapia.
- La profilassi dell’emicrania offre l’opportunità di ridurre significativamente lo stress dei pazienti nella vita quotidiana.
Letteratura:
- Stovner LJ, Andree C: Prevalenza della cefalea in Europa: una revisione per il progetto Eurolight. J Headache Pain 2010; 11(4): 289-299.
- Lampl C, et al: Carico interictale attribuibile alla cefalea episodica: risultati del progetto Eurolight. J Headache Pain 2016; 17: 9.
- Comitato di classificazione delle cefalee della Società internazionale delle cefalee (IHS): Classificazione internazionale dei disturbi da cefalea, 3a edizione. Cefalalgia 2018; 38(1): 1-211.
- Linde M, et al: Il costo dei disturbi da cefalea in Europa: il progetto Eurolight. Eur J Neurol 2012; 19(5): 703-711.
- Westergaard ML, et al: Prevalenza di cefalea cronica con e senza uso eccessivo di farmaci: associazioni con la posizione socioeconomica e lo stato di salute fisica e mentale. Dolore 2014; 155(10): 2005-2013.
- Andrée C, et al: Raccomandazioni di trattamento per la cefalea primaria. Società Svizzera delle Cefalee SKG, 2019.
- Krogh AB, et al: Un confronto tra le registrazioni prospettiche del diario basato su Internet e quelle cartacee del mal di testa tra gli adolescenti nella popolazione generale. Cefalalgia 2016; 36(4): 335-345.
- Hepp Z, Bloudek LM, Varon SF: Revisione sistematica dell’aderenza e della persistenza della profilassi dell’emicrania. J Manag Care Pharm 2014; 20(1): 22-33.
- Danesh A, Gottschalk PCH: Beta-bloccanti per la prevenzione dell’emicrania: un articolo di revisione. Curr Treat Options Neurol 2019; 21(4): 20.
- Schoenen J, et al: Potenziali evocati e stimolazione magnetica transcranica nell’emicrania: dati pubblicati e punto di vista sul loro significato fisiopatologico. Clin Neurophysiol 2003; 114(6): 955-972.
- Brinciotti M, et al: La reattività del sistema visivo nell’emicrania infantile studiata attraverso i PEV. Cefalalgia 1986; 6(3): 183-185.
- Gerwig M, et al: La profilassi dell’emicrania con beta-bloccanti influisce sull’eccitabilità della corteccia visiva, come rivelato dalla stimolazione magnetica transcranica. J Headache Pain 2012; 13(1): 83-89.
- Nyrke T, et al: Potenziali evocati visivi allo stato stazionario durante la profilassi dell’emicrania con propranololo e femoxetina. Acta Neurol Scand 1984; 69(1): 9-14.
- Linde K, Rossnagel K: Propranololo per la profilassi dell’emicrania. Cochrane Database Syst Rev 2004(2): CD003225.
- Hedman C, et al: Sintomi degli attacchi classici di emicrania: modifiche apportate dal metoprololo. Cefalalgia 1988; 8(4): 279-284.
- Langohr HD, et al: Clomipramina e metoprololo nella profilassi dell’emicrania – uno studio crossover in doppio cieco. Cefalea 1985; 25(2): 107-113.
- Istituto svizzero per gli agenti terapeutici Swissmedic. Informazioni sul farmaco. Ultimo accesso il 31.07.2019.
- Stovner LJ, et al: Uno studio comparativo di candesartan rispetto a propranololo per la profilassi dell’emicrania: uno studio randomizzato, in triplo cieco, controllato con placebo, con doppio cross-over. Cefalalgia 2014; 34(7): 523-532.
- Schrader H, et al: Trattamento profilattico dell’emicrania con un inibitore dell’enzima di conversione dell’angiotensina (lisinopril): studio randomizzato, controllato con placebo, crossover. BMJ 2001; 322(7277): 19-22.
- Schuh-Hofer S, et al: Efficacia del lisinopril nella profilassi dell’emicrania – uno studio in aperto. Eur J Neurol 2007; 14(6): 701-703.
- Stubberud A, et al: Flunarizina come profilassi dell’emicrania episodica: una revisione sistematica con meta-analisi. Dolore 2019; 160(4): 762-772.
- Ye Q, et al.: La flunarizina blocca le correnti Na(+) e Ca(2+) voltaggio-gate nei neuroni corticali di ratto in coltura: un possibile luogo d’azione nella prevenzione dell’emicrania. Neurosci Lett 2011; 487(3): 394-399.
- Xu XM, et al: Antidepressivi triciclici per prevenire l’emicrania negli adulti. Medicina 2017; 96(22): e6989.
- Burch R: Antidepressivi per il trattamento preventivo dell’emicrania. Curr Treat Options Neurol 2019; 21(4): 18.
- Ayata C, et al: Soppressione della depressione da diffusione corticale nella profilassi dell’emicrania. Ann Neurol 2006; 59(4): 652-661.
- Sprenger T, Viana M, Tassorelli C: Gli attuali farmaci profilattici per l’emicrania e i loro potenziali meccanismi d’azione. Neuroterapeutica 2018; 15(2): 313-323.
- Steiner TJ, et al: S-fluoxetina nella profilassi dell’emicrania: uno studio di fase II in doppio cieco randomizzato controllato con placebo. Cefalalgia 1998; 18(5): 283-286.
- Saper JR, et al: Studio in doppio cieco della fluoxetina per la cefalea cronica quotidiana e l’emicrania. Cefalea 1994; 34(9): 497-502.
- Landy S, et al: Inibitori selettivi della ricaptazione della serotonina per la profilassi dell’emicrania. Cefalea 1999; 39(1): 28-32.
- Ozyalcin SN, et al: L’efficacia e la sicurezza della venlafaxina nella profilassi dell’emicrania. Cefalea 2005; 45(2): 144-152.
- Taylor AP, Adelman JU, Freeman MC: Efficacia della duloxetina come farmaco preventivo dell’emicrania: possibili predittori di risposta in una revisione retrospettiva della cartella clinica. Cefalea 2007; 47(8): 1200-1203.
- Young WB, et al: Profilassi con duloxetina per l’emicrania episodica in persone senza depressione: uno studio prospettico. Cefalea 2013; 53(9): 1430-1437.
- Brandes JL, et al: Topiramato per la prevenzione dell’emicrania: uno studio controllato randomizzato. JAMA 2004; 291(8): 965-973.
- Storey JR, et al: Topiramato nella prevenzione dell’emicrania: uno studio in doppio cieco, controllato con placebo. Cefalea 2001; 41(10): 968-975.
- Diener HC, et al: Topiramato nella profilassi dell’emicrania – risultati di uno studio controllato con placebo e propranololo come controllo attivo. J Neurol 2004; 251(8): 943-950.
- Ashtari F, Shaygannejad V, Akbari M: Studio randomizzato in doppio cieco di topiramato a basso dosaggio vs. propranololo nella profilassi dell’emicrania. Acta Neurol Scand 2008; 118(5): 301-305.
- Keskinbora K, Aydinli I: Studio randomizzato controllato in doppio cieco di topiramato e amitriptilina da soli o in combinazione per la prevenzione dell’emicrania. Clin Neurol Neurosurg 2008; 110(10): 979-984.
- Silberstein SD, et al: Efficacia e sicurezza del topiramato per il trattamento dell’emicrania cronica: uno studio randomizzato, in doppio cieco, controllato con placebo. Cefalea 2007; 47(2): 170-180.
- Hering R, Kuritzky A: Sodio valproato nel trattamento profilattico dell’emicrania: uno studio in doppio cieco contro placebo. Cefalalgia 1992; 12(2): 81-84.
- Jensen R, Brinck T, Olesen J: Il valproato di sodio ha un effetto profilattico nell’emicrania senza aura: uno studio crossover in triplo cieco, controllato con placebo. Neurologia 1994; 44(4): 647-651.
- Afshari D, Rafizadeh S, Rezaei M: Uno studio comparativo degli effetti del topiramato a basso dosaggio rispetto al valproato di sodio nella profilassi dell’emicrania. Int J Neurosci 2012; 122(2): 60-68.
- Istituto di Farmacologia Clinica e Tossicologia della Charité-Universitätsmedizin di Berlino. Centro di farmacovigilanza e consulenza per la tossicologia embrionale. 2019. www.embryotox.de, ultimo accesso 30.07.2019
- Parikh SK, Silberstein SD: Stato attuale dei farmaci antiepilettici come terapia preventiva dell’emicrania. Curr Treat Options Neurol 2019; 21(4): 16.
- Linde M, et al: Gabapentin o pregabalin per la profilassi dell’emicrania episodica negli adulti. Cochrane Database Syst Rev 2013(6): CD010609.
- Linde M, et al: Antiepilettici diversi da gabapentin, pregabalin, topiramato e valproato per la profilassi dell’emicrania episodica negli adulti. Cochrane Database Syst Rev 2013(6): CD010608.
- Rosenfeld MG, et al: Produzione di un nuovo neuropeptide codificato dal gene della calcitonina attraverso l’elaborazione dell’RNA tessuto-specifico. Natura 1983; 304(5922): 129-135.
- Edvinsson L, et al.: I peptidi perivascolari rilassano le arterie cerebrali in concomitanza con la stimolazione dell’accumulo di adenosina monofosfato ciclico o il rilascio di un fattore rilassante derivato dall’endotelio nel gatto. Neurosci Lett 1985; 58(2): 213-217.
- Goadsby PJ, Edvinsson L: Il sistema trigeminovascolare e l’emicrania: studi che caratterizzano i cambiamenti cerebrovascolari e neuropeptidici osservati nell’uomo e nel gatto. Ann Neurol 1993; 33(1): 48-56.
- Olesen J, et al: l’antagonista del recettore del peptide legato al gene della calcitonina BIBN 4096 BS per il trattamento acuto dell’emicrania. N Engl J Med 2004; 350(11): 1104-1110.
- o TW, et al: Studio controllato randomizzato di un antagonista orale del recettore CGRP, MK-0974, nel trattamento acuto dell’emicrania. Neurologia 2008; 70(16): 1304-1312.
- Ho TW, et al: Studio controllato randomizzato dell’antagonista del recettore CGRP telcagepant per la prevenzione dell’emicrania. Neurologia 2014; 83(11): 958-966.
- Dodick DW, et al: ARISE: uno studio randomizzato di fase 3 su erenumab per l’emicrania episodica. Cefalalgia 2018; 38(6): 1026-1037.
- Goadsby PJ, et al: Uno studio controllato di Erenumab per l’emicrania episodica. N Engl J Med 2017; 377(22): 2123-2132.
- Tepper S, et al: Sicurezza ed efficacia di erenumab per il trattamento preventivo dell’emicrania cronica: uno studio di fase 2 randomizzato, in doppio cieco, controllato con placebo. The Lancet Neurology 2017; 16(6): 425-434.
- Stauffer VL, et al: Valutazione del galcanezumab per la prevenzione dell’emicrania episodica: lo studio clinico randomizzato EVOLVE-1. JAMA Neurol 2018; 75(9): 1080-1088.
- Skljarevski V, et al: Efficacia e sicurezza di galcanezumab per la prevenzione dell’emicrania episodica: risultati dello studio clinico randomizzato e controllato di fase 3 EVOLVE-2. Cefalalgia 2018; 38(8): 1442-1454.
- Silberstein SD, et al: Fremanezumab per il trattamento preventivo dell’emicrania cronica. N Engl J Med 2017; 377(22): 2113-2122.
- Detke HC, et al: Galcanezumab nell’emicrania cronica: lo studio REGAIN, randomizzato, in doppio cieco e controllato con placebo. Neurologia 2018; 91(24): e2211-e2221.
- Ufficio federale della sanità pubblica: Aimovig, in Bollettino UFSP. Ufficio federale della sanità pubblica, Berna, 2018: 1.
- Ufficio federale della sanità pubblica: Emgality, in Bollettino UFSP. Ufficio federale della sanità pubblica, Berna, 2019: 1.
- Schoenen J, Sianard-Gainko J, Lenaerts M: Livelli di magnesio nel sangue nell’emicrania. Cefalalgia 1991; 11(2): 97-99.
- Ramadan NM, et al: Basso livello di magnesio cerebrale nell’emicrania. Cefalea 1989; 29(9): 590-593.
- Morris ME: Concentrazioni di magnesio nel cervello e nel liquor durante il deficit di magnesio negli animali e nell’uomo: sintomi neurologici. Magnes Res 1992; 5(4): 303-313.
- Mayer ML, Westbrook GL, Guthrie PB: Blocco voltaggio-dipendente da Mg2+ delle risposte NMDA nei neuroni del midollo spinale. Natura 1984; 309(5965): 261-263.
- Pearson PJ, et al: L’ipomagnesemia inibisce il rilascio di ossido nitrico dall’endotelio coronarico: ruolo protettivo dell’infusione di magnesio dopo la chirurgia cardiaca. Annali di Chirurgia Toracica 1998; 65(4): 967-972.
- de Baaij JH, Hoenderop JG, Bindels RJ: Il magnesio nell’uomo: implicazioni per la salute e la malattia. Physiol Rev 2015; 95(1): 1-46.
- Pfaffenrath V, et al: Magnesio nella profilassi dell’emicrania – uno studio in doppio cieco controllato con placebo. Cefalalgia 1996; 16(6): 436-440.
- Cete Y, et al: Uno studio prospettico randomizzato controllato con placebo sul solfato di magnesio per via endovenosa rispetto alla metoclopramide nella gestione degli attacchi di emicrania acuta nel Dipartimento di Emergenza. Cefalalgia 2005; 25(3): 199-204.
- Chiu HY, et al: Effetti del magnesio per via endovenosa e orale sulla riduzione dell’emicrania: una meta-analisi di studi controllati randomizzati. Pain Physician 2016; 19(1): e97-112.
- integratore proprietario contenente riboflavina, magnesio e Q10: uno studio randomizzato, controllato con placebo, in doppio cieco, multicentrico. J Headache Pain 2015; 16: 516.
- Choi H, Parmar N: L’uso del solfato di magnesio per via endovenosa per l’emicrania acuta: meta-analisi di studi controllati randomizzati. Eur J Emerg Med 2014; 21(1): 2-9.
- Montagna P, et al: L’emicrania come difetto del metabolismo ossidativo cerebrale: un’ipotesi. J Neurol 1989; 236(2): 124-125.
- Arts WFM, et al: Miopatia da deficit di nadh-coq reduttasi: trattamento di successo con riboflavina. The Lancet 1983; 322(8349): 581-582.
- Schoenen J, Jacquy J, Lenaerts M: Efficacia della riboflavina ad alto dosaggio nella profilassi dell’emicrania. Uno studio controllato randomizzato. Neurologia 1998; 50(2): 466-470.
- Boehnke C, et al.: Il trattamento con riboflavina ad alto dosaggio è efficace nella profilassi dell’emicrania: uno studio aperto in un centro di cura terziario. Eur J Neurol 2004; 11(7): 475-477.
- MacLennan SC, et al.: Riboflavina ad alto dosaggio per la profilassi dell’emicrania nei bambini: uno studio in doppio cieco, randomizzato, controllato con placebo. J Child Neurol 2008; 23(11): 1300-1304.
- Sandor PS, et al: Efficacia del coenzima Q10 nella profilassi dell’emicrania: uno studio randomizzato controllato. Neurologia 2005; 64(4): 713-715.
- Ernster L, Dallner G: Aspetti biochimici, fisiologici e medici della funzione dell’ubichinone. BBA Molecular Basis of Disease 1995; 1271(1): 195-204.
- Shoeibi A, et al: Efficacia del coenzima Q10 nel trattamento profilattico dell’emicrania: uno studio in aperto, add-on, controllato. Acta Neurol Belg 2017; 117(1): 103-109.
- Rozen TD, et al: Studio in aperto del coenzima Q10 come preventivo dell’emicrania. Cefalalgia 2002; 22(2): 137-141.
- Slater SK, et al: Uno studio randomizzato, in doppio cieco, controllato con placebo, crossover, con aggiunta di CoEnzima Q10 nella prevenzione dell’emicrania pediatrica e adolescenziale. Cefalalgia 2011; 31(8): 897-905.
- Granella F, et al: Emicrania con aura ed eventi della vita riproduttiva: uno studio caso-controllo. Cefalalgia 2000; 20(8): 701-707.
- Maggioni F, et al: Cefalea in gravidanza. Cefalalgia 1997; 17(7): 765-769.
- Sances G., et al: Decorso dell’emicrania durante la gravidanza e il post-partum: uno studio prospettico. Cefalalgia 2003; 23(3): 197-205.
- MacGregor EA: Emicrania in gravidanza e allattamento. Neurol Sci 2014; 35(Suppl 1): 61-64.
- Calhoun AH: Trattamento dell’emicrania in gravidanza e allattamento. Curr Pain Headache Rep 2017; 21(11): 46.
- Kaplan W, et al.: Effetti osteopenici di MgS04 nelle gravidanze multiple. Journal of Pediatric Endocrinology and Metabolism 2006; 19(10): 1225-1230.
- Associazione statunitense per gli alimenti e i farmaci: la FDA raccomanda di non usare il solfato di magnesio per interrompere il travaglio pretermine a causa dei cambiamenti ossei nei bambini esposti. Comunicazione sulla sicurezza dei farmaci 2013. www.fda.gov/media/85971/download, ultimo accesso 30 luglio 2019.
- Tepper D: Gravidanza e allattamento – gestione dell’emicrania. Cefalea 2015; 55(4): 607-608.
- MacGregor EA: Gestione dell’emicrania durante le mestruazioni e la menopausa. Continuum (Minneap Minn) 2015; 21(4 Headache): 990-1003.
- MacGregor EA: Classificazione della cefalea perimestruale: rilevanza clinica. Curr Pain Headache Rep 2012; 16(5): 452-460.
- Vetvik KG, et al: Attacchi mestruali rispetto a quelli non mestruali di emicrania senza aura in donne con e senza emicrania mestruale. Cefalalgia 2015; 35(14): 1261-1268.
- MacGregor EA, et al: Prevenzione degli attacchi mestruali di emicrania: uno studio crossover in doppio cieco controllato con placebo. Neurologia 2006; 67(12): 2159-2163.
- MacGregor EA: Contraccezione e cefalea. Cefalea 2013; 53(2): 247-276.
- Shufelt CL, Bairey Merz CN: Uso di ormoni contraccettivi e malattie cardiovascolari. J Am Coll Cardiol 2009; 53(3): 221-231.
- Natoli JL, et al: Prevalenza globale dell’emicrania cronica: una revisione sistematica. Cefalalgia 2010; 30(5): 599-609.
- Straube A, et al.: Prevalenza dell’emicrania cronica e della cefalea da uso eccessivo di farmaci in Germania – lo studio tedesco DMKG sulle cefalee. Cefalalgia 2010; 30(2): 207-213.
- Diener HC, et al: Il topiramato riduce i giorni di cefalea nell’emicrania cronica: uno studio randomizzato, in doppio cieco, controllato con placebo. Cefalalgia 2007; 27(7): 814-823.
- Silvestrini M, et al: Topiramato nel trattamento dell’emicrania cronica. Cefalalgia 2003; 23(8): 820-824.
- Aurora SK, et al: OnabotulinumtoxinA per l’emicrania cronica: efficacia, sicurezza e tollerabilità nei pazienti che hanno ricevuto tutti i cinque cicli di trattamento nel programma clinico PREEMPT. Acta Neurol Scand 2014; 129(1): 61-70.
- Aurora SK, et al: OnabotulinumtoxinA per il trattamento dell’emicrania cronica: analisi congiunte del programma clinico PREEMPT di 56 settimane. Cefalea 2011; 51(9): 1358-1373.
- Diener HC, et al: OnabotulinumtoxinA per il trattamento dell’emicrania cronica: risultati della fase in doppio cieco, randomizzata, controllata con placebo, dello studio PREEMPT 2. Cefalalgia 2010; 30(7): 804-814.
- Dodick DW, et al: OnabotulinumtoxinA per il trattamento dell’emicrania cronica: risultati raggruppati delle fasi in doppio cieco, randomizzate e controllate con placebo del programma clinico PREEMPT. Cefalea 2010; 50(6): 921-936.
- Yurekli VA, et al: L’effetto del valproato di sodio sulla cefalea cronica quotidiana e i suoi sottogruppi. J Headache Pain 2008; 9(1): 37-41.
- Westergaard ML, et al: Definizioni di cefalea da uso eccessivo di farmaci negli studi basati sulla popolazione e loro implicazioni sulle stime di prevalenza: una revisione sistematica. Cefalalgia 2014; 34(6): 409-425.
- Tassorelli C, et al: Un protocollo di consenso per la gestione della cefalea da uso eccessivo di farmaci: valutazione in uno studio multicentrico e multinazionale. Cefalalgia 2014; 34(9): 645-655.
InFo NEUROLOGIA & PSICHIATRIA 2019; 17(5): 10-14.