Gli studi suggeriscono che la sorveglianza attiva è un’opzione di trattamento per i tumori con un basso rischio di progressione (tumori a basso rischio). Il team terapeutico deve collaborare con il paziente per determinare le strategie di trattamento in base alle linee guida esistenti e alle prove attuali. Nella Sorveglianza Attiva, il follow-up del paziente e il monitoraggio regolare sono un fattore cruciale nella strategia di trattamento. Sempre più carcinomi della prostata vengono diagnosticati sulla base delle misurazioni del PSA. Circa il 90% di questi tumori è localizzato. Una grande percentuale di tumori diagnosticati non rappresenta un rischio per i pazienti interessati; il rischio di morbilità derivante dagli interventi è più alto per questi pazienti rispetto al rischio di morbilità derivante dal tumore.
Secondo le attuali linee guida (S3 Guideline DGU, EAU Guideline on Prostate Cancer), esistono diverse opzioni alternative per il trattamento del carcinoma prostatico localizzato a basso rischio: prostatectomia radicale, radioterapia locale, sorveglianza attiva e, a seconda dell’età, il concetto di vigile attesa. Per sorveglianza attiva (AS) si intende l’attento monitoraggio delle persone a cui è stata diagnosticata una malattia durante il suo decorso. L’AS deve essere distinto dall’Attesa vigile. Questo include le strategie di trattamento sintomatico di una malattia nel suo decorso, senza l’obiettivo di trasferire i pazienti alla terapia curativa, ad esempio a causa dell’età avanzata e/o di gravi comorbilità. L’AS deve anche essere distinta dalla sorveglianza clinica/di salute pubblica, che mira a raccogliere, analizzare e interpretare i dati relativi alla salute su popolazioni specifiche [1].
Sorveglianza attiva per i tumori a basso rischio
L’analisi e l’interpretazione dei trattamenti oncologici per alcune malattie oncologiche selezionate negli uomini hanno recentemente perseguito l’obiettivo di evitare il sovratrattamento con opzioni terapeutiche invasive. Soprattutto per il cancro alla prostata e al testicolo, sono stati sviluppati criteri che portano a non trattare immediatamente o addirittura a non trattare. Per entrambe le entità, le linee guida sul trattamento stabiliscono che, oltre alle opzioni terapeutiche consolidate (prostatectomia, radioterapia, terapia farmacologica del tumore, ablazione ormonale, orchiectomia), la SA per la malattia a basso rischio è disponibile come ulteriore opzione di trattamento primario [2,3]. La decisione a favore o contro la SA come strategia di trattamento è determinata dalla classificazione del tumore come “a basso rischio”.
Utilizzando l’esempio del carcinoma prostatico, di seguito verranno dimostrate le difficoltà pratiche nella scelta del possibile trattamento. Il fatto che la classificazione del cancro sia ancora – nonostante molti anni di ricerca – caratterizzata da una pratica molto eterogenea è dimostrato dagli studi attuali [4–11]. Ad esempio, il tasso di pazienti con un tumore a basso rischio è sceso dal 60% nel 2004 al 27% nel 2013 – in base alle definizioni riviste di tumori a basso rischio [12].
Epidemiologia ed eziologia
Il cancro alla prostata è il tumore più comune negli uomini in Svizzera [13]. C’è un’incidenza diversa nelle varie popolazioni: negli Stati Uniti, le persone con la pelle scura sono colpite più spesso dei bianchi e questi ultimi più spesso degli asiatici. Questo suggerisce una predisposizione genetica allo sviluppo del carcinoma [9]. Presumibilmente, la predisposizione genetica è anche influenzata e modificata da fattori socio-demografici [14–16]. Per esempio, l’incidenza del cancro alla prostata aumenta tra gli asiatici che immigrano negli Stati Uniti. L’incidenza del cancro alla prostata clinicamente non significativo è paragonabile in tutto il mondo, ma esistono differenze per il cancro alla prostata clinicamente rilevante. Gli uomini con un parente di primo grado affetto da cancro alla prostata hanno un rischio doppio di sviluppare anch’essi il cancro alla prostata. Se ci sono diversi parenti di primo grado con la malattia, il rischio aumenta da 5 a 11 volte [10,17].
La maggior parte di tutti i carcinomi della prostata probabilmente insorge a causa di molteplici polimorfismi genetici [10]. Il testosterone non è attualmente considerato un agente precancerogeno, ma probabilmente svolge un ruolo di promotore tumorale nei tumori già progressivi. I componenti della dieta influenzano il cancro alla prostata in molti modi [18]. Le proteine animali sembrano favorire il rischio di sviluppare un cancro alla prostata avanzato. L’oligoelemento selenio è stato discusso per qualche tempo in relazione a un possibile beneficio protettivo. Tuttavia, lo studio SELECT non ha potuto dimostrare tale beneficio ed è stato quindi interrotto prematuramente nel 2008. Il fumo di tabacco al momento della diagnosi iniziale aumenta il rischio di tumore avanzato, recidiva (38 vs. 26%) e morte per carcinoma (15,3 vs. 9,6/1000 anni-persona) [15]. La sindrome metabolica aumenta anche il rischio di cancro alla prostata. Finora non è stato possibile dimostrare un collegamento tra il rischio di cancro alla prostata e il consumo di alcol.
Alta percentuale di sovratrattamento
Per oltre 30 anni, la prostatectomia radicale è stata considerata la terapia standard per il trattamento curativo del cancro alla prostata; circa il 70% dei pazienti di età inferiore ai 70 anni si sottopone alla prostatectomia [8,12]. Questa strategia viene perseguita con il presupposto che il paziente sia guarito dopo l’intervento. Queste considerazioni devono essere sempre più messe in prospettiva: In circa il 30% degli uomini che hanno subito un intervento chirurgico, si verifica una progressione del PSA nel corso dell’operazione. Alcuni dei pazienti hanno tumori che non devono necessariamente essere trattati con un intervento; questi pazienti non morirebbero a causa del tumore anche senza intervento chirurgico o radiazioni. Tuttavia, le possibilità di valutare la biologia individuale del tumore sono ancora oggi limitate. Pertanto, l’équipe curante e i pazienti scelgono spesso il percorso dell’intervento, spesso per la preoccupazione che il tumore possa svilupparsi in uno stadio che non può più essere trattato in modo curativo a causa della rapida progressione.
L’osservazione attiva regolare dei pazienti con carcinomi a basso rischio clinicamente non rilevanti, adatti alla SA, può prevenire le morbilità legate alla terapia (disfunzione erettile, incontinenza, complicazioni legate alla chirurgia e alle radiazioni, ecc. Anche il carico psicologico sul paziente e sul partner, sotto la guida di un urologo esperto, è considerato appropriato [6,18]. Lo studio ERSPC ha mostrato un tasso di sovratrattamento del 54%. Risparmiare a questi uomini le morbilità della terapia interventistica è lo scopo della SA [5].
Criteri per la sorveglianza attiva
L’attuale linea guida S3 sulla diagnosi precoce, la diagnosi e il trattamento dei diversi stadi del cancro alla prostata include la SA come strategia di trattamento per i carcinomi definiti a basso rischio che soddisfano determinati criteri (Tab. 1).

La linea guida definisce i seguenti criteri decisionali rilevanti:
- I pazienti con tumore alla prostata localizzato che possono essere sottoposti a un trattamento curativo locale devono essere informati non solo sulle procedure di trattamento come la prostatectomia radicale, la radioterapia e la brachiterapia, ma anche sulla SA.
- Nei pazienti con carcinoma prostatico localizzato candidati al trattamento curativo, gli effetti avversi e le conseguenze terapeutiche della prostatectomia radicale, della radioterapia percutanea e della brachiterapia devono essere soppesati rispetto al rischio di un trattamento ritardato nel caso di una strategia AS.
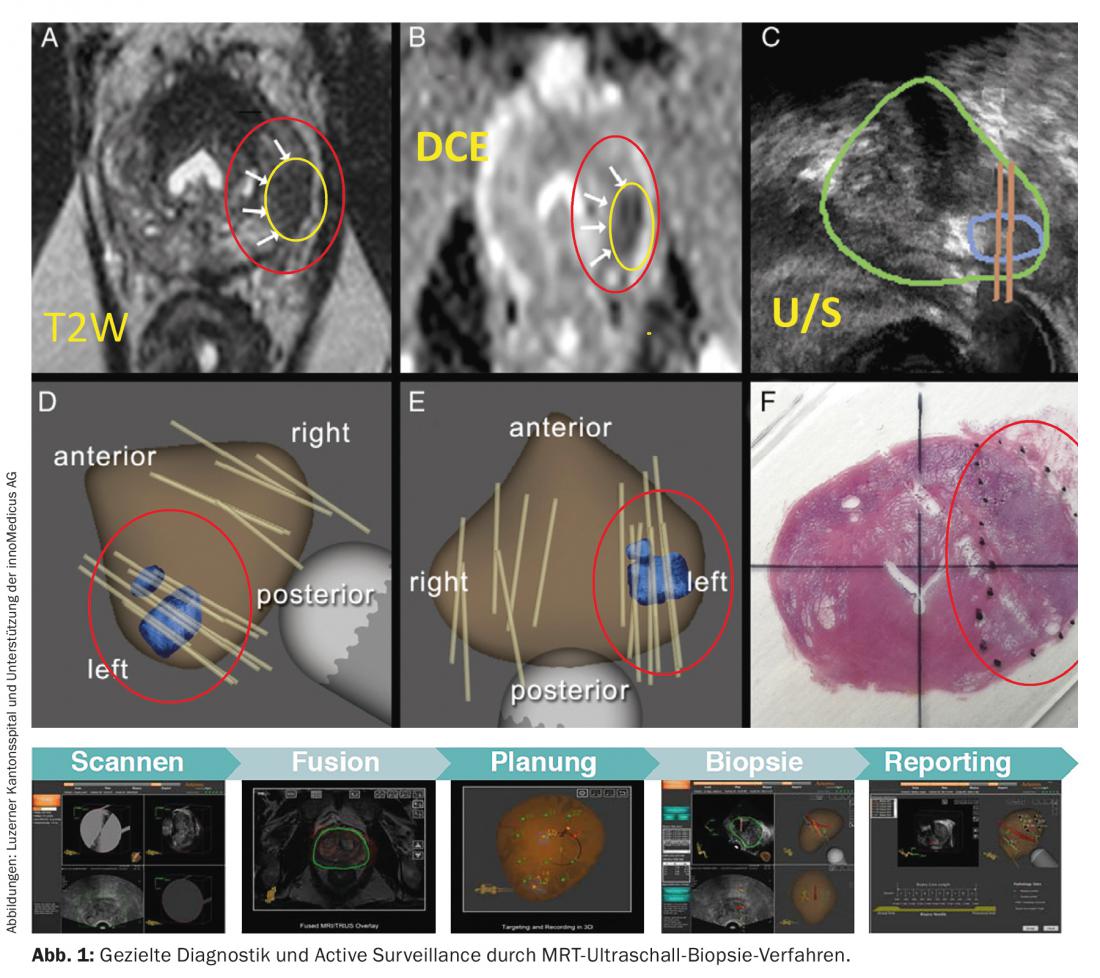
- Il tumore deve essere monitorato ogni tre mesi per i primi due anni dopo la diagnosi, utilizzando la determinazione del PSA e l’esame rettale digitale. Se il valore del PSA rimane stabile, deve essere controllato successivamente ogni sei mesi. Le biopsie devono essere effettuate ogni 12-18 mesi. Attualmente si stanno studiando nuovi metodi per aumentare l’importanza delle biopsie prostatiche (Fig. 1).
- La SA deve essere abbandonata se il tempo di raddoppio del PSA si riduce a meno di tre anni o se il grado di malignità si deteriora fino a un punteggio Gleason >6.
La misura in cui il trattamento deve essere adattato nel corso individuale (ad esempio, prostatectomia radicale o radiazione locale) dipende direttamente dalla dinamica individuale del tumore. Ogni paziente viene informato su tutte le opzioni terapeutiche e gli viene offerta principalmente una procedura che gli consenta di trascorrere inizialmente gli anni di vita rimanenti senza limitazioni legate alla terapia e con un’elevata qualità di vita. I centri oncologici certificati contribuiscono in modo comprovabile a garantire la qualità dell’assistenza.
Conclusione per la pratica
- Attualmente, il primo test PSA di base è raccomandato in Svizzera tra i 40 e i 45 anni.
- Se il livello di PSA è <1 ng/ml, la determinazione del PSA è raccomandata ogni tre anni, per PSA ≥1 a <2 ng/ml ogni due anni e per PSA ≥2 a <3 ng/ml annualmente. Il paziente deve essere informato dettagliatamente in anticipo.
- Le misurazioni eccessive del PSA provocano la diagnosi di un numero crescente di carcinomi prostatici che altrimenti sarebbero rimasti inosservati per tutta la vita, data la costellazione dell’età, le comorbidità e/o la biologia tumorale favorevole dei pazienti.
- Circa il 90% dei pazienti diagnosticati negli ultimi anni presenta un carcinoma prostatico localizzato.
- Gli studi suggeriscono che la SA è un’opzione di trattamento per i tumori con un basso rischio di progressione (tumori a basso rischio). I pazienti devono essere informati su tutte le opzioni di trattamento.
- Il team di trattamento (medici di base, urologi, radioterapisti, oncologi) deve definire e seguire le strategie di trattamento insieme al paziente e ai suoi familiari, soprattutto in caso di possibile AS, sulla base delle linee guida esistenti e delle prove attuali.
- La Società Svizzera di Urologia ha creato un database di sorveglianza attiva (SIP-CAS) per garantire e ampliare continuamente la base di prove.
Letteratura:
- OMS, Sorveglianza della salute pubblica, 2015. www.who.int/topics/public_health_surveillance/en/.
- Kollmannsberger C, et al: Modelli di recidiva nei pazienti con tumore testicolare in stadio clinico I, gestiti con sorveglianza attiva. J Clin Oncol 2015; 33(1): 51-57.
- Coursey Moreno C, et al: Tumori del testicolo: cosa devono sapere i radiologi – diagnosi differenziale, stadiazione e gestione. Radiographics 2015; 35(2): 400-415.
- Loeb S, et al: Sorveglianza attiva per il cancro alla prostata: una revisione sistematica delle variabili clinicopatologiche e dei biomarcatori per la stratificazione del rischio. Urologia europea 2015; 67(4): 619-626.
- Klotz L: Sorveglianza attiva per il cancro alla prostata: dibattito sull’applicazione, non sul concetto. European Urology 2015 Jan 24. doi: 10.1016/j.eururo.2015.01.007. [Epub ahead of print]
- Bellardita L, et al: Come la sorveglianza attiva per il cancro alla prostata influisce sulla qualità della vita? Una revisione sistematica. Urologia europea 2015; 67(4): 637-645.
- Bangma CH, et al: Sorveglianza attiva per il cancro alla prostata a basso rischio: gli sviluppi fino ad oggi. Urologia europea 2015; 67(4): 646-648.
- Saman DM, et al: Una revisione dell’attuale epidemiologia e delle opzioni di trattamento del cancro alla prostata. Dis Mon 2014; 60(4): 150-154.
- Helfand BT, Catalona WJ: L’epidemiologia e le implicazioni cliniche della variazione genetica nel cancro alla prostata. Urol Clin North Am 2014; 41(2): 277-297.
- Eeles R, et al: L’epidemiologia genetica del cancro alla prostata e le sue implicazioni cliniche. Nat Rev Urol 2014; 11(1): 18-31.
- Berman DM, Epstein J: Quando il cancro alla prostata è davvero un cancro? Urol Clin North Am 2014; 41(2): 339-346.
- Huland H, Graefen M: Tendenze in evoluzione nella gestione chirurgica del cancro alla prostata: la fine del sovratrattamento? Eur Urol 2015 Feb 27. doi: 10.1016/j.eururo. 2015.02.020. [Epub ahead of print]
- Ufficio federale di statistica, 2015. www.bfs.admin.ch/bfs/portal/de/index/themen/14/02/05/key/01/02.html.
- Kasperzyk JL, et al: La vigile attesa e la qualità della vita tra i sopravvissuti al cancro alla prostata nel Physicians’ Health Study. J Urol 2011; 186(5): 1862-1867.
- Kenfield SA, et al: Fumo e sopravvivenza e recidiva del cancro alla prostata. JAMA 2011; 305(24): 2548-2555.
- Kenfield SA, et al: Attività fisica e sopravvivenza dopo la diagnosi di cancro alla prostata nello studio di follow-up dei professionisti della salute. J Clin Oncol 2011; 29(6): 726-732.
- Bratt O: Cancro alla prostata ereditario: aspetti clinici. J Urol 2002; 168(3): 906-913.
- Masko EM, et al: Il rapporto tra nutrizione e cancro alla prostata: è sempre meglio? Eur Urol 2013; 63(5): 810-820.
InFo ONCOLOGIA & EMATOLOGIA 2015; 3(5): 8-11