Al giorno d’oggi, la psoriasi è considerata una malattia infiammatoria sistemica, in cui le citochine proinfiammatorie svolgono un ruolo importante. Nella patogenesi della psoriasi sono coinvolti diversi circuiti infiammatori. Le citochine delle famiglie IL-23 e IL-17 sono bersagli comprovati, ma si stanno studiando anche altri bersagli terapeutici.
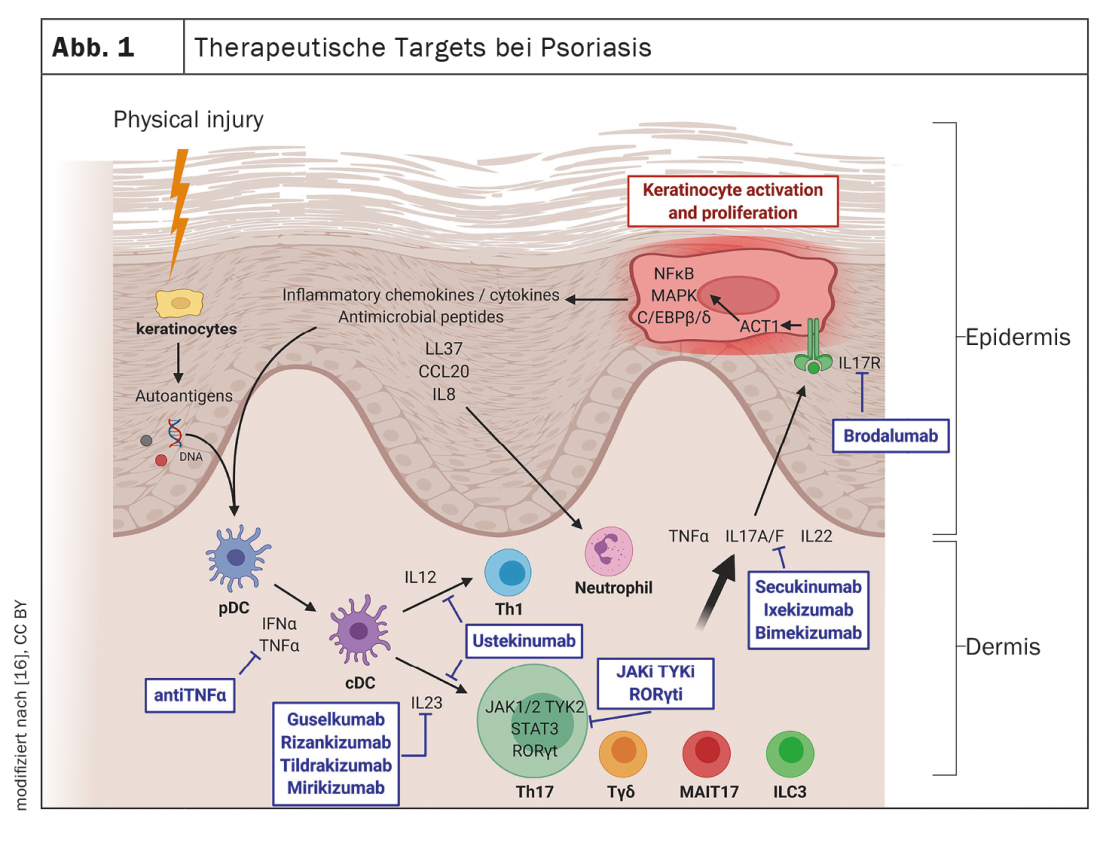
L’efficacia e la sicurezza dell’immunoterapia sistemica sono migliorate in modo significativo negli ultimi anni, grazie all’introduzione di nuovi agenti appartenenti alle classi di inibitori dell’IL-17 e dell’IL-23. “Negli ultimi anni abbiamo assistito a un rapido aumento del numero di preparazioni”, afferma la Dr. med. Sylvie Haase, specialista in malattie cutanee e veneree in uno studio dermatologico di gruppo a Costanza [2]. Oggi è disponibile un’ampia gamma di agenti sistemici, diretti contro diversi bersagli, e poiché i pato-meccanismi molecolari continuano ad essere decifrati, si prevede che questa tendenza continui in futuro (Fig. 1). Sempre più spesso, la sfida consiste nell’abbinare i pazienti alle opzioni di trattamento appropriate. Si scopre che tra i pazienti con psoriasi da moderata a grave, ci sono quelli che rispondono molto bene alla prima opzione di terapia sistemica e rimangono in trattamento per anni, ma anche quelli in cui la psoriasi si dimostra refrattaria alla terapia, ha spiegato il relatore.
Analisi della risposta ai biologici: cosa si può dedurre da esse?
La caratteristica patologica principale della psoriasi è considerata l’infiammazione cronica della pelle, che porta alla proliferazione incontrollata e alla differenziazione disfunzionale dei cheratinociti. A livello molecolare, il ruolo fisiopatologico centrale dell’asse TNF-α-IL-23-Th17 è molto ben caratterizzato. Gli anticorpi monoclonali attualmente approvati in Svizzera per il trattamento della psoriasi sono diretti contro le seguenti citochine: TNF-α, interleuchina(IL)-12/IL-23, IL-23, IL-17A o IL-17A/F [1]. Secondo le meta-analisi di rete, i gruppi di inibitori dell’IL-17 (IL-17-i) e di inibitori dell’IL-23 (IL-23-i) mostrano un’efficacia maggiore in termini di PASI*-90 e PASI-100 rispetto al TNF-α-i [8]. Per quanto riguarda l’IL-23-i, il Dr. Haase spiega: “L’effetto si verifica un po’ più lentamente rispetto agli inibitori dell’IL-17, ma i preparati non hanno uno spettro di effetti collaterali specifico”. In Svizzera, l’IL-17A-i secukinumab e ixekizumab sono attualmente approvati, così come recentemente l’IL17A/F-i bimekizumab, e tra gli IL-23-i sono in commercio guselkumab, risankizumab e tildrakizumab.
* PASI = Indice di Area e Severità della Psoriasi
In uno studio di coorte, un team di ricerca danese ha analizzato la risposta a diversi biologici [3]. I 2022 risultati pubblicati nel Journal of the European Academy of Dermatology and Venereology mostrano che dei 3280 pazienti totali inclusi (età media 45,0 anni, 37% donne), il 6,3% è stato classificato come super-responder e il 6,5% come refrattario al trattamento. Questi ultimi avevano un IMC medio più alto rispetto agli altri pazienti (32,2 vs. 29,4, p<0,0001), mentre i super-responder avevano meno comorbidità e uno stato socioeconomico più elevato.
L’inibitore di IL-17A/F, bimekizumab, è un nuovo giocatore
Il fatto che l’IL-17A svolga un ruolo centrale nella patogenesi della psoriasi è stato dimostrato più volte dal successo dell’uso degli anticorpi inibitori corrispondenti. Tuttavia, l’IL-17F è anche sovraespressa nella pelle e nel tessuto sinoviale delle persone affette da psoriasi [4]. Bimekizumab, un anticorpo monoclonale IgG1 che inibisce selettivamente le interleuchine IL-17F e IL-17A, è diventato recentemente disponibile in Svizzera. Nei tre studi pivotal, bimekizumab ha dimostrato una buona efficacia e ha ottenuto risultati migliori rispetto all’antagonista dell’IL-12/IL-23 ustekinumab e all’inibitore del TNF-α adalimumab sugli endpoint co-primari PASI-90 e IGA# 0/1 alla settimana 16 [5–7]. Il profilo di sicurezza di bimekizumab è caratterizzato dagli effetti di classe noti dell’inibizione dell’IL-17; gli effetti collaterali comuni includono la candidosi orale. Un nuovo nano-corpo trivalente contro l’IL-17A e l’IL-17F, attualmente in fase di studio per l’uso nella psoriasi, è il sonelokimab. Negli studi di fase I e II sono stati ottenuti risultati promettenti [4]. I nanocorpi sono anticorpi ricombinati, specifici per l’antigene, che consistono solo del dominio variabile necessario per il legame con l’antigene e sono quindi relativamente piccoli.
# IGA=Investigator ‘s Global Assessment (valutazione globale dell’investigatore): pazienti con IGA: 0 = pelle senza aspetto, 1 = sintomi cutanei lievi.
Sono in cantiere anche diversi agenti applicati per via orale o topica.
La ricerca di nuovi agenti antipsoriatici è un campo di ricerca in rapido sviluppo. I seguenti agenti sistemici sono stati recentemente approvati per la psoriasi a placche dalla Food and Drug Administration (FDA) statunitense quest’anno (Tabella 1):
- Deucravacitinib (BMS-986165) è un inibitore altamente selettivo di TYK2 in forma di dosaggio orale da usare una volta al giorno nella psoriasi a placche da moderata a grave (approvazione FDA 09/09/22) [9,10].
- Roflumilast (ARQ-151) è un inibitore topico della PDE-4 per il trattamento della psoriasi a placche nei pazienti di età ≥12 anni (approvazione FDA 07/29/22) [11–13].
- Tapinarof-Crème 1% (Vtama) è un modulatore del recettore degli idrocarburi arilici per il trattamento della psoriasi a placche negli adulti (approvazione FDA 24/05/22) [18,19].
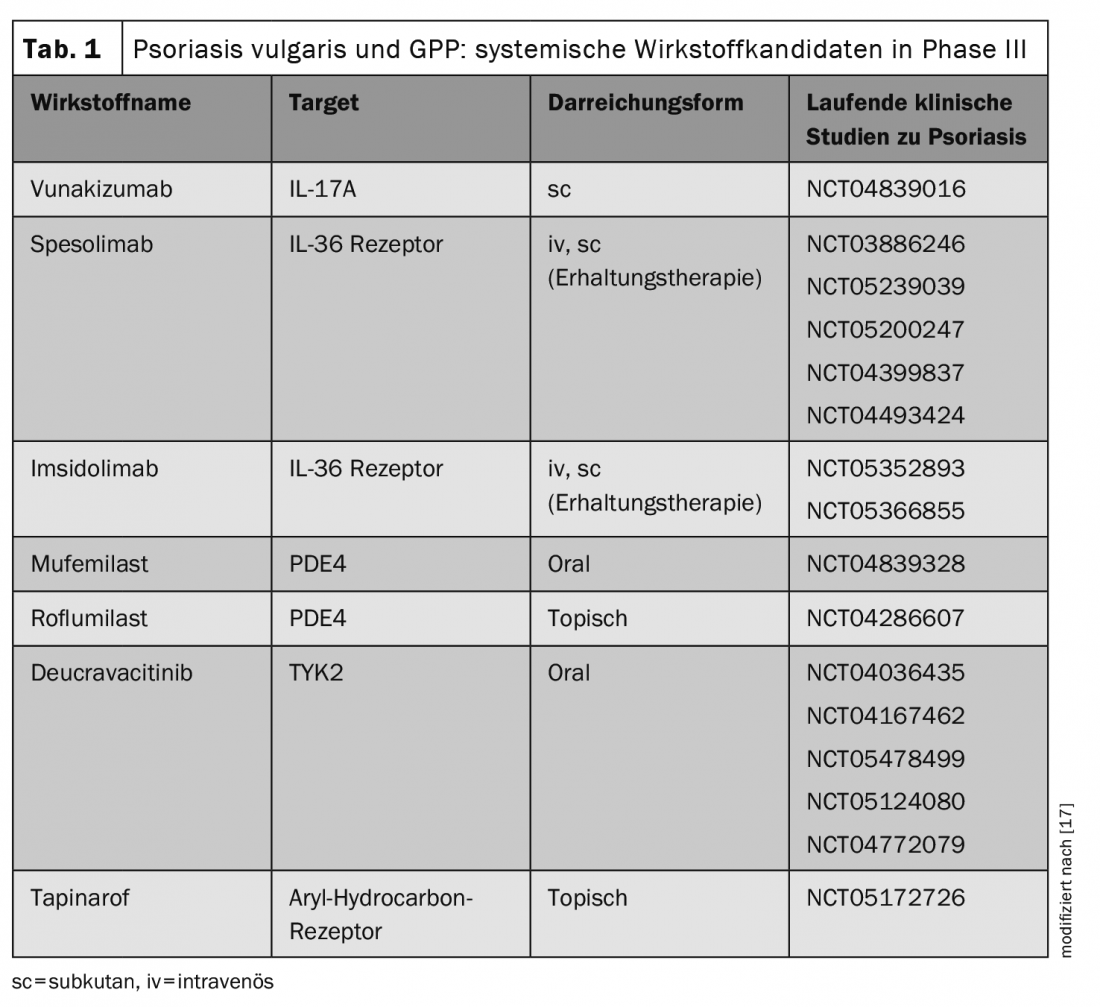
Inoltre, spesolimab, un anticorpo monoclonale umanizzato contro IL36-R, è stato approvato dalla FDA per il trattamento delle riacutizzazioni della GPP (Psoriasi Pustolosa Generalizzata) (approvazione FDA 01.09.22). La decisione di approvazione si basa sullo studio di fase II Effisayil-1 [14,15]. Altri agenti sistemici innovativi sono attualmente in fasi avanzate di sviluppo clinico (Tab. 1) [17]. È quindi possibile che lo spettro terapeutico venga ampliato anche in Europa, in un futuro non troppo lontano, per includere ulteriori terapie di sistema. Soprattutto per i pazienti refrattari, sono benvenute nuove alternative terapeutiche. Per quanto riguarda i profili degli effetti collaterali, il dottor Haase sottolinea che gli effetti noti della classe di sostanze degli inibitori della JAK includono un numero leggermente maggiore di infezioni del tratto respiratorio superiore e di herpes simplex, e che occasionalmente può verificarsi un esantema simile all’acne. Sono necessari dati a lungo termine per comprendere meglio le differenze tra le varie opzioni di trattamento e per poter fare una scelta orientata al paziente.
Congresso: Bodensee Dermaconsil
Letteratura:
- Lauffer F, et al: Citochine della famiglia IL-17 nella psoriasi. JDDG; 1610-0379/2020/1807
- “Psoriasi – c’è qualcosa di nuovo?”, Dr. med. Sylvie Haase, 3° Bodensee Dermaconsil, 22.10.2022.
- Loft N, et al: Prevalenza e caratterizzazione della psoriasi refrattaria al trattamento e dei super-rispondenti al trattamento biologico: uno studio a livello nazionale. J Eur Acad Dermatol Venereol 2022; 36(8): 1284-1291.
- Iznardo H, Puig L: Doppia inibizione di IL-17A e IL-17F nella malattia psoriasica. Ther Adv Chronic Dis 2021 Aug 12;12:20406223211037846
- Warren RB, et al: Bimekizumab rispetto ad adalimumab nella psoriasi a placche. N Engl J Med 2021; 385: 130-141.
- Reich K, et al: Bimekizumab versus ustekinumab per il trattamento della psoriasi a placche da moderata a grave (BE VIVID): efficacia e sicurezza di uno studio di fase 3 di 52 settimane, multicentrico, in doppio cieco, con comparatore attivo e controllato con placebo. Lancet 2021; 397: 487-498.
- Gordon KB, et al: Efficacia e sicurezza di Bimekizumab nella psoriasi a placche da moderata a grave (BE READY): uno studio multicentrico, in doppio cieco, controllato con placebo, randomizzato di fase 3. Lancet 2021; 397: 475-486.
- Yasmeen N, et al: Terapie mirate per i pazienti con psoriasi da moderata a grave: una revisione sistematica e una meta-analisi di rete della risposta PASI a 1 anno. J Dermatolog Treat 2022; 33(1): 204-218.
- Boerner LK. L’incontro ibrido divulga le strutture dei candidati farmaci [Internet]. Notizie di chimica e ingegneria. 2022. Disponibile su: https://cen.acs.org/acs-news/acs-meeting-news/Hybrid-meeting-divulges-st…,(ultimo accesso 15.11.2022)
- Chimalakonda A, et al.: Profilo di selettività dell’inibitore della tirosin-chinasi 2 deucravacitinib rispetto agli inibitori della Janus chinasi 1/2/3. Dermatol Ther (Heidelb) 2021; 11(5): 1763-1776.
- Lebwohl MG, et al: Prova di roflumilast crema per la psoriasi cronica a placche. N Eng J Med 2020; 383(3): 229-239.
- Arcutis Biotherapeutics. La FDA approva ZORYVE (roflumilast) Crema 0,3% di Arcutis per il trattamento della psoriasi a placche nei soggetti di età pari o superiore a 12 anni [Internet]. 2022. Disponibile su: www.arcutis.com/fda-approves-arcutis-zoryve-roflumilast-cream-0-3-for-th…,(ultimo accesso 15.11.2022)
- Lebwohl M, et al.: Sicurezza ed efficacia di roflumilast Cream 0,3% una volta al giorno, un potente inibitore della fosfodiesterasi-4 per il trattamento della psoriasi negli studi di fase 3 DERMIS-1 e DERMIS-2. Poster presentato alla conferenza:30° Congresso EADV, 29 settembre-2 ottobre 2021; virtuale
- Boehringer Ingelheim. L’FDA approva la prima opzione di trattamento per le riacutizzazioni della psoriasi pustolosa generalizzata negli adulti [Internet]. 2022. Disponibile su: www.boehringer-ingelheim.us/press-release/fda-approves-first-treatment-o…,(ultimo accesso 15.11.2022)
- Bachelez H, et al: Prova di spesolimab per la psoriasi pustolosa generalizzata. N Engl J Med 2021; 385(26): 2431-2440.
- Bugaut H, Aractingi S: Il ruolo principale dell’asse IL17/23 nella psoriasi supporta lo sviluppo di nuove terapie mirate. Front Immunol 2021;12:621956. www.frontiersin.org,(ultimo accesso 15 nov 2022).
- Drakos A, Vender RA: Revisione del panorama degli studi clinici nella psoriasi: un aggiornamento per i medici. Dermatol Ther (Heidelb) 2022, https://doi.org/10.1007/s13555-022-00840-9,(ultimo accesso 15 nov 2022).
- Keam SJ: Tapinarof crema 1%: prima approvazione. Farmaci 2022; 82(11): 1221-1228.
- Lebwohl MG, et al: Studi di fase 3 sulla crema tapinarof per la psoriasi a placche. N Engl J Med 2021; 385(24): 2219-2229.











