I tumori del sistema biliare, come il colangiocarcinoma o il carcinoma della cistifellea, sono tra le entità tumorali maligne rare, ma in costante aumento. A volte si può prendere in considerazione la chemioterapia combinata sistemica e locoregionale. In ogni caso, la terapia deve avvenire in un centro specializzato con un team multidisciplinare.
I tumori del sistema biliare, come il colangiocarcinoma o il carcinoma della cistifellea, sono tra le entità tumorali maligne rare, ma sono aumentati costantemente in Europa e in Svizzera negli ultimi due decenni. Questa entità tumorale si diffonde lungo il sistema dei dotti biliari e spesso viene diagnosticata correttamente solo in fase avanzata. Ecco perché il tasso di mortalità di questa malattia continua ad aumentare. Se c’è il minimo sospetto, il paziente deve essere indirizzato tempestivamente a un centro specializzato. La diagnosi precisa dei tumori biliari richiede un alto livello di competenza da parte di un team interdisciplinare. Un algoritmo di chiarificazione errato può trasformare un’opzione terapeutica potenzialmente curabile in una situazione palliativa o ritardare la terapia curativa. Il trattamento dei pazienti colpiti segue solitamente un concetto di terapia multimodale con resezione chirurgica, chemioterapia sistemica e, in casi selezionati, radioterapia. Il tipo di intervento dipende dalla localizzazione del tumore. In rari casi, il trapianto di fegato è una potenziale opzione di trattamento per i pazienti con colangiocarcinoma perilare. Questo articolo di revisione riporta i rischi e i fattori di rischio di questa grave malattia e spiega le moderne strategie di trattamento multimodale che hanno portato a un vantaggio decisivo in termini di sopravvivenza per i pazienti colpiti nell’ultimo decennio.
Come vengono classificati i tumori del dotto biliare?
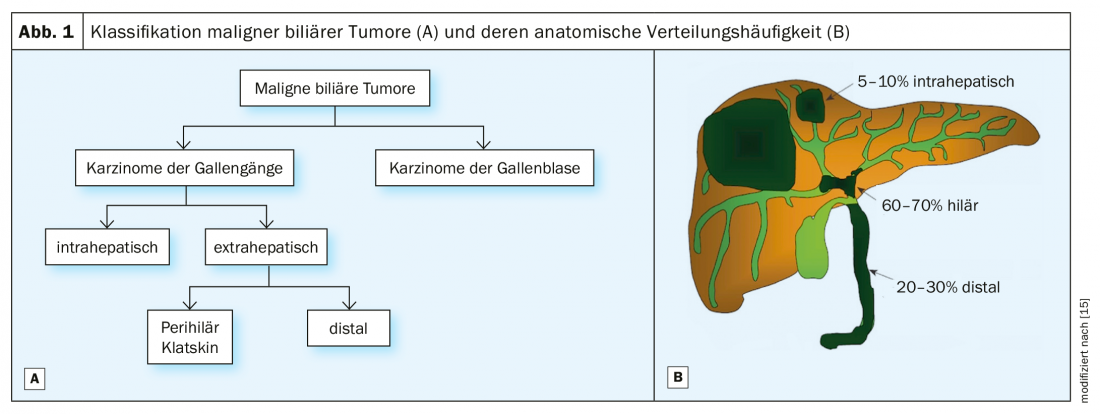
I tumori maligni delle vie biliari si dividono in carcinomi dei dotti biliari (colangiocarcinomi) e della cistifellea; i primi sono classificati in tumori intraepatici ed extraepatici in base alla loro localizzazione anatomica (Fig. 1) . I tumori extraepatici sono ulteriormente suddivisi in colangiocarcinomi perihiliari e distali. I tumori perilari, chiamati anche tumori di Klatskin, sono localizzati direttamente sul ramo del sistema dei dotti biliari extraepatici, mentre i colangiocarcinomi distali insorgono più distalmente nel dotto coledochale a livello della testa del pancreas [1]. La strategia di trattamento chirurgico si basa su questa classificazione anatomica del tumore.
Quanto è comune il colangiocarcinoma in Svizzera?
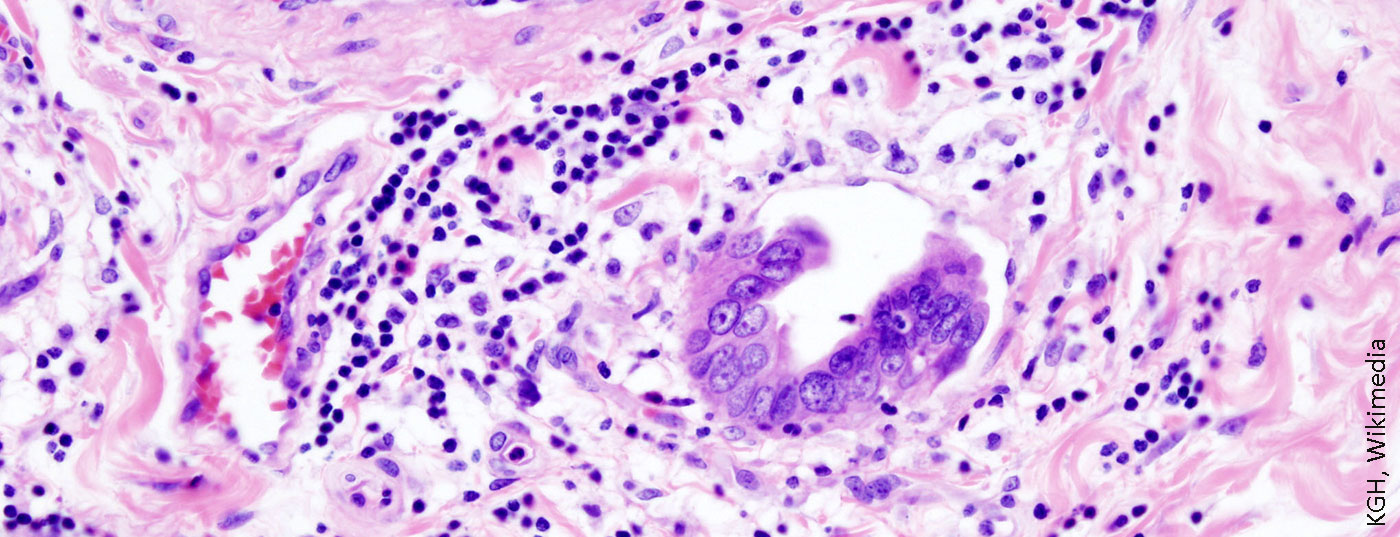
Il colangiocarcinoma è una malattia tumorale molto rara, maligna ed eterogenea che nasce dalle cellule epiteliali dei dotti biliari intra ed extraepatici. Questo tipo di cancro rappresenta il 3% di tutti i tumori maligni gastrointestinali [2]. Nel 2018, sono stati diagnosticati 334 nuovi casi in Svizzera. Tuttavia, nella maggior parte dei pazienti, questo tumore viene purtroppo rilevato in uno stadio localmente avanzato, motivo per cui la mortalità di questa malattia tumorale rimane elevata. Ogni anno, quasi la metà dei pazienti in Svizzera muore dopo la diagnosi (180 decessi all’anno; corrispondenti all’1% di tutti i decessi per cancro all’anno) [2].
Chi è colpito e quali sono i fattori di rischio noti?
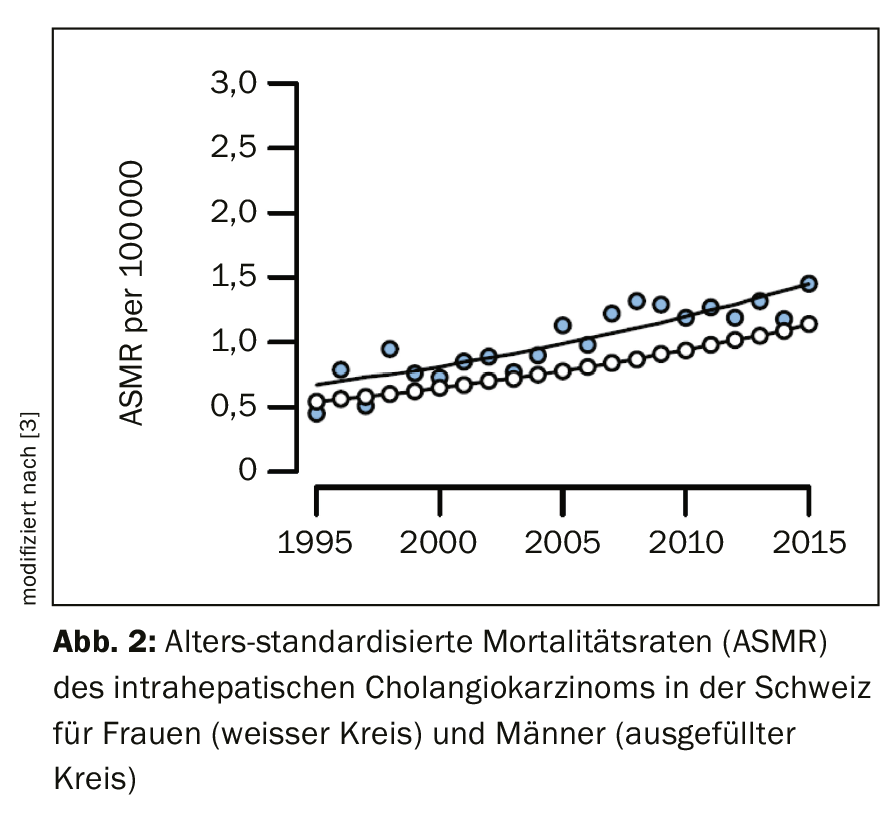
Per ragioni ancora poco chiare, l’incidenza del colangiocarcinoma intraepatico è aumentata in Svizzera e nel mondo negli ultimi due decenni (Fig. 2), mentre i tassi di colangiocarcinoma extraepatico sono diminuiti [3]. Di norma, l’incidenza del cancro delle vie biliari aumenta con l’età, raggiungendo il picco tra i 50 e i 70 anni [4,5]. I pazienti con diagnosi di colangite sclerosante primaria (PSC) o cisti coledochali note sviluppano il carcinoma quasi due decenni prima, in media. A differenza del cancro alla cistifellea, dove le donne sono significativamente più colpite, l’incidenza del colangiocarcinoma è leggermente superiore negli uomini [4]. Questo probabilmente riflette la maggiore incidenza della PSC negli uomini.
Sono noti diversi fattori di rischio per il colangiocarcinoma, anche se non è possibile identificare chiaramente un fattore di rischio specifico per molti pazienti [5]. In Europa, i principali fattori di rischio sono la colangite sclerosante primaria (PSC) e le cisti coledochali. Esiste un chiaro legame tra l’epatolitiasi intraepatica cronica, che porta alla colangite piogenica ricorrente, e il colangiocarcinoma. Le malattie croniche del fegato, come la cirrosi o l’epatite B e C, sono fattori di rischio noti, soprattutto per il colangiocarcinoma intraepatico [5,6]. Inoltre, almeno quattro malattie genetiche come la sindrome di Lynch, la sindrome di predisposizione al tumore associata a BRCA-1 (BAP1), la fibrosi cistica e la papillomatosi biliare sembrano aumentare il rischio di colangiocarcinoma [6].
Quali chiarimenti moderni sono necessari?
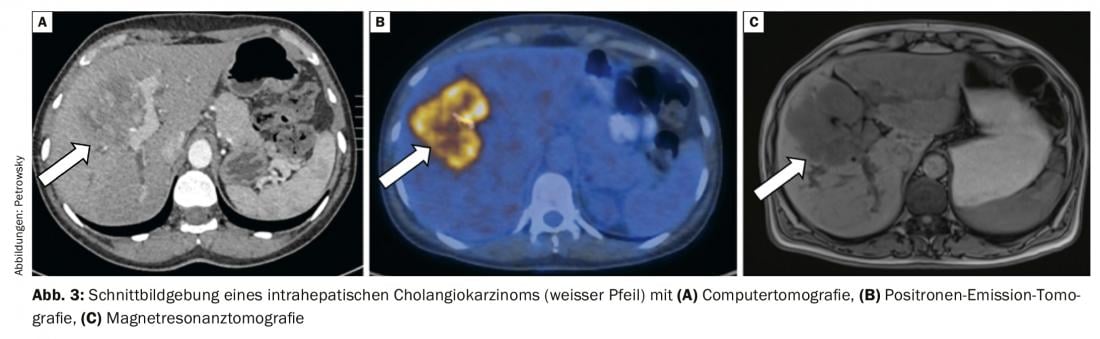
La diagnosi dei colangiocarcinomi di solito segue algoritmi diagnostici complessi e spesso richiede un’infrastruttura con una marcata esperienza nella gastroenterologia endoscopica e nella radiologia interventistica. Se si sospetta che un paziente abbia una neoplasia dei dotti biliari, il primo passo è la classificazione topografica. La colangiopancreaticografia a risonanza magnetica (MRCP) è il miglior metodo non invasivo per l’imaging anatomico spaziale del tumore e, in particolare, dei dotti biliari [7]. Oggi è quasi uguale in sensibilità e specificità alla più invasiva colangiografia retrograda endoscopica (ERC) e alla colangiografia transepatica percutanea (PTC) [7]. La risonanza magnetica con MRCP consente di valutare la resecabilità locale e, allo stesso tempo, serve come ‘pianificatore di percorso’ per qualsiasi drenaggio endoscopico o percutaneo che potrebbe essere necessario. La tomografia computerizzata mostra una maggiore sensibilità se il tumore si infiltra nelle arterie e nelle vene per la valutazione prima della resezione pianificata (Fig. 3) [7].
Nel caso di un ispessimento del dotto biliare a lunga estensione, si deve considerare anche una colangiopatia autoimmune come diagnosi differenziale. In questo caso, sono utili la determinazione delle IgG4 nel siero e un’endosonografia (EUS) per valutare il dotto biliare [8]. Se i linfonodi retroperitoneali e perihiliari sono cospicui, si deve eseguire anche un EUS per determinare la dignità dei linfonodi accessibili mediante un’aspirazione con ago sottile.
La PET/TC è particolarmente preziosa per un’ulteriore stadiazione, soprattutto per la diagnosi di metastasi a distanza, che spesso non vengono sempre diagnosticate con la normale diagnostica per immagini, come la risonanza magnetica o la TAC. La PET/CT fa parte del work-up standardizzato nella nostra clinica e influisce in modo significativo sulla selezione della terapia adeguata (Fig. 3) [7,9].
Dopo la diagnostica per immagini, tutti i pazienti, senza eccezioni, vengono presentati e discussi nel nostro comitato tumori interdisciplinare. In particolare, questo è essenziale prima della diagnostica invasiva come l’ERCP o la PTCD, poiché qualsiasi manipolazione dei dotti biliari rende difficile la valutazione dell’imaging a fette.
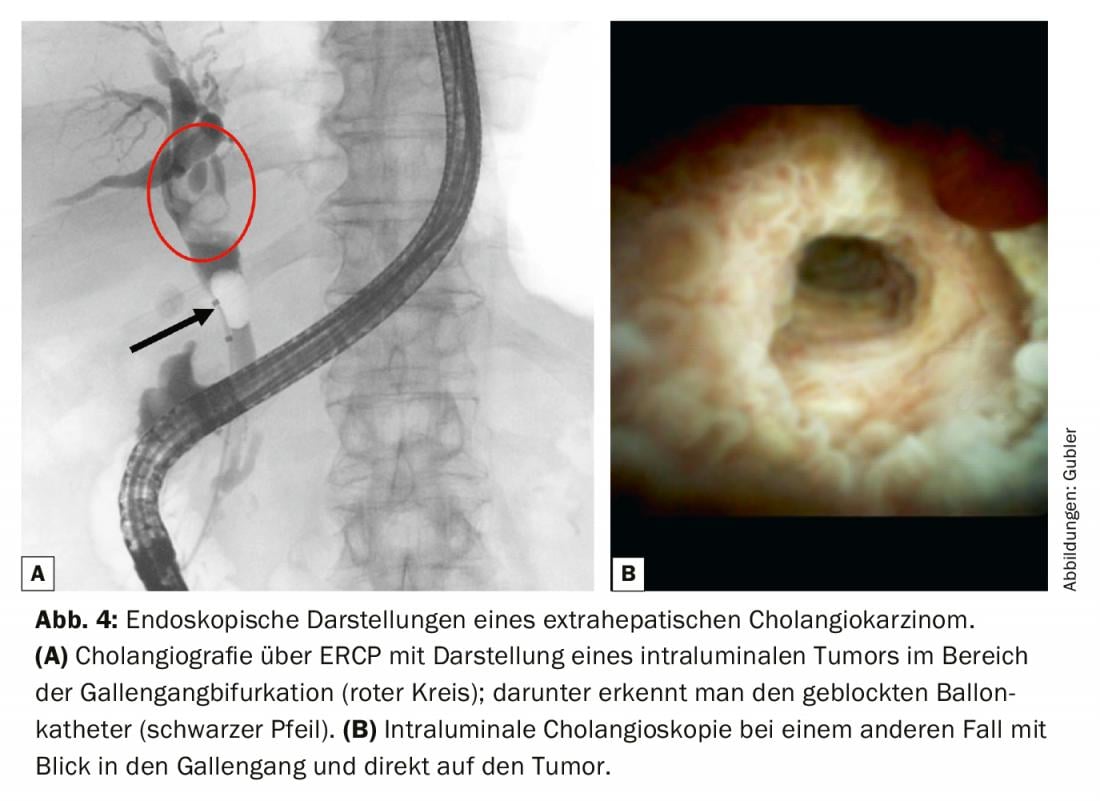
Per i tumori resecabili nel fegato o nell’ilo epatico, un PTCD viene preferibilmente inserito prima dell’intervento sul fegato parziale da conservare, per decomprimere il sistema dei dotti biliari [10]. Nella diagnosi istologica dei colangiocarcinomi perihiliari e distali, l’ERCP [11] è fermamente stabilita, per cui il drenaggio deve essere effettuato anche quando i dotti biliari sono pieni, perché altrimenti c’è il rischio di colangite con potenziali ascessi epatici. Il passo iniziale più importante è ottenere un colangiogramma di alta qualità con citologia a pennello focalizzata (Fig. 4). Di solito viene combinata con una biopsia intraluminale per aumentare la sensibilità. Nel caso, non raro, di diagnosi tissutale negativa, in un secondo tempo si può eseguire una colangioscopia perorale (POCS) con mappatura del dotto biliare sotto visione. In questo caso, è necessario raffigurare la biforcazione del dotto biliare, nonché il dotto biliare destro e sinistro, al fine di utilizzare i risultati della mappatura per la pianificazione chirurgica con la stima dell’estensione della resezione preoperatoria [12]. La laparoscopia di stadiazione può essere utile per individuare piccole metastasi e carcinomatosi peritoneali che non sono visibili alla TAC o alla risonanza magnetica [13].
Cosa si deve considerare nella resecabilità chirurgica?
Per la valutazione della resezione chirurgica, è fondamentale la posizione della lesione tumorale, compresa la sua relazione con le strutture vascolari e biliari, nonché il volume e la qualità del parenchima epatico rimasto dopo la resezione del tumore (tab. 1).
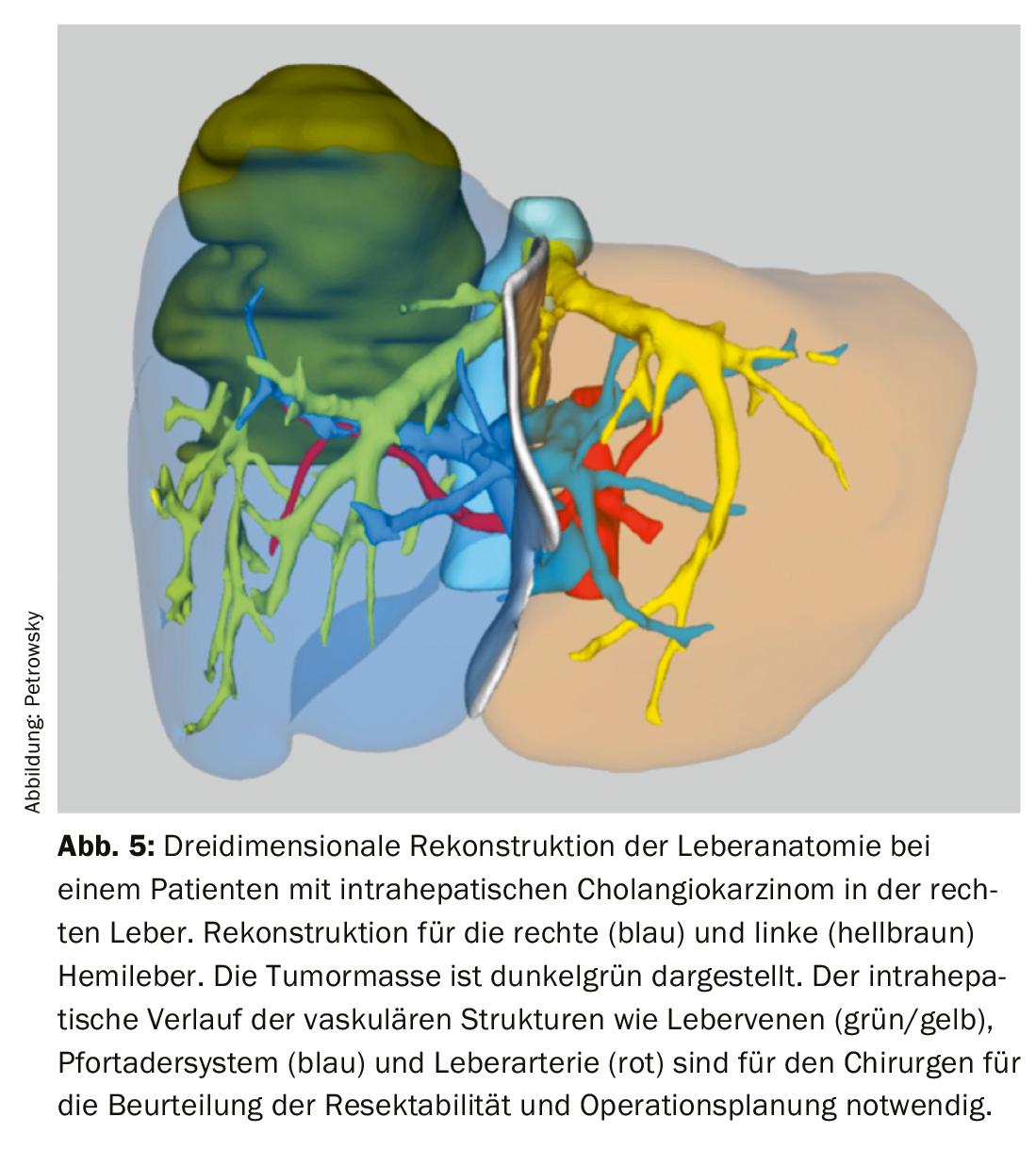
Le ricostruzioni di immagini tridimensionali dell’anatomia vascolare e biliare del fegato sono oggi disponibili nella maggior parte dei centri per una valutazione precisa della resecabilità tecnica e una migliore pianificazione chirurgica (Fig. 5). La diagnosi istologica preoperatoria del tumore è sempre ricercata prima dell’intervento chirurgico, ma non è sempre possibile nel caso del colangiocarcinoma perilare. In questi casi, una massa sospetta sull’imaging trasversale, combinata con dati clinici appropriati, è sufficiente per sospettare una malignità e indicare la resezione.
Il trattamento chirurgico rimane l’unica modalità di trattamento curativo, ma solo se la resezione può essere eseguita en-bloc con margini resecati liberi da tumore (istologicamente R0) [14]. Nel valutare la resecabilità, si devono prendere in considerazione le dimensioni del tumore, le lesioni satelliti, il coinvolgimento vascolare, le metastasi linfonodali e le metastasi a distanza. Sebbene le dimensioni del tumore siano state controverse negli ultimi anni, sono state reintrodotte nel sistema di stadiazione dell’ottava edizione dell’AJCC [4]. L’aumento delle dimensioni del tumore è associato a una maggiore incidenza di metastasi satellitari, metastasi linfonodali, tumori vascolari e scarsamente differenziati e quindi a una biologia complessiva del tumore peggiore [10,15].
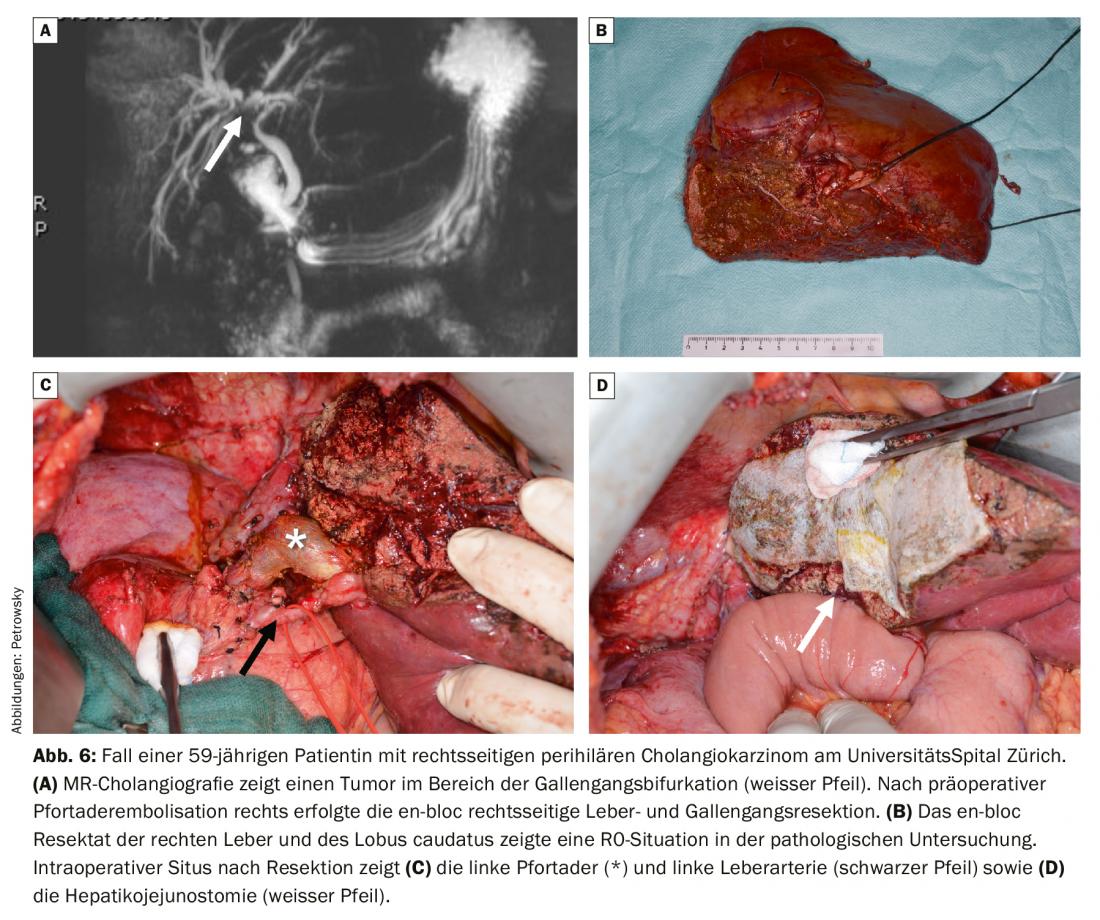
La procedura chirurgica primaria dipende principalmente dalla posizione del tumore. Ad esempio, la classica resezione della testa del pancreas (Whipple) è adatta per i colangiocarcinomi localizzati nel dotto biliare distale. La resezione epatica dei colangiocarcinomi perihiliari è orientata verso il lato con il coinvolgimento dominante del tumore. Gli interventi per i tumori dei dotti biliari ilari sono molto complessi e di solito richiedono la resezione dei dotti biliari extraepatici e l’emiepatectomia estesa, compresa la resezione del lobo caudato (Fig. 6) [15]. In caso di infiltrazione tumorale della biforcazione portale, è necessaria la resezione della vena porta con ricostruzione primaria [16]. In questi interventi vengono sempre eseguiti una volumetria e test funzionali della funzione epatica. Spesso questi interventi di chirurgia epatica molto estesi richiedono l’embolizzazione preoperatoria della vena porta per l’induzione dell’ipertrofia, quando il fegato rimanente è troppo piccolo. In alcuni casi, tuttavia, il tumore provoca l’autoipertrofia attraverso l’occlusione tumorale di un ramo della vena porta, che in questa situazione non richiede più l’embolizzazione preoperatoria della vena porta. Nel nostro centro epatobiliare, dreniamo anche il lato rimanente del fegato, di solito utilizzando un PTCD (colangiodrenaggio transepatico percutaneo), che può poi essere utilizzato come stecca interna e struttura guida durante l’intervento. Questi interventi altamente specializzati devono essere eseguiti solo dopo un’attenta pianificazione presso un centro specializzato.
I colangiocarcinomi intraepatici si concentrano sulla resezione del lato interessato del fegato. Le procedure di resezione epatica necessarie non sono diverse da quelle per altri tumori epatici, come le metastasi epatiche del colon-retto. A seconda delle dimensioni e della localizzazione del tumore, offriamo ai nostri pazienti l’intero spettro di tecniche chirurgiche, dall’asportazione minimamente invasiva del tumore assistita da robot alla chirurgia epatica più complessa. Un prerequisito importante è un volume di residui epatici sufficiente per quantità e qualità [15]. Se, a causa delle dimensioni del tumore, l’estensione della resezione non consente un volume sufficiente del fegato rimanente, si può eseguire un’embolizzazione della vena porta per l’ipertofia del volume preoperatoria o, in casi selezionati, una procedura di chirurgia epatica in due fasi (chirurgia ALPPS) [17]. Nella procedura ALPPS, un ramo della vena porta della metà del fegato circondata dal tumore viene chiuso in un primo intervento e il parenchima epatico tra le metà del fegato viene tagliato. Questo innesca una crescita rapida e sostanziale su quel lato del fegato con una vena porta ancora aperta. Dopo 1-2 settimane, il tumore può essere facilmente asportato con un secondo intervento, lasciando una quantità sufficiente di tessuto epatico. Questa strategia raggiunge tassi di resezione R0 superiori all’85%, ma dovrebbe essere riservata ai casi con carico tumorale unilaterale del fegato e crescita adeguata della metà del fegato libera dal tumore dopo l’embolizzazione della vena porta [17].
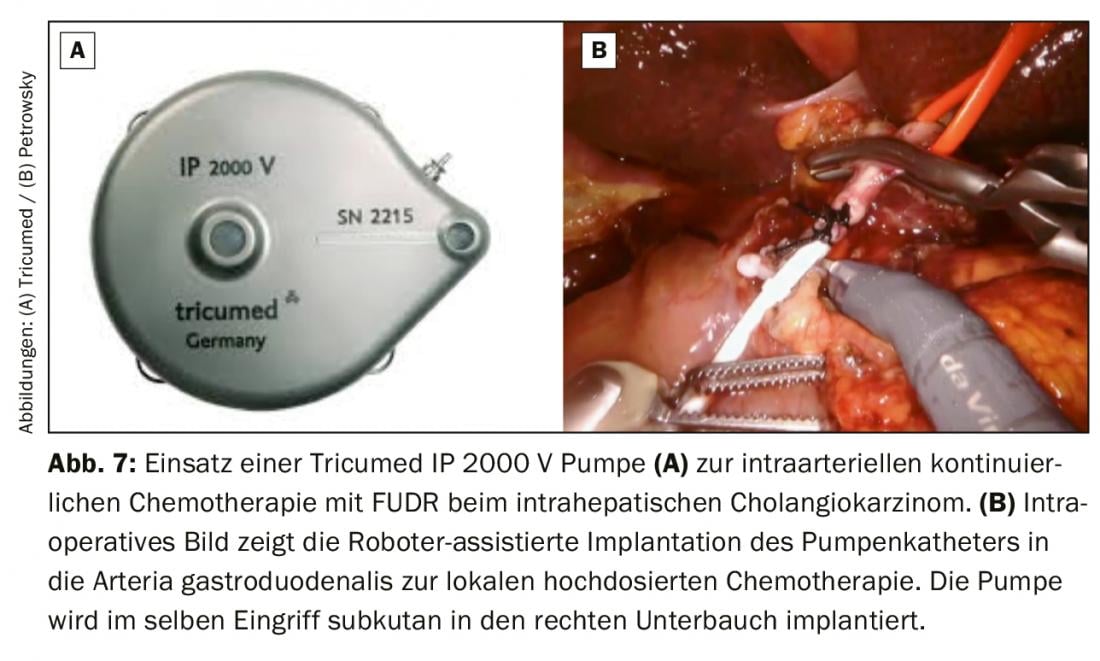
Per i colangiocarcinomi intraepatici inizialmente non resecabili, si può ricorrere alla chemioterapia combinata di conversione sistemica e intra-arteriosa. In questa procedura, la chemioterapia ad alto dosaggio viene somministrata in modo continuo direttamente nell’arteria gastroduodenale tramite una pompa. La terapia intra-arteriosa può raggiungere livelli di farmaco significativamente più elevati nel fegato rispetto a quella sistemica. Il tasso di risposta di questa chemioterapia locoregionale intensificata, soprattutto con floxuridina (FUDR), è del 60% e prolunga significativamente la sopravvivenza dei pazienti anche in situazioni palliative [18]. Nel nostro centro, offriamo questa terapia ai pazienti con situazioni palliative e potenzialmente curative nel colangiocarcinoma intraepatico. Di solito impiantiamo la pompa sottocute nell’area dell’addome inferiore destro e inseriamo il catetere della pompa in modo minimamente invasivo con il sistema robotico da Vinci (Fig. 7). Questa procedura chirurgica minimamente invasiva è molto delicata per i pazienti e garantisce un rapido recupero post-operatorio e quindi un rapido inizio della chemioterapia dopo l’impianto della pompa.
Il trapianto di fegato è un’opzione di trattamento?
Sebbene il trapianto di fegato offra tecnicamente la migliore possibilità di resezione R0, l’immunosoppressione post-operatoria comporta un rischio elevato di recidiva del tumore. Finora, i criteri stabiliti per il trapianto di fegato esistono solo per il colangiocarcinoma perilare. Questi sono definiti da un tumore con dimensioni massime di 3 cm senza evidenza di metastasi locoregionali linfonodali e a distanza. I pazienti con o senza PSC che soddisfano questi criteri e non sono primariamente resecabili dovrebbero essere valutati per il trapianto di fegato con una precedente radiochemioterapia neoadiuvante. Si possono raggiungere alti tassi di sopravvivenza del 60-70% a 5 anni dal trapianto di fegato [19,20]. I criteri di indicazione per il trapianto di fegato per il colangiocarcinoma intraepatico sono meno stabiliti, anche se alcuni studi recenti riportano buoni dati di sopravvivenza dopo il trapianto in pazienti selezionati [21,22].
Chemioterapia e immunoterapia – Cosa è consolidato e cosa è nuovo?
Nella malattia avanzata o metastatica, la chemioterapia sistemica rimane lo standard di cura per l’adenocarcinoma delle vie biliari. Per la chemioterapia, finora non è stata fatta alcuna distinzione tra i singoli sottogruppi anatomici. Lo standard di cura nella terapia di prima linea è la combinazione di gemcitabina e cisplatino, basata sui dati dello studio ABC02 [23], che ha dimostrato la superiorità di questo protocollo rispetto alla gemcitabina mono. Per i pazienti anziani e quelli con performance status ridotto, sono più adatti protocolli più blandi, probabilmente la monoterapia con gemcitabina.
Finora ci sono pochi studi sulla terapia di seconda linea. Solo lo studio ABC0624 ha dimostrato un beneficio di sopravvivenza per i pazienti trattati con FOLFOX in seconda linea rispetto all’osservazione attiva. I protocolli alternativi di terapia di seconda linea che non sono stati convalidati da studi randomizzati più ampi, ma sono comuni nella pratica, sono FOLFIRI e 5-FU/capecitabina.
Tuttavia, la chemioterapia sistemica non viene utilizzata solo per la malattia non resecabile o metastatica, ma anche per il trattamento di follow-up dopo l’intervento chirurgico. In questo caso, lo studio BILCAP è stato in grado di dimostrare un piccolo ma significativo beneficio di sopravvivenza per il post-trattamento con capecitabina [25]. I risultati dello studio ACTICCA1, che confronta la capecitabina mono con la combinazione gemcitabina/cisplatino attivata nel trattamento post-resezione, sono molto attesi. Altre sperimentazioni stanno studiando il ruolo della terapia neoadiuvante, anche nel carcinoma incisionale della cistifellea (AIO-HEP-0118, studio GAIN).
Attualmente, la risposta al trattamento viene valutata principalmente attraverso l’imaging trasversale. I parametri di progressione biochimica sono principalmente i marcatori tumorali consolidati CEA e CA19-9. Estremamente interessanti e di importanza clinica in rapido aumento sono i sottogruppi molecolari dei tumori biliari. A seconda della localizzazione primaria, nei colangiocarcinomi si riscontra un’intera gamma di diversi driver oncogenici con frequenza variabile. Esistono nuove sostanze a bersaglio molecolare contro molti di questi fattori, alcune delle quali sono già in fase avanzata di sviluppo clinico e la cui approvazione è prevista a breve. Gli inibitori del recettore del fattore di crescita dei fibroblasti (FGFR), che mostrano un’eccellente efficacia nei carcinomi colangiocellulari con alterazione oncogenica FGFR (soprattutto fusioni FGFR2, ma anche amplificazioni elevate) (ad esempio, pemigatinib o TAS-120), sono di primaria importanza. Fino al 20% dei colangiocarcinomi intraepatici presenta tali alterazioni FGFR, mentre sono rare nelle localizzazioni tumorali extraepatiche. Le mutazioni di IDH1 e IDH2 sono un altro bersaglio terapeutico. Questi sono comuni anche nei colangiocarcinomi intraepatici e i primi studi randomizzati mostrano un’efficacia [26]. Altri bersagli molecolari sono BRAF-V600E, le alterazioni BRAF di classe II e III e HER2. Un gruppo più piccolo di colangiocarcinomi presenta instabilità dei microsatelliti (MSI-H) e risponde di conseguenza bene al blocco del checkpoint immunitario [27]. Le combinazioni di terapie a bersaglio molecolare e immunoterapie sono attualmente oggetto di studi (ad esempio, pembrolizumab più lenvatinib).
Quando la radiazione stereotassica è un’opzione?
Anche se la terapia sistemica è stata in primo piano nel trattamento dei carcinomi del dotto biliare non resecabili localmente avanzati, la radioterapia dei risultati locali ha il suo ruolo nel controllo locale del tumore e quindi nell’evitare o ridurre i sintomi o le complicanze. I nuovi sviluppi tecnici, come l’irradiazione stereotassica, consentono di coprire l’area tumorale (Fig. 8 ) in poche sedute (di solito da 5 a 8), con un basso profilo di effetti collaterali e senza interferenze o ritardi della terapia sistemica [28–30].
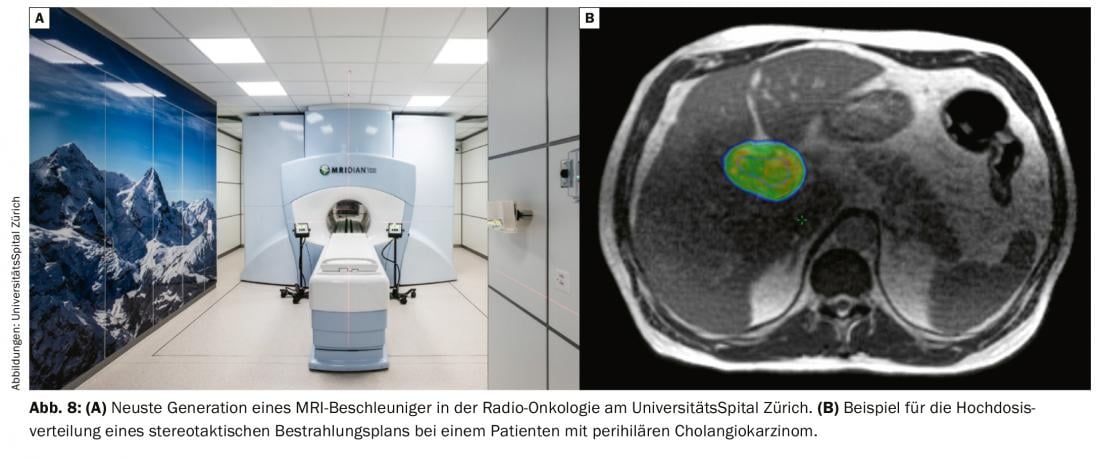
L’ultimo sviluppo in questo campo, la cosiddetta irradiazione guidata dalla risonanza magnetica, è finora disponibile solo in Svizzera, presso l’Ospedale Universitario di Zurigo, sotto forma di un acceleratore ibrido di risonanza magnetica. (Fig. 7). Questa tecnologia consente di individuare in modo ottimale il tumore con un migliore risparmio degli organi a rischio, grazie a un migliore contrasto dei tessuti molli, all’imaging in tempo reale durante l’irradiazione e alla possibilità di ottimizzare il piano giornaliero in base all’anatomia quotidiana degli organi adiacenti.
In un ampio studio retrospettivo, è stato osservato un vantaggio assoluto di sopravvivenza anche aggiungendo la radioterapia alla terapia di sistema [28]. Pertanto, nei pazienti con carcinoma del dotto biliare non resecabile che non presentano metastasi nel corso della terapia sistemica, la radioterapia locale aggiuntiva deve sempre essere discussa su base interdisciplinare.
In quali strutture è integrato il trattamento del colangiocarcinoma presso l’Ospedale Universitario?
Il trattamento chirurgico dei colangiocarcinomi, mediante resezione del fegato o del pancreas, fa parte della Medicina altamente specializzata (HSM) in Svizzera. All’Ospedale Universitario, i colangiocarcinomi sono trattati da specialisti altamente qualificati in collaborazione con tutti i reparti medici. Questi includono la chirurgia del fegato e del pancreas, l’oncologia medica, la gastroenterologia endoscopica, la radiologia interventistica e la radioterapia. L’Ospedale Universitario di Zurigo offre le opzioni di trattamento più recenti ed efficaci per questi tumori ed è un centro certificato per il cancro al fegato, che comprende anche i colangiocarcinomi. I trattamenti di tutti i pazienti con diagnosi di colangiocarcinoma sono integrati nelle strutture del Centro per i tumori epatici del Comprehensive Cancer Center di Zurigo (CCCZ) e del Centro svizzero per le malattie del fegato, del pancreas e delle vie biliari (Swiss HPB Center). I pazienti vengono discussi settimanalmente in un comitato tumori interdisciplinare, che si concentra sui tumori del fegato, del pancreas e dei dotti biliari. Non solo vengono determinate le ulteriori diagnosi necessarie e le possibili strategie di trattamento al momento della diagnosi iniziale, ma vengono anche discussi i risultati post-terapeutici e gli intervalli di controllo necessari o le terapie secondarie. Inoltre, i nostri pazienti hanno l’opportunità di partecipare agli studi scientifici condotti presso l’Ospedale Universitario e possono beneficiare delle innovazioni.
Messaggi da portare a casa
- I colangiocarcinomi intraepatici mostrano un aumento a livello mondiale, mentre si osserva una tendenza alla diminuzione per i colangiocarcinomi extraepatici.
- Se si sospetta un tumore del dotto biliare, il paziente deve essere indirizzato a un centro specializzato il prima possibile; il coinvolgimento di un team multidisciplinare e di una commissione tumori è fondamentale.
- Le resezioni tumorali dei colangiocarcinomi fanno parte della medicina altamente specializzata in Svizzera e spesso richiedono procedure interventistiche endoscopiche e radiologiche per la preparazione preoperatoria.
- Anche i colangiocarcinomi perilari (tumori di Klatskin), che si localizzano principalmente alla biforcazione dei dotti biliari, possono essere curati con un trapianto di fegato in casi selezionati e con l’applicazione di un concetto terapeutico multidisciplinare.
- Per i colangiocarcinomi intraepatici, si può prendere in considerazione la chemioterapia combinata sistemica e locoregionale; i tassi di risposta sono superiori al 60%.
- La patologia molecolare deve essere sempre presa in considerazione, soprattutto nel colangiocarcinoma intraepatico, per identificare i driver oncogenici che consentono una terapia molecolarmente mirata.
Letteratura:
- Malhi H, Gores GJ: Colangiocarcinoma: progressi moderni nella comprensione di una vecchia malattia mortale. J Hepatol 45, 856-867, doi:10.1016/j.jhep.2006.09.001 (2006).
- Svizzera K: Cancro in Svizzera: cifre chiave. (2018).
- Bertuccio P, et al: Tendenze globali della mortalità per colangiocarcinoma intraepatico ed extraepatico. J Hepatol 71, 104-114, doi:10.1016/j.jhep.2019.03.013 (2019).
- Mazzaferro V, Gorgen A, Roayaie S, et al: Resezione epatica e trapianto per il colangiocarcinoma intraepatico. J Hepatol 72, 364-377, doi:10.1016/j.jhep.2019.11.020 (2020).
- Dervin D: Edmond: esiste un gioco malato? Psychoanal Rev 73, 111-119 (1986).
- Chapman RW: Fattori di rischio per la carcinogenesi delle vie biliari. Ann Oncol 10 Suppl 4, 308-311 (1999).
- Olthof SC, et al: Imaging del colangiocarcinoma. Visc Med 32, 402-410, doi:10.1159/000453009 (2016).
- Strongin A, Singh H, Eloubeidi MA, Siddiqui AA: Ruolo dell’ecografia endoscopica nella valutazione del colangiocarcinoma extraepatico. Endosc Ultrasound 2, 71-76, doi:10.4103/2303-9027.117690 (2013).
- Petrowsky H, et al: Impatto della tomografia ad emissione di positroni e della tomografia computerizzata integrate sulla stadiazione e sulla gestione del cancro della cistifellea e del colangiocarcinoma. J Hepatol 45, 43-50, doi:10.1016/j.jhep.2006.03.009 (2006).
- Rassam F, et al: Work-up moderno e resezione estesa nel colangiocarcinoma perilare: l’esperienza AMC. Langenbecks Arch Surg 403, 289-307, doi:10.1007/s00423-018-1649-2 (2018).
- Abu-Hamda EM, Baron TH: Gestione endoscopica del colangiocarcinoma. Semin Liver Dis 24, 165-175, doi:10.1055/s-2004-828893 (2004).
- Ishida Y, Itoi T, Okabe Y: La colangioscopia a immagini può distinguere le lesioni benigne da quelle maligne nel dotto biliare? Best Pract Res Clin Gastroenterol 29, 611-625, doi:10.1016/j.bpg.2015.05.007 (2015).
- Bird N, et al: Ruolo della laparoscopia di stadiazione nella stratificazione dei pazienti con colangiocarcinoma perilare. Br J Surg 104, 418-425, doi:10.1002/bjs.10399 (2017).
- Matull WR, et al: La resezione R0 ma non R1/R2 è associata a una migliore sopravvivenza rispetto alla terapia fotodinamica palliativa nel cancro delle vie biliari. Liver Int 31, 99-107, doi:10.1111/j.1478-3231.2010.02345.x (2011).
- Petrowsky H, Hong JC: L’attuale gestione chirurgica del colangiocarcinoma ilare e intraepatico: il ruolo della resezione e del trapianto ortotopico di fegato. Transplant Proc 41, 4023-4035, doi:10.1016/j.transproceed.2009.11.001 (2009).
- Hemming AW, Mekeel K, Khanna A, et al: Resezione della vena porta nella gestione del colangiocarcinoma ilare. J Am Coll Surg 212, 604-613; discussione 613-606, doi:10.1016/j.jamcollsurg.2010.12.028 (2011).
- Li J, et al: ALPPS per il colangiocarcinoma intraepatico localmente avanzato: la chirurgia aggressiva ha portato al beneficio oncologico? Uno studio multicentrico internazionale. Ann Surg Oncol, doi:10.1245/s10434-019-08192-z (2020).
- Konstantinidis IT, et al: Colangiocarcinoma intraepatico non resecabile: la chemioterapia sistemica più infusione arteriosa epatica è associata a una sopravvivenza più lunga rispetto alla sola chemioterapia sistemica. Cancer 122, 758-765, doi:10.1002/cncr.29824 (2016).
- Darwish Murad S, et al: Efficacia della chemioradioterapia neoadiuvante, seguita da trapianto di fegato, per il colangiocarcinoma perihilare in 12 centri statunitensi. Gastroenterologia 143, 88-98 e83; quiz e14, doi:10.1053/j.gastro.2012.04.008 (2012).
- Ethun CG, et al: Trapianto rispetto alla resezione per il colangiocarcinoma ilare: un argomento per spostare i paradigmi di trattamento per la malattia resecabile. Ann Surg 267, 797-805, doi:10.1097/SLA.00000000002574 (2018).
- Sapisochin G, et al: Trapianto di fegato per colangiocarcinoma intraepatico “molto precoce”: studio retrospettivo internazionale a supporto di una valutazione prospettica. Epatologia 64, 1178-1188, doi:10.1002/hep.28744 (2016).
- Lunsford KE, et al: Trapianto di fegato per il colangiocarcinoma intraepatico localmente avanzato trattato con terapia neoadiuvante: una serie di casi prospettici. Lancet Gastroenterol Hepatol 3, 337-348, doi:10.1016/S2468-1253(18)30045-1 (2018).
- Valle J, et al: Cisplatino più gemcitabina rispetto alla gemcitabina per il tumore delle vie biliari. N Engl J Med 362, 1273-1281, doi:10.1056/NEJMoa0908721 (2010).
- ABC-06 | Studio randomizzato di fase III, m.-c., in aperto, di controllo attivo dei sintomi (ASC) da solo o ASC con chemioterapia a base di oxaliplatino / 5-FU (ASC+mFOLFOX)
- Lamarca A, et al: Standard attuali e prospettive future nel trattamento adiuvante dei tumori del tratto biliare. Cancer Treat Rev 84, 101936, doi:10.1016/j.ctrv.2019.101936 (2019).
- Abou-Alfa GK, Javle TMM, Kelley RK, et al: Studio globale, di fase 3, randomizzato, in doppio cieco, di ivosidenib (IVO) vs placebo in pazienti con colangiocarcinoma avanzato (CC) con mutazione dell’isocitrato deidrogenasi 1 (IDH1). Congresso ESMO (2019).
- Le DT, et al: La carenza di Mismatch Repair predice la risposta dei tumori solidi al blocco PD-1. Science 357, 409-413, doi:10.1126/science.aan6733 (2017).
- Jackson MW, et al: Selezione del trattamento e risultati di sopravvivenza con e senza radiazioni per il colangiocarcinoma intraepatico non resecabile e localizzato. Cancer J 22, 237-242, doi:10.1097/PPO.00000000000213 (2016).
- Gkika E, et al: Radioterapia stereotassica del corpo (SBRT) per il colangiocarcinoma intraepatico ed extraepatico localmente avanzato. BMC Cancer 17, 781, doi:10.1186/s12885-017-3788-1 (2017).
- Brunner TB, et al.: Dose di radioterapia stereotassica corporea e suo impatto sul controllo locale e sulla sopravvivenza globale dei pazienti con colangiocarcinoma intraepatico ed extraepatico localmente avanzato. Radiother Oncol 132, 42-47, doi:10.1016/j.radonc.2018.11.015 (2019).
InFo ONCOLOGIA & EMATOLOGIA 2020; 8(1): 9-16