L’anemia preoperatoria è un fattore predittivo indipendente di un aumento del rischio di infezione e tromboembolismo e di un aumento della mortalità. Le trasfusioni di sangue allogenico, da parte loro, contribuiscono ulteriormente al peggioramento degli esiti attraverso rischi aspecifici e specifici. Un approccio all’anemia basato su un algoritmo è utile. In base al volume delle cellule EC (MCV) e ai reticolociti, è possibile classificare e trattare l’anemia da lieve a moderata nel contesto perioperatorio. L’anemia grave deve essere valutata e gestita da un esperto. In caso di perdita ematica elevata prevista nel corso di un intervento chirurgico maggiore, il fabbisogno di ferro può essere stimato e sostituito già prima dell’intervento. Secondo i dati attuali, l’anemia grave è considerata una controindicazione all’intervento chirurgico elettivo.
La medicina basata sull’evidenza è ormai ampiamente accettata che l’anemia è associata a molteplici rischi [1]: L’anemia preoperatoria è un fattore predittivo indipendente di aumento del rischio di infezione e di tromboembolismo (TE) [2], di aumento della mortalità e di prolungamento dell’ospedalizzazione [3]. L’anemia è quindi un fattore di rischio serio e rilevante per il risultato della guarigione o l’esito dei pazienti sottoposti a chirurgia elettiva e deve essere trattata [4]. Nonostante la chiara letteratura, il problema dell’anemia pre o perioperatoria è ancora oggi molto spesso “curato” con la somministrazione di trasfusioni di sangue allogenico, con tutti i rischi aggiuntivi, specifici e non, ad esso associati [5].
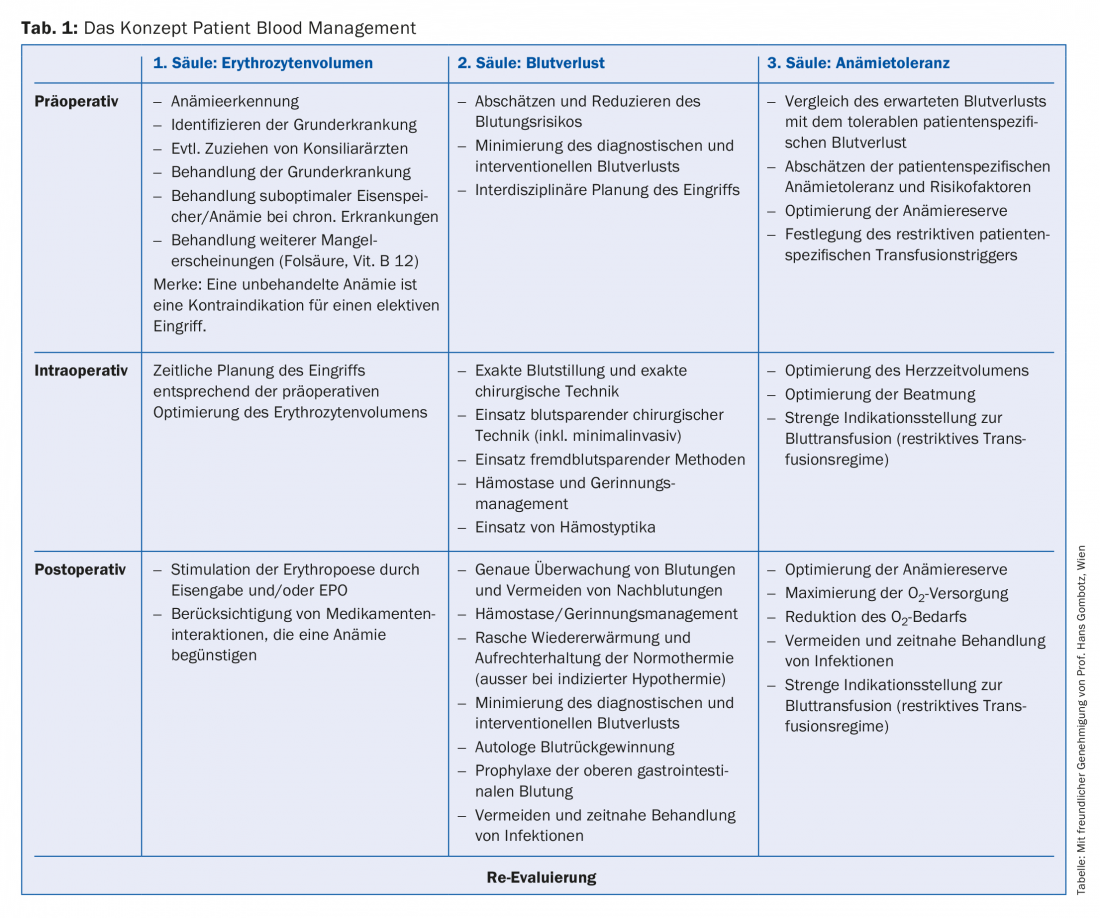
Il concetto clinico di Patient Blood Management (PBM) è la risposta centrata sul paziente, interdisciplinare e basata sull’evidenza, come approccio moderno alla terapia dell’anemia, spostando l’attenzione dalla trasfusione di sangue all’uso delle risorse proprie del paziente. Il PBM si basa su tre pilastri (Tabella 1), di cui il primo pilastro in particolare consiste nell’ottimizzare il volume dei globuli rossi nel contesto pre e perioperatorio. Ciò comporta l’identificazione dell’anemia come sintomo, la diagnosi della malattia di base e, per quanto possibile, il trattamento. L’anemia non trattata è ora considerata una controindicazione all’intervento chirurgico elettivo.
Chiarimenti e algoritmo terapeutico
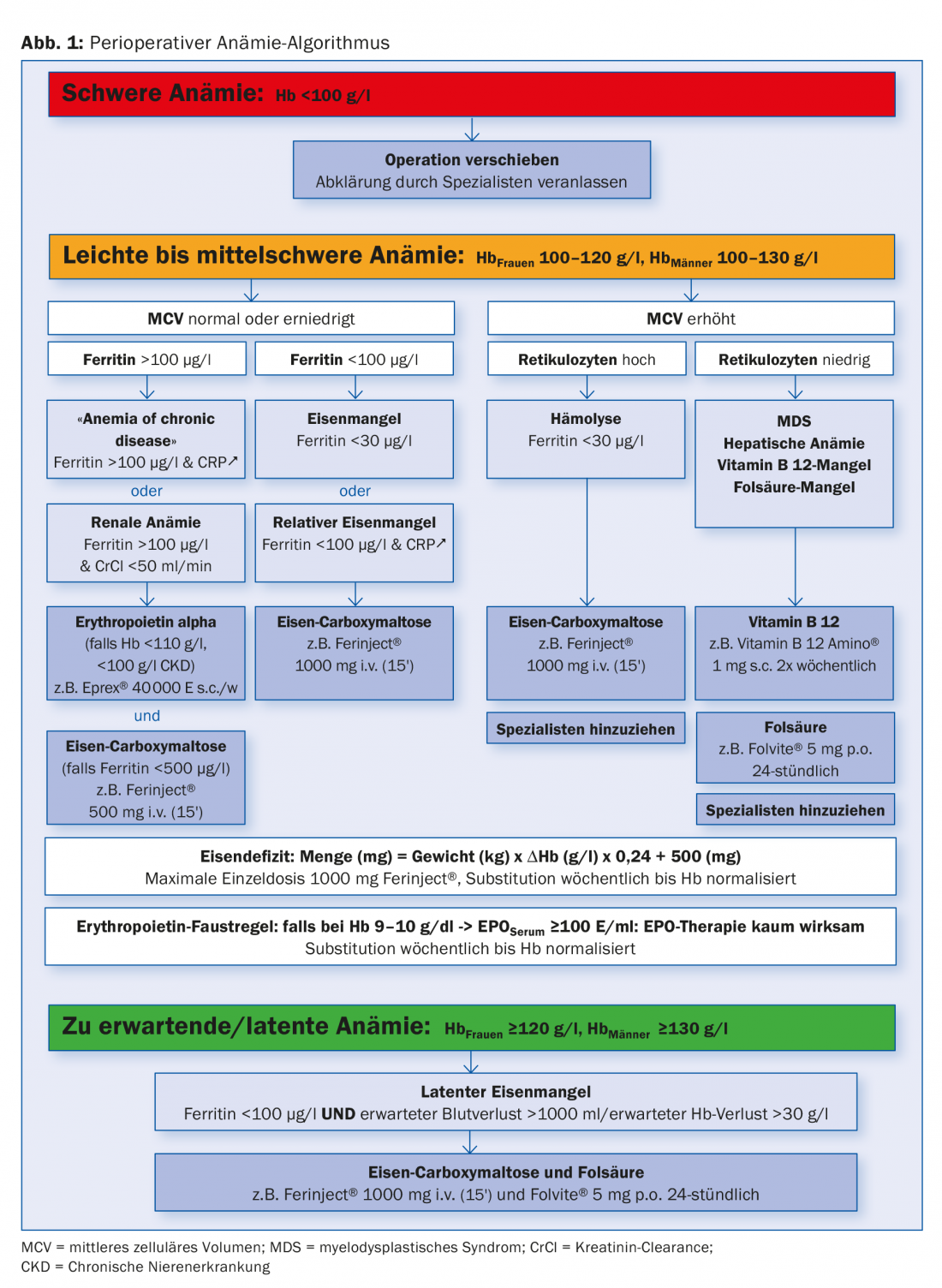
Un algoritmo è enormemente utile in questa situazione, perché può prendere in considerazione le caratteristiche specifiche del sito del medico curante, come l’accessibilità degli specialisti e la disponibilità di esami di laboratorio complementari. La maggior parte delle anemie preoperatorie può essere diagnosticata, classificata e trattata in una popolazione standard utilizzando un algoritmo diagnostico e terapeutico (Fig. 1 e Tab. 2). Di conseguenza, i pazienti arrivano in tempo e preparati in modo ottimale per l’intervento chirurgico previsto.
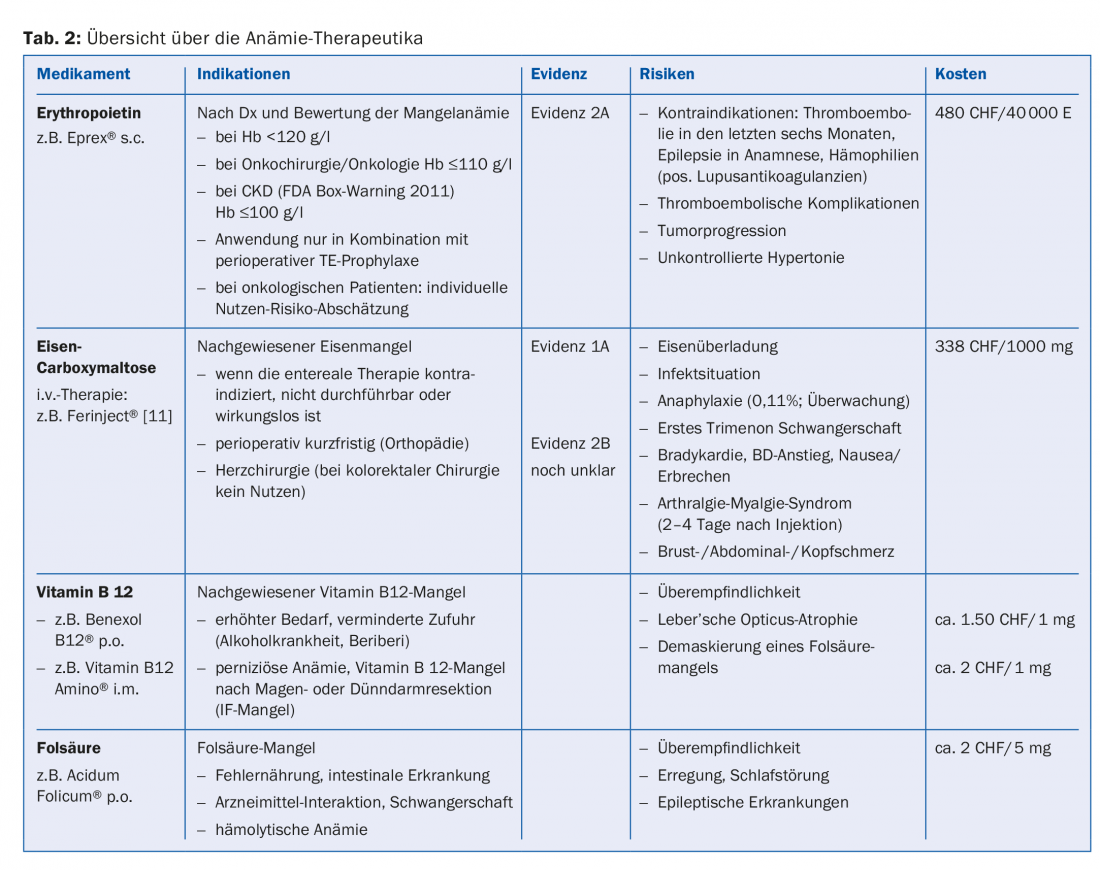
La sfida più grande è e rimane l’equilibrio tra la correttezza medica da un lato e la concisione o la semplicità dall’altro.
Le cause dell’anemia variano a seconda del contesto clinico dell’intervento chirurgico programmato. Le cause comuni di anemia preesistente sono la carenza di ferro, l’alterato utilizzo del ferro nel contesto di sindromi infiammatorie o di malattie maligne e l’insufficiente sintesi di eritropoietina nell’insufficienza renale cronica [6].
Seguendo la definizione di anemia dell’OMS, nel nostro algoritmo definiamo tre gradi di gravità:
- anemia grave (Hb <100 g/l)
- Anemia da lieve a moderata (Hb 100-120 o 130 g/l).
- anemia latente o attesa (Hb >120 o 130 g/l).
Anemia grave
In caso di anemia grave <100 g/l, l’operazione programmata deve essere rimandata e il paziente deve essere chiarito da uno specialista.
Anemia da lieve a moderata
Secondo l’OMS, l’anemia da lieve a moderata è definita da un valore di Hb di 100-120 g/l nelle donne e di 100-130 g/l negli uomini.
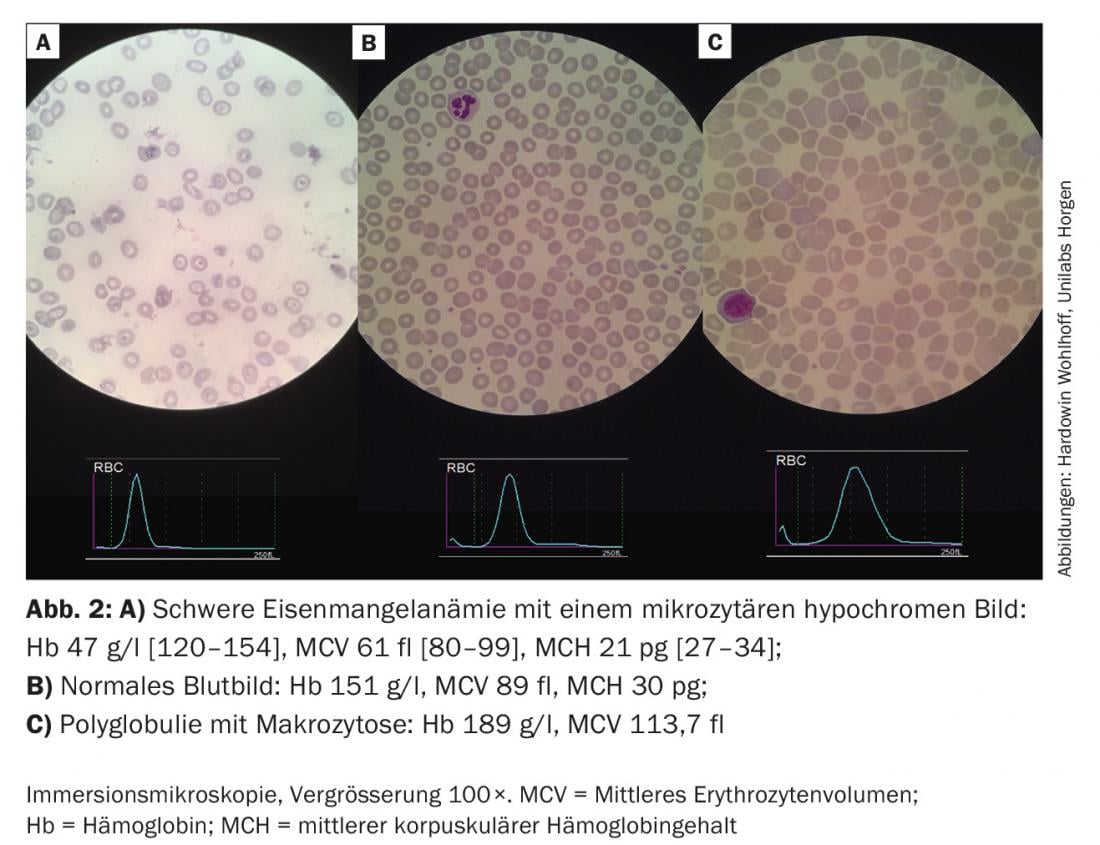
Per questa anemia, siamo guidati principalmente dal volume cellulare medio (MCV). Nella maggior parte dei casi di MCV normale o ridotto, c’è una carenza di ferro manifesta o nascosta. (Fig.2A). Con ferritina superiore a 100 μg/l con CRP elevata nel senso di “anemia da malattia cronica” o con funzione renale compromessa nel senso di “anemia renale”, si consiglia una terapia combinata di eritropoietina (Epo) e ferro nel dosaggio indicato nell’algoritmo. La frequenza e il dosaggio ideali della terapia con Epo non sono stati stabiliti. Tre giorni dopo una prima dose, i reticolociti aumentano, dopo sette giorni si genera il volume di sangue di un concentrato di EC (dopo 28 giorni di cinque concentrati di EC). Nel caso di un valore di ferritina inferiore a 30 μg/l o di un valore inferiore a 100 μg/l in combinazione con segni di infiammazione, si raccomanda la sostituzione isolata del ferro nel senso di una carenza assoluta o relativa di ferro.
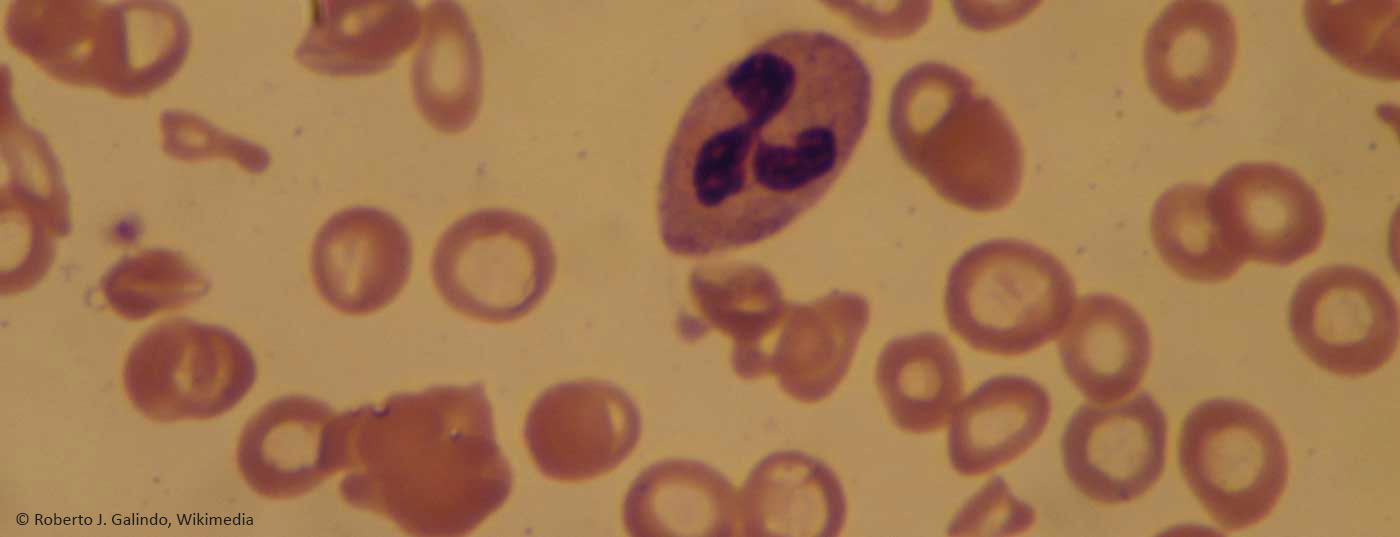
La Figura 2B mostra il riferimento normale tra i due strisci di sangue patologici.
Nelle anemie macrocitiche (Fig. 2C), i reticolociti forniscono informazioni sul fatto che l’anemia sia iper- o iporegenerativa. L’anemia iporegenerativa è solitamente causata da carenze (ferro, acido folico, vitamina B 12). Più raramente, indicano un’insufficienza del midollo osseo. Le anemie iperrigenerative sono il risultato di un aumento (emolisi) e/o di un’alterata produzione (neoplasie mieloproliferative, talassemie).
Raccomandiamo che il chiarimento e la sostituzione di una “semplice” carenza di ferro siano effettuati dai medici di base e dai medici di riferimento. Nel caso di forme di anemia più complesse e di concetti di trattamento, può essere utile il coinvolgimento di un ematologo.
In linea di principio, la terapia con il ferro può essere somministrata per via enterale, a condizione che vi sia una tolleranza gastrointestinale e un tempo di attesa sufficiente. Tuttavia, i dati mostrano che l’integrazione di ferro per via parenterale è associata a una maggiore compliance e porta a un aumento dell’emoglobina più precoce e più pronunciato [7–12].
La tollerabilità del ferro somministrato per via parenterale è circa uguale a quella della terapia enterale, senza i frequenti effetti collaterali gastrointestinali. Le reazioni di ipersensibilità temute, comprese le reazioni anafilattiche, si verificano in modo imprevedibile e con Ferinject® secondo il compendio con una frequenza dallo 0,1 all’1%. Un monitoraggio adeguato dei pazienti è quindi obbligatorio.
Nel caso dell’anemia in gravidanza, è importante ricordare che l’integrazione orale di ferro è spesso insufficiente in questo contesto. Le pubblicazioni e le linee guida nazionali e internazionali raccomandano la terapia con ferro per via endovenosa nel secondo e terzo trimestre [13–15].
La somministrazione di eritropoietina nel contesto preoperatorio è raccomandata dalle società professionali NATA, ESA, STS e ASA con evidenza 2A. La discussione sui rischi e sugli effetti collaterali dell’eritropoietina si concentra attualmente su tre argomenti:
L’aumento del rischio di complicanze tromboemboliche è sempre più accettato in letteratura e trova risposta nelle società professionali con la raccomandazione di una profilassi TE coerente [16–20].
I dati sull’influenza dell’Epo sulla progressione del tumore non sono ancora del tutto conclusivi. Nel 2009, Bohlius è riuscito a dimostrare un’influenza negativa dell’Epo sulla progressione del tumore in una revisione che comprendeva più di 14.000 pazienti [21]. L’ESA raccomanda quindi una valutazione del rischio individuale di ogni paziente e limita l’uso alle anemie con una Hb <110 g/l. Se l’Hb sale oltre i 120 o 130 g/l, la terapia deve essere interrotta immediatamente.
L’uso dell’Epo nell’insufficienza renale cronica è limitato all’anemia grave a causa dell’aumento della mortalità, delle gravi complicazioni cardiovascolari e dell’aumento del rischio di ictus [22,23].
A causa di questi rischi, che non sono ancora stati chiariti nel dettaglio, l’obbligo di pagare l’eritropoietina è attualmente ancora limitato all’ambito ortopedico. Solo i pazienti con anemia sintomatica preoperatoria o anemia moderata (Hb 100-130 g/l) e perdita ematica prevista di 900-1800 ml, nei quali le misure emostatiche non sono disponibili, sono insufficienti o sono controindicate, beneficeranno del rimborso.
Anemia attesa / latente
Il terzo gruppo di pazienti con emoglobina normale con ferritina borderline di <100 μg/l, per i quali si prevede una perdita di sangue superiore a 1000 ml o un calo di Hb superiore a 30 g/l, deve essere trattato preventivamente con 1000 mg di Fe e, per ragioni pragmatiche, insieme a 5 mg di acido folico.
Fattore tempo
Questo algoritmo è rivolto ai pazienti prima di un intervento chirurgico maggiore elettivo. Naturalmente, può essere utilizzato con successo solo se i pazienti vengono anche registrati preoperatoriamente in tempo utile e portati a un chiarimento. Raccomandiamo pertanto una diagnosi iniziale e l’avvio di una terapia appropriata subito dopo aver stabilito l’indicazione all’intervento chirurgico, idealmente almeno 28 giorni prima della data dell’intervento.
Prospettiva
I dati sull’impatto dell’anemia sull’esito dei pazienti nel contesto chirurgico elettivo appaiono chiari. Tuttavia, bisogna considerare che mancano ancora dati di alta qualità sull’esito terapeutico dell’anemia e che finora sono contraddittori. Mentre la terapia di ferro a breve termine riduce i tassi di trasfusione e la mortalità nei pazienti in ambito ortopedico [24], la terapia anemica preoperatoria nei pazienti con carcinoma colorettale non migliora gli esiti secondo le prove attuali [25].
Al contrario, la correzione dell’anemia con ferro ed eritropoietina in presenza di stenosi aortica e insufficienza cardiaca porta a un miglioramento della funzione di pompa del ventricolo sinistro, a una diminuzione del BNP e a una riduzione della mortalità – con e senza intervento chirurgico [26].
Gli studi che analizzano questo approccio [27] si spera che presto forniranno maggiore chiarezza.
Il trattamento dell’anemia senza trasfusioni di sangue estraneo prima di un intervento chirurgico elettivo è parte integrante della moderna gestione del sangue del paziente, è scientificamente “all’avanguardia”, migliora la sicurezza del paziente e supporta positivamente il processo di guarigione [28].
Ringraziamenti: Gli autori desiderano ringraziare il Prof. Hans Gombotz per aver messo a disposizione la sua presentazione del concetto di gestione del sangue del paziente in modo non burocratico e gentile e Hardowin Wohlhoff, Unilabs Horgen, per il materiale illustrativo delle immagini ematologiche.
Dichiarazione degli autori: Gli autori dichiarano di non avere legami finanziari con alcuna azienda il cui prodotto svolge un ruolo importante in questo articolo, né di essere legati ad alcuna azienda che commercializza un prodotto concorrente.
Letteratura:
- Shander A, et al: Anemia da carenza di ferro – colmare il divario tra conoscenza e pratica. Transfus Med Rev 2014; 28: 156-166.
- Musallam KM, et al: Anemia preoperatoria ed esiti post-operatori nella chirurgia non cardiaca: uno studio di coorte retrospettivo. Lancet 2011; 378 (9800): 1396-1407
- Baron DM, et al: L’anemia preoperatoria è associata a un cattivo esito clinico nei pazienti sottoposti a chirurgia non cardiaca. Br J Anaesth 2014; 113(3): 416-423.
- Karkouti k, et al: Rischio associato all’anemia preoperatoria nella chirurgia cardiaca: uno studio di coorte multicentrico. Circolazione 2008; 117(4): 478-484.
- Lasocki S, et al: PREPARE: la prevalenza dell’anemia perioperatoria e la necessità di gestione del sangue del paziente nella chirurgia ortopedica elettiva: uno studio osservazionale multicentrico. Eur J Anaesthesiol 2015; 32(3): 160-167.
- Clevenger B, et al: Anemia pre-operatoria. Anestesia 2015; 70(Suppl 1): 20-28.
- Ng O, et al: Terapia del ferro per l’anemia pre-operatoria. Cochrane Database Syst Rev 2015; 12: CD011588
- Pattakos G, et al: Esito dei pazienti che rifiutano la trasfusione dopo un intervento di cardiochirurgia: un esperimento naturale con una grave conservazione del sangue. Arch Intern Med 2012; 172(15): 1154-1160.
- Murphy MF, et al: Pratica e sicurezza delle trasfusioni: stato attuale e possibilità di miglioramento. Vox Sang 2011; 100(1): 46-59.
- Nat Kidney Foundation KDOQI: Linee guida di pratica clinica e raccomandazioni di pratica clinica per l’anemia nella malattia renale cronica negli adulti. Am J Kidney Dis 2006; 47(5 Suppl 3): 16-85.
- Gupta A, et al: Patogenesi delle reazioni anafilattoidi al ferro per via endovenosa. Am J Kidney Dis 2000; 35(2): 360-361.
- Elhenawy AM, et al: Ruolo della terapia preoperatoria con ferro per via endovenosa per correggere l’anemia prima di un intervento chirurgico maggiore: protocollo di studio per una revisione sistematica e una meta-analisi. Syst Rev 2015; 4: 29.
- Khalafallah AA, et al: Follow-op di tre anni di uno studio clinico randomizzato sul ferro per via endovenosa rispetto a quello orale per l’anemia in gravidanza. BMJ Open 2012; 2(5): piie000998.
- Pavord S, et al: Linee guida britanniche sulla gestione della carenza di ferro in gravidanza. Br J Haematol 2012; 2156(5): 588-600.
- Christoph P, et al: Trattamento con ferro per via endovenosa in gravidanza: confronto tra carbossimaltosio ferrico ad alto dosaggio e ferro saccarosio. J Perinat Med 2012; 40(5): 469-474.
- Kumar A, et al: Gestione perioperatoria dell’anemia: limiti della trasfusione di sangue e alternative ad essa. Cleve Clin J Med 2009; 76(Suppl 4): 112-118.
- Stowell CP, et al: Uno studio in aperto, randomizzato, a gruppi paralleli di epoetina alfa perioperatoria rispetto allo standard di cura per la conservazione del sangue nella chirurgia spinale elettiva maggiore: analisi della sicurezza. Spine 2009; 34(23): 2479-2485.
- Lippi G, et al: Complicazioni trombotiche degli agenti stimolanti l’eritropoiesi. Semin Thromb Hemost 2010; 36(5): 537-549.
- Goodnough LT, et al: Rilevazione, valutazione e gestione dell’anemia preoperatoria nel paziente chirurgico ortopedico elettivo: linee guida NATA. Br J Anaesth 2011; 106(1): 13-22.
- Kozek-Langenecker SA, et al.: Gestione dell’emorragia perioperatoria grave: linee guida dell’Associazione europea per l’emorragia perioperatoria.
- Società di Anestesiologia. Eur J Anaesthesiol 2013; 30(6): 270-382.
- Bohlius J, et al: Agenti stimolanti l’eritropoiesi umana ricombinante e mortalità nei pazienti con cancro: una meta-analisi di studi randomizzati. Lancet 2009; 373(9674): 1532-1542.
- Saran R, et al: Stabilire un sistema nazionale di sorveglianza della malattia renale cronica per gli Stati Uniti. Clin J Am Soc Nephrol 2010; 5(1): 152-161.
- Cody JD, et al: Eritropoietina umana ricombinante rispetto al placebo o a nessun trattamento per l’anemia della malattia renale cronica nelle persone che non richiedono la dialisi. Cochrane Database Syst Rev 2016; CD 003266.
- Munoz M, et al: Somministrazione perioperatoria di ferro per via endovenosa a brevissimo termine ed esito postoperatorio nella chirurgia ortopedica maggiore: un’analisi congiunta dei dati osservazionali di 2547 pazienti. Trasfusione 2014; 54(2): 289-299.
- Hallet J, et al: L’impatto del ferro perioperatorio sull’uso di trasfusioni di globuli rossi nella chirurgia gastrointestinale: una revisione sistematica e una meta-analisi. Transfus Med Rev 2014; 28(4): 205-211.
- Gomez M, et al: Effetto della correzione dell’anemia sui parametri ecocardiografici e clinici nei pazienti con stenosi aortica con valvola aortica tricuspide e frazione di eiezione ventricolare sinistra normale. Am J Cardiol 2015; 116(2): 270-274.
- Elhenawy AM, et al: Ruolo della terapia preoperatoria con ferro per via endovenosa per correggere l’anemia prima di un intervento chirurgico maggiore: protocollo di studio per una revisione sistematica e una meta-analisi. Syst Rev 2015; 4: 29.
- Choorapoikayil S, et al: Gestione del sangue del paziente: vale la pena di essere impiegato? Curr Opin Anesthesiol 2016; 29(2): 186-191.
PRATICA GP 2016; 11(5): 23-28