Al congresso di quest’anno della Società Svizzera di Allergologia e Immunologia (SGAI), sono stati evidenziati gli sviluppi attuali nei campi della terapia e della ricerca. Oltre ai nuovi approcci terapeutici per la dermatite atopica, sono stati presentati anche i risultati degli studi attuali sul trattamento farmacologico della mastocitosi (omalizumab) e dell’angioedema ereditario (lanadelumab).
Quest’anno, la Società Svizzera di Allergologia e Immunologia (SGAI) ha tenuto il suo congresso annuale insieme alla Società Svizzera di Reumatologia (SGR). Come hanno sottolineato il Presidente della SGAI, Prof. Daniel Speiser, dell’Università di Losanna, e il Presidente della SGR, Prof. Diego Kyburz, dell’Ospedale Universitario di Basilea, nei loro commenti di benvenuto, le due discipline condividono molti interessi comuni, in quanto l’immunologia occupa anche una posizione centrale nella cura dei pazienti con malattie reumatologiche.
L’anno in rassegna
In una delle sessioni, è stato presentato un bilancio dell’anno incentrato sulle allergie. Il Prof. Dr. med. Schmid-Grendelmeier, medico senior di Allergologia presso l’Ospedale Universitario di Zurigo, era responsabile dell’area delle malattie allergiche della pelle e si è concentrato qui sulla dermatite atopica (AD). “Dopo un lungo periodo in cui non è successo nulla in questa zona, ora posso riferire alcune notizie”, ha spiegato. Nel frattempo, è diventato chiaro che l’AD è molto più eterogeneo di quanto ipotizzato in precedenza. Ad esempio, le biopsie cutanee hanno dimostrato che esistono differenze immunologiche tra l’AD nei neonati e negli adulti [1]. “Questo potrebbe anche avere un’influenza sul successo di un trattamento”, ha detto il Prof. Schmid-Grendelmeier.
Nel contesto dei nuovi approcci terapeutici, il relatore ha sottolineato i buoni risultati degli studi attualmente disponibili su dupilumab, un anticorpo monoclonale che si lega alla subunità α del recettore dell’interleuchina-4 e dell’interleuchina-13, nei pazienti con AD da moderato a grave [2]. In uno studio di fase III randomizzato, controllato con placebo, della durata di un anno, è stato dimostrato anche un effetto sostenuto di dupilumab (in combinazione con steroidi topici) nei pazienti affetti da AD per un periodo più lungo [3]. “Ma se interrompiamo il trattamento, la malattia tornerà”, ha sottolineato il Prof. Schmid-Grendelmeier. In base alla sua esperienza personale, ha riferito: “Finora siamo stati in grado di utilizzare dupilumab in diversi pazienti con malattia grave e refrattaria, ottenendo un grande miglioramento in alcuni di loro”. Per quanto riguarda gli effetti collaterali, ha indicato in particolare la congiuntivite. “Questo non si verifica così raramente e può richiedere l’uso di steroidi topici”.
Un’altra sostanza attualmente in fase di sperimentazione clinica nei pazienti con MA è l’anticorpo anti-interleuchina-31 nemolizumab [4]. “Questo anticorpo ha mostrato un buon effetto, ma quasi esclusivamente sul prurito”, ha sottolineato il Prof. Schmid-Grendelmeier.
Studio controllato con placebo di omalizumab nella mastocitosi
Distler et al. hanno utilizzato l’anticorpo anti-IgE omalizumab nel loro studio multicentrico in doppio cieco, controllato con placebo, su sette pazienti (66% donne) con varie forme di mastocitosi, mentre nove pazienti (85,7% donne) hanno ricevuto il placebo [5]. Omalizumab è stato dosato in base al peso corporeo e alle IgE sieriche totali, come di consueto per il suo utilizzo nei pazienti asmatici. I risultati del lavoro sono stati presentati come poster al congresso. Dopo sei mesi di trattamento, il punteggio mediano AFIRMM (Association Française pour les Initiatives de Recherche sur le Mastocyte et les Mastocytoses) è migliorato da 104,0 a 102,0 con il placebo e da 52,0 a 26,0 con omalizumab (p=0,286). L’entità del miglioramento non era significativamente diversa (p=0,941). Gli autori hanno dichiarato che l’interpretazione dei risultati di questo primo studio in doppio cieco, controllato con placebo, di omalizumab nella mastocitosi, a loro conoscenza, era difficile a causa del numero ridotto di pazienti e delle differenze nelle caratteristiche basali tra i due gruppi. Tuttavia, oltre al miglioramento del punteggio AFIRRM, hanno osservato anche un miglioramento di vari sintomi associati alla mastocitosi, tra cui in particolare diarrea, vertigini, vampate e reazioni anafilattiche. Gli effetti collaterali del trattamento sono stati rari e comparabilmente frequenti in entrambi i gruppi. Saranno necessari studi più ampi per confermare questi risultati.
Lanadelumab nell’angioedema ereditario
Lanadelumab è un anticorpo anti-callikreina completamente umano, potente, specifico e di lunga durata [6]. Nei pazienti con angioedema ereditario (HAE) di tipo I/II, lanadelumab (150 mg ogni quattro settimane, 300 mg ogni quattro settimane, 300 mg ogni quindici giorni rispetto al placebo) si è dimostrato efficace e sicuro nel prevenire gli attacchi per un periodo di 26 settimane (da 0 a 182 giorni) nello studio di fase III HELP [7]. Un documento presentato a Interlaken ha ora analizzato il profilo di efficacia dell’anticorpo durante la fase di stato stazionario dello studio (giorni da 70 a 182, 16 settimane di trattamento) [8].
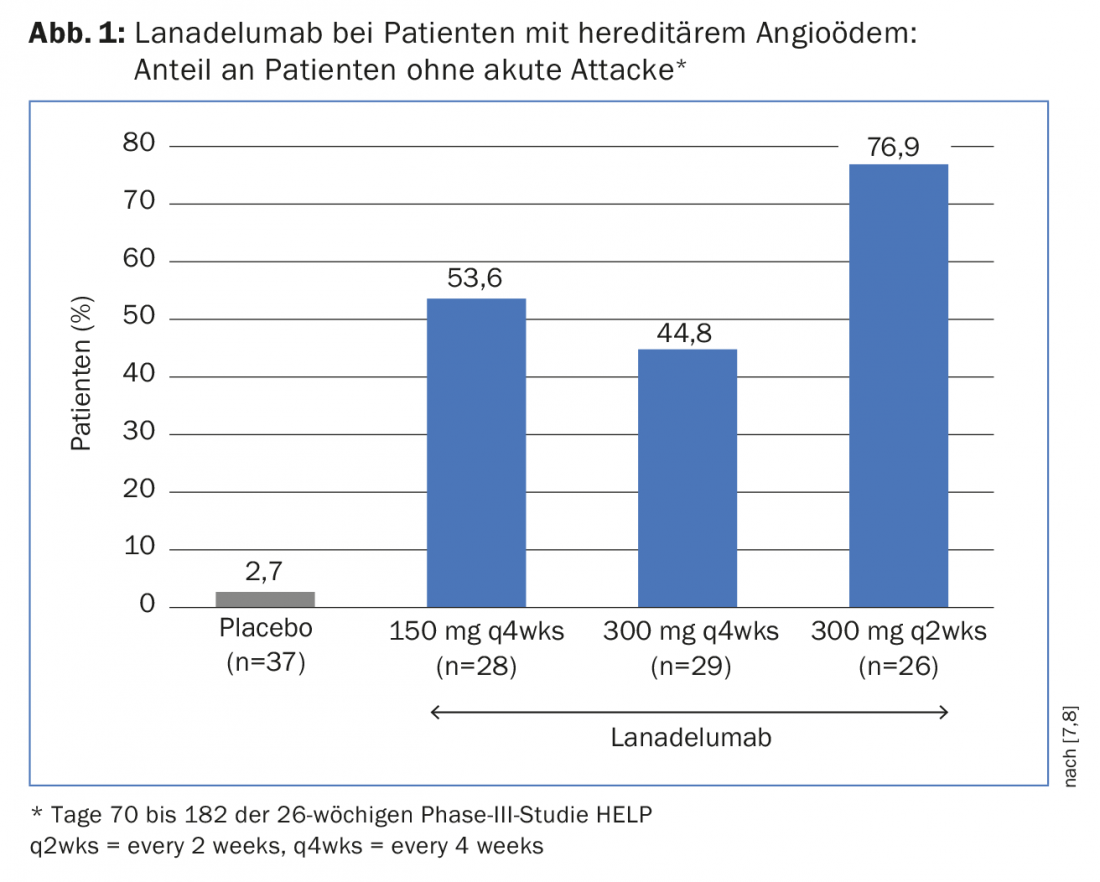
Tra i pazienti trattati con lanadelumab 300 mg ogni due settimane, il 76,9% è rimasto libero da attacchi durante questo periodo, rispetto al 2,7% dei pazienti del gruppo placebo (Fig. 1). Il tasso medio di attacchi mensili è stato ridotto del 91,5% rispetto ai pazienti trattati con placebo. Su 26 pazienti trattati con lanadelumab, uno ha avuto un attacco grave, mentre questo è avvenuto in 31 dei 37 pazienti del gruppo placebo. Anche le altre due dosi di lanadelumab hanno ridotto efficacemente il numero di attacchi rispetto al placebo. Questa analisi supporta quindi i risultati dell’analisi primaria di HELP e dimostra nuovamente l’efficacia di lanadelumab come profilassi a lungo termine per i pazienti con HAE.
Fonte: Congresso annuale SGAI, 30-31 agosto 2018, Interlaken
Letteratura:
- Brunner PM, et al: L’immunologia della dermatite atopica e la sua reversibilità con terapie ad ampio spettro e mirate. J Allergy Clin Immunol 2017; 139(4S): S65-S76.
- Simpson EL, et al: Due studi di fase 3 su dupilumab rispetto al placebo nella dermatite atopica. N Engl J Med 2016; 375: 2335-2348.
- Blauvelt A, et al: Gestione a lungo termine della dermatite atopica da moderata a grave con dupilumab e corticosteroidi topici concomitanti (LIBERTY AD CHRONOS): uno studio di fase 3 di 1 anno, randomizzato, in doppio cieco, controllato con placebo. Lancet 2017; 389: 2287-2303.
- Ruzicka T, et al: Anticorpo contro il recettore A dell’Interleuchina-31 per la dermatite atopica. N Engl J Med 2017; 376: 826-835.
- Distler M, et al: L’effetto di omalizumab nei pazienti affetti da mastocitosi. Studio prospettico multicentrico in doppio cieco, controllato con placebo. Swiss Medical Weekly 2018; 148 (Suppl 231): Estratto SSAIO 10.
- Kenniston JA, et al: Inibizione della callicreina plasmatica da parte di un anticorpo bloccante del sito attivo altamente specifico. J Biol Chem 2014; 289: 23596-23608.
- Banerji A, et al: Lanadelumab per la prevenzione degli attacchi nell’angioedema ereditario: risultati dello studio di fase 3 HELP. Ann Allergy Asthma Immunol 2017; 119 (suppl): S5 (Abstract OR034).
- Maurer M, et al: Lanadelumab è altamente efficace allo stato stazionario nell’angioedema ereditario (HAE): risultati dello studio di fase 3 HELP. Swiss Medical Weekly 2018; 148 (Suppl 231): Estratto SSAIPeF16.
PRATICA DERMATOLOGICA 2018; 28(5): 36-37











