L’elettroforesi delle proteine è un test di laboratorio economico e ampiamente disponibile, che esamina proteine specifiche nel sangue. In medicina interna, viene utilizzato principalmente per diagnosticare il sospetto di mieloma multiplo. Il seguente articolo mostra perché è utile anche in gastroenterologia.
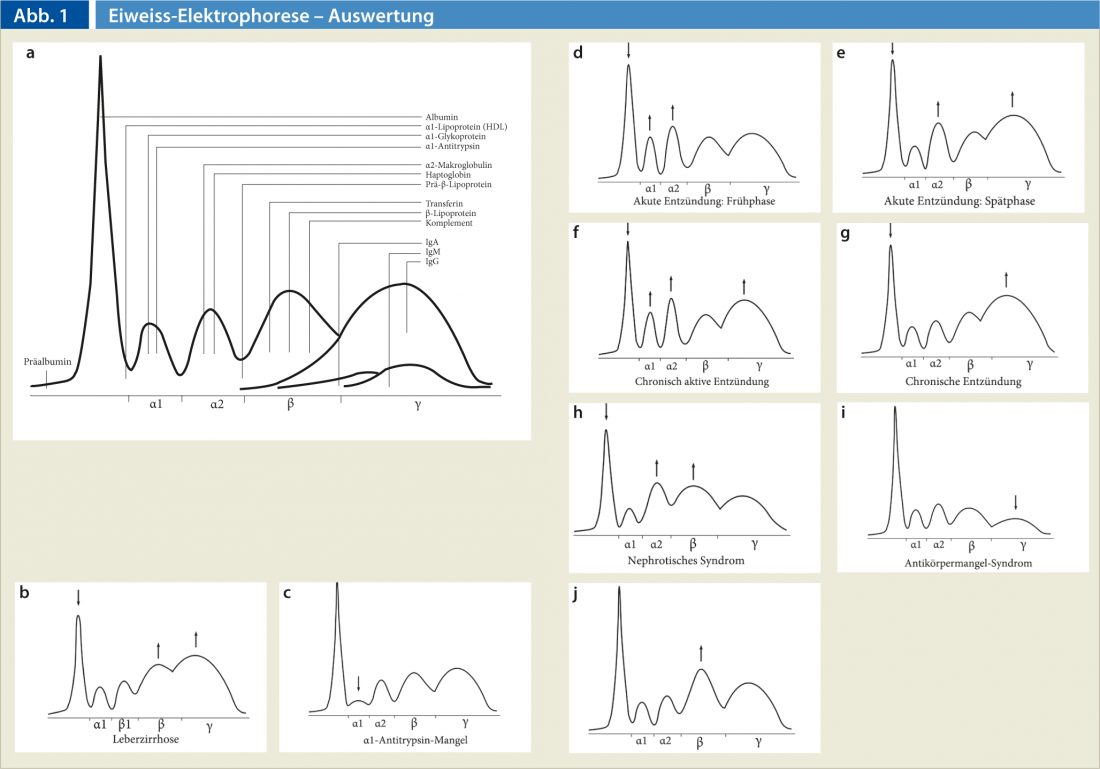
Nell’elettroforesi delle proteine, il siero (cioè le parti liquide del sangue quando i componenti cellulari vengono separati da un campione di sangue coagulato mediante centrifugazione) viene posto su un tampone speciale, trattato con un gel e sottoposto a una carica elettrica. In base alle diverse proprietà fisiche (dimensioni, carica elettrica) delle proteine del siero, esse vengono suddivise in cinque classi principali (Fig. 1a) [1]:
L’albumina
- Alfa-1 globuline (α1)
- Alfa-2-globuline (α2)
- Beta globuline (β)
- Gamma globuline (γ)
L’elettroforesi proteica viene utilizzata principalmente per diagnosticare il sospetto di mieloma multiplo, ma è anche molto utile come test di screening per molte altre malattie in medicina interna e soprattutto in gastroenterologia, di cui vorremmo parlare in modo un po’ più dettagliato in questo articolo.
Componenti dell’elettroforesi delle proteine
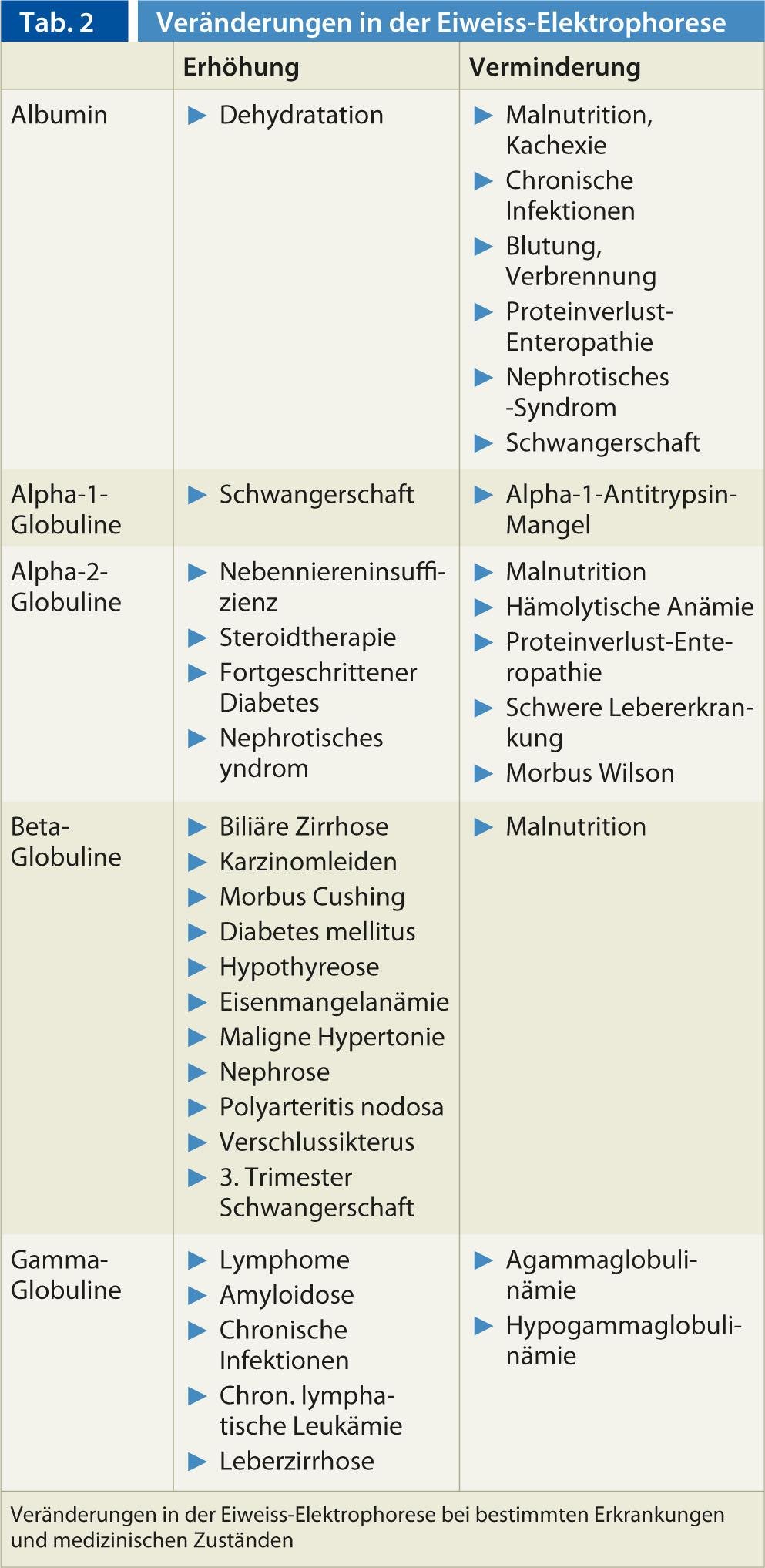
Fondamentalmente, si possono distinguere due tipi principali di proteine: Albumina e globuline, che sono presenti nel siero secondo un modello di distribuzione specifico (Tab. 1) . Alcune condizioni mediche e malattie determinano un modello elettroforetico caratteristico (Tab. 2) [2]. Di seguito, i vari componenti dell’elettroforesi proteica vengono discussi in modo un po’ più dettagliato.
Albumina: l’ albumina viene prodotta nel fegato ed è il componente principale delle proteine nel siero. Rappresenta il picco più alto nell’elettroforesi delle proteine ed è il più vicino all’elettrodo positivo (anodo). L’albumina diminuisce in situazioni di ridotta produzione nel fegato o di aumentata perdita o degradazione. È necessario un calo di albumina di almeno il 30% perché sia visibile nell’elettroforesi proteica. Esempi importanti di riduzione dei livelli di albumina sono la malnutrizione, le malattie epatiche gravi, la perdita renale (ad esempio nella sindrome nefrosica), la terapia ormonale, le ustioni o la gravidanza. Livelli elevati di albumina possono essere osservati nei pazienti con disidratazione.
Globuline: Il gruppo delle globuline comprende una frazione significativamente più piccola delle proteine totali del siero. Come già descritto, questo gruppo comprende i quattro sottogruppi alfa-1, alfa-2, beta e gamma. Le punte delle globuline sono più vicine all’elettrodo negativo (catodo) rispetto all’albumina, con la frazione gamma più vicina al catodo.
Zona intermedia albumina-alfa-1: in questa zona dell’elettroforesi proteica, viene fotografata la lipoproteina alfa-1 (lipoproteina ad alta densità-LDL). Una diminuzione si verifica in condizioni infiammatorie gravi, epatite acuta, cirrosi epatica o sindrome nefrosica. Un aumento si riscontra negli alcolisti gravi, nelle donne in gravidanza o durante la pubertà.
Zona alfa-1: la frazione alfa-1 è composta dall’antitripsina alfa-1, dalla glicoproteina alfa-1, dalla globulina legante la tiroxina e dalla transcortina. Una riduzione di questa frazione si osserva, ad esempio, nella carenza di alfa-1 antitripsina, nella sindrome nefrosica o nella ridotta produzione di globulina nelle malattie epatiche gravi. La neoplasia e gli stati infiammatori acuti possono portare ad un aumento delle alfa-1 globuline.
Zona alfa-2: la coeruloplasmina, l’alfa-2-macroglobulina e l’aptoglobina appartengono alla frazione delle alfa-2-globuline. In genere, una riduzione della zona alfa-2 si osserva nelle anemie emolitiche (consumo di aptoglobina, che si lega all’emoglobina) o nella malattia di Wilson (riduzione della coeruloplasmina). La frazione alfa-2 è aumentata nei pazienti con sindrome nefrosica (l’alfa-2 macroglobulina è una molecola grande che non può passare attraverso i glomeruli) o negli stati infiammatori (nel senso di una reazione di fase acuta).
Frazione beta: la frazione beta è composta da transferrina, fattore di complemento C3, lipoproteina beta e immunoglobuline IgA e (parzialmente) IgM. Un aumento può essere riscontrato nell’anemia da carenza di ferro, nella gravidanza o nei pazienti sottoposti a terapia estrogenica.
Frazione gamma: la regione gamma è costituita prevalentemente dalle immunoglobuline (per la maggior parte IgG), per cui le varie classi di immunoglobuline (IgG, IgA, IgM, IgD e IgE) sono anche parzialmente mappate nella regione beta e alfa-2. La zona delle gammaglobuline è diminuita nell’ipo- o agammaglobulinemia. Le malattie che comportano un aumento della produzione di gamma globuline includono i linfomi maligni (compresi il mieloma multiplo e la malattia di Waldenström), l’amiloidosi, la leucemia linfocitica cronica, le malattie della pelle, le malattie reumatologiche (ad esempio, l’artrite reumatoide o il lupus eritematoso sistemico), le malattie granulomatose o la cirrosi epatica.
Principali indicazioni in medicina interna
L’elettroforesi delle proteine (con immunofissazione, che è più sensibile nel rilevare la piccola proteina M monoclonale o paraproteina) deve essere eseguita in tutti i pazienti con sospetto mieloma multiplo, malattia di Waldenström o sospetta amiloidosi. Queste malattie appartengono al gruppo delle gammopatie monoclonali, che si distinguono dalle gammopatie policlonali (Tabella 3) [3]. Le gammopatie monoclonali sono un gruppo di malattie caratterizzate dalla proliferazione di un singolo clone di plasmacellule. Queste producono una proteina immunologicamente omogenea chiamata paraproteina o proteina M (M sta per monoclonale).
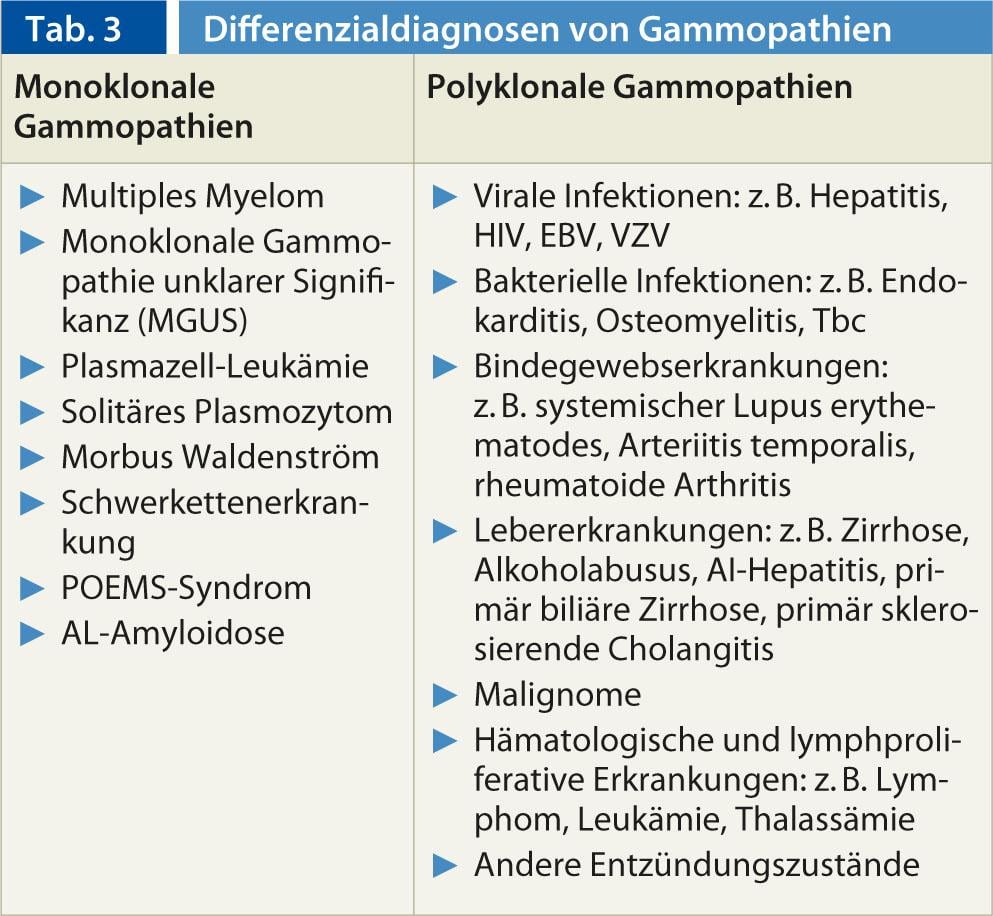
Al contrario, nelle gammopatie policlonali non si può rilevare alcuna proteina M. Le gammopatie policlonali sono spesso causate da processi reattivi o infiammatori.
Indicazioni in gastroenterologia
L’elettroforesi delle proteine viene utilizzata principalmente in gastroenterologia per chiarire le epatopatie poco chiare. Nella malattia epatica, l’albumina è tipicamente diminuita, le alfa-2 globuline possono essere diminuite e la frazione gamma è spesso policlonale (Fig. 1b). Le cause più rare di epatopatia, come l’epatite autoimmune, il deficit di alfa-1 antitripsina (Fig. 1c) o la malattia di Wilson, possono essere escluse in modo rapido ed economico con un’elettroforesi proteica normale.
Tuttavia, anche i pazienti con amiloidosi, mieloma multiplo o malattia di Waldenström presentano relativamente spesso sintomi gastrointestinali [4, 5]. In caso di sintomi gastrointestinali poco chiari, l’indicazione per l’elettroforesi proteica dovrebbe quindi essere data con generosità, soprattutto se i pazienti lamentano anche sintomi generali come perdita di peso o febbre.
Interpretazione dei risultati dell’elettroforesi proteica
Fase iniziale dell’infiammazione acuta (Fig. 1d): Questa immagine può essere osservata in caso di infezioni acute, traumi, formazione di necrosi (ad esempio, infarto del miocardio) o ustioni. Si osservano livelli elevati di fibrinogeno, alfa-1-antitripsina, aptoglobina, coeruloplasmina, CRP, complemento C3 e glicoproteina alfa-1-acido.
Albumina normale-↓, alfa-1↑, alfa-2↓, gamma normale
Fase tardiva dell’infiammazione (Fig. 1e): Questo quadro si presenta nella fase avanzata delle infezioni. Rispetto alla fase iniziale dell’infiammazione, sono evidenti la riduzione dell’albumina e l’aumento delle gammaglobuline.
Albumina↓ alfa-1↑, alfa-2↓, gamma↑
Infiammazione cronica (attiva): Queste condizioni includono malattie virali (ad esempio epatiti, mononucleosi, tubercolosi), malattie reumatologiche o malattie infiammatorie croniche dell’intestino.
Infiammazione cronica attiva (Fig. 1f):
Albumina↓, alfa-1↑, alfa-2↑, beta normale, gamma↑
Infiammazione cronica (Fig. 1g):
Albumina↓, alfa-1, alfa-2 e beta normale, gamma↑
Tumori maligni: Tutti i tumori maligni mostrano un aumento delle alfa-globuline (soprattutto alfa-2) nel senso di una reazione di fase acuta. I tumori con proprietà immunosoppressive (linfomi) possono portare a una riduzione della frazione gamma.
Albumina↓, alfa-1 e alfa-2↑, beta normale,
gamma normale, ↓ o ↑
Epatite autoimmune: oltre ai segni di epatopatia cronica (diminuzione dell’albumina e spesso bassa frazione alfa), l’epatite autoimmune mostra un marcato aumento della frazione gamma.
Albumina↓, alfa-1 e alfa-2 normali o↓, beta normale, gamma ↑ ↑ ↑
Sindrome nefrosica (Fig. 1h): La malattia renale con danno glomerulare e una perdita di proteine nelle urine di almeno 3 g al giorno può portare a questo schema. La frazione alfa-2 può essere a volte molto pronunciata e assomigliare a una gammopatia monoclonale con un gradiente M.
Albumina↓, alfa-1↓, alfa-2↑ ↑, beta↑, gamma↓
Carenza di anticorpi (Fig. 1i) : Le carenze anticorpali possono riguardare una singola frazione o tutte le frazioni. La sindrome da carenza congenita di anticorpi si presenta con infezioni multiple già durante l’infanzia. Una carenza di anticorpi acquisita può essere causata da farmaci (ad esempio, citostatici o prednisone), leucemia linfocitica cronica, mieloma multiplo, tumori maligni o nefropatia.
Albumina, alfa-1, alfa-2 e beta normale, gamma↓
gravidanza (fig. 1j): Nel primo trimestre, aumentano le globuline alfa-2 e nel secondo e terzo trimestre anche la frazione beta (a causa dell’anemia da carenza di ferro).
Albumina↓, alfa-1 normale, alfa-2 e beta↑,
gamma normale
CONCLUSIONE PER LA PRATICA
- L’elettroforesi delle proteine è un test di laboratorio poco costoso e facilmente disponibile, che può identificare o escludere rapidamente alcune malattie.
- Nell’elettroforesi proteica, le proteine vengono separate in base a diverse proprietà fisiche, ottenendo un modello specifico. Questo schema indica una malattia specifica (ad esempio, il mieloma multiplo) o una condizione medica (ad esempio, un’infiammazione acuta).
- In genere, l’elettroforesi proteica viene utilizzata in medicina interna per identificare i pazienti con mieloma multiplo o altre gammopatie monoclonali.
- In gastroenterologia, l’elettroforesi delle proteine può fornire indizi importanti sulla presenza di epatopatia o di altre patologie sottostanti che si manifestano nel tratto gastrointestinale.
Letteratura:
- O’Connell TX, Horita TJ, Kasravi B: Capire e interpretare l’elettroforesi delle proteine del siero. Am Fam Physician 2005; 71: 105-112.
- Kyle RA: Le gammopatie monoclonali. Clin Chem 1994 ; 40: 2154-2161.
- Dispenzieri A, Gertz MA, Therneau TM, Kyle RA: Studio retrospettivo di coorte su 148 pazienti con gammopatia policlonale. Mayo Clin Proc 2001; 76: 476-487.
- Kyle RA, Grepp PR : Amiloidosi (AL): caratteristiche cliniche e di laboratorio in 229 casi. Mayo Clin Proc 1983; 58: 665-683.
- Bohus R, et al: Emorragia retroperitoneale con formazione di ascesso che complica la macroglobulinemia di Waldenström. Int Urol Nephrol 1985; 17: 255-259.