Du 7 au 10 décembre 2021, le 44e San Antonio Breast Cancer Symposium s’est déroulé dans le cadre d’un événement hybride physique/virtuel. Une série de présentations passionnantes a permis de présenter les dernières avancées cliniques et précliniques en matière de traitement du cancer du sein et de susciter de vives discussions. Nous avons résumé pour vous les principales études sur le cancer du sein localement avancé et métastatique présentées lors des quatre sessions générales.
Avec la supériorité révolutionnaire du trastuzumab-deruxtecan (T-DXd) sur le trastuzumab-emtansine en deuxième ligne dans les tumeurs HER2-positives et l’introduction du sacituzumab-govitecan dans le cancer du sein triple négatif (TNBC) – pour ne citer que deux exemples – les choses ont déjà bien évolué l’année dernière dans le cancer du sein avancé/métastasé. D’autres nouvelles de la recherche ont été présentées au San Antonio Breast Cancer Symposium (SABCS) en décembre 2021.
Celles-ci pourraient en partie marquer la pratique clinique quotidienne dans un avenir proche – aussi bien pour le cancer du sein HER2-positif que pour le cancer du sein HR (récepteur hormonal) positif/HER2-négatif et triple-négatif. Outre les nouvelles molécules et indications, la biopsie liquide pour le suivi et l’adaptation des thérapies était également sous les feux de la rampe.
Cancer du sein HER2-positif : une cible évidente
La cible thérapeutique des tumeurs HER2-positives semble établie. Ainsi, les études sur cette entité présentées au SABCS portaient principalement sur des thérapies ciblant HER2 (tableau 1). Comme lors des congrès précédents, une substance en particulier a suscité l’enthousiasme : le conjugué anticorps/principe actif trastuzumab-deruxtecan (T-DXd). Ce dernier est désormais autorisé en Suisse en monothérapie pour les patientes dont la maladie a progressé après au moins deux régimes de traitement ciblant HER2, y compris le trastuzumab et le trastuzumab emtansine (T-DM1) [1]. Une autorisation qui pourrait changer dans un avenir proche – et qui devrait le faire selon les résultats de l’étude DESTINY-Breast03. En effet, dans l’étude de phase III, déjà présentée au congrès ESMO 2021, la comparaison directe avec le trastuzumab-emtansine en deuxième ligne de traitement après trastuzumab/taxane a montré une nette supériorité du T-DXd en termes de survie sans progression (PFS). Alors que le taux de PFS à 1 an était de 75,8% dans le groupe T-DXd, il était de 34,1% sous traitement par trastuzumab-emtansine (hazard ratio HR 0,28, intervalle de confiance à 95% 0,22-0,37) [2]. De nouvelles données issues d’une analyse de sous-groupe ont été présentées lors du 44e SABCS. En bref, l’avantage du T-DXd en termes de PFS et de taux de réponse a été confirmé dans tous les sous-groupes. Il a été clairement et nettement démontré, indépendamment du statut des récepteurs hormonaux, de l’administration préalable de pertuzumab, de la présence d’une maladie viscérale ou de métastases cérébrales cliniquement stables, ainsi que du nombre de traitements antérieurs [3]. Ainsi, le T-DXd semble également efficace sur les métastases cérébrales – un signal important si l’on considère que celles-ci se développent chez jusqu’à la moitié des patientes. Une étude préclinique/clinique mixte, également présentée au SABCS, a analysé spécifiquement l’efficacité du T-DXd dans les métastases cérébrales actives – et est parvenue à la même conclusion. L’efficacité du conjugué anticorps-médicament a été confirmée sur des lignées cellulaires et sur 16 premières patientes présentant des métastases cérébrales actives [4].
Une équipe de recherche chinoise a présenté une nouvelle substance, le pyrotinib, comme autre traitement alternatif ciblant HER2 [5]. Il s’agit d’un inhibiteur de tyrosine kinase (ITK) dont les cibles sont EGFR, HER2 et HER4. Celui-ci s’est montré convaincant dans une étude précédente en combinaison avec la capécitabine par rapport au lapatinib + capécitabine en deuxième ligne de traitement après le trastuzumab/taxane [6]. Sur cette base, le pyrotinib a déjà été approuvé en Chine. Dans une mise à jour, des données positives de PFS et d’OS issues d’une étude de phase III ont été présentées au SABCS (tableau 1) [5].
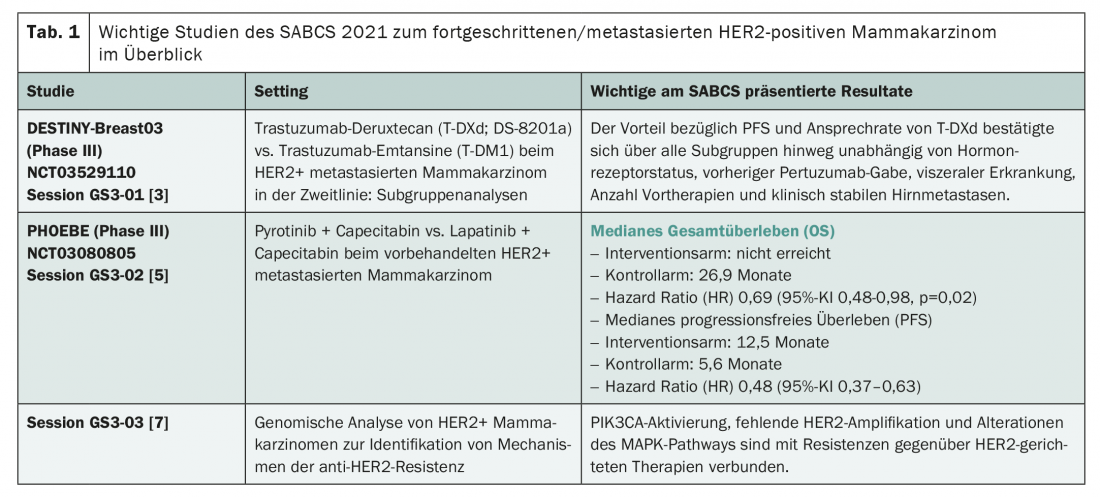
Outre les agents ciblant HER2, le symposium a également porté sur la recherche des mécanismes de résistance anti-HER2. Elles peuvent non seulement contribuer à une meilleure compréhension de l’échec thérapeutique, mais aussi proposer des solutions, comme l’a démontré une étude présentée au SABCS [7]. Les auteurs ont effectué des analyses génomiques à grande échelle des cancers du sein HER2+. Ils ont identifié des activations de PIK3CA et, pour la première fois, des altérations de la voie de signalisation de la kinase MAP comme déclencheurs possibles de la résistance. Alors que les premiers sont présents dans environ un tiers des cas, les seconds concernent environ 12,8% des tumeurs et surviennent plus souvent dans un contexte métastatique. De même, l’absence d’amplification de HER2 a été constatée dans de nombreux cancers résistants au traitement. La conséquence ? La voie de signalisation de la kinase MAP ainsi que PI3K pourraient servir de cibles supplémentaires – après tout, des agents correspondants tels que l’alpelisib existent déjà et sont (comme l’alpelisib) déjà partiellement autorisés [1].
Cancer du sein HER2-négatif avec récepteurs hormonaux positifs : focus sur les nouvelles molécules, les analyses de sous-groupes et la biopsie liquide
Les données présentées au SABCS ne laissent pas présager de changements immédiats dans la pratique clinique quotidienne du cancer du sein HR+/HER, mais il y a eu quelques analyses de sous-groupes intéressantes et des découvertes sur de nouvelles substances. Le rôle de la biopsie liquide dans la gestion a également fait l’objet de discussions animées. – qui pourrait bientôt fournir des informations précieuses sur le pronostic et la réponse au traitement, voire influencer les décisions thérapeutiques (tableau 2) .
Le SABCS a donné des nouvelles du pipeline concernant principalement trois substances actives : Entinostat, Samuraciclib et Elacestrant. Alors que l’entinostat, développé en Chine, est un inhibiteur sélectif de l’histone déacétylase (HDAC), le samuraciclib est un inhibiteur de CDK7 et l’élascestrant est un destructeur sélectif des récepteurs d’œstrogènes(SERD) par voie orale [8–10]. Alors que les résultats des études de phase III ont déjà été publiés pour l’entinostat et l’élacestrant, le samuraciclib en est encore à une phase de développement plus précoce (tableau 2). Néanmoins, son développement est remarquable, puisqu’il s’agit de la première molécule d’une nouvelle classe. Selon les premiers résultats de phase I/II, celui-ci semble efficace et sûr après une progression sous traitement par inhibiteur de CDK4/6 dans une population d’étude fortement prétraitée et au pronostic extrêmement défavorable.
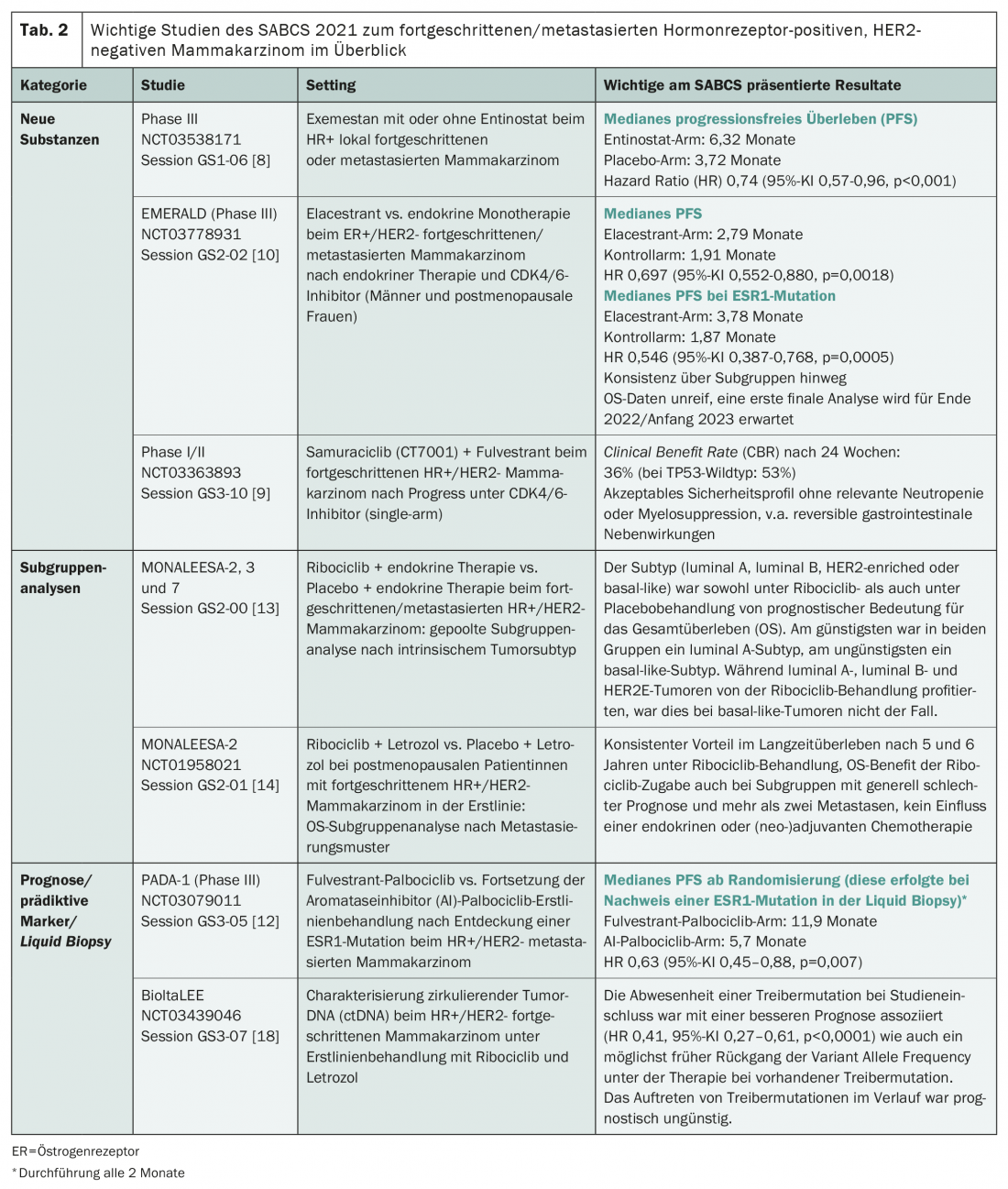
De même, après l’échec du traitement de première ligne par un inhibiteur de CDK4/6 et un traitement endocrinien, l’élacestrant fait actuellement l’objet d’essais cliniques et est comparé au standard de soins – un traitement endocrinien au choix du médecin traitant : Dans l’étude de phase III EMERALD [10]. Les premiers résultats positifs concernant la PFS ont été présentés au SABCS, l’effet du traitement étant particulièrement important chez les patientes porteuses de la mutation ESR1. Les approbations de la FDA et de l’EMA sont prévues pour 2022 [11].
Cependant, les mutations ESR1 n’ont pas seulement joué un rôle important dans l’étude sur l’élascestrant lors du symposium, mais aussi dans l’étude PADA-1 [12]. Mais de quoi s’agit-il exactement ? Les mutations ESR1, c’est-à-dire les mutations du récepteur 1 des œstrogènes, sont des moteurs connus de la résistance aux inhibiteurs de l’aromatase. Elles sont plutôt rares dans le cancer du sein métastatique et concernent <5% des patientes. Cependant, ils sont plus fréquents en cas de progression sous traitement de première ligne par inhibiteurs de l’aromatase. Dans ces conditions, l’étude PADA-1 a cherché à savoir si, en cas de découverte d’une modification génétique correspondante, le passage de l’inhibiteur de l’aromatase au fulvestrant était bénéfique. Pour ce faire, le sang des personnes concernées par un traitement de première ligne par palbociclib/inhibiteur d’aromatase a été analysé tous les deux mois. En cas de détection d’une mutation ESR1, une randomisation a été effectuée dans le groupe d’intervention (palbociclib/fulvestrant) ou le groupe témoin (palbociclib/inhibiteur de l’aromatase). Les résultats de la PFS présentés au SABCS plaident clairement en faveur d’un switch du traitement en présence d’une mutation ESR1, avec un doublement de la PFS médiane ( tableau 2) [12].
Outre la détection des mutations ESR1, la biopsie liquide pourrait également gagner en importance clinique dans le cancer du sein au cours des prochaines années. C’est ce qu’a montré une étude sur l’ADN tumoral circulant (ctDNA) [18]. Les auteurs ont caractérisé ces derniers sous traitement de première ligne par ribociclib et létrozole en termes de valeur pronostique et prédictive. L’absence de mutation pilote à l’inclusion dans l’étude était associée à un meilleur pronostic. Si une mutation pilote était présente lors de la détection de base, une diminution aussi précoce que possible de la fréquence de l’allèle variant sous traitement s’est avérée bénéfique pour le pronostic. En revanche, l’apparition de mutations pilotes au cours de l’évolution s’est révélée défavorable pour le pronostic [18]. Cette étude suggère également un bénéfice possible de la biopsie liquide pour le suivi du traitement et, le cas échéant, l’adaptation du traitement. Cependant, il n’existe pas encore de procédures standardisées et plusieurs études doivent être menées avant de pouvoir les utiliser dans la pratique clinique quotidienne.
Deux analyses de sous-groupes des études MONALEESA ont également été passionnantes lors du SABCS, même si elles ont été réalisées dans un contexte connu. Ces derniers ont préalablement étudié avec succès l’ajout du ribociclib, un inhibiteur de CDK4/6, au traitement endocrinien du cancer du sein HR+ avancé/métastasé – avec des autorisations correspondantes dès la première ligne de traitement [1]. L’impact du sous-type de tumeur intrinsèque et celui du schéma métastatique sur la survie globale ont été examinés de plus près (tableau 2) [13,14]. La conclusion est que le sous-type a une pertinence pronostique sous ribociclib et sous placebo, contrairement au schéma métastatique. Les tumeurs basal-like et HER2-elevated (HER2E) ont généralement un pronostic moins favorable que les tumeurs de sous-type luminal. Mais alors que les cancers HER2E répondent à l’ajout de ribociclib, les tumeurs basal-like ne le font pas [13]. Sur la base de ces données, la gestion moléculaire du cancer du sein HR+/HER2 pourrait prendre de l’importance à l’avenir. Et : le bénéfice OS sous ribociclib persiste même en cas de mauvais pronostic général, il y a un avantage consistant dans la survie à long terme [14].
Cancer du sein triple-négatif : un adversaire ingrat
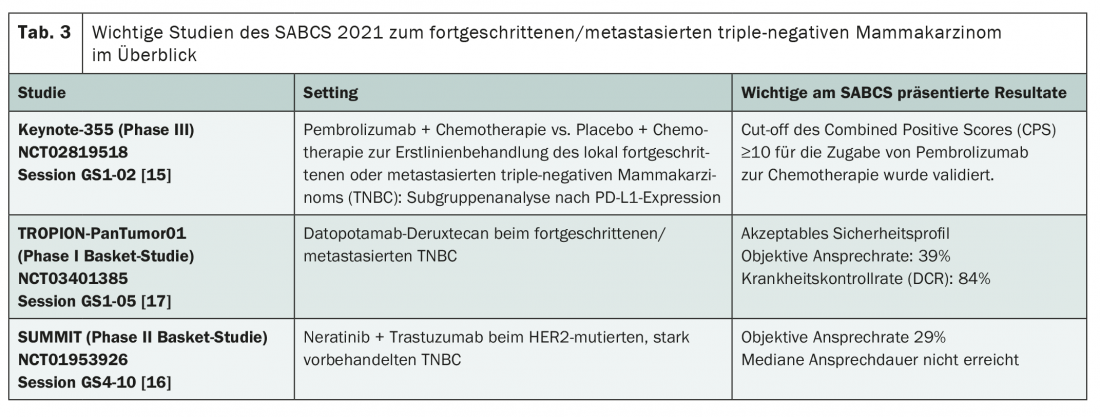
L’OS médian du TNBC métastasé est aujourd’hui d’environ 14,5 mois, et la chimiothérapie avec ou sans bevacizumab est toujours considérée comme le standard de première ligne. Les efforts déployés ces dernières années ont certes débouché sur les premières approches thérapeutiques dans le domaine de l’immunothérapie et de l’immunothérapie ciblées, mais la grande percée n’a pas eu lieu – et cette tendance semble se poursuivre sur la base des études présentées au SABCS. Les développements à ce jour concernent principalement l’introduction d’inhibiteurs de PARP tels que l’olaparib et le talazoparib en cas de mutation BRCA et l’atezolizumab en cas d’expression de PD-L1 ≥1%. De plus, le conjugué anticorps-médicament sacituzumab-govitecan a été approuvé à partir de la troisième ligne de traitement. Désormais, sur la base des données de l’étude Keynote 355, le pembrolizumab pourrait également être ajouté – du moins en cas d’expression élevée de PD-L1, cette restriction a été confirmée lors d’une analyse de sous-groupe présentée au SABCS [15]. En outre, la nouvelle substance active datopotamab-deruxtecan (Dato-DXd) est dans le pipeline ainsi que le traitement combiné de trastuzumab et de neratinib (tab. 3) [16,17]. Les deux approches sont actuellement étudiées dans le cadre d’études de paniers. Alors que le conjugué anticorps-médicament Dato-DXd cible TROP2 comme le sacituzumab-govitecan, le neratinib est testé dans les tumeurs mutées HER2 sans amplification. Le pan-HER-TKI peut déjà être utilisé dans le traitement adjuvant étendu du cancer du sein HR+, amplifié par HER2 [1]. Bien que la mutation HER2 ne soit présente que dans environ 2 à 4% des cancers du sein métastatiques, il pourrait être intéressant de la tester à l’avenir, comme c’est déjà le cas pour l’expression de PD-L1 et la mutation BRCA.
Source : Best of SABCS : https://bestofsabcsnews.com (dernier accès le 16.12.2021)
Littérature :
- Information sur les médicaments de Swissmedic : www.swissmedicinfo.ch (dernier accès le 16.12.2021)
- Cortés J, et al. : Trastuzumab deruxtecan (T-DXd) vs trastuzumab emtansine (T-DM1) chez des patients (Pts) atteints de cancer du sein métastatique HER2+ (mBC) : Résultats de l’étude randomisée de phase III DESTINY-Breast03. Congrès ESMO 2021, Symposium présidentiel 1, Abstract #LBA1.
- Hurvitz S, et al : Trastuzumab deruxtecan (T-DXd ; DS-8201a) vs trastuzumab emtansine (T-DM1) chez des patients (pts) atteints de cancer du sein métastatique HER2+ (mBC) : analyses de sous-groupes de l’étude randomisée de phase 3 DESTINY-Breast03. GS3-01, SABCS 2021 ; San Antonio, Texas, États-Unis.
- Kabraji S, et al. : Efficacité préclinique et clinique du trastuzumab deruxtecan dans les métastases cérébrales du cancer du sein (BCBM). PD4-05, SABCS 2021 ; San Antonio, Texas, États-Unis.
- Xu B, et al : Résultats mis à jour de la survie globale (OS) de la phase 3 PHOEBE du pyrotinib versus lapatinib en association avec la capécitabine chez les patients atteints de cancer du sein métastatique HER2-positif. GS3-02, SABCS 2021 ; San Antonio, Texas, États-Unis.
- Xu B, et al. : Pyrotinib plus capécitabine versus lapatinib plus capécitabine pour le traitement du cancer du sein métastatique HER2-positif (PHOEBE) : une étude multicentrique, en ouvert, randomisée, contrôlée, de phase 3. Lancet Oncol. 2021 ; 22(3) : 351-360.
- Ferraro E, et al : L’analyse génomique de 733 cancers du sein HER2+ identifie des altérations récurrentes de la voie associées à la résistance anti-HER2 et de nouvelles vulnérabilités thérapeutiques. GS3-03, SABCS 2021 ; San Antonio, Texas, USA.
- Xu B, et al : A randomized control phase III trial of entinostat, a one-weekly, class I selective histone deacetylase inhibitor, in combination with exemestane in patients with hormone receptor positive advanced breast cancer. GS1-06, SABCS 2021 ; San Antonio, Texas, États-Unis.
- Coombes C, et al : Étude du samuraciclib (CT7001), un inhibiteur sélectif de CDK7 de première classe, administré par voie orale, en association avec le fulvestrant chez des patientes atteintes d’un cancer du sein négatif HER2 à récepteurs hormonaux positifs en phase avancée (HR+BC). GS3-10, SABCS 2021 ; San Antonio, Texas, États-Unis.
- Bardia A, et al : Elacestrant, un inhibiteur sélectif des récepteurs d’œstrogènes (SERD) par voie orale, vs le choix de l’investigateur d’une monothérapie endocrinienne pour le cancer du sein avancé/métastatique ER+/HER2 (mBC) après progression sous traitement endocrinien et inhibiteur de CDK4/6 antérieur : résultats de l’essai EMERALD phase 3. GS2-02, SABCS 2021 ; San Antonio, Texas, États-Unis.
- Communiqué de presse : Le groupe Menarini et Radius Health annoncent des résultats positifs de phase 3 en amont de l’essai EMERALD évaluant l’élacestrant dans le cancer du sein. 20.10.2021, Radius Health.
- Bidard F-C, et al : Fulvestrant-palbociclib vs continuing aromatase inhibitor-palbociclib upon detection of circulating ESR1 mutation in HR+ HER2- metastatic breast cancer patients : Results of PADA-1, a UCBG-GINECO randomized phase 3 trial. GS3-05, SABCS 2021 ; San Antonio, Texas, USA.
- Carey L, et al : Analyse corrélative de la survie globale par sous-type intrinsèque à travers les études MONALEESA-2, -3, et -7 du ribociclib + traitement endocrinien chez les patients atteints de cancer du sein HR+/HER2- en progression. GS2-00, SABCS 2021 ; San Antonio, Texas, États-Unis.
- O’Shaughnessy et al. : Overall survival subgroup analysis by metastatic site from the phase 3 MONALEESA-2 study of first-line ribociclib + letrozole in postmenopausal patients with advanced HR+/HER2- breast cancer. GS2-01, SABCS 2021 ; San Antonio, Texas, États-Unis.
- Cortes J, et al. : Résultats finaux de KEYNOTE-355 : étude de phase 3, randomisée, en double aveugle, de pembrolizumab + chimiothérapie versus placebo + chimiothérapie pour le cancer du sein triple négatif localement récurrent et non traité auparavant. GS1-02, SABCS 2021 ; San Antonio, Texas, États-Unis.
- Jhaveri K, et al : Neratinib + fulvestrant + trastuzumab pour le cancer du sein métastatique HER2-mutant avec récepteurs hormonaux positifs et neratinib + trastuzumab pour la maladie triple-négative : dernières mises à jour du trial SUMMIT. GS4-10, SABCS 2021 ; San Antonio, Texas, États-Unis.
- Krop I, et al. : Datopotamab deruxtecan dans le cancer du sein HER2 avancé/métastatique : résultats de l’étude de phase 1 TROPION-PanTumor01. GS1-05, SABCS 2021 ; San Antonio, Texas, USA.
- Bianchini G, et al : Circulating tumor DNA (ctDNA) dynamics in patients with hormone receptor positive (HR+)/HER2 negative (HER2-) advanced breast cancer (aBC) treated in first line with ribociclib (R) and letrozole (L) in the BioItaLEE trial. GS3-07, SABCS 2021 ; San Antonio, Texas, USA.
InFo ONKOLOGIE & HÉMATOLOGIE 2022 ; 10(1) : 24-28