La mémoire immunologique joue un rôle important dans la pathogenèse du psoriasis. Les chercheurs s’intéressent de plus en plus aux cellules T à mémoire résidant dans les tissus (cellules TRM). En effet, la persistance des cellules TRM dans les lésions psoriasiques guéries est un élément d’explication de la réapparition des lésions au même endroit après l’arrêt du traitement systémique.
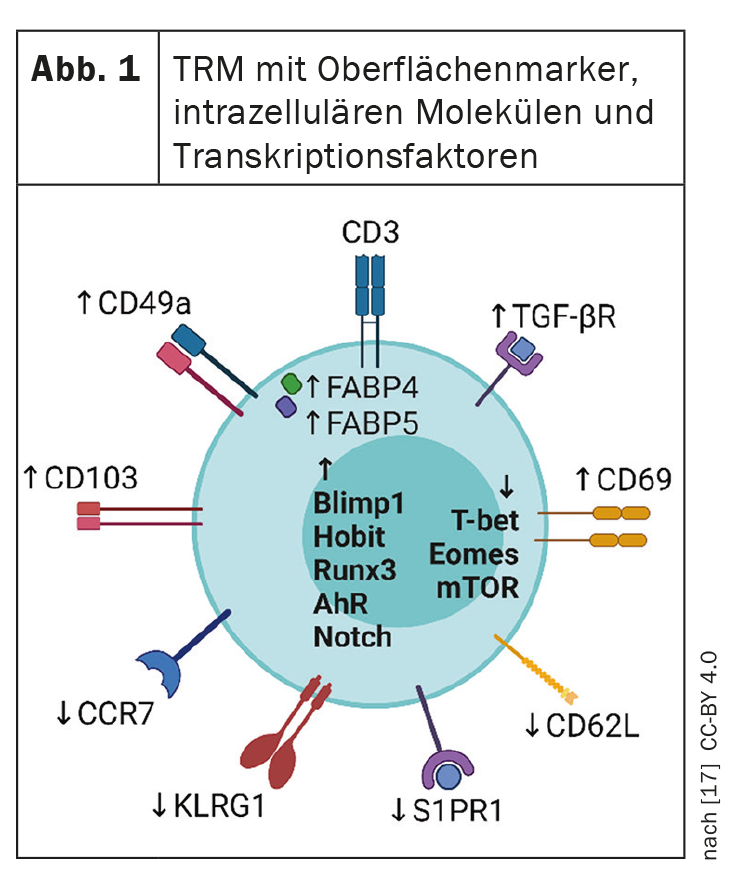
Les traitements systémiques modernes du psoriasis, très efficaces, transforment la peau lésionnelle en un état sans manifestations cliniques visibles. Cependant, dès que le traitement est arrêté, les lésions cutanées psoriasiques réapparaissent souvent sur les zones précédemment touchées. Cela suggère qu’une activité résiduelle de la maladie persiste au niveau des lésions apparemment guéries, prédisposant les personnes concernées à une récidive [2]. Les cellules T mémoires résidentes des tissus ( Fig. 1) font partie du système immunitaire adaptatif et stockent des informations sur les antigènes auxquels le système immunitaire a été précédemment confronté. Les cellules TRM jouent probablement un rôle clé dans la réactivation de l’inflammation latente et donc dans l’évolution à long terme de la maladie (encadré) .
Les cellules CD8+ TRM, biomarqueurs de l’activité du psoriasis ?
Wolf Henning Boehncke, des Hôpitaux Universitaires de Genève [1]. Plusieurs études sont en cours pour déterminer si une intervention précoce avec des médicaments biologiques peut avoir un effet durable sur l’évolution du psoriasis et empêcher le développement de l’arthrite psoriasique ou d’un handicap cumulatif tout au long de la vie (“Cumulative life course impairment”, CLCI) [3–7]. Une autre question est de savoir si les cellules TRM peuvent être utilisées comme biomarqueurs de l’activité du psoriasis, selon le professeur Boehncke [1]. Dans un article de synthèse publié en 2022 par Puig et al. présente l’état actuel des connaissances à ce sujet [8]. Les cellules TRM peuvent être divisées en sous-groupes CD8+ et CD4+. Les cellules TRM CD8+ sont localisées dans l’épiderme, où elles jouent un rôle crucial dans les réactions immunitaires, les cellules TRM CD4+ sont moins bien caractérisées et pourraient être impliquées dans l’immunité protectrice contre les infections bactériennes et mycosiques dans la peau [9,10]. La majorité des cellules TRM CD8+ expriment le marqueur cellulaire CD103. CD103 est la sous-unité αE de αEβ7. La E-cadhérine est un ligand de l’intégrine αE(CD103)β7. Les interactions intégrine-αEβ7-E-cadhérine jouent un rôle dans l’organisation de l’épithélium de la peau atteinte de psoriasis ainsi que dans la localisation spécifique à chaque organe des lymphocytes T dans l’épiderme [11,12].
|
Les psoriasiques ont également plus de cellules CD8+ TRM dans la peau non lésionnelle Lorsqu’elles sont actives, les cellules TRM CD8+ produisent les cytokines pro-inflammatoires IL-17 et IL-22, expriment le récepteur IL-23 et sont réactivées par l’IL-23. Vo et al. ont rapporté que les cellules CD8+ TRM sont enrichies à la fois dans la peau lésionnelle et non lésionnelle des personnes atteintes de psoriasis par rapport à la peau normale [15]. Cela suggère que ces cellules TRM favorisent la réactivation des inflammations latentes et donc la réapparition des lésions. Par conséquent, les nouveaux traitements du psoriasis visant à obtenir une rémission durable de la maladie devraient viser la déplétion des cellules pathogènes CD8+ TRM, selon une conclusion des chercheurs [16]. |
Pertinence pour la modification à long terme de l’évolution de la maladie
A l’avenir, on espère pouvoir modifier durablement la pathophysiologie du psoriasis grâce à des médicaments biologiques, en modulant les cellules TRM. Les premières indications suggèrent que l’inhibition de l’IL-23 inhibe l’activation des cellules TRM et empêche ainsi l’inflammation systémique à long terme. Dans l’étude ECLIPSE, une analyse des biopsies de lésions psoriasiques a montré que le nombre de cellules TRM CD8+ dans les efflorescences pouvait être réduit au niveau de la peau non lésionnelle après 24 semaines de traitement avec le guselkumab [13,14]. L’étude GUIDE examine l’hypothèse selon laquelle un traitement précoce par le guselkumab pourrait réduire l’accumulation de cellules TRM dans la peau et ainsi influencer positivement l’évolution à long terme de la maladie [18].
Congrès : Skin Inflammation & Psoriasis International Network
Littérature :
- “Pathogenetics : psoriasis vs atopic dermatitis”, session plénière 4, Prof. Dr Wolf Henning Boehncke, SPIN, Congrès du réseau international Skin Inflammation & Psoriasis, 07.07.2022.
- Clark RA : J Invest Dermatol 2011 ; 131 : 283-285.
- Gisondi P, et al : Expert Rev Clin Immunol 2020 ; 16 : 591-598.
- Gisondi P, et al : Ann Rheum Dis 2022 ; 81 : 68-73.
- Acosta Felquer ML, et al : Ann Rheum Dis. 2021 Ann Rheum Dis 2022 ; 81(1) : 74-79.
- von Stülpnagel CC, et al : J Eur Acad Dermatol Venereol 2021 ; 35 : 2166-2184.
- Iversen L, et al : J Eur Acad Dermatol Venereol 2018 ; 32 : 1930-1939.
- Puig L, et al : Br J Dermatol 2022 ; 186(5) : 773-781.
- Chen L, Shen Z : Cell Mol Immunol 2020 ; 17 : 64-75.
- Ho AW, Kupper TS : Nat Rev Immunol 2019 ; 19 : 490-502.
- Watanabe R, et al : Sci Transl Med 2015 ; 7:279ra39.
- Pauls K, et al : J Invest Dermatol 2001 ; 117 : 569-575.
- Warren RB, et al : J Eur Acad Dermatol Venereol 2021 ; 35 : 919-927.
- Mehta H, et al : J Invest Dermatol 2021 ; 141 : 1707-1718.
- Vo S, et al : Br J Dermatol 2019 ; 181:410-12.
- Armstrong AW, et al : Br J Dermatol 2020 ; 182 : 1484-1487.
- Vu TT, et al : J Clin Med 2021 ; 10(17) : 3822.
- Eyerich K, et al : BMJ Open 2021 ; 11(9) : e049822
DERMATOLOGIE PRAXIS 2022 ; 32(4) : 20 (publié le 21.8.22, ahead of print)