Ces dernières années, une meilleure compréhension de la pathogenèse des maladies psoriasiques a contribué à l’émergence d’une nouvelle génération de médicaments biologiques. Les représentants modernes actuellement autorisés de ce groupe de médicaments systémiques interagissent tous avec la réponse immunitaire Th17. La multiplicité des options thérapeutiques systémiques a rendu plus difficile le choix d’un traitement adapté à chaque individu.
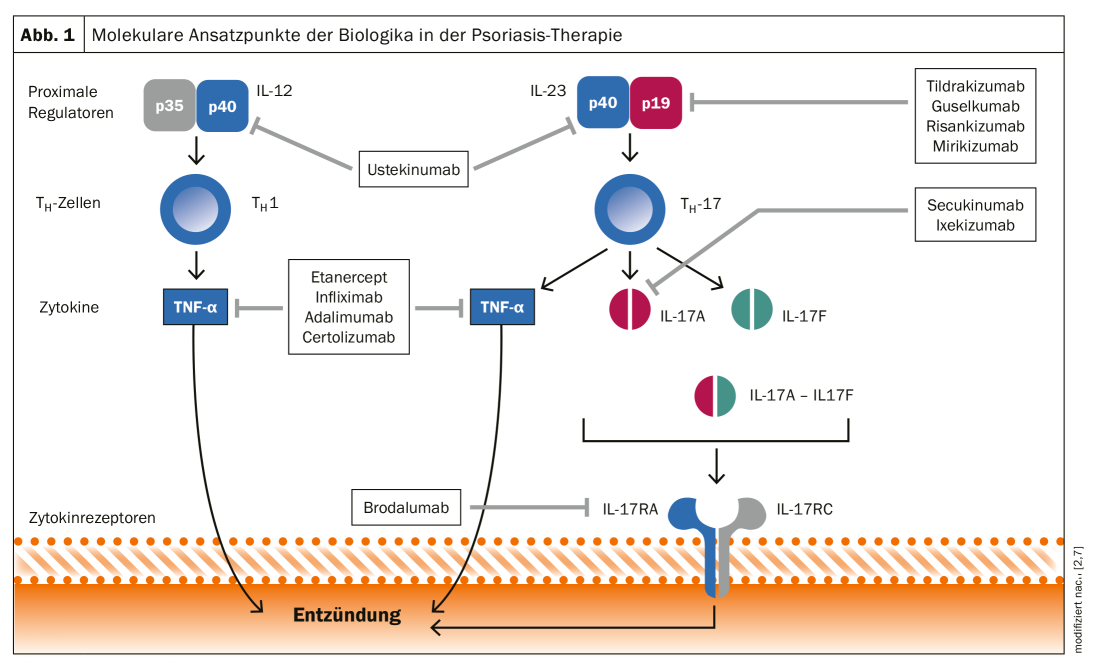
L’éventail des substances actives à usage systémique s’est considérablement élargi au cours des deux dernières décennies. Alors que l’éventail des traitements du psoriasis en plaques* modéré à sévère se limitait initialement aux thérapies systémiques orales que sont le méthotrexate, la ciclosporine, l’acitrétine, le fumarate de diméthyle et l’aprémilast, il existe aujourd’hui, outre les inhibiteurs du TNF-α, un grand nombre de produits biologiques et de biosimilaires plus modernes. Cette évolution repose sur une compréhension de plus en plus fine des bases pathogéniques du psoriasis. Comme on le sait aujourd’hui, la réponse immunitaire Th17 en particulier, avec ses cytokines IL23 et IL17, joue un rôle central [10]. C’est sur cette base que repose la nouvelle génération de produits biologiques qui interagissent avec la réponse immunitaire Th17 (Fig. 1) [2].
* BSA = Body Surface Area >10%, PASI = Psoriasis Area and Severity Index >10, DLQI = Dermatological Life Quality Index >10
Selon la compréhension actuelle, le psoriasis est considéré comme une maladie systémique dans laquelle il existe une mauvaise régulation génétique du système immunitaire et une auto-immunité contre les propres antigènes de la peau de l’organisme. Des troubles comorbides sont également fréquents. Outre les manifestations cutanées, l’arthrite psoriasique se caractérise par des douleurs articulaires rhumatismales. En outre, les maladies intestinales, l’obésité, le diabète et les maladies cardiovasculaires sont des comorbidités fréquemment rapportées. De plus, la prévalence des maladies mentales telles que les troubles anxieux et la dépression est également plus élevée chez les personnes atteintes de psoriasis. Alors que le PASI-50 ou le PASI-75 étaient des objectifs réalistes pour le traitement du psoriasis, le PASI-90 et le PASI-100 sont aujourd’hui dans le domaine du possible [3]. Cependant, avec le grand nombre de produits biologiques disponibles, le choix de la thérapie optimale pour le traitement du psoriasis modéré à sévère devient un défi.
Thérapie adaptée au patient
Les facteurs de décision pour la thérapie systémique peuvent être divisés en quatre clusters (aperçu 1) : Critères cliniques, caractéristiques des médicaments, caractéristiques des patients, autorisation de mise sur le marché et réglementation [8]. En plus des recommandations basées sur des preuves, d’autres critères doivent être examinés au cas par cas pour choisir le traitement. D’autres études sont nécessaires pour mieux comprendre des facteurs tels que l’efficacité à long terme, le délai de réponse, la sécurité et les effets sur les comorbidités. Des données empiriques valides peuvent faciliter la mise en place d’un traitement adapté à chaque patient, caractérisé par une absence d’apparition de la peau à long terme, une longue “survie médicamenteuse” et des taux élevés de satisfaction des patients [9]. Il est également important de prendre en compte les préférences des patients. En général, une amélioration rapide des symptômes cutanés et l’absence de lésions comptent parmi les principaux critères de réussite [1]. Selon les données du Swiss Dermatology Network of Targeted Therapies (SDTT), l’âge et le sexe sont des facteurs de stratification concernant les besoins des patients. Alors que les personnes de plus de 65 ans considèrent qu’il est important de réduire la fréquence des consultations médicales, de bien tolérer le médicament, ainsi que la qualité du sommeil et la confiance dans le traitement, les patients plus jeunes ont tendance à considérer qu’il est important que leur vie sociale ne soit pas entravée [1].

La perte d’efficacité comme défi
L’un des plus grands défis dans le développement des traitements systémiques du psoriasis concerne la perte d’efficacité secondaire des produits biologiques [3]. Après une certaine période de traitement, l’effet thérapeutique diminue, ce qui entraîne le passage à une autre substance active. On parle aussi dans ce contexte de “Drug survival”, c’est-à-dire la durée entre l’initiation d’un traitement et son arrêt [4,11]. Les prédicteurs de la “survie au médicament” peuvent être utiles pour le choix entre différents médicaments biologiques [11]. Une méta-analyse publiée en 2019 a identifié, à partir des données de 16 études de cohorte, différents prédicteurs (dont le sexe, l’obésité et l’arthrite psoriasique) qui se sont révélés pertinents pour l’arrêt ou la poursuite du traitement [12].
Il y a également une composante psychologique : Chez les personnes atteintes de psoriasis qui ont déjà subi plusieurs traitements biologiques différents, la connaissance d’une éventuelle nouvelle perte d’efficacité peut éclipser les scores de satisfaction des patients. Ce que l’on espère pour l’avenir, c’est un traitement systémique dont l’efficacité dure dix ans ou plus. En démontrant des résultats thérapeutiques durables à partir d’études à long terme, on se rapproche de cet objectif.
Les cibles moléculaires des différents médicaments biologiques
Le psoriasis est une maladie inflammatoire médiée par les lymphocytes T. Il se caractérise par une inflammation de la peau et des muqueuses. Le système immunitaire est activé et les cellules T helper (Th) produisent dans la peau différentes cytokines qui agissent sur les kératinocytes épidermiques, entraînant une prolifération excessive et une différenciation anormale des kératinocytes, caractéristiques du psoriasis, ainsi qu’une infiltration de cellules inflammatoires [2]. Les cellules Th17, qui produisent différents médiateurs de l’inflammation, jouent un rôle clé [5]. Des facteurs déclencheurs externes entraînent une interaction entre les kératinocytes résidents de la peau, les lymphocytes Th17 et les cellules dendritiques et macrophages dermiques [6]. L’activation des lymphocytes Th17 induit la libération de cytokines pro-inflammatoires telles que l’IL-17A, l’IL-17F, l’IL-22 et le facteur de nécrose tumorale (TNF)-α. Ceux-ci agissent à leur tour sur les kératinocytes et contribuent à l’hyperplasie épidermique, à l’acanthose et à l’hyperparakératose, ainsi qu’à l’activation endothéliale, ce qui entraîne un recrutement supplémentaire de cellules pro-inflammatoires telles que les granulocytes neutrophiles dans les tissus cutanés [6].
La stimulation par des facteurs déclencheurs tels que le stress, les infections ou le tabagisme peut déclencher la production d’IL-6 et d’IL-23 chez des personnes génétiquement prédéterminées, ce qui favorise la différenciation des cellules T CD4+ productrices d’IL-17A (cellules Th17). D’autre part, les cellules Th1 sont impliquées et produisent principalement de l’interféron-γ, ce qui a notamment pour conséquence la destruction des kératinocytes de la couche basale [5].
Les différentes cibles de différents représentants du groupe des produits biologiques sont schématisées dans la figure 1 [2]. Il existe désormais des antagonistes du TNF-α (adalimumab, certolizumab, étanercept et infliximab), mais aussi des anticorps anti-IL12/23 (ustékinumab), des inhibiteurs de l’IL17A (sécukinumab, ixekizumab) et des bloqueurs des récepteurs de l’IL17 (brodalumab), ainsi que des antagonistes de l’IL23 (risankizumab, guskumab, tildrakizumab) [6]. Alors que l’ustekinumab, un inhibiteur d’IL12/IL23, se lie à la sous-unité p40 des cytokines IL12 et IL23, les nouveaux inhibiteurs d’IL23 (risankizumab, guselkumab, tildrakizumab) inhibent la sous-unité p19 d’IL23.
Littérature :
- Maul JT, et al : Le genre et l’âge déterminent de manière significative les besoins des patients et les objectifs de traitement dans le psoriasis – une leçon pour la pratique. J Eur Acad Dermatol Venereol 2019, 33(4) : 700-708.
- Sator P : État de l’art : traitement du psoriasis vulgaire. Focus : Peau et rhumatismes, FdR 01|2019, 16.04.2019
- Yawalkar N : Psoriasis sans symptômes – le nouvel espoir pour les patients. Assemblée annuelle de la SSDP, Bâle 20.09.2019.
- Egeberg A, Bryld LE, Skov L : Drug survival of secukinumab and ixekizumab for moderate-to-severe plaque psoriasis. J Am Acad Dermatol 2019 ; 81(1) : 173-178.
- Eyerich K : Psoriasis – Où allons-nous ? Key Lecture 3, présentation de transparents, Prof. Dr. med. Kilian Eyerich, TU München, SGDV Assemblée annuelle, Bâle 20.09.2019.
- Wild J, Wegner J, Karbach S : De la peau au système vasculaire – le psoriasis et le risque cardiovasculaire. Cardiologue 2020 ; 14, 205-211.
- Bartlett HS, Million RP : Ciblage de la voie IL-17-T(H)17. Nat Rev Drug Discov 2015 ; 14(1) : 11-12.
- Augustin M : S09/04 Facteurs de différenciation dans la décision thérapeutique, JDDG 2019, https://onlinelibrary.wiley.com/doi/10.1111/ddg.13793
- Kamata M, Tada Y : Efficacité et sécurité des produits biologiques pour le psoriasis et l’arthrite psoriasique et leur impact sur les comorbidités : une revue de la littérature. Int J Mol Sci 2020 ; 21(5) : 1690.
- Volc S, Ghoreschi K : Bases physiopathologiques des thérapies systémiques du psoriasis. JDDG 2016. DOI : 10.1111/ddg.13050, https://onlinelibrary.wiley.com/doi/pdf/10.1111/ddg.13050_g
- Mourad A, et al : Factors predicting persistence of biologic drugs in psoriasis : a systematic review and meta-analysis. Br J Dermatol 2019 ; 181 : 450-458.
- Yiu ZZN : Drug survival of adalimumab, ustekinumab and secukinumab in patients with psoriasis : a prospective cohort study from the British Association of Dermatologists Biologics and Immunomodulators Register (BADBIR). BJD 2020 ; 183(2) : 294-302.
DERMATOLOGIE PRATIQUE 2020 ; 30(5) : 30-32