Au fil du temps, une multitude de nouveaux traitements de plaies et de pansements se sont accumulés. Dans le cadre de cet article, les auteurs présentent les principes du traitement local des plaies ainsi que quelques méthodes de traitement récentes.
Afin de pouvoir traiter la pathologie sous-jacente de manière adéquate, une évaluation des causes est la condition sine qua non de tout traitement des ulcères avant de commencer à traiter les plaies. De nombreuses études montrent que le traitement des facteurs causaux est beaucoup plus important que le traitement local pour permettre la guérison.
L’objectif de tout traitement local des plaies est de créer un environnement optimal pour la plaie, en créant un fond de plaie bien irrigué et stable avec peu d’exsudat. Ceci est obtenu en éliminant les cellules vieillissantes ou anormales, en réduisant la charge bactérienne, en réduisant l’exsudation de la plaie et en favorisant la formation de tissu granulaire et épithélial. En anglais, ces principes de traitement des plaies sont connus sous l’acronyme T.I.M.E. (tissue management, inflammation and infection control, moisture balance and epithelial (edge) advancement).
Débridement
Une plaie chronique stagne dans la phase inflammatoire de la cascade de cicatrisation. Il existe ainsi dans la plaie un environnement local qui ne permet qu’une cicatrisation limitée. Les dépôts de fibrine et les nécroses freinent la cicatrisation et constituent un terrain propice à la prolifération des micro-organismes.
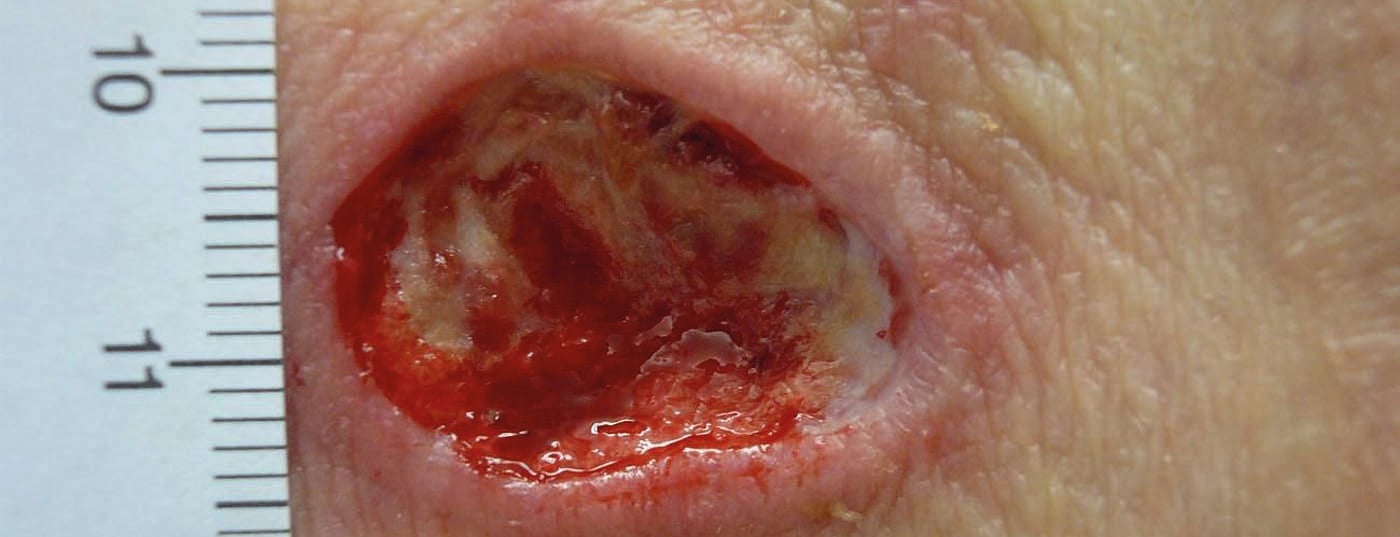
Le débridement permet d’éliminer les tissus avitaux, infectés et endommagés, favorisant ainsi la cicatrisation de la plaie et minimisant le risque d’infection (Fig. 1a et b).
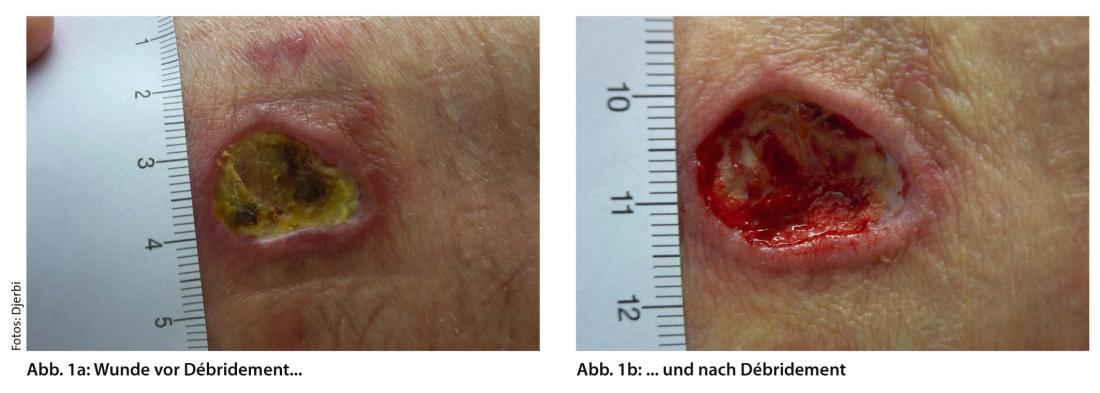
Le débridement peut en principe être effectué sur toutes les plaies, à l’exception du pyoderma gangraenosum, pour lequel on pourrait induire un élargissement de la plaie en raison du phénomène de pathergie. On distingue différentes formes de débridement (tab. 1). La méthode de débridement dépend de l’état du patient, de l’état de la plaie, des compétences de l’équipe de soins et des ressources disponibles.

Contrôle de l’inflammation et de l’infection
La charge microbienne d’une plaie peut aller d’une colonisation à une infection locale (colonisation critique), à une infection avec infiltration des tissus ou à une réaction systémique. De plus en plus de travaux montrent que des biofilms se forment sur les plaies chroniques et qu’ils nuisent à la cicatrisation. Il est recommandé de prélever un échantillon microbiologique de chaque nouvelle plaie afin de pouvoir commencer un traitement adéquat conformément à l’antibiogramme et d’exclure les germes multirésistants en cas de suspicion de colonisation ou d’infection.
Pour le traitement des plaies, les antiseptiques et les antibiotiques peuvent réduire la charge bactérienne. Les antiseptiques ont un spectre antimicrobien plus large et la résistance, qui est un problème important pour les antibiotiques sélectifs, est rare. De plus, les antibiotiques utilisés localement présentent un risque de sensibilisation allergique.
Certains antiseptiques, comme le PVP iodé concentré, sont toxiques pour les tissus et inhibent la formation du tissu de granulation. Lors de l’utilisation des antiseptiques les plus courants, tels que l’octenisept et le polihexanide, il convient de faire attention au temps d’action. Alors qu’Octenisept atteint son effet désinfectant au bout d’une minute, le polihexanide (PHMB) doit agir pendant au moins 10 à 15 minutes.
Il existe de multiples pansements qui contiennent des substances antiseptiques intégrées telles que l’argent, le PHMB, l’iode ou la chlorhexidine.
Outre les signes classiques d’infection, les patients souffrant de plaies chroniques doivent être attentifs aux signes discrets d’infection locale, tels que l’augmentation de la douleur, la progression de la taille de la plaie, l’augmentation de l’exsudat, l’excès de tissu de granulation rougeâtre facilement vulnérable ou la stagnation dans le processus de guérison. Si des signes cliniques clairs d’infection sont présents, tels que des symptômes systémiques, des rougeurs ou des échauffements, des antibiotiques systémiques doivent être utilisés.
Équilibre de l’hydratation et Stimulation de l’épithélialisation
On sait depuis quelques décennies que les plaies guérissent plus rapidement dans un milieu humide ; celui-ci favorise l’activité des facteurs de croissance, des cytokines et la migration cellulaire. De plus, le milieu humide de la plaie favorise le débridement autolytique et facilite ainsi le débridement de la plaie. Cependant, si l’exsudat de la plaie est trop important, il peut détruire les tissus nouvellement formés en raison d’une prédominance de protéases et inhiber les processus de cicatrisation et de macération de la peau environnante.
Les pansements doivent donc assurer un équilibre adéquat de l’humidité et empêcher à la fois la macération et le dessèchement du lit de la plaie (Fig. 2a et b).
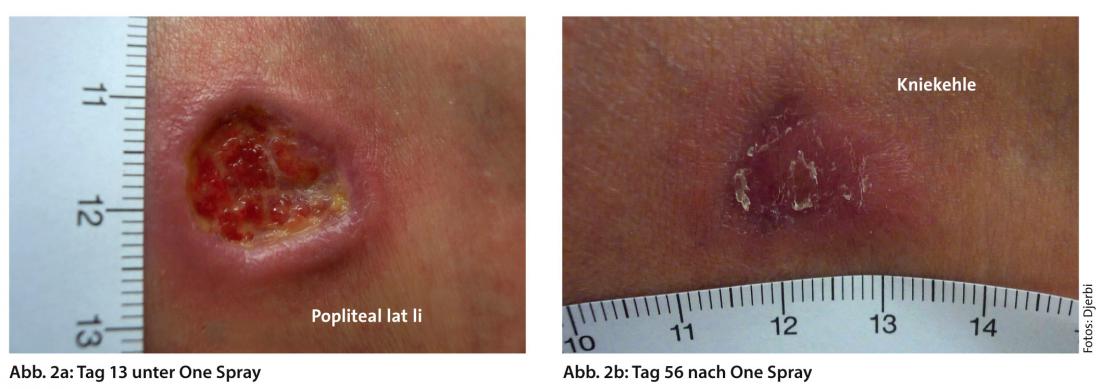
Le choix du pansement est crucial à cet égard, car certains pansements peuvent absorber de grandes quantités d’humidité (alginates, mousses), tandis que d’autres ont tendance à conserver ou à libérer l’humidité (hydrocolloïdes, hydrogels). Les pansements permettent de réduire les facteurs limitant la qualité de vie tels que la douleur, l’exsudation excessive et le fœtus. Le tableau 2 présente un aperçu des pansements les plus couramment utilisés.
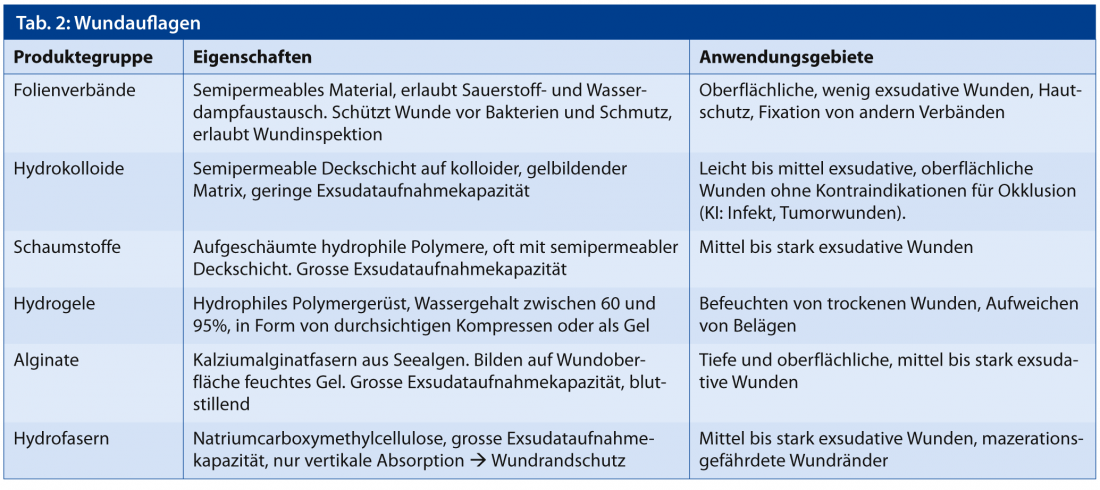
Outre les pansements courants, il existe sur le marché d’autres technologies et matériaux plus récents qui doivent être utilisés principalement en cas de retard de cicatrisation. Il s’agit notamment de la thérapie par pression négative, des matrices de collagène, des huiles végétales et des équivalents de peau vivante.
La thérapie par pression négative (également appelée “vacuum assisted closure therapy” ou “negative pressure wound therapy”) est une technologie éprouvée, en particulier pour les plaies très exsudatives. Après application d’une mousse sur la plaie, les sécrétions de la plaie sont régulièrement aspirées à l’aide d’une pompe. Cette méthode entraîne une réduction de l’exsudation excessive, de l’œdème, des micro-organismes et favorise la formation de tissu de granulation ainsi que la circulation sanguine. Ce traitement des plaies nécessite toutefois une certaine infrastructure et de l’expérience. Alors que l’expérience clinique montre une induction parfois impressionnante du tissu de granulation, les preuves d’une fermeture plus rapide des plaies ne sont pas claires pour tous les types de plaies.
Nouvelles options thérapeutiques
Comme mentionné ci-dessus, on pense que la production excessive de protéases inhibe la cicatrisation des plaies. C’est pourquoi des pansements tels que la matrice de modulation de la protéase (Promogran®, Promogran Prisma®, Urgo Start®) ont été développés pour réduire cette activité de manière prouvée. La réalisation d’un test rapide de la protéase permet de mieux décider du traitement.
Une matrice tridimensionnelle de collagène provenant de la muqueuse de l’intestin grêle de porc, qui facilite la croissance des cellules, peut également accélérer la cicatrisation de différents types d’ulcères. Les deux matrices sont complètement absorbées et ne doivent pas être retirées lors du changement de pansement.
Une autre nouvelle option thérapeutique est l’application d’un mélange d’huile de neem et d’huile de millepertuis. Les premières expériences cliniques montrent une induction impressionnante du tissu de granulation pour ces substances végétales, en particulier dans les plaies postopératoires. Il n’existe cependant pas encore d’études prouvant cette hypothèse.
Une méthode de traitement bien établie est la greffe de peau autologue de peau fendue ou de peau pleine. Cependant, comme cette opération est très coûteuse et ne peut pas être réalisée chez tous les patients, de nouveaux équivalents cutanés ont été développés, comme Epidex® et Apligraf®.
Alors que l’Epidex® est cultivé à partir des propres cellules du follicule pileux du patient, l’Apligraf® est obtenu à partir du prépuce d’un nouveau-né non patient. Certaines études ont montré un bénéfice de ces équivalents de peau vivante pour une cicatrisation plus rapide des plaies par rapport aux pansements conventionnels.
Toutefois, en raison de leur coût élevé, les directives de la SAfW et de la SGDV doivent être prises en compte avant d’utiliser les équivalents cutanés et la matrice de collagène, afin de garantir leur remboursement par l’assurance maladie (www.safw.ch/index.php/aktuell/bag-richtlinien).
Conclusion pour la pratique
Avant de traiter une plaie, il est nécessaire d’en déterminer la cause. En principe, il convient d’éliminer les tissus avitaux (débridement), de contrôler l’infection et l’inflammation et d’équilibrer l’humidité. Pour maintenir l’équilibre de l’humidité, la règle générale est humide sur sec et sec sur mouillé. Outre le traitement causal, les traitements d’accompagnement importants comprennent une analgésie adéquate, un soulagement de la pression et une alimentation adaptée/suffisante.
Nous recommandons à chaque praticien de se familiariser avec une sélection de pansements. Pour les pansements plus récents, les directives suisses doivent être prises en compte (www.safw.ch).
Dr. med. Nadia Djerbi
DERMATOLOGIE PRATIQUE 2013 ; 23(3) : 6-8