L’obligation de maintenance des dispositifs médicaux incombe à celui qui les utilise sur des tiers. Les violations de l’obligation de maintenance sont sanctionnées comme des délits par Swissmedic. La publicité pour les médecins doit être objective, répondre à un besoin du public et ne doit pas être trompeuse ou intrusive. Les informations qui servent principalement une fin en soi ne sont pas autorisées.
Les questions suivantes à l’interface de la médecine et du droit sont consacrées à trois aspects fréquents : L’obligation de maintenance et les défauts des dispositifs médicaux, les questions relatives à la légitimité de la publicité pour les médecins et les médicaments ou traitements, et les questions relatives à la prise en charge des coûts des médicaments et des traitements par les caisses d’assurance maladie.
À qui incombe l’obligation de maintenance ?
Selon l’art. 4 al. 1 let. b LPTh, les dispositifs médicaux sont “…des produits, y compris des instruments, des appareils, des dispositifs médicaux de diagnostic in vitro, des logiciels et d’autres objets ou substances, qui sont destinés ou annoncés comme étant à usage médical et dont l’action principale n’est pas obtenue par un médicament”.
L’obligation de maintenance des dispositifs médicaux incombe à la personne qui utilise le dispositif médical sur des tiers [1]. La maintenance doit être effectuée conformément aux instructions du premier responsable de la mise sur le marché. Il est recommandé de répertorier les dispositifs médicaux dans un registre qui indique clairement l’identification des appareils, le type et la fréquence de la maintenance ainsi que les personnes et les organismes responsables de la maintenance. En plus de ce registre, il est utile de tenir ce que l’on appelle un journal de l’équipement, dans lequel sont indiqués les mesures de maintenance prévues, les défauts ou pannes, les mesures prises et le résultat de la maintenance [2].
C’est la seule façon de prouver ultérieurement que l’obligation de maintenance a été remplie conformément à la loi. Les violations de l’obligation de maintenance sont sanctionnées comme des délits par Swissmedic [3].
Un cabinet médical a-t-il besoin d’un responsable de la protection laser ?
Si des traitements au laser de classe 3B ou 4 sont effectués dans un cabinet, un responsable de la protection laser doit être désigné par la direction de l’établissement. Le responsable laser doit établir un concept de sécurité et informer toutes les personnes qui travaillent avec des lasers des classes correspondantes sur les dangers ainsi que sur la manière correcte d’utiliser les appareils [4]. À des fins de preuve, il est recommandé d’établir un cahier des charges du responsable de la protection laser et de documenter le concept de sécurité [5].
Que faire en cas de dispositif médical défectueux ?
L’acheteur a l’obligation d’inspecter le produit à la réception et de signaler immédiatement les éventuels défauts au cocontractant. Une réclamation doit contenir les éléments suivants : une description aussi détaillée que possible du défaut et l’affirmation que la chose est reconnue comme non conforme au contrat en raison du défaut et que l’autre partie en est responsable [6]. Il est recommandé, à des fins de preuve, d’envoyer une notification de défaut par courrier recommandé à la partie contractante et de conserver une copie de la lettre ainsi que la preuve d’envoi de la poste. Le suivi des envois ne peut être consulté que pendant une période déterminée sur le site Internet de la Poste Suisse. Les données sont ensuite supprimées. Il est donc judicieux d’archiver également le suivi électronique des envois après la livraison, sous forme imprimée ou électronique au format PDF. La charge de la preuve de la ponctualité et de l’existence des défauts au moment de la conclusion du contrat incombe à l’acheteur. Les défauts qui ne peuvent être constatés qu’à un stade ultérieur (appelés vices cachés) doivent également faire l’objet d’une réclamation dès leur découverte. Dans tous les cas, la réclamation doit être faite immédiatement. Selon la jurisprudence, cela signifie généralement une réclamation dans les deux à trois jours ou, selon le défaut, dans les sept jours suivant l’examen de la chose ou la découverte du défaut [7]. En l’absence de réclamation immédiate, tous les droits de l’acheteur en matière de vices de la marchandise sont perdus [8].
Qu’est-ce qu’une publicité illicite et quelles en sont les conséquences ?
La LPMéd stipule que la publicité doit être objective, répondre à un besoin public et ne pas être trompeuse ou intrusive [9].
Si une publicité médicale ne répond pas à ces critères, il s’agit d’une violation des obligations professionnelles, sanctionnée par un blâme, un avertissement ou une amende pouvant atteindre 20 000 CHF, voire une interdiction d’exercer prononcée par l’autorité de surveillance cantonale [10]. Pour interpréter les obligations professionnelles, on peut se référer au code de déontologie [11]. Toutefois, une infraction au code de déontologie de la FMH n’entraîne pas nécessairement des conséquences disciplinaires en vertu de la loi sur les professions médicales. En effet, le code de déontologie est un droit associatif, qui ne peut donc s’appliquer qu’aux membres de l’association, contrairement aux obligations professionnelles, qui sont de droit public et doivent être respectées par tous les professionnels. Le code de déontologie prévoit comme sanctions le blâme, une amende pouvant aller jusqu’à CHF 50’000, la suspension de la qualité de membre pour une durée déterminée, l’exclusion de la société/FMH, la publication dans les organes de publication des sociétés cantonales de médecine, de l’ASMAC, de l’AMDHS ou de la FMH, la communication à la direction de la santé publique compétente ou aux organes d’assurance-maladie appropriés ainsi que la mise en place d’une supervision. Les différentes sanctions peuvent également être associées ou combinées entre elles [12].
Le code de déontologie de la FMH définit les informations autorisées comme suit : Les femmes médecins peuvent “[…] communiquer leurs qualifications professionnelles ainsi que toute autre information nécessaire au patient ou au collègue, de manière réservée et discrète”. [13] et doivent ” […] s’abstenir, dans le cadre de leur activité médicale, de toute publicité non objective, fondée sur des allégations mensongères ou de nature à porter atteinte à la réputation de la profession de médecin […] “. [14] et de s’engager “[…] à ce qu’aucun tiers ne se livre à une publicité illicite à son profit direct ou indirect”. [15].
Une information est considérée comme nécessaire si sa connaissance permet au patient de choisir plus facilement un médecin approprié [16]. Les directives “Information et publicité” (tab. 1) mentionnent explicitement différentes informations considérées comme nécessaires.

Les informations qui, par exemple, servent à l’autopromotion du médecin et ont pour but premier de faire de la publicité sont interdites [17]. La publication d’informations sous forme d’envois en masse tels que les envois postaux ou les médias électroniques à la population n’est pas autorisée [18]. Du point de vue de la déontologie, il serait sans doute problématique qu’un médecin fasse connaître au grand public des informations générales sur sa pratique via un compte Twitter public [19]. En vertu du code de déontologie, il serait également interdit, le cas échéant, de proposer des traitements sur des plateformes d’achat numériques.
En outre, la loi sur les produits thérapeutiques interdit la publicité auprès du public pour les médicaments soumis à prescription médicale [20]. Des rapports faisant la promotion d’une maladie et de l’indication d’un médicament – sans mentionner le nom de ce dernier – peuvent déjà être qualifiés de publicité auprès du public illicite si le tableau clinique est indissociable du remède, de sorte que l’un des termes renvoie inévitablement à l’autre [21]. Le critère déterminant est l’impression générale de la façon dont le public est objectivement interpellé [22]. La publicité illicite pour les médicaments est sanctionnée par Swissmedic en tant que contravention [23].
Qu’est-ce que la publicité autorisée pour les traitements à la toxine botulique ?
Les règles de publicité relatives aux produits thérapeutiques sont strictes en ce qui concerne la toxine botulique. Par exemple, un site Internet qui vantait les possibilités d’utilisation et les modes d’action de la toxine botulique et qui contenait des liens vers des articles de presse et des publicités a été qualifié de publicité grand public illicite. Il a été reproché à l’exploitant du site web de présenter la toxine botulique comme un principe actif fascinant et l’utilisation hors étiquette comme une méthode “moderne et particulièrement efficace”, ainsi que de ne pas faire correspondre les effets secondaires avec les informations correspondantes sur les médicaments, minimisant ainsi le principe actif afin d’inciter les clients à se faire traiter contre les rides avec des produits contenant le principe actif de la toxine botulique [24]. Swissmedic déclare que “seules les informations de nature générale sur la santé ou sur les maladies” [25] sont autorisées. Il est important que les informations ne se rapportent pas directement ou indirectement à un médicament spécifique. La désignation de la substance active “toxine botulique” peut être utilisée comme titre d’une rubrique ou dans l’explication du terme “traitement au Botox” au sein d’un texte courant [25]. En aucun cas, les promotions spéciales pour les traitements à la toxine botulique, qui ont un impact sur le prix des traitements, ne sont autorisées [26].
Quels sont les médicaments pris en charge par l’assurance maladie ?
Les médicaments qui doivent être pris en charge par l’assurance de base sont explicitement réglementés par la loi. L’Office fédéral de la santé publique établit la liste des spécialités, dans laquelle figurent les produits, y compris leur coût, qui sont pris en charge au maximum par l’assurance de base. Il s’agit d’une liste exhaustive, ce qui signifie que si un produit ne figure pas sur la liste, l’assurance de base refusera de le prendre en charge. Une prise en charge par une assurance complémentaire souscrite n’est toutefois pas exclue. La prise en charge des coûts dépend de l’assurance complémentaire concernée.
La liste actuelle des spécialités peut être consultée en ligne sur www.spezialitätenliste.ch. La fonction de recherche comprend les noms des préparations, les titulaires des autorisations de mise sur le marché ou les substances actives.
Quels sont les traitements pris en charge par l’assurance maladie ?
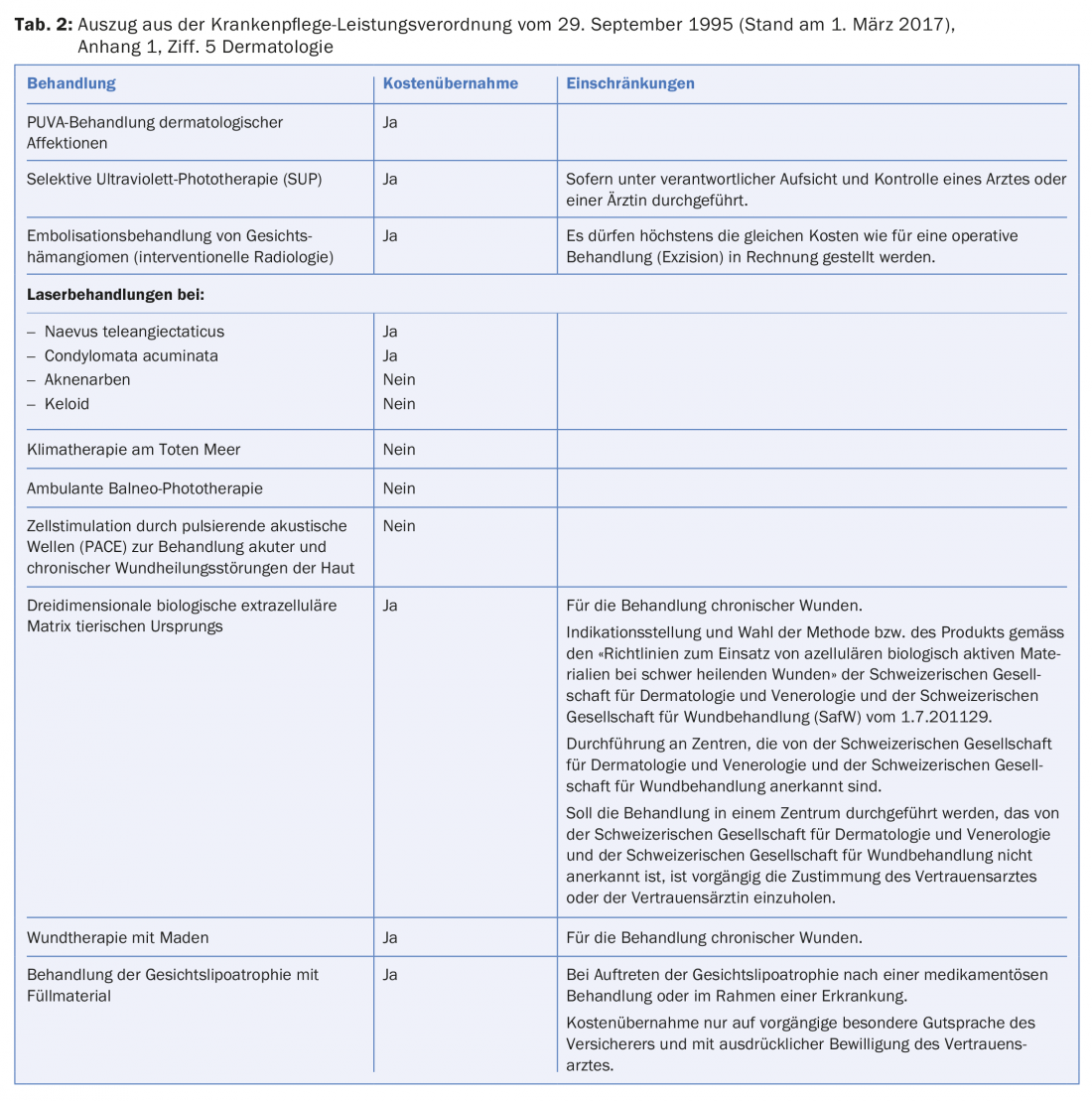
Il n’existe pas de liste exhaustive pour les prestations médicales. Cependant, la caisse d’assurance maladie doit en principe prendre en charge une prestation dermatologique parce qu’elle est supposée répondre aux critères d’efficacité, d’adéquation et d’économicité. Ces critères sont présupposés pour la prise en charge des coûts par l’assurance de base [27]. La caisse d’assurance maladie peut refuser la prestation en démontrant que ces critères ne sont pas remplis. Or, l’annexe 1 de l’Ordonnance sur les prestations de l’assurance des soins contient une liste de traitements qui comporte une énumération obligatoire non exhaustive des prestations médicales obligatoires ou non. Par exemple, le traitement PUVA des affections dermatologiques est pris en charge par l’assurance maladie, alors que la balnéo-photothérapie ambulatoire ne l’est pas (tableau 2) [28].
Messages Take-Home
- L’obligation de maintenance des dispositifs médicaux incombe à celui qui les utilise sur des tiers.
- Les violations de l’obligation de maintenance sont sanctionnées comme des délits par Swissmedic.
- Les cabinets qui effectuent des traitements au laser de classe 3B ou 4 doivent désigner un responsable de la protection laser.
- La publicité pour les médecins doit être objective, répondre à un besoin du public et ne doit pas être trompeuse ou intrusive. Les informations qui servent principalement une fin en soi ne sont pas autorisées.
- Il convient de faire preuve de retenue dans les informations et les mesures publicitaires concernant le traitement à la toxine botulique.
- L’ordonnance sur les prestations de soins contient une réglementation claire sur la prise en charge des coûts de certains traitements dermatologiques.
Sources :
- Art. 49 al. 1 LPTh ; art. 20 ODim ; feuille d’information de l’Institut suisse des produits thérapeutiques, Dispositifs médicaux : Maintenance, retraitement, modification par des professionnels, état juin 2005, p. 1.
- Cf. fiche d’information de l’Institut suisse des produits thérapeutiques, Dispositifs médicaux : Maintenance, retraitement, modification par des professionnels, état juin 2005, p. 2 et suivantes.
- Cf. art. 86 al. 1 lit. f LPTh.
- Directive CFST n° 6508, directive MSST du 14 décembre 2006 (état au 1er janvier 217), ch. 2 en relation avec l’annexe 2. Annexe 1 ; SUVA, Attention, rayon laser !, p. 12 ; voir également la norme de sécurité laser EN 60825-1.
- Cf. SUVA, Attention, rayon laser !, p. 12.
- Cf. 101 II 84 s. E. 3 ; 107 II 175 E. a.
- Voir par exemple l’arrêt du TF 4C.82/2004 ; l’arrêt du TF 4D_25/2010.
- Voir pour l’ensemble les articles 197 et suivants du Code civil.
- Art. 40 lit. d LPMéd.
- Art. 43 al. 1 MedBG.
- Message relatif à la loi fédérale sur les professions médicales universitaires (LPMéd) du 3 décembre 2004, p. 228.
- Art. 43 StaO FMH.
- Art. 20 al. 1 StaO FMH.
- Art. 20 al. 2 StaO FMH.
- Art. 20 al. 3 StaO FMH.
- Chiffre. 1.1. L’annexe 2 du Code de déontologie de la FMH (“StaO FMH”) contient les directives “Information et publicité”.
- Chiffre. 2.3. Annexe 2 du StaO FMH.
- Chiffre. 3.2. Annexe 2 du StaO FMH.
- Keller Claudia, Chapitre 4 : Droit de la publicité, dans : Médias sociaux et droit pour les entreprises, ch. marg. 4.26.
- Art. 32 al. 2 lit. a LPTh.
- Arrêt du BVerwG C-546/2010 ; ATF 129 V 32.
- Arrêt du BVerwG C-546/2010 ; arrêt du BGer 2A.63/2006.
- Art. 87 al. 1 lit. b HMG.
- Voir l’arrêt du BVerwG C-546/2010.
- Swissmedic, Aide-mémoire AW, Toxine botulique – Lignes directrices, Botox : information versus publicité, p. 1.
- Cf. Swissmedic, notice AW, toxine botulique – lignes directrices, Botox : information versus publicité, p. 3.
- ATF 129 V 167, consid. 3.2 ; ATF 125 V 28 consid. 5b.
- Cf. ch. 5 Dermatologie, annexe 1 de l’OPAS.
DERMATOLOGIE PRATIQUE 2017 ; 27(3) : 25-28