Les dermatoses cutanées auto-immunes avec formation de bulles font partie des maladies rares et sont souvent mortelles en l’absence de traitement. Un traitement intensif permet d’améliorer considérablement le pronostic et la qualité de vie des personnes concernées. Comme le montre une analyse de données de patients récemment publiée, l’obtention d’un contrôle de la maladie est un objectif thérapeutique réalisable, bien que cela nécessite des stratégies individuelles et puisse impliquer plusieurs changements de traitement. Pour contrer la réaction immunitaire dysfonctionnelle contre les protéines structurelles de l’organisme, il existe aujourd’hui différentes possibilités d’intervention médicamenteuse.
Ce qui est vrai pour de nombreuses autres maladies dermatologiques l’est tout particulièrement pour le pemphigus vulgaire, une dermatose auto-immune : choisir et mettre en œuvre le traitement le plus adapté à chaque individu parmi les nombreuses possibilités de traitement est la clé du succès. Margitta Worm de la Charité Berlin, a donné un aperçu actuel de la maladie pemphigus dans le cadre du FOMF Allergologie et Dermatologie Hofheim (D) et a présenté les principaux points des directives pour le diagnostic et le traitement de la pemphigoïde bulleuse et du pemphigus vulgaire/foliaceus, révisées en 2019 par la Société allemande de dermatologie. [1,2]. Les deux sont des maladies rares avec une “charge de morbidité” élevée.

Détection des auto-anticorps comme étalon-or du diagnostic
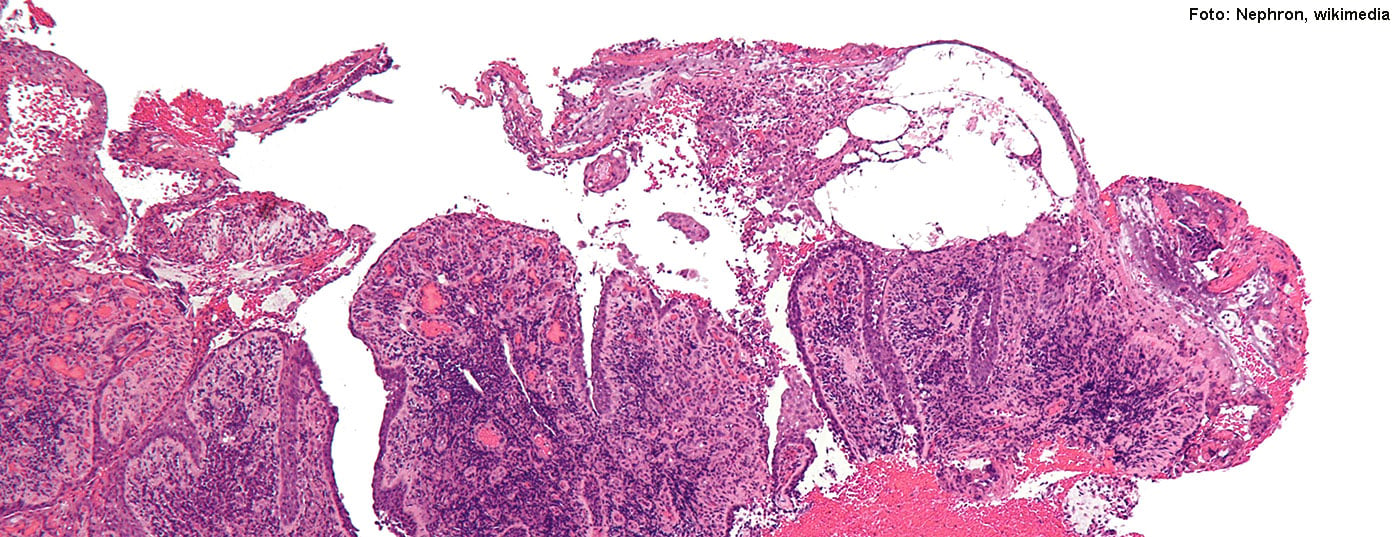
Le pemphigus vulgaire est, avec la pemphigoïde bulleuse, le principal représentant des dermatoses auto-immunes bulleuses (fig. 1A, C). Environ 80% des pemphigus sont des pemphigus vulgaires, qui apparaissent généralement entre la 4e et la 6e décennie , la deuxième variante la plus fréquente étant le pemphigus foliacé, les autres formes étant très rares [2]. Le diagnostic est réalisé par une combinaison de différentes méthodes. En cas de suspicion clinique, outre les examens histopathologiques (Fig. 1B) , il est recommandé de procéder à un test in vivo des immunoglobulines autoréactives par immunofluorescence directe et de détecter les auto-anticorps pathologiques par un diagnostic sérologique. Selon les lignes directrices, les tests les plus appropriés sont les tests ELISA antidesmogléine 3 et antidesmogléine 1 ( 1). Les auto-anticorps pathologiques jouent un rôle important dans le mécanisme pathologique des maladies pemphigus. Alors que dans le pemphigus vulgaire, les auto-anticorps dirigés contre la desmogléine 3 provoquent la formation d’une fente suprabasale sur les muqueuses, dans le pemphigus foliacé, seuls les auto-anticorps contre la desmogléine 1 sont détectables, ce qui se traduit cliniquement par le fait que seule la peau kératinisée est atteinte, et non les muqueuses.(encadré). En l’absence de traitement, les pemphigus peuvent être mortels, généralement en raison des infections provoquées par les lésions cutanées ouvertes. Un traitement intensif permet de réduire la dangerosité de la maladie et d’améliorer considérablement la qualité de vie. Pour cela, des rendez-vous de contrôle réguliers chez le dermatologue sont nécessaires [3].

Les glucocorticoïdes et les immunomodulateurs non stéroïdiens sont les principaux piliers du traitement de première ligne
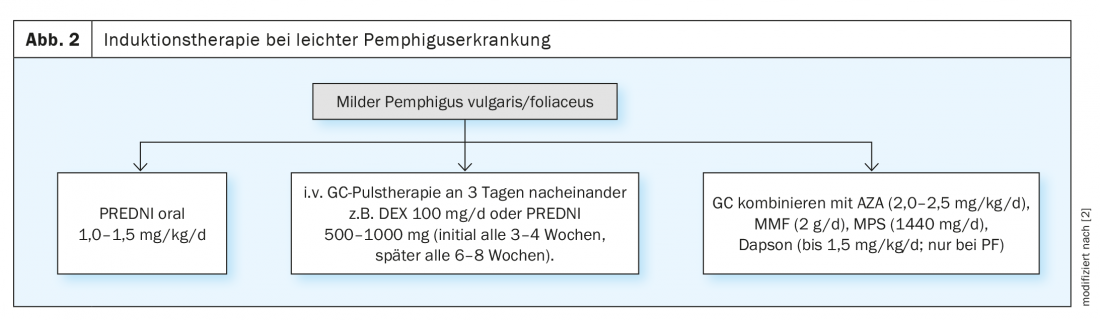
Le traitement de la pemphigus dépend de la sévérité et du type d’atteinte de la maladie ainsi que des comorbidités liées au traitement. Un aperçu compact est présenté dans les figures 2 et 3. Pour atténuer les défenses immunitaires excessives de leur propre organisme, la plupart des personnes atteintes doivent subir une immunosuppression à long terme à l’aide de médicaments administrés par voie systémique. L’objectif thérapeutique du traitement d’induction est de contrôler l’activité de la maladie, ce qui est considéré comme atteint lorsqu’aucune nouvelle lésion n’apparaît et que l’on observe un début de guérison des lésions existantes [2]. La ligne directrice recommande d’associer les corticostéroïdes à un agent immunosuppresseur non stéroïdien, comme l’azathioprine ou le mycophénolate mofétil. Au lieu de comprimés de cortisone, les glucocorticostéroïdes peuvent également être administrés en perfusion [2,4]. La “thérapie pulsée à la dexaméthasone” consiste à perfuser de la dexaméthasone dans la veine pendant trois jours consécutifs, ce qui est d’abord répété toutes les trois à quatre semaines, puis à des intervalles plus importants. Pour prévenir les effets secondaires de la cortisonothérapie, tels que les ulcères gastro-intestinaux, on utilise généralement des inhibiteurs de la pompe à protons. Pour prévenir l’ostéoporose, une supplémentation en calcium et en vitamine D3 peut être envisagée, ainsi qu’une ostéodensitométrie tous les deux ans si nécessaire. Parallèlement au traitement systémique, des mesures de traitement externe sont également importantes, comme par exemple des bains de bouche, des pommades et des compresses ou des compresses antiseptiques.

Le rituximab bientôt disponible en Suisse comme traitement de deuxième ligne ?
Si l’objectif thérapeutique n’est pas atteint par l’utilisation de glucocorticoïdes en association avec des immunomodulateurs/immunosuppresseurs, les options thérapeutiques de seconde ligne sont les immunoglobulines intraveineuses à haute dose ou la procédure d’immuno-absorption (lavage de sang). En cas de pemphigus vulgaire/foliacé modéré ou sévère, un traitement systémique avec un anticorps anti-CD20 (par ex. rituximab) associé à la prednisolone est recommandé comme traitement d’induction, en alternative aux options de traitement déjà mentionnées. Une étude publiée en 2017 a montré que chez les patients atteints de pemphigus vulgaire/foliacé, l’administration de rituximab permettait d’obtenir la guérison de toutes les lésions de la peau et des muqueuses dans 90% des cas [2]. Le rituximab est déjà autorisé dans l’UE pour le traitement du pemphigus modéré et sévère. En Suisse, une demande d’autorisation pour cette indication est actuellement en cours d’examen par Swissmedic [5]. Pour passer du traitement d’induction au traitement d’entretien, aucune nouvelle lésion ne doit apparaître au cours d’une phase de consolidation de deux semaines et environ 80% des lésions initiales doivent être guéries [2].

Conclusion d’une étude rétrospective : le contrôle de la maladie est réalisable
Une analyse des données des patients publiée en 2020 par des chercheurs de la Charité Universitätsmedizin de Berlin et de l’hôpital universitaire du Schleswig-Holstein a révélé que la majorité des patients parvenaient à un bon contrôle de la maladie sur une période de deux ans, mais qu’il existait de grandes différences individuelles en ce qui concerne les stratégies thérapeutiques ciblées [6]. Les chercheurs ont examiné rétrospectivement les données de 77 patients atteints de pemhigus (81% de pemphigus vulgaire, 19% de pemphigus foliacé) avec des consultations répétées concernant la médication, la posologie, l’activité de la maladie, la raison d’un changement de traitement et les concentrations d’auto-anticorps. L’analyse a montré que 86% des patients ont atteint le contrôle de la maladie (“presque sans lésions” ou “sans lésions”) après une moyenne de 2 ans de traitement, avec une moyenne de 4 régimes thérapeutiques différents utilisés au cours de cette période. La grande dispersion des données reflète la variabilité de l’évolution de la maladie et du traitement, la durée du contrôle de la maladie allant de 0 à 11 ans et le nombre de changements de traitement variant de 1 à 18. Les chercheurs ont également constaté que les concentrations d’antidesmogléine 3 et d’antidesmogléine 1 étaient corrélées à la gravité de la maladie mais pas au nombre de changements de traitement. En conclusion de leur étude, les auteurs concluent que l’identification d’un traitement efficace et sûr pour chaque patient atteint de pemphigus est un défi et nécessite souvent de la patience. Afin d’optimiser les options de traitement adaptées aux patients, des paramètres prédictifs permettant de prédire la réponse au traitement seraient nécessaires.
Pour plus d’informations sur les implications de la coronapandémie pour les pemphigus, veuillez consulter le site www.pemphigus.org.
Source : FomF (D) Dermatologie et Allergie 2020
Littérature :
- Worm M : Reconnaître et traiter les dermatoses bulleuses. Margitta Worm FOMF de dermatologie et d’allergologie, Hofheim (D), 11.09.2020.
- AWMF : Diagnostic et traitement du pemphigus vulgaire/foliacé et de la pemphigoïde bulleuse. Numéro d’enregistrement 013-071. www.awmf.org
- Cabinet de dermatologie au Alleecenter Remscheid (D), www.hautaerzte-remscheid.de/faq-15/autoimmunerkrankung-pemphigus-vulgaris.html
- Centre des dermatoses bulleuses auto-immunes : traitement des dermatoses bulleuses auto-immunes, Clinique universitaire du Schleswig-Holstein, Clinique de dermatologie, d’allergologie et de vénérologie (Clinique dermatologique), www.uksh.de
- Swissmedic : Journal Swissmedic 07/2020, www.swissmedic.ch (dernière consultation 17.2.2021)
- Scarpone R, et al. : Therapy Changes During Pemphigus Management : A Retrospective Analysis. Frontiers in Medicine 2020 ; https://doi.org/10.3389/fmed.2020.581820
- Mindorf S, et al : La détection de routine des autoanticorps antidesmocolline sériques n’est utile que chez les patients atteints de pemphigus atypique. Exp Dermatol 2017 ; 26(12) : 1267-1270.
- Xuan RR, Yang A, Murrell DF : New biochip immunofluorescence test for the serological diagnosis of pemphigus vulgaris and foliaceus : A review of the literature. International journal of women’s dermatology 2018 ; 4(2) : 102-108. Epub 2018/06/07
DERMATOLOGIE PRAXIS 2021 ; 31(1) : 41-43 (publié le 23.2.21, ahead of print)