Les options thérapeutiques immunomodulatrices modernes permettent une réduction beaucoup plus importante et rapide des symptômes par rapport au passé. Pour contrôler le risque de réactivation d’une infection par une hépatite antérieure, il convient d’effectuer des tests appropriés.
L’hépatite B (VHB) est l’une des maladies infectieuses les plus courantes. En l’absence de traitement, des complications graves telles que l’insuffisance hépatique sont possibles. Il s’agit d’une maladie virale qui se manifeste généralement de manière aiguë, mais il existe également des évolutions chroniques. Dans une revue publiée en 2019 dans le JAAD, il est recommandé d’effectuer un dépistage chez tous les patients atteints de psoriasis avant de commencer un traitement systémique, y compris les paramètres suivants : Anticorps anti-core de l’hépatite B (anti-Hbc), antigène de surface de l’hépatite B (HbsAg) et anticorps anti-VHC (anti-HCV) [1].
La prophylaxie, un facteur important
En cas d’AgHbs+ ou de risque élevé/moyen de réactivation de l’hépatite B (HBVr), un traitement prophylactique avec un analogue de nucléos(t-id) (entécavir, ténofovir) est proposé avant/au début du traitement systémique. En cas de risque faible, un suivi de l’ADN du VHB est suffisant. Si les résultats sont négatifs pour l’AgHBs et l’anti-HBc, la vaccination préventive est la meilleure méthode de prévention [2,3]. Les résultats sont variables en ce qui concerne les profils de risque concrets des différentes substances actives par rapport au VHBr.
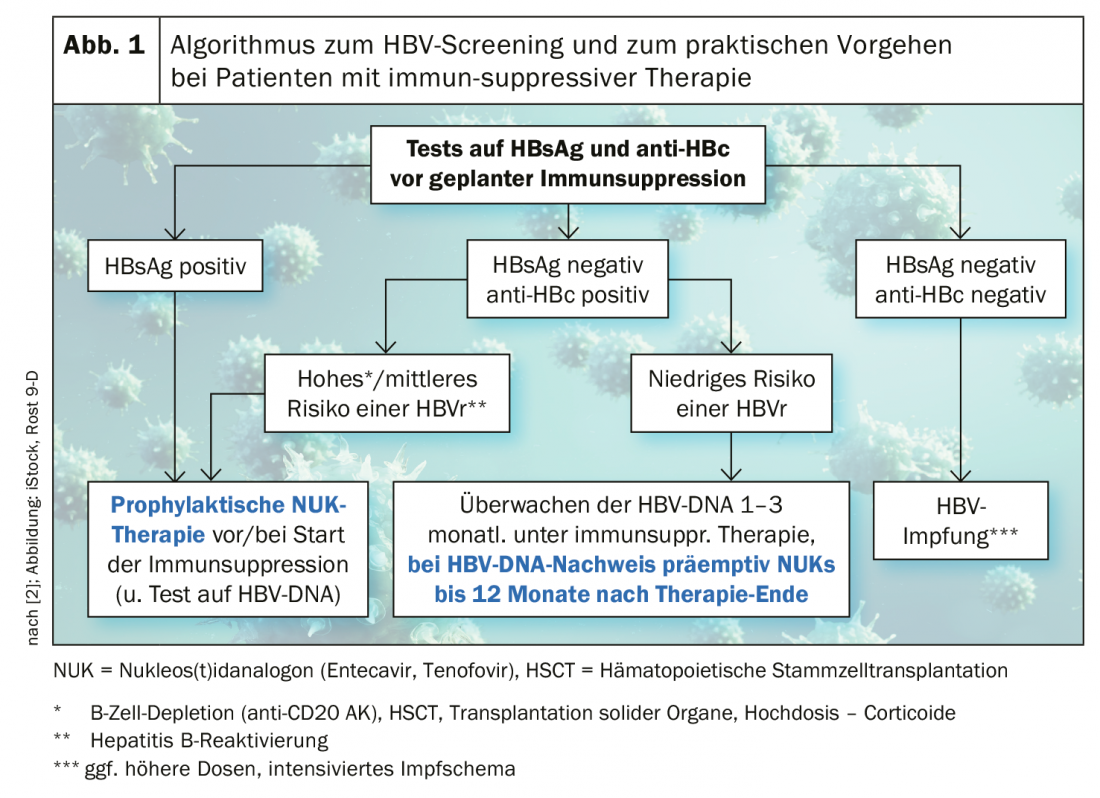
En ce qui concerne le méthotrexate (MTX), on sait qu’il existe un risque accru de VHBr [1,4,5]. Il n’existe à ce jour aucune donnée fondée sur des preuves concernant l’apremilast et le diméthylfumarate. En ce qui concerne les inhibiteurs du TNF-alpha, une étude a montré que 39% des patients testés positifs pour les marqueurs du VHB présentaient une réactivation de l’ADN sérique du VHB, et que le taux de réactivation était plusieurs fois plus élevé chez les sujets anti-HBc+ que chez les porteurs d’AgHBs+ [6]. En ce qui concerne les antagonistes de l’interleukine, les données empiriques sont jusqu’à présent plutôt limitées. Une étude de cohorte prospective sur l’ustékinumab a démontré que le VHBr était relativement rare sous cet inhibiteur d’IL12/23 [7]. Les données sont basées sur un échantillon de 93 patients traités par ustékinumab pendant 24 ± 12 mois entre 2011 et 2016. A l’état de référence, tous les sujets ont été soumis à un test sérologique et un test ADN du VHB a été effectué chaque année. Parmi les 54 sujets qui étaient porteurs d’un VHB inactif ou guéri ou qui présentaient un résultat anti-HBC+ isolé, seuls 3 patients ont connu une réactivation virologique.
| Message Take-Home Plusieurs lignes directrices internationales recommandent de procéder à un dépistage de l’hépatite avant de commencer un traitement systémique du psoriasis [4]. Selon les résultats, une vaccination préventive ou une prophylaxie antivirale peuvent être envisagées. Les thérapies systémiques qui interfèrent avec le système immunitaire peuvent être associées à un risque de réactivation d’infections antérieures par l’hépatite. Les données empiriques concernant les profils de risque des différentes substances actives à cet égard sont encore peu nombreuses. Un monitoring régulier des valeurs hépatiques permet de contrôler ce facteur et, le cas échéant, de prendre les mesures appropriées. |
Le suivi des tests hépatiques est essentiel
Selon les directives S3 actuelles de l’AWMF, les traitements systémiques contre le psoriasis doivent être évités pendant une hépatite B aiguë jusqu’à ce que l’infection ait pu être contrôlée par un traitement antiviral [4].
Il n’existe pas de vaccin contre l’hépatite C (VHC), mais les médicaments antiviraux permettent de guérir 90% des personnes traitées [8]. Le méthotrexate est contre-indiqué en cas de VHC en raison de son potentiel hépatotoxique et de sa tendance à favoriser la réplication virale [4]. Bonifati et al. recommandent de réaliser un monitoring des tests hépatiques ainsi que de la charge virale du VHC tous les 3 à 6 mois et d’envisager une collaboration interdisciplinaire avec l’hépatologie si nécessaire [9].
Littérature :
- Kaushik SB, Lebwohl MG : Psoriasis : Quel traitement pour quel patient : J Am Acad Dermatol 2019 ; 80(1) : 43-53.
- Zachoval R : Prévention de la réactivation de l’hépatite B, Hepatitis &more 1/2017.
- Lockwood SJ, Prens LM, Kimball AB : Karger Kompass Dermatol 2017 ; 5 : 195-199. DOI : 10.1159/000481335, www.karger.com/Article/Pdf/481335
- AWMF 2017, www.awmf.org/uploads/tx_szleitlinien/013-001l_S3_Therapie_Psoriasis-vulgaris_2017-12.pdf
- Patterson AT : JAAD 2020 ; 82(2) : 532.
- Perez-Alvarez R, et al : Medicine (Baltimore) 2011 ; 90 : 359-371.
- Ting S-W, Chen Y-C, Huang Y-H. Clin Drug Investig 2018, doi:10.1007/s40261-018-0671-z.
- Office fédéral de la santé publique Suisse (OFSP) : www.bag.admin.ch
- Bonifati C, Lora V, Graceffa D, Nosotti L : World J Gastroenterol 2016 ; 22 : 6444-6455.
- EADV : Kirby B : Psoriasis treatment, diaporama, Professeur Brian Kirby, MD FRCPI, Congrès EADV, Madrid, 12.10.2019.
DERMATOLOGIE PRATIQUE 2020 ; 30(3) : 26