Le nombre de personnes atteintes de diabète continue d’augmenter. Selon une estimation de la Fédération internationale du diabète, environ 592 millions de personnes seront touchées en 2035. Cette maladie s’accompagne d’un risque accru de mortalité, surtout si elle est insuffisamment traitée. Un aperçu pratique de la meilleure stratégie thérapeutique individuelle possible.
Le nombre de patients atteints de diabète continue d’augmenter. Selon une estimation de la Fédération internationale du diabète, le nombre de personnes atteintes passera de 382 millions en 2013 à 592 millions en 2035 dans le monde [1]. La maladie s’accompagne d’un risque accru de mortalité. Ainsi, une personne de 50 ans atteinte de diabète perd en moyenne six années de vie par rapport à une personne en bonne santé, dont une grande partie en raison de maladies cardiovasculaires [2]. Des thérapies de plus en plus efficaces et adaptées à chaque individu tentent de contrer ce risque. En 2008, il a été démontré que les patients âgés de 55 ans atteints de diabète de type 2 et présentant une microalbuminurie pouvaient bénéficier d’un traitement intensif du diabète avec de multiples combinaisons de médicaments et des adaptations du mode de vie. L’incidence de la mortalité a diminué de 46% dans le groupe d’intervention (p=0,02) [3]. Il ressort de ces données qu’une approche thérapeutique réussie est une approche multimodale. En fonction des résultats, inclut l’arrêt du tabac, la réduction des lipides à l’aide de statines, le contrôle de la tension artérielle à l’aide d’inhibiteurs de l’ECA/de sartans, la prévention secondaire à l’aide d’aspirine en présence de maladies cardiovasculaires et, bien entendu, le traitement du diabète dans le concept global.
Étape par étape
Roger Lehmann, directeur du service de diabétologie de la clinique d’endocrinologie, de diabétologie et de nutrition clinique de l’hôpital universitaire de Zurich.
Étape 1 : Définition de l’objectif individuel HA1c
Étape 2 : Déterminer le meilleur traitement individuel : définir les préférences personnelles et les priorités médicales
Étape 3 : Penser en termes de classes de substances – à partir de là, utiliser le médicament avec le meilleur niveau de preuve.
Outre les résultats cliniques, les souhaits du patient sont également déterminants pour une planification et une mise en œuvre réussies du traitement. Les exigences suivantes sont souvent formulées du point de vue du patient :
- l’absence d’hypoglycémie
- la prévention de la prise de poids
- une préférence pour l’administration orale plutôt que l’injection
- une administration hebdomadaire de préférence à une administration quotidienne
- réduire au maximum le nombre total de comprimés nécessaires (privilégier les thérapies combinées)
La prise en compte de ces préférences personnelles est en partie déterminante pour le maintien de la motivation du patient et donc pour le succès du traitement envisagé.
Quatre questions importantes
Outre les préférences personnelles, les circonstances cliniques concomitantes sont également un facteur à prendre en compte lors de la détermination de l’action médicamenteuse contre le diabète. Pour déterminer le meilleur traitement individuel, le professeur Lehmann a fourni aux cliniciens un catalogue de quatre questions.
La première chose à faire est de déterminer s’il existe un déficit en insuline . Celui-ci se manifeste par une hyperglycémie symptomatique, qui se traduit cliniquement par une polyurie, une polydipsie, une perte de poids et un manque de volume, avec dans le pire des cas un risque de décompensation métabolique. Si c’est le cas, le patient a besoin d’insuline. En principe, il existe différents schémas au choix, du principe du bolus de base à l’insuline mixte avec composants à action longue et courte, en passant par la combinaison d’insuline mixte et de GLP-1 RA. Selon l’intervenant, l’étape 3 consiste à favoriser l’insuline mixte, et plus particulièrement Tresiba, car elle est supérieure à l’insuline standard Lantus en termes de prévention des hypoglycémies sévères et nocturnes et de réduction du MACE (major adverse cardiovascular events) en trois points. Le cas échéant, l’insuline peut être administrée de manière temporaire et éventuellement arrêtée au cours du traitement individuel du diabète sucré de type 2.
La deuxième question clinique porte sur le débit de filtration glomérulaire (DFG). Si le DFG est <30 ml/min, il convient d’administrer des inhibiteurs de la DPP-4 et, si nécessaire, de l’insuline basale en complément. Cette combinaison représente toutefois un compromis, car elle peut entraîner des hypoglycémies et une prise de poids. Parmi les inhibiteurs de la DPP-4, la linagliptine serait à privilégier, car elle ne nécessite pas d’ajustement de dose au DFG mentionné.
Si le DFG est compris entre >45-60 ml/min, la metformine est recommandée en premier lieu, avec une association précoce avec des inhibiteurs du SGLT2 ou, si l’IMC est de >28 kg/m², une association avec le GLP-1 RA. Le professeur Lehmann a souligné qu’une combinaison précoce avec des doses plus faibles est plus judicieuse et souvent moins sujette aux effets secondaires qu’une monothérapie avec une augmentation constante de la dose. Si cette combinaison ne suffit pas à atteindre l’objectif fixé conjointement, il est également possible d’ajouter un inhibiteur de la DPP-4 ou de l’insuline basale ou du gliclazide, représentant des sulfonylurées. Il convient de noter que la combinaison de plusieurs médicaments ayant le même mécanisme d’action ne présente aucun avantage. Il convient donc de s’abstenir d’associer GLP-1 RA et inhibiteurs de la DPP-4. Le GLP-1 RA et les inhibiteurs du SGLT2 sont particulièrement indiqués en cas d’altération de la fonction rénale, car plusieurs études ont démontré que ces médicaments avaient un effet néphroprotecteur en plus d’une réduction de la mortalité [4–6]. Les inhibiteurs du SGLT2 ont l’avantage de pouvoir être pris par voie orale et le coût du traitement est moins élevé que celui des agonistes des récepteurs du GLP-1, qui doivent être injectés. L’orateur a cité l’empagliflozine parmi les inhibiteurs du SGLT2 et le liraglutide et le semaglutide dans le groupe des GLP-1RA comme les médicaments présentant les meilleures preuves.
Si le DFG chute à >30 à <45 ml/min, seule la moitié de la dose de metformine doit être administrée.
Outre la question de la fonction rénale, la présence d’une maladie cardiovasculaire est également déterminante pour le choix du médicament. Si elle est avérée, on peut procéder de la même manière que celle recommandée pour un DFG >45-60 ml/min. Même chez les patients asymptomatiques, c’est-à-dire non diagnostiqués pour la plupart, cette approche ne change guère. Seule la première ligne de traitement bénéficie ici d’une option supplémentaire avec l’association directe de metformine et d’inhibiteurs de la DPP-4, en plus des possibilités d’association déjà mentionnées ci-dessus. L’escalade se fait avec le gliclazide (sulfonylurée) ou l’insuline basale.
La quatrième question clinique est de savoir si le patient diabétique souffre d’une insuffisance cardiaque . Si répond par l’affirmative, la metformine associée aux inhibiteurs du SGLT2 est le premier choix.
Au cours de l’évolution, des inhibiteurs de la DPP-4 ou, par la suite, de l’insuline basale peuvent être ajoutés.
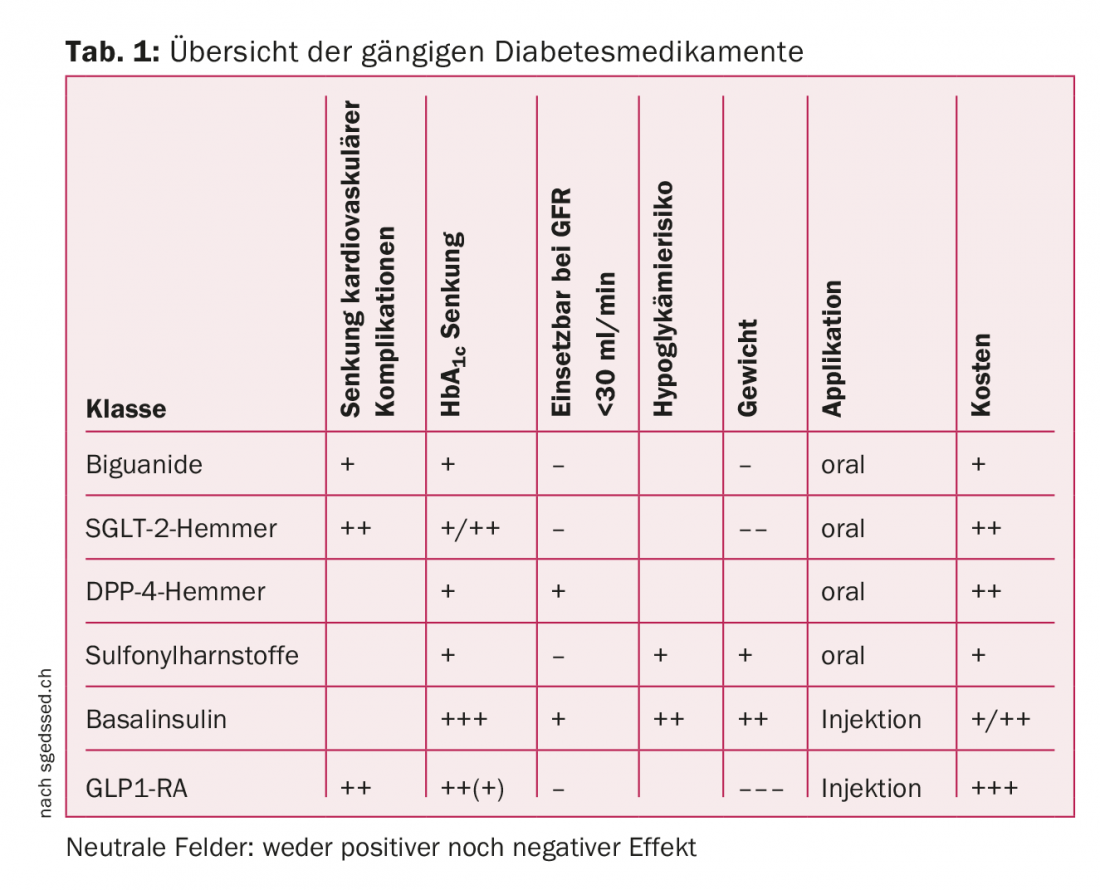
Le tableau 1 donne un aperçu des différents médicaments mentionnés.
Take-Home
Le professeur Lehmann a souligné, sur la base des données disponibles, l’importance des inhibiteurs du SGLT2 et du GLP 1 RA dans le régime thérapeutique du diabète de type 2. Dans de grandes études en point final, l’empagliflozine (GLP 1 RA) et le liraglutide (inhibiteur du SGLT 2) ont pu démontrer une réduction de la mortalité globale et cardiovasculaire, une néphroprotection ainsi qu’un bénéfice supplémentaire dans le cadre du traitement multifactoriel du diabète grâce à leur effet favorable sur l’évolution du poids et le risque d’hypoglycémie. [4–6]. Il convient de discuter explicitement avant le début du traitement du fait que les inhibiteurs du SGLT-2 présentent un risque accru de développer des infections urogénitales en raison de la glucosurie.
Si les résultats cliniques ou les souhaits du patient changent au cours du traitement, le régime thérapeutique établi doit être reconsidéré. Selon le conférencier, l’intensification du traitement en temps opportun est décisive pour un traitement adéquat. Si celle-ci est retardée d’un an et que la glycémie est mal contrôlée, cela entraîne une augmentation significative des événements cardiovasculaires [7].
Source : Medidays Zurich, 4-8 septembre 2017
Littérature
- www.idf.org/diabetesatlas, 6e édition, 2013
- Rao Kondapally Seshasai S, et al : Diabetes mellitus, fasting glucose, and risk of cause-specific death. N Engl J Med 2011 ; 364(9) : 829-841.
- Gaede P, et al : Effect of a multifactorial intervention on mortality in type 2 diabetes. N Engl J Med 2008 ; 358(6) : 580-591.
- Marso SP, et al : Liraglutide and Cardiovascular Outcomes in Type 2 Diabetes. N Engl J Med 2016 ; 375(4) : 311-322.
- Zinman B, et al : Empagliflozin, Cardiovascular Outcomes, and Mortality in Type 2 Diabetes. N Engl J Med 2015 ; 373(22) : 2117-2128.
- Wanner C, et al : Empagliflozin and Progression of Kidney Disease in Type 2 Diabetes. N Engl J Med 2016 ; 375(4) : 323-334.
- Paul SK, et al : Delay in treatment intensification increases the risks of cardiovascular events in patients with type 2 diabetes. Cardiovasc Diabetol 2015 ; 14 : 100.
CARDIOVASC 2017 ; 16(5) : 36-38
PRATIQUE DU MÉDECIN DE FAMILLE 2017 ; 12(10) : 36-38











