Les symptômes cutanés sont, avec l’atteinte articulaire, l’une des atteintes d’organes les plus fréquentes du lupus érythémateux disséminé (LED). Les diagnostics de laboratoire indiquent la présence d’autres anticorps en plus des ANA positifs. Si les patients sont suspectés d’avoir une CLE, le CLASI peut être utilisé – un test court validé pour évaluer l’activité de la maladie. Pour confirmer le diagnostic de suspicion clinique, une preuve histologique est obligatoire, l’immunofluorescence directe ou les tests de photoprovocation sont moins utilisés.
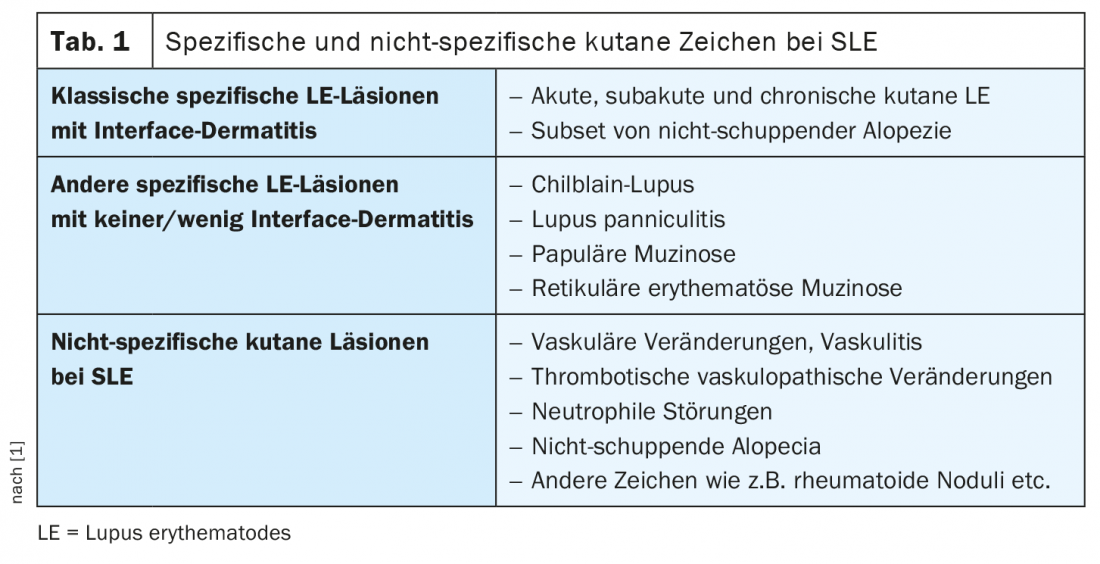
Le fait qu’un grand nombre de modifications cutanées spécifiques et non spécifiques puissent être associées au lupus érythémateux disséminé (LED) (tableau 1) représente un défi, selon le professeur Luca Borradori, médecin-chef de la clinique universitaire de dermatologie de l’Hôpital de l’Île à Berne [1]. Pour exclure une atteinte extracutanée, des examens de laboratoire – y compris des anticorps antinucléaires (ANA), des tests de la fonction rénale et des anticorps antiphospholipides – sont indiqués en plus de l’anamnèse et de l’inspection clinique. Dans environ 10 à 15% des cas, le lupus érythémateux cutané (LEC) est la première manifestation du LED. Les patients devraient être informés de cela, souligne le conférencier. L’éducation des patients est généralement importante pour les patients atteints de LEC. Le test “CLASI” (“The Cutaneous Lupus Erythematosus Disease Area and Severity Index”), réalisable en quelques minutes, est un outil de diagnostic idéal pour la première ou la deuxième consultation. Ce score clinique validé évalue d’une part la présence d’érythèmes, de squames et d’hypertrophie et d’autre part la dyspigmentation, la cicatrisation ou l’atrophie.
Examen histopathologique – à quoi faut-il faire attention ?
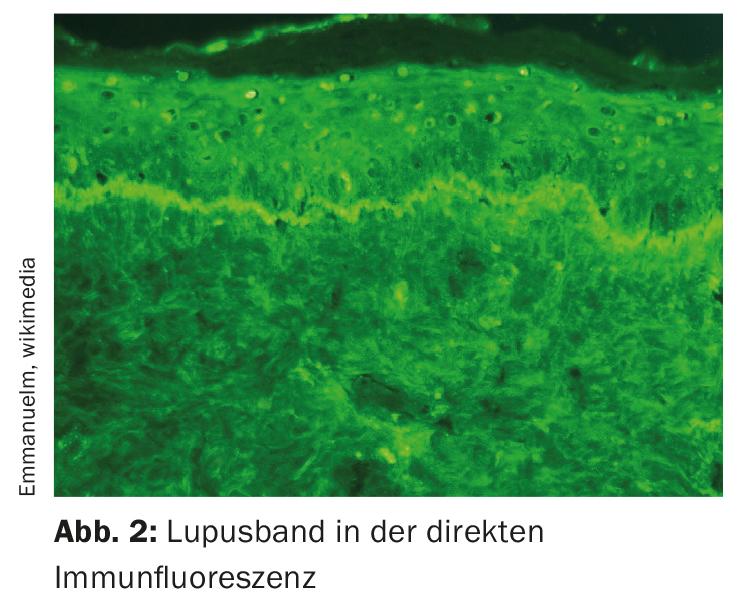
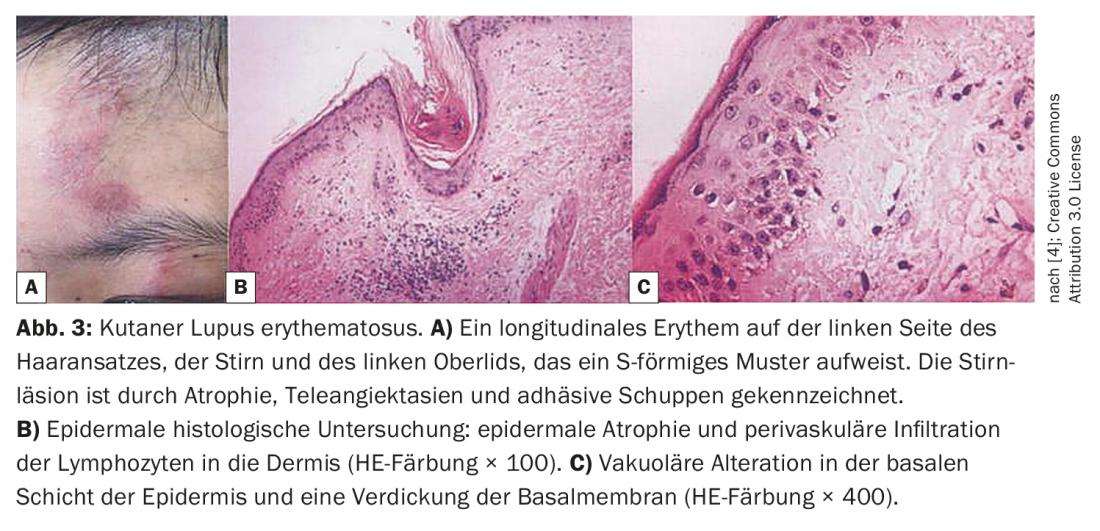
Si les examens cliniques sont en faveur du diagnostic de CLE, il convient de procéder à une évaluation histologique – à la fois des lésions typiques et atypiques – pour s’en assurer. On trouve soit une dermatite d’interface, soit une dégénérescence vacuolaire de la couche cellulaire basale, soit des inflitres lymphocytaires et périvasculaires. Il ne faut pas oublier qu’il existe des CLE sans atteinte particulière de la zone de jonction dermo-épidermique ou sans dermatite d’interface, explique le professeur Borradori [1]. C’est le cas, par exemple, de la panniculite ou du lupus de Chilblain et, bien sûr, du lupus tumidus, qui ne s’accompagne que d’infiltrats lymphocytaires. L’immunofluorescence directe n’est utilisée que lorsque le diagnostic de CLE n’est pas clair. L’orateur cite en exemple certains cas d’alopécie cicatricielle dans lesquels il est extrêmement difficile de distinguer le lichen du lupus. Pour ces cas particuliers, l’immunofluorescence pourrait être très utile. Les tests de photoprovocation sont une autre méthode parfois utilisée dans le cadre d’une évaluation diagnostique de l’ECL. Dans environ 60% des cas, il permet de détecter une sensibilité à la lumière chez les patients atteints de lupus.
Contrôles de laboratoire – quels paramètres déterminer et à quelle fréquence ?
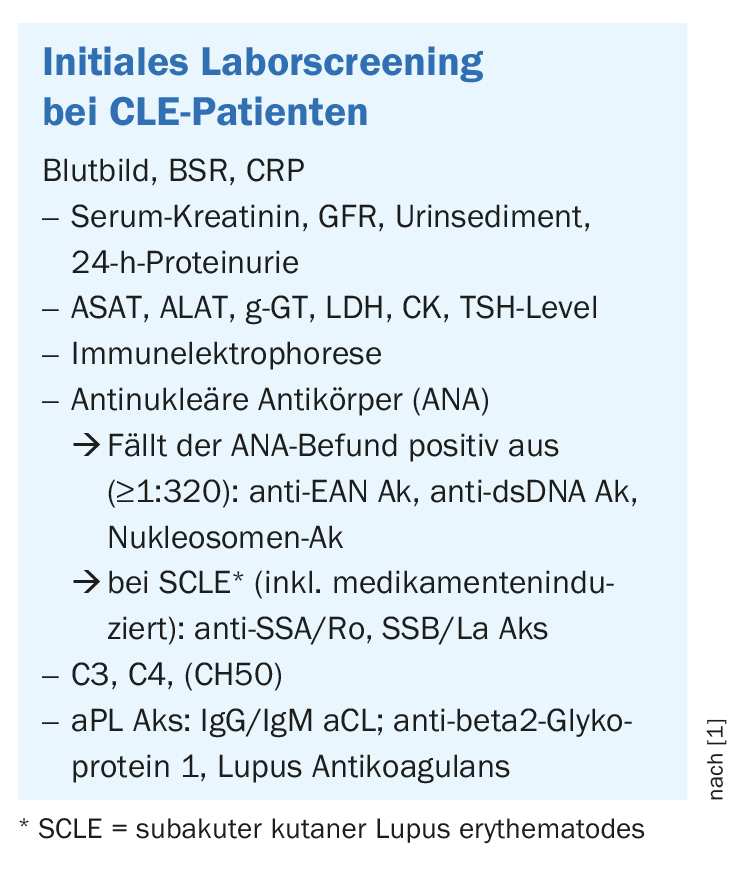
Si les patients présentent des signes d’un possible lupus érythémateux cutané, les mesures initiales en laboratoire présentées dans l’encadré sont recommandées afin de mieux évaluer une éventuelle implication des organes et d’identifier les patients présentant un risque accru de développer un lupus érythémateux systémique [1]. Si le résultat de l’ANA est positif, les titres seraient souvent faibles (≤1:320). L’ADN anti-ds et l’abs anti-Sm ne sont pas caractéristiques du LED, mais sont généralement associés au LED. Il est également important de déterminer les anticorps antiphospholipides (Ak) suivants : Ac anti-cardiolipine IgG/IgM, Ac anti-bêta-2-glycoprotéine, Ac anti-lupus anticoagulant. Ils sont également mentionnés dans les critères de classification du LED de l’ACR/SLICC/EULAR. Dans le cas de la LEC, il n’y a un résultat positif que dans environ 5% des cas, mais il est important de rechercher ces anticorps, car ces patients ont un risque accru d’accidents cérébrovasculaires, de complications thrombotiques ou de problèmes de valves cardiaques, souligne l’orateur. En outre, les patients atteints de LED/LEA et d’anticorps antiphospholipides ne doivent pas prendre d’anticonceptionnels contenant des œstrogènes. Il n’existe pas de recommandation fondée sur des preuves concernant la fréquence des contrôles de laboratoire au cours de l’évolution, a déclaré le professeur Borradori. Son conseil à ce sujet est de procéder à un examen de laboratoire au moins une fois par an, même chez les patients présentant des symptômes légers et limités d’ECL. Chez les patients présentant une activité élevée de la maladie et des symptômes supplémentaires, il est généralement recommandé de déterminer les paramètres de laboratoire suivants au cours de l’évolution [1] :
- Petite numération sanguine, vitesse de sédimentation, créatinine, débit de filtration glomérulaire (DFG), analyse d’urine, protéinurie, C3, C4
- anti-ANA, anti-ds DNA, ENA Screen
- pour certaines thérapies médicamenteuses : éventuellement d’autres examens de laboratoire
- en fonction des antécédents médicaux et des caractéristiques cliniques : éventuellement d’autres examens hémotologiques, rénaux, cardiopulmonaires, neurologiques, musculosquelettiques
Quels sont les signes avant-coureurs du développement d’un LED ?
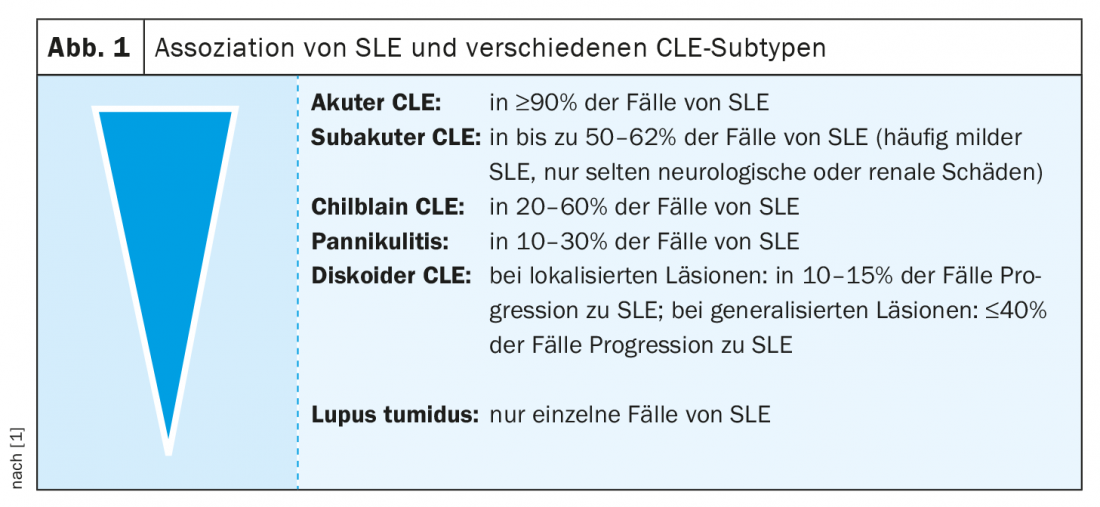
Les patients atteints de LED qui souffrent d’arthralgies/d’arthrite ou qui présentent des signes d’anémie, une forte augmentation des paramètres inflammatoires, des modifications de la formule sanguine ou des titres élevés d’ANA sont des indices d’une progression potentielle vers le LED. “Ce sont généralement des signes d’alerte”, résume le professeur Borradori [1]. Le risque de LED dépend entre autres de la sous-forme de CLE (Fig. 1). En cas d’érythème papillaire comme manifestation d’un LED aigu, le risque de progression vers un LED est relativement élevé. La panniculite est diagnostiquée dans 10 à 30% des cas au cours d’un LED. En revanche, si les lésions cutanées sont localisées et n’affectent qu’une seule partie du corps, par exemple le visage, le risque serait relativement faible. Par exemple, dans le cas d’un LED discoïde, la probabilité de développer un LED dans les 5 à 10 ans à venir est d’environ 10 à 15%. “Un lupus tumidus n’est pratiquement jamais associé à un LED”, ajoute le conférencier.
Quelles sont les mesures prophylactiques recommandées ?
Les rayons UV sont considérés comme l’un des principaux facteurs déclencheurs du lupus érythémateux [2]. Les patients atteints de lupus doivent donc se protéger du soleil, en particulier pendant les mois de printemps et d’été. Il s’agit notamment d’utiliser des produits de protection solaire avec un indice de protection élevé. Une supplémentation en vitamine D est recommandée pour tous les patients atteints de LEC [3]. Le tabagisme étant un facteur de risque de développement du LED et d’aggravation des lésions cutanées, il est conseillé d’arrêter de fumer. En ce qui concerne les vaccinations, les experts suggèrent que les patients âgés soient surtout vaccinés contre le pneumocoque et la grippe. Chez les personnes âgées de plus de 50 ans, la vaccination contre le zona doit également être envisagée. Il est conseillé de vérifier les antécédents médicamenteux de tous les patients atteints de lupus subaigu ou aigu. Un lupus induit par un médicament peut régresser après l’arrêt de la prise du produit.
Congrès : SwissDermaDay
Littérature :
- Borradori L : Le lupus érythémateux cutané (LEC) : diagnostic et suivi pratique. Dr. med. Luca Borradori, SwissDermaDays, 13.01.2022.
- Kuhn A, Beissert S. Photosensibilité dans le lupus érythémateux. Autoimmunité 2005 ; 38(7) : 519-529.
- Cutillas-Marco E, et al : Vitamin D and cutaneous lupus erythematosus : effect of vitamin D replacement on disease severity. Lupus 2014 ; 23(7) : 615-623.
- Xin R, et al : Lupus érythémateux : Perspectives dermatologiques sur la diversité, 20 août 2019, DOI : 10.5772/intechopen.88446
DERMATOLOGIE PRATIQUE 2022 ; 32(1) : 38-39