Certaines caractéristiques morphologiques des kératoses actiniques (KA) sont considérées comme prédictives du développement d’un carcinome épidermoïde invasif. La classification des scores PRO I-III est basée sur ce principe, ce qui correspond à trois niveaux de risque
pour le risque de progression des lésions AK. Une étude publiée en 2023 montre qu’une classification automatisée PRO-Score basée sur l’IA et sur les données d’imagerie LC-OCT a le potentiel de faciliter le diagnostic et le suivi des AK à l’avenir.
L’un des objectifs de l’étude de Thamm et al. était d’entraîner les réseaux de neurones convolutionnels à être utilisés pour la segmentation épidermique automatisée dans des ensembles de données d’images de tomographie par cohérence optique à champ linéaire confocal (LC-OCT), afin d’évaluer en temps réel la pathologie épidermique et dermique des lésions AK [1]. Les AK sont considérés comme des carcinomes épidermoïdes in situ qui peuvent évoluer vers des carcinomes épidermoïdes cutanés (CES) invasifs. L’évaluation du risque de progression des lésions AK par imagerie LC-OCT présente des avantages par rapport à l’histologie classique, car il s’agit d’une méthode non invasive de haute technologie. Macroscopiquement, les lésions AK apparaissent comme des taches roses à brunes dans les zones de peau exposées au soleil et elles sont généralement accompagnées d’une hyperkératose [2]. Alors que dans les AK, l’atypie des kératinocytes est limitée à l’épiderme, on peut au contraire observer dans le SCC la perte de la zone de jonction dermoépidermique (DEJ), ce qui définit sa prolifération invasive [3]. Bien que la DEJ reste intacte dans les lésions AK, ses modèles de croissance basaux changent au cours du processus de transformation maligne [4]. Il est de plus en plus important d’évaluer quelles AK présentent un risque élevé de développer une transformation maligne. C’est pourquoi une classification histologique a été développée, le PRO-Score, qui classe les AK en fonction des changements dans la zone de prolifération basale [4,5]. Les lésions AK PRO III sont associées à un risque plus élevé de développer un SCC invasif que les lésions PRO II ou PRO I. Les lésions AK PRO II sont associées à un risque plus élevé de développer un SCC invasif que les lésions AK PRO I.
Analyse d’images à l’aide d’une approche d’apprentissage en profondeur
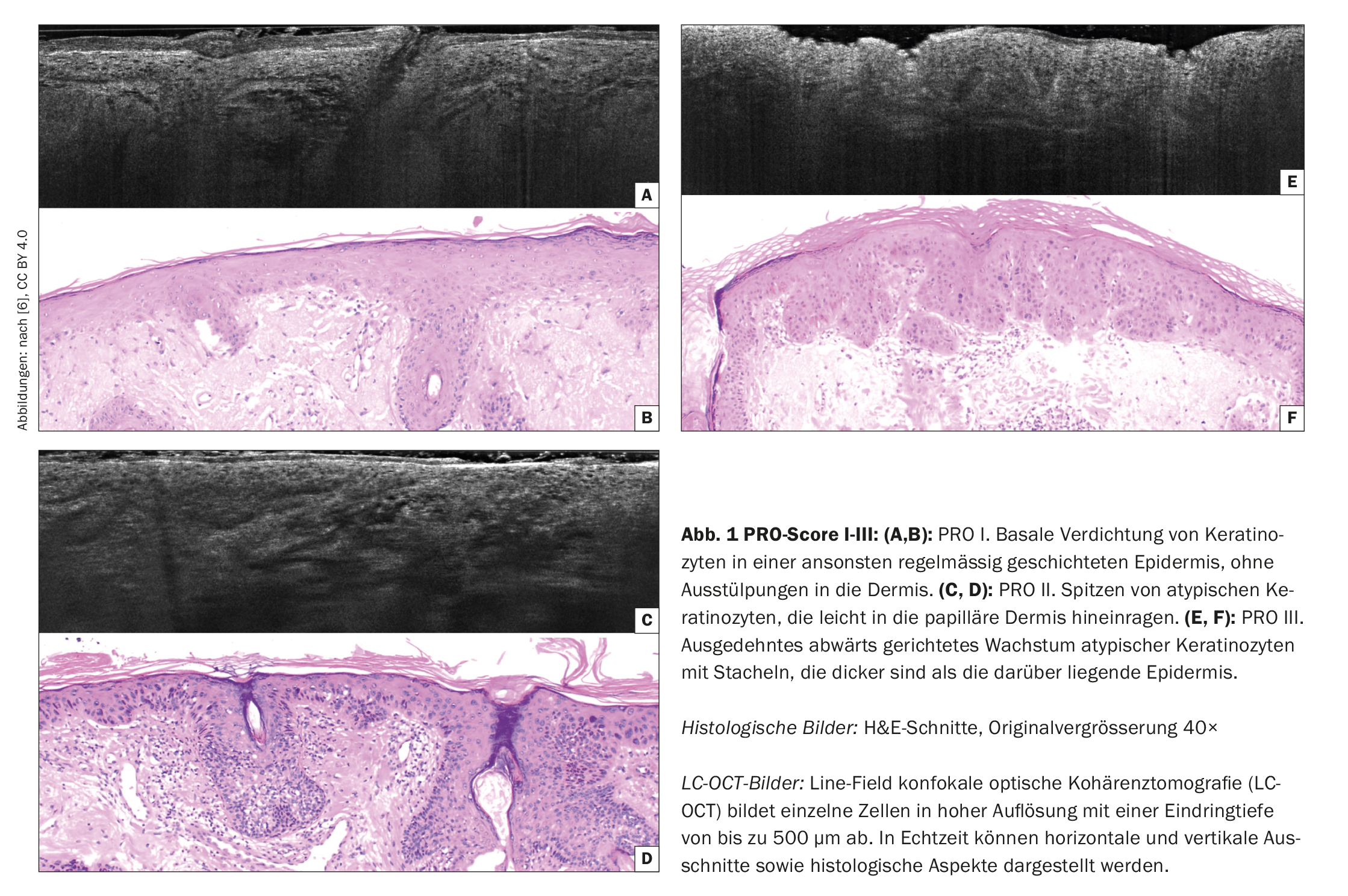
Le PRO-Score I-III (Fig. 1) est basé sur des images obtenues par tomographie confocale à cohérence optique à champ linéaire (LC-OCT) [1,5]. La LC-OCT permet d’examiner une lésion cutanée suspecte de tumeur sans qu’il soit nécessaire de prélever un échantillon de tissu de manière invasive. Les caractéristiques suivantes sont déterminantes pour la classification du risque de transformation :
- PRO I : Accumulation de kératinocytes atypiques dans la couche de cellules basales
- PRO II : protrusions épidermiques dans le derme papillaire supérieur, plus fines que l’épiderme sus-jacent.
- PRO III : prolifération épidermique profonde de kératinocytes atypiques qui s’étendent plus profondément dans le derme que l’épaisseur de l’épiderme.
Une évaluation manuelle du score PRO peut être biaisée par l’évaluation subjective de l’examinateur. Cette source d’erreur est réduite dans le cas d’une quantification automatique basée sur l’IA. Les jeux de données d’images tridimensionnelles de l’épiderme et du derme supérieur créés par LC-OCT ont une résolution supérieure à celle de la tomographie par cohérence optique (OCT) traditionnelle et, par rapport à la microscopie confocale à laser, une profondeur de pénétration plus importante est possible [6]. Les réseaux de neurones convolutionnels (CNN) – les architectures d’apprentissage profond les plus utilisées aujourd’hui – sont utilisés pour l’analyse automatisée des données visuelles [7]. UNet est une architecture de CNN spécialement conçue pour la segmentation d’images biomédicales. Dans l’étude de Thamm et al. de tels CNN ont été entraînés à segmenter des images LC-OCT de peau saine et de lésions AK [1]. L’entraînement du CNN a été réalisé sur la base d’une base de données d’images en coupe verticale obtenues par LC-OCT à l’aide d’un appareil LC-OCT (deepLive™ DAMAE Medical, Paris, France) chez des volontaires à la peau saine et chez des patients atteints de CA [1]. Conformément au gold standard histopathologique, des modèles de score PRO ont été développés, entraînés sur 237 images LC-OCT-AK et testés sur 76 images, le score PRO calculé par l’IC étant comparé au consensus visuel des experts en imagerie en utilisant le coefficient de Cohen-Kappa linéairement pondéré avec un intervalle de confiance (IC) de 95%. Les analyses statistiques ont été effectuées avec la bibliothèque SciPy de Python [1].
Haut degré d’accord entre l’IA et les experts
Le consensus de deux dermatologues et d’un interne a servi d’évaluation de référence en aveugle pour l’évaluation du score PRO des 76 images du kit de test [1]. Aperçu des principaux résultats :
La quantification automatique du score PRO basée sur l’IA, dérivée de l’indice d’inversion et de la profondeur maximale de la protrusion, était en accord avec le classement visuel des experts dans 75% (57/76) des cas, avec un kappa pondéré statistiquement significatif κ=0,60 (p=6×10-8 <0,001, IC 95%=[0,43, 0,77]). Cela a permis d’exclure toute correspondance aléatoire entre le classement basé sur l’IA et le classement visuel, ce qui indique que l’entraînement de l’algorithme a été efficace et proche du consensus des experts.
L’évaluation du score PRO basée sur l’IA était la mieux corrélée avec le score visuel pour PRO II (84,8%), suivi de PRO III (69,2%) et PRO I (66,6%). Les erreurs d’interprétation étaient le plus souvent dues à un ombrage de la DEJ ainsi qu’à des caractéristiques gênantes telles que les follicules pileux et concernaient 25% des cas. Dans l’ensemble, l’IC a surestimé les protrusions dans 14,5% (11/76) des cas, tandis qu’il les a sous-estimées dans 10,5% (8/76). En ce qui concerne PRO I, 10/30 a été surestimé en tant que PRO II. Pour les PRO II, 4/33 ont été sous-estimés comme PRO I, tandis que 1/33 a été attribué au PRO III. Pour PRO III, 3/13 ont été classés à tort comme PRO I et 1/13 comme PRO II
Dans l’ensemble, les résultats de l’étude suggèrent que les CNN sont utiles pour quantifier automatiquement le score PRO dans les jeux de données d’images LC-OCT et peuvent éventuellement être utilisés pour évaluer de manière non invasive le risque de prolifération dans le diagnostic et le suivi des AK, selon les auteurs de l’étude [1].
Résumé
- Des réseaux neuronaux convolutifs (CNN) ont été entraînés à segmenter des images LC-OCT de peau saine et d’AK.
- Les modèles PRO-Score ont été entraînés sur un sous-ensemble de 237 images LC-OCT-AK et testés sur 76 images, en comparant le PRO-Score calculé par l’IA au consensus visuel des experts en imagerie.
- Une concordance significative entre le classement basé sur l’IA et l’évaluation des experts a été observée dans 75% des cas.
Littérature :
- Thamm JR, et al : [Détermination par IA du score PRO dans les kératoses actiniques à partir de jeux de données d’images LC-OCT : Artificial intelligence-based PRO score assessment in actinic keratoses from LC-OCT imaging Usingen Convolutional Neural Networks]. J Dtsch Dermatol Ges 2023 ; 21(11) : 1359-1368.
- Schmitz L, Oster-Schmidt C, Stockfleth E : Nonmelanoma skin cancer – from actinic keratosis to cutaneous squamous cell carcinoma. J Dtsch Dermatol Ges 2018 ; 16(8) : 1002-1013.
- Cockerell CJ : Histopathologie du carcinome spinocellulaire intraépidermique incipient (“kératose actinique”). J Am Acad Dermatol 2000 ; 42(1Pt 2) : 11-17.
- Schmitz L, et al. Les carcinomes épidermoïdes cutanés sont associés à des kératoses actiniques prolifératives basales. Br J Dermatol 2019 ; 180(4) : 916-921.
- Schmitz L, et al : Actinic keratoses show variable histological basal growth patterns – a proposed classification adjustment. J Eur Acad Dermatol Venereol 2018 ; 32(5) : 745-751.
- Ruini C, et al : Évaluation in vivo par LC-OCT du profil de prolifération vers le bas des kératinocytes dans la kératose actinique en comparaison avec l’histologie : premières impressions d’une étude pilote. Cancers (Bâle) 2021 ; 13(12).
- Yamashita R, et al : Convolutional neural networks : an overview and application in radiology. Insights Imaging 2018 ; 9(4) : 611-629.
DERMATOLOGIE PRATIQUE 2024 ; 34(2) : 21-22