Une hypertension artérielle insuffisamment traitée pendant des années conduit généralement à une insuffisance cardiaque. Il n’est pas du tout surprenant que l’apparition de l’insuffisance cardiaque puisse être retardée par le traitement de la pression artérielle, de l’obésité et du diabète.
Une hypertension artérielle insuffisamment traitée pendant des années conduit généralement à une insuffisance cardiaque, si aucune autre maladie limitant le pronostic vital n’est survenue entre-temps. Inversement, les patients souffrant d’insuffisance cardiaque présentent souvent une hypertension artérielle des années auparavant. Dans la cohorte de Framingham, sur une période d’observation de 20 ans, 91% de tous les patients chez qui une insuffisance cardiaque vient d’être diagnostiquée avaient déjà reçu un diagnostic préalable d’hypertension artérielle [1]. Le risque de développer une insuffisance cardiaque chez les sujets hypertendus par rapport aux sujets normotendus, corrigé pour l’âge et les autres facteurs déclenchant l’insuffisance cardiaque, était deux fois plus élevé chez les hommes et trois fois plus élevé chez les femmes. Les facteurs de risque de l’insuffisance cardiaque sont par exemple l’infarctus du myocarde, le diabète sucré, l’hypertrophie ventriculaire gauche et les maladies valvulaires. Le risque de développer une insuffisance cardiaque est doublé chez les patients dont la pression artérielle est de 160/100 mmHg par rapport à ceux dont la pression artérielle est de 140/90 mmHg [2].
Il n’est donc pas du tout surprenant que l’apparition d’une insuffisance cardiaque puisse être retardée par le traitement de la pression artérielle, de l’obésité et du diabète. Hommes resp. Les femmes sans hypertension, sans obésité et sans diabète âgées de 45 ans vivent en moyenne 3 à 15 ans de plus sans développer d’insuffisance cardiaque par rapport aux patients présentant ces facteurs de risque [3]. Un poids corporel normal, l’absence de diabète et surtout l’absence d’hypertension artérielle sont associés à une réduction de 86% du risque de survenue d’une insuffisance cardiaque au cours de la vie. Dans l’étude SHEP (Systolic Hypertension in the Elderly Program), sur une période de suivi de 4,5 ans, la vie des patients sous chlorthalidone a été prolongée d’un jour par mois par rapport à ceux sous placebo [4].
Physiopathologie
La dysfonction diastolique est la première manifestation de la cardiopathie hypertensive. Le remodelage cardiaque dû à une charge de pression (par ex. hypertension artérielle, sténose aortique) entraîne une hypertrophie ventriculaire gauche concentrique en vertu de la loi de Laplace. Pour compenser l’augmentation de la tension de la paroi due à la pression, le muscle s’épaissit et la cavité du ventricule diminue. En revanche, une charge volumique (par exemple, insuffisance valvulaire aortique, obésité, insuffisance rénale chronique, anémie) entraîne une hypertrophie excentrique du ventricule gauche (augmentation du volume du ventricule et augmentation de la masse musculaire) [5].
Si la charge de pression persiste, que la dysfonction diastolique augmente et que le ventricule gauche hypertrophique concentrique décompense, il en résulte une insuffisance cardiaque avec fonction systolique ventriculaire gauche préservée (HFpEF – “heart failure with preserved ejection fraction”). En revanche, lorsque le ventricule gauche présente une hypertrophie excentrique, si la charge volumique persiste et que le ventricule gauche décompense, il en résulte une insuffisance cardiaque avec réduction de la fonction ventriculaire gauche (HFrEF – “heart failure with reduced ejection fraction”).
L’hypertrophie du ventricule gauche (VG) et l’augmentation des biomarqueurs d’atteinte myocardique infraclinique (troponine ultrasensible, peptide natriurétique pro-B de type N-terminal [NT-pro BNP]) sont associées à un risque accru de développer une insuffisance cardiaque symptomatique, en particulier une FHFR [6]. Dans le cas de l’HFpEF, les valeurs de NT-pro BNP sont généralement plus basses, ce qui s’explique par un stress moindre de la paroi et donc par moins de peptides natriurétiques circulants [7]. Des protéines natriurétiques normales sont présentes chez 30% des patients atteints d’HFpEF [8], en particulier chez les patients obèses [9] ou présentant des symptômes uniquement à l’effort [10]. Enfin, le stade final de la cardiopathie hypertensive, généralement le résultat de plusieurs années de pression et de volume, est la cardiopathie dilatée. D’un point de vue clinique, la cardiopathie hypertensive peut être divisée en quatre stades (Fig. 1) :
- Grade 1 : Dysfonctionnement diastolique du ventricule gauche sans hypertrophie du VG
- Grade 2 : Dysfonctionnement diastolique du ventricule gauche avec hypertrophie du VG
- Grade 3 : symptômes d’insuffisance cardiaque (dyspnée, œdème pulmonaire) avec fonction systolique du VG préservée
- Grade 4 : cardiopathie dilatée avec fonction systolique du VG réduite et symptômes d’insuffisance cardiaque [11].
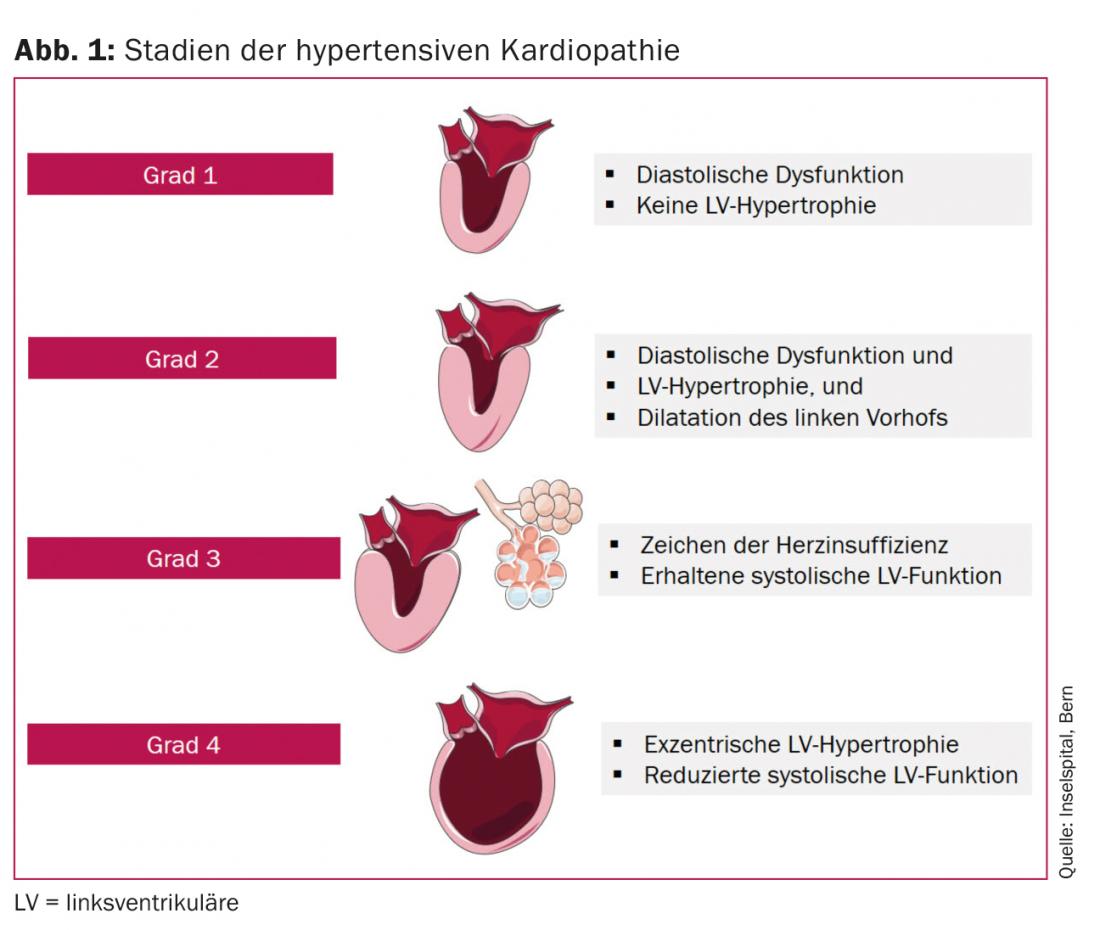
La dysfonction diastolique est l’effet le plus courant d’une hypertension de longue durée. Cependant, tous les patients atteints de dysfonctionnement diastolique ne présentent pas de FEHP [12], et le dysfonctionnement diastolique peut être totalement absent chez les patients bien traités atteints de FEHP ou chez les patients qui présentent des symptômes à l’effort en premier lieu [10,13]. L’oreillette gauche est souvent dilatée et la pression pulmonaire systolique estimée par Doppler est élevée (>35 mmHg) [14]. Les patients atteints d’HFpEF présentent davantage d’hypertrophie du VG, de lésions dans les coronaires épicardiques, de diminution de la microcirculation coronaire et de fibrose myocardique qu’un collectif de contrôle. La cause de la perturbation de la microcirculation coronaire pourrait être une augmentation de l’inflammation systémique et du stress oxydatif en raison des comorbidités de l’HFpEF [15,16].
Même un dysfonctionnement diastolique isolé peut étonnamment déclencher un œdème pulmonaire, comme l’ont montré Gandhi et al. montré [17]. Les patients ayant connu un épisode d’œdème pulmonaire d’origine hypertensive ont présenté une fonction ventriculaire gauche systolique normale inchangée pendant et après l’épisode, lorsque la pression artérielle était bien contrôlée. La pression artérielle systolique moyenne était initialement de 200 +/- 26 mmHg pendant l’œdème pulmonaire et de 139 +/- 17 mmHg au moment du suivi. La seule cause de l’œdème pulmonaire restait la dysfonction diastolique, car une dysfonction systolique transitoire avec ou sans insuffisance mitrale était absente chez ces patients [17].
“Cardiopathie hypertensive “épuisée
Dans l’insuffisance cardiaque avancée, la pression artérielle systolique est souvent basse, même chez les patients qui ont toujours été hypertendus. Ce phénomène est appelé cardiopathie hypertensive “brûlée”. Les patients souffrant d’hypertension depuis de nombreuses années peuvent devenir de plus en plus normo-hypertendus à mesure que l’insuffisance cardiaque s’aggrave, c’est-à-dire que la fonction systolique du VG diminue. Une fonction systolique du VG sévèrement réduite entraîne une diminution du débit cardiaque, les mécanismes compensatoires tels que la vasoconstriction périphérique ne permettant pas de maintenir le débit cardiaque et donc d’arrêter la chute de la pression artérielle. Les patients atteints de cardiopathie hypertensive “épuisée” tolèrent mal les médicaments antihypertenseurs tels que les antagonistes des récepteurs de l’angiotensine (ARA), les inhibiteurs de l’enzyme de conversion de l’angiotensine (ECA), les bêtabloquants (BB) et les diurétiques.
L’interaction entre l’hypertension artérielle, la cardiopathie hypertensive et la cardiopathie dilatée (qui est le signe d’une cardiopathie hypertensive “épuisée”, c’est-à-dire le stade final de la cardiopathie hypertensive) est complexe. Souvent, ce n’est que rétrospectivement que l’on découvre que l’hypertension artérielle était (co)responsable de la cardiopathie dilatée. Si la fonction systolique du VG se rétablit, la pression artérielle augmente à nouveau.
Hypertension artérielle chez les patients atteints d’HFrEF
Même si l’hypertension artérielle est un facteur de risque connu de l’insuffisance cardiaque, une pression artérielle systolique élevée chez les patients HFrEF semble être associée à une mortalité plus faible. Plusieurs études ont montré une amélioration des résultats en cas d’hypertension systolique chez les patients souffrant d’insuffisance cardiaque aiguë ou chronique [18–24]. Ainsi, chez 2289 patients de l’étude COPERNICUS (Carvedilol Prospective Randomized Cumulative Survival), une pression artérielle systolique plus basse était également associée à un risque plus élevé de décès [25]. L’augmentation de la pression artérielle centrale pourrait également contribuer à l’effet positif du traitement par bêtabloquants sur la survie en cas d’insuffisance cardiaque. En conséquence, la diminution de la fréquence cardiaque sous traitement bêtabloquant (qui est indirectement proportionnelle à l’augmentation de la pression centrale) est associée à une meilleure survie chez les patients souffrant d’insuffisance cardiaque dans l’étude SHEP [26]. Le même phénomène pourrait s’appliquer à l’ivabradine, où une réduction des hospitalisations pour insuffisance cardiaque a été obtenue dans l’étude SHIFT (“Systolic Heart failure treatment with the If inhibitor ivabradine”) [27]. Contrairement aux patients hypertendus normaux, chez lesquels une réduction de la fréquence cardiaque est associée à une augmentation de la mortalité cardiovasculaire, l’inverse est vrai chez les patients souffrant d’insuffisance cardiaque [26,28].
Syndrome cardiorénal
L’hypertension artérielle de longue durée entraîne des lésions des organes terminaux, tant au niveau du cœur que des reins. Ainsi, ces patients souffrent non seulement d’insuffisance cardiaque, mais aussi d’insuffisance rénale. L’interaction entre le cœur et les reins se fait dans les deux sens par différents mécanismes [29]. Les syndromes cardiorénaux les plus fréquents chez les patients souffrant d’insuffisance cardiaque sont les suivants [30]:
- Type 1 (aigu) : Insuffisance cardiaque aiguë entraînant une atteinte rénale aiguë (insuffisance rénale)
- Type 2 (chronique) : Insuffisance cardiaque chronique entraînant une maladie rénale croissante
- Type 3 : détérioration aiguë de la fonction rénale entraînant une insuffisance cardiaque
- Type 4 : apparition d’une insuffisance cardiaque due à une maladie rénale sous-jacente croissante
Du point de vue du clinicien, la survenue d’une insuffisance rénale complique le traitement de l’insuffisance cardiaque. Lorsque l’insuffisance rénale progresse, l’insuffisance cardiaque s’accroît, et inversement. Les comorbidités correspondantes et de nombreux médicaments pour l’insuffisance cardiaque augmentent le risque d’hyperkaliémie. Un syndrome cardiorénal prononcé limite drastiquement le choix des médicaments et leur dosage pour atteindre la dose cible. Une combinaison de fixateurs de K+ récemment étudiés (par exemple le patiromère) et d’un antagoniste minéralocorticoïde pourrait à l’avenir réduire la mortalité et la morbidité cardiovasculaires chez les patients souffrant d’insuffisance cardiaque [31].
Syndrome de Pickering
En 1988, le Dr Pickering et al. sur onze patients atteints d’hypertension et de sténose bilatérale de l’artère rénale athéroscléreuse, qui se sont présentés avec plusieurs épisodes d’œdème pulmonaire d’apparition soudaine [32]. Le syndrome de Pickering, œdème pulmonaire soudain (“flash pulmonary edema”) et sténose bilatérale de l’artère rénale, est un syndrome cardiorénal de type 3. Les patients atteints du syndrome de Pickering se présentent généralement avec une dysfonction diastolique et une hypertrophie du VG, la fonction systolique du VG étant normale ou seulement légèrement altérée. Ceci, associé à une natriurèse insuffisante due à la sténose bilatérale des artères rénales, est le mécanisme qui conduit à l’œdème pulmonaire (Fig. 2). Le fait que cet œdème pulmonaire survienne soudainement et entraîne une urgence vitale distingue le syndrome de Pickering des autres formes de décompensation cardiaque [33]. La récurrence d’un œdème pulmonaire soudain, l’absence d’angine de poitrine typique, une pression artérielle élevée et des taux de créatinine élevés doivent faire penser à une sténose bilatérale de l’artère rénale, c’est-à-dire à un syndrome de Pickering, comme cause de l’œdème pulmonaire soudain. Dans les séries de cas du syndrome de Pickering, plusieurs œdèmes pulmonaires d’apparition soudaine ont généralement précédé le diagnostic de sténoses bilatérales des artères rénales [32].
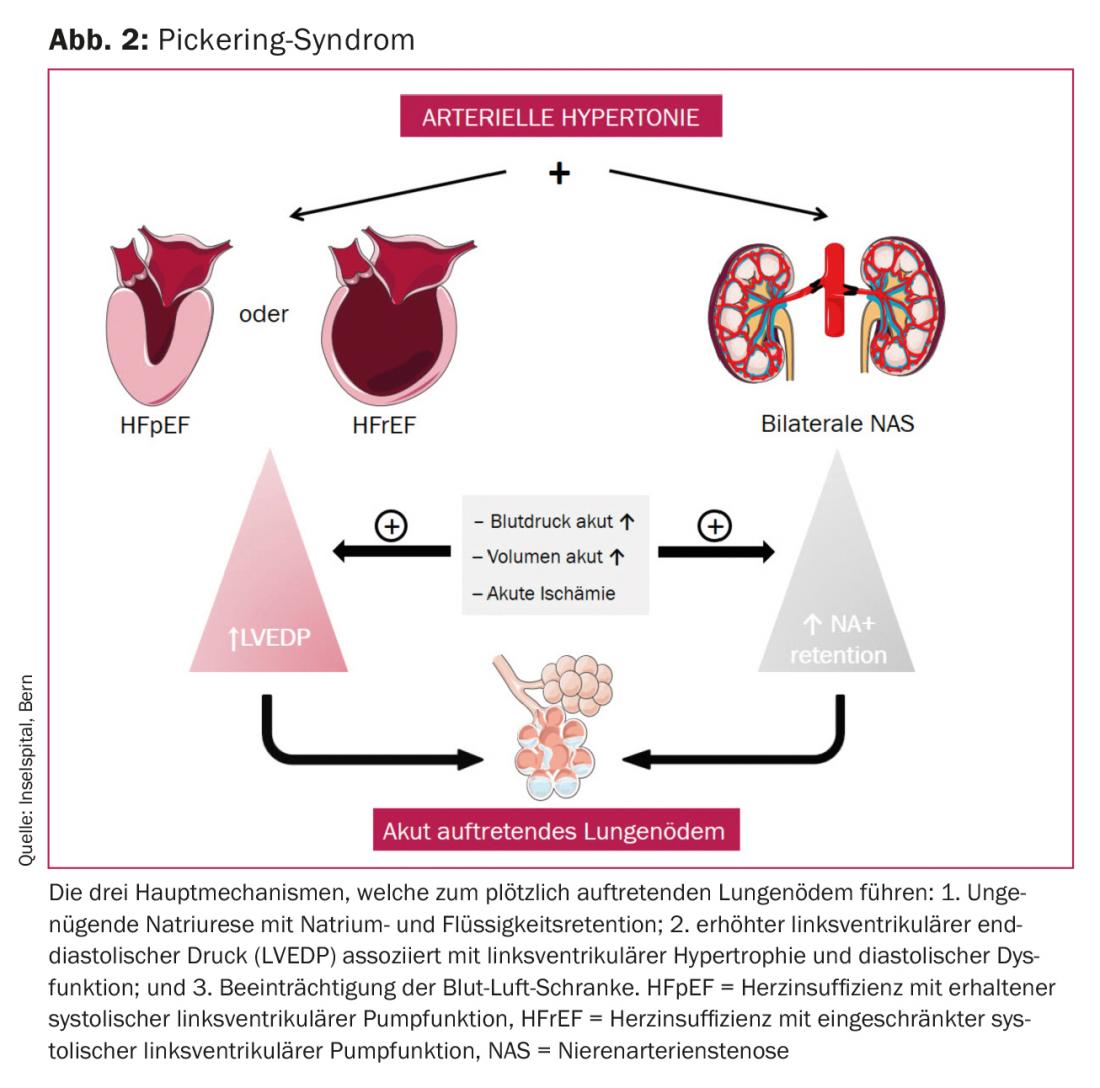
L’objectif du traitement aigu de l’œdème pulmonaire soudain est d’obtenir une oxygénation suffisante en réduisant la postcharge pour abaisser la pression post-capillaire et maintenir une diurèse suffisante. La suppression de la cause, c’est-à-dire l’angioplastie de la sténose de l’artère rénale, est essentielle une fois que le patient est stabilisé.
Traitement antihypertenseur pour réduire l’incidence de l’insuffisance cardiaque
Par définition, tous les médicaments antihypertenseurs réduisent la pression artérielle. Mais, si l’on examine attentivement la littérature, tous les médicaments n’ont pas la même efficacité pour réduire l’incidence de l’insuffisance cardiaque. Les bêtabloquants sont une pierre angulaire du traitement de l’insuffisance cardiaque avec réduction de la fonction systolique du VG (HFrEF) [34]. Par rapport aux autres médicaments antihypertenseurs, ils n’ont toutefois pas un meilleur caractère préventif concernant l’insuffisance cardiaque. Chez 112 177 patients issus de douze essais contrôlés randomisés différents, le traitement par BB a probablement entraîné une réduction de la pression artérielle de 12,6/6,1 mmHg par rapport au placebo. Cependant, aucune réduction significative de l’incidence de l’insuffisance cardiaque n’a été observée [35]. Comparés à d’autres médicaments antihypertenseurs, les BB n’apportent aucun effet supplémentaire en termes de réduction de la mortalité globale, de la mortalité cardiovasculaire ou de l’infarctus du myocarde. On observe toutefois une augmentation de la prévalence des accidents vasculaires cérébraux chez les patients âgés. Les BB ne devraient donc pas être le premier choix d’un traitement antihypertenseur.
Dans une méta-analyse Cochrane, les inhibiteurs des canaux calciques (CCB) ont augmenté le risque d’insuffisance cardiaque (Risk Ratio [RR]: 1,37 ; intervalle de confiance (IC) à 95% : 1,25-1,51) par rapport aux diurétiques. Bien que les ACO réduisent le risque d’accident vasculaire cérébral (AVC) par rapport aux IEC et le risque d’infarctus du myocarde et d’AVC par rapport aux ARA, les ACO semblent augmenter l’incidence de l’insuffisance cardiaque par rapport aux IEC (RR 1,16 ; IC à 95% : 1,06-1,27) et aux ARA (RR 1,2 ; IC à 95% : 1,06-1,36). [36]. Une méta-analyse récente remet cependant en question cette affirmation : dans cette étude, une réduction de la pression artérielle par CCB semble prévenir l’apparition d’une insuffisance cardiaque aussi efficacement qu’une réduction de la pression artérielle par d’autres médicaments [37]. Ainsi, l’infériorité de la CCB démontrée précédemment pourrait être due à une meilleure médication concomitante dans le bras contrôle.
Dans l’étude ALLHAT (Antihypertensive and Lipid-Lowering Treatment to Prevent Heart Attack Trial), les accidents vasculaires cérébraux et les maladies cardiovasculaires étaient plus fréquents avec l’alpha-bloquant doxazosine qu’avec la chlorthalidone. Le risque d’insuffisance cardiaque sous traitement par doxazosine était deux fois plus élevé (RR 2,04, IC 95% 1,79-2,32, p>0,001) [35]. Il semble donc que le traitement par alpha-bloquants doive être évité chez les patients présentant un risque d’insuffisance cardiaque.
Le blocage du système rénine-angiotensine entraîne une réduction efficace de la pression artérielle et réduit l’incidence de l’insuffisance cardiaque. Les inhibiteurs de l’ECA sont aussi efficaces que les ARA [38,39]. Il convient de mentionner en particulier le valsartan/sacubitril, un inhibiteur de l’ARB/néprilysine récemment approuvé, qui est non seulement un médicament puissant dans le traitement de l’insuffisance cardiaque avec réduction de la fonction systolique du VG, mais qui est également susceptible de bien réduire la pression artérielle [40]. Dans l’étude PARADIGM (Prospective Comparision of ARNI with ACEI to Determine Impact on Global Mortalitiy and Morbidity in Heart Failure), valsartan/sacubitril a montré une réduction spectaculaire de la mortalité et de la morbidité cardiovasculaires chez les patients dont la fonction systolique du VG était réduite [41]. Toutefois, il reste à voir si le rapport bénéfice/risque du valsartan/sacubitril est bon à long terme chez les hypertendus.
Enfin, les diurétiques de type thiazidique tels que la chlorthalidone ou l’indapamide constituent un excellent choix de médicament antihypertenseur pour la prévention de l’insuffisance cardiaque. Dans l’étude SHEP-[42] comme dans l’étude HYVET (Hypertension in the Very Elderly Trial) [43], ils ont entraîné une réduction significative de l’insuffisance cardiaque par rapport au placebo, pour la chlorthalidone (RR 0,51 ; IC à 95% 0,37-0,71) et pour l’indapamide (RR 0,36 ; IC à 95% 0,22-0,58 ; p<0,001). Les diurétiques de type thiazidique sont supérieurs à tous les autres médicaments antihypertenseurs en termes de prévention de l’insuffisance cardiaque dans dix essais contrôlés randomisés (RR 0,84 ; IC 95% 0,73-0,98) [37]. Or, de tels résultats n’existent pas pour l’hydrochlorothiazide, que ce soit pour l’insuffisance cardiaque ou pour tout autre critère cardiovasculaire. Contrairement à l’indapamide ou à la chlorthalidone, l’hydrochlorothiazide doit donc être évité chez les patients hypertendus présentant un risque d’insuffisance cardiaque.
Dans l’étude TOPCAT (Treatment of Preserved Cardiac function Heart Failure with an Aldosterone Antagonist), chez des patients atteints de HFpEF, l’antagoniste de l’aldostérone Spirinolactone n’a pas eu d’impact sur un critère composite de décès cardiovasculaire ou d’hospitalisation [44]. Le traitement par spirinolactone a toutefois entraîné une réduction du nombre d’hospitalisations pour insuffisance cardiaque, mais aussi une augmentation de l’insuffisance rénale et de l’hyperkaliémie. Cependant, une analyse post-hoc portant uniquement sur des patients du continent nord-américain montre un point final composite positif [45]. Il est surprenant de constater qu’en Géorgie et en Russie, il y a eu davantage de points finaux dans le groupe d’intervention par rapport au groupe de contrôle. Si l’on recherche ensuite les métabolites de la spirinolactone dans le sang, on constate qu’ils sont indétectables chez 30% des patients russes qui devaient prendre le médicament, contre 3% en Amérique du Nord [46].
En résumé, la plupart des classes de médicaments antihypertenseurs ralentissent le passage de l’hypertension à l’insuffisance cardiaque, même si toutes les classes ne sont pas aussi efficaces à cet égard. L’hydrochlorothiazide administré une fois par jour doit être évité, d’autant plus qu’il existe deux très bonnes alternatives : la chlorthalidione et l’indapamide.
Antihypertenseurs chez les patients atteints d’insuffisance cardiaque et dont la pression artérielle reste élevée
Généralement, chez les patients souffrant d’insuffisance cardiaque [47], le problème le plus courant est une pression artérielle basse. Cependant, il arrive que les patients en HFpEF, plus rarement en HFrEF, présentent une hypertension persistante. En raison du manque de preuves, nos recommandations sont empiriques, basées sur des considérations cliniques et physiopathologiques [48]. Ces recommandations s’appliquent aux patients qui continuent à présenter des valeurs tensionnelles élevées (>140/90 mmHg en cabinet/à l’hôpital) malgré un traitement par inhibiteur de l’ECA ou ARA à dose mesurée, bêtabloquant et diurétique.
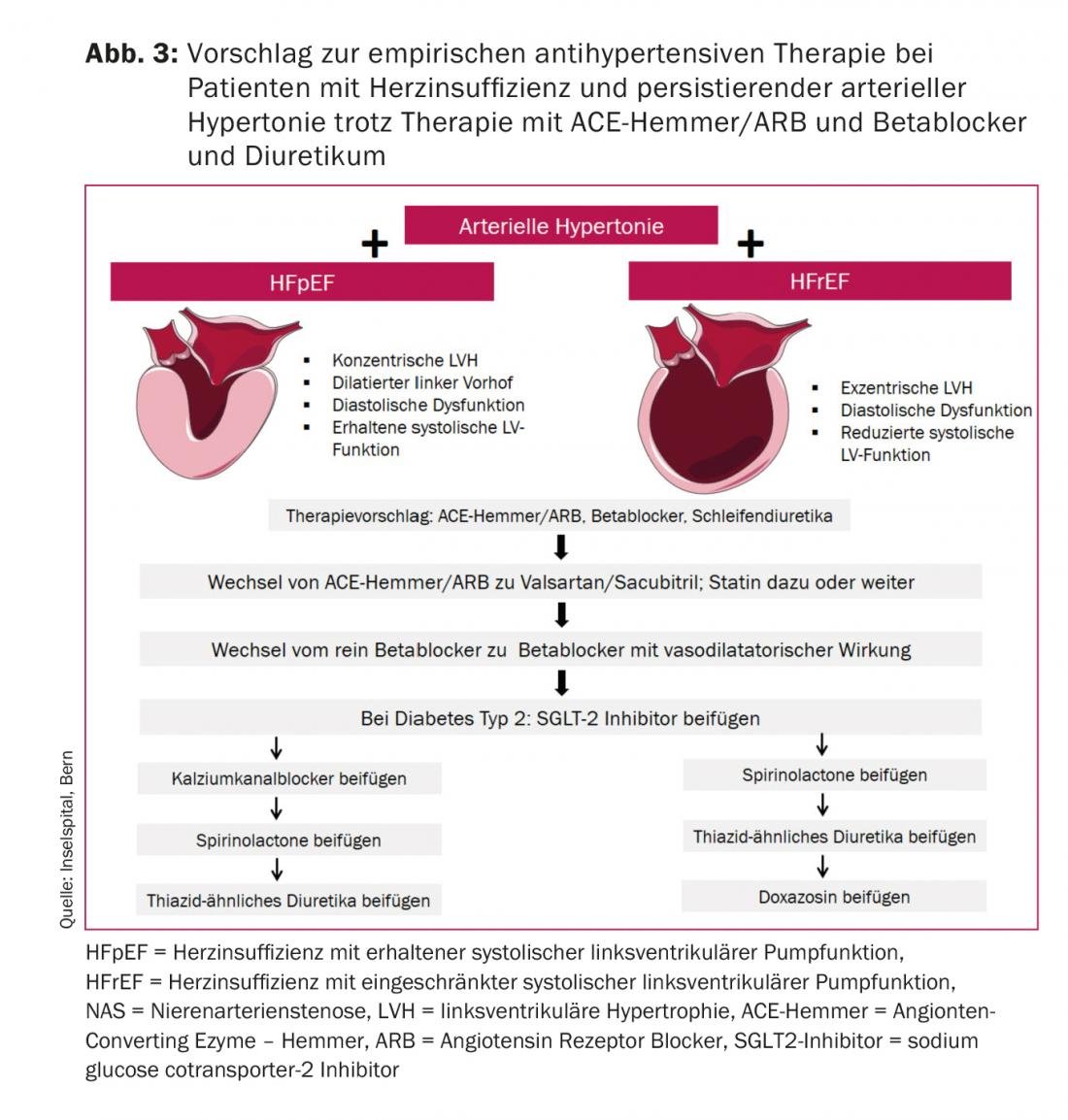
La première chose à faire est de toujours contrôler l’adhésion au traitement. L’objectif de la poursuite du traitement après bêtabloquant, IEC ou ARA et diurétiques de l’anse est, dans l’HFpEF, d’améliorer la dysfonction diastolique et microvasculaire et, dans l’HFrEF, de maintenir ou éventuellement d’améliorer la fonction systolique ventriculaire gauche limitée. La figure 3 présente notre recommandation avec une réduction initiale accrue de la postcharge avec le valsartan/sacubitril au lieu de l’IEC/ARB et un changement pour un bêtabloquant vasodilatateur comme le carvédilol ou le nébivolol. De même, une statine doit être initiée chez les patients atteints d’HFpEF et dont la pression artérielle reste élevée.
Messages Take-Home
- 90% des patients chez qui une insuffisance cardiaque vient d’être diagnostiquée ont déjà souffert d’hypertension artérielle.
- La dysfonction diastolique, l’hypertrophie ventriculaire gauche et la dilatation de l’oreillette gauche sont les signes de la cardiopathie hypertensive.
- On trouve des peptides natriurétiques normaux chez 30% des patients atteints d’insuffisance cardiaque avec une fonction systolique préservée, en particulier chez les patients obèses.
- En cas de cardiopathie dilatée (dans le cadre d’une cardiopathie hypertensive “épuisée”), ce n’est souvent que rétrospectivement, après la récupération de la fonction systolique du VG, que l’on découvre que l’hypertension en était la cause.
- Les inhibiteurs de l’ECA, les bloqueurs des récepteurs de l’angiotensine et l’indapamide ou la chlorthalidone sont les médicaments antihypertenseurs de choix pour prévenir l’insuffisance cardiaque.
Littérature :
- Levy D, Larson MG, et al : The progression from hypertension to congestive heart failure. JAMA 1996 ; 275 : 1557-1562.
- Lloyd-Jones DM, Larson MG, et al : Lifetime risk for developing congestive heart failure : the Framingham Heart Study. Circulation 2002 ; 106 : 3068-3072.
- Ahmad FS, Ning H, et al : Hypertension, obésité, diabète, et survie sans défaillance cardiaque : Le projet de mise en commun des risques sur la durée de vie des maladies cardiovasculaires. JACC Heart Fail 2016 ; 4 : 911-919.
- Kostis JB, Cabrera J, et al : Association entre le traitement par chlorthalidone de l’hypertension systolique et la survie à long terme. JAMA 2011 ; 306 : 2588-2593.
- Messerli FH : Effets cardiovasculaires de l’obésité et de l’hypertension. Lancet 1982 ; 1 : 1165-1168.
- Seliger SL, de Lemos J, et al : Les personnes âgées, l’hypertrophie ventriculaire gauche “maligne”, et les phénotypes de biomarqueurs cardiaques associés pour identifier le risque différentiel d’insuffisance cardiaque à fraction d’éjection réduite ou préservée : CHS (Cardiovascular Health Study). JACC Heart Fail 2015 ; 3 : 445-455.
- Iwanaga Y, Nishi I, et al : B-type natriuretic peptide reflects strongly diastolic wall stress in patients with chronic heart failure : comparison between systolic and diastolic heart failure. J Am Coll Cardiol 2006 ; 47 : 742-748.
- Anjan VY, Loftus TM, et al : Prévalence, phénotype clinique, et résultats associés à des niveaux normaux de peptide natriurétique de type B dans la défaillance cardiaque avec fraction d’éjection préservée. Am J Cardiol 2012 ; 110 : 870-876.
- Bishu K, Deswal A, et al : Biomarkers in acutely decompensated heart failure with preserved or reduced ejection fraction. Am Heart J 2012 ; 164 : 763-770 e3.
- Borlaug BA, Nishimura RA et al : Exercise heodynamics enhance diagnosis of early heart failure with preserved ejection fraction. Circ Heart Fail 2010 ; 3 : 588-595.
- Iriarte M, Murga N, et al : Classification de la cardiomyopathie hypertensive. Eur Heart J 1993 ; 14 Suppl J : 95-101.
- Redfield MM, Jacobsen SJ et al : Burden of systolic and diastolic ventricular dysfunction in the community : appreciating the scope of the heart failure epidemic. JAMA 2003 ; 289 : 194-202.
- Franssen C, Paulus WJ : Normal resting artery wedge pressure : a diagnostic trap for heart failure with preserved ejection fraction. Eur J Heart Fail 2015 ; 17 : 132-134.
- Thenappan T, Prins KW, et al : Hypertension pulmonaire secondaire à une insuffisance cardiaque avec fraction d’éjection préservée. Can J Cardiol 2015 ; 31 : 430-439.
- Paulus WJ, Tschope C : A novel paradigm for heart failure with preserved ejection fraction : comorbidities drive myocardial dysfunction and remodeling through coronary microvascular endothelial inflammation. J Am Coll Cardiol 2013 ; 62 : 263-271.
- Mohammed SF, Hussain S, et al. : Raréfaction microvasculaire coronaire et fibrose myocardique dans la défaillance cardiaque avec fraction d’éjection préservée. Circulation 2015 ; 131 : 550-559.
- Gandhi SK, Powers JC, et al : The pathogenesis of acute pulmonary edema associated with hypertension. N Engl J Med 2001 ; 344 : 17-22.
- Adamopoulos C, Zannad F, et al : Ejection fraction and blood pressure are important and interactive predictors of 4-week mortality in severe acute heart failure. Eur J Heart Fail 2007 ; 9 : 935-941.
- Bhatia RS, Tu JV, et al : Outcome of heart failure with preserved ejection fraction in a population-based study. N Engl J Med 2006 ; 355 : 260-269.
- Fonarow GC, Adams KF, et al : Risk stratification for in-hospital mortality in acutely decompensated heart failure : classification and regression tree analysis. JAMA 2005 ; 293 : 572-580.
- Gheorghiade M, Abraham WT, et al : Systolic blood pressure at admission, clinical characteristics, and outcomes in patients hospitalized with acute heart failure. JAMA 2006 ; 296 : 2217-2226.
- Lee TT, Chen J, Cohen DJ, Tsao L : The association between blood pressure and mortality in patients with heart failure. Am Heart J 2006 ; 151 : 76-83.
- Pulignano G, Del Sindaco D, et al : Clinical features and outcomes of elderly outpatients with heart failure followed up in hospital cardiology units : data from a large nationwide cardiology database (IN-CHF Registry). Am Heart J 2002 ; 143 : 45-55.
- Schrier RW, Abraham WT : Hormones et hémodynamique dans l’insuffisance cardiaque. N Engl J Med 1999 ; 341 : 577-585.
- Rouleau JL, Roecker EB, et al : Influence du prétraitement de la pression artérielle systolique sur l’effet du carvédilol chez les patients atteints d’insuffisance cardiaque chronique sévère : l’étude Carvedilol Prospective Randomized Cumulative Survival (COPERNICUS). J Am Coll Cardiol 2004 ; 43 : 1423-1429.
- McAlister FA, Wiebe N, et al : Meta-analysis : beta-blocker dose, heart rate reduction, and death in patients with heart failure. Ann Intern Med 2009 ; 150 : 784-794.
- Swedberg K, Komajda M, et al : Ivabradine and outcomes in chronic heart failure (SHIFT) : a randomised placebo-controlled study. Lancet 2010 ; 376 : 875-885.
- Rimoldi SF, Messerli FH, et al : Selective Heart Rate Reduction With Ivabradine Increases Central Blood Pressure in Stable Coronary Artery Disease. Hypertension 2016 ; 67 : 1205-1210.
- Bock JS, Gottlieb SS : Syndrome cardiorénal : nouvelles perspectives. Circulation 2010 ; 121 : 2592-2600.
- Ronco C, Cicoira M, McCullough PA : Cardiorenal syndrome type 1 : pathophysiological crosstalk leading to combined heart and kidney dysfunction in the setting of acutely decompensated heart failure. J Am Coll Cardiol 2012 ; 60 : 1031-1042.
- Epstein M, Pitt BC : A propitious time for initiating clinical trials in patients with heart failure with reduced ejection fraction and an estimated glomerular filtration rate <30 mL/min with an mineralocorticoid receptor antagonist and a K+ binder : “the forbidden fruit”. Eur Heart J 2016 ; 37 : 3130-3134.
- Pickering TG, Herman L, et al : Œdème pulmonaire récurrent dans l’hypertension due à une sténose bilatérale de l’artère rénale : traitement par angioplastie ou revascularisation chirurgicale. Lancet 1988 ; 2 : 551-552.
- Rimoldi SF, Yuzefpolskaya M, et al : Flash pulmonary edema. Prog Cardiovasc Dis 2009 ; 52 : 249-259.
- Kotecha D, Manzano L, et al : Effet de l’âge et du sexe sur l’efficacité et la tolérance des bêta-bloquants chez les patients souffrant d’insuffisance cardiaque avec réduction de la fraction d’éjection : méta-analyse des données individuelles des patients. BMJ 2016 ; 353 : i1855.
- Bangalore S, Wild D, et al : Beta-blockers for primary prevention of heart failure in patients with hypertension insights from a meta-analysis. J Am Coll Cardiol 2008 ; 52 : 1062-1072.
- Chen N, Zhou M, et al : Bloqueurs des canaux calciques versus autres classes de médicaments pour l’hypertension. Cochrane Database Syst Rev 2010 : CD003654.
- Thomopoulos C, Parati G, Zanchetti A : Effets du traitement hypotenseur. 6. prévention de la défaillance cardiaque et de la nouvelle défaillance cardiaque – méta-analyses d’essais randomisés. J Hypertens 2016 ; 34 : 373-384 ; discussion 84.
- Bangalore S, Fakheri R, et al : Angiotensin-Converting Enzyme Inhibitors or Angiotensin Receptor Blockers in Patients Without Heart Failure ? Insights From 254,301 Patients From Randomized Trials. Mayo Clin Proc 2016 ; 91 : 51-60.
- Messerli FH, Bangalore S : Angiotensin Receptor Blockers Reduce Cardiovascular Events, Including the Risk of Myocardial Infarction. Circulation 2017 ; 135 : 2085-2087.
- Bavishi C, Messerli FH, et al : Role of neprilysin inhibitor combinations in hypertension : insights from hypertension and heart failure trials. Eur Heart J 2015 ; 36 : 1967-1973.
- McMurray JJ, Packer M, et al : Angiotensin-neprilysin inhibition versus enalapril in heart failure. N Engl J Med 2014 ; 371 : 993-1004.
- SHEP Cooperative Research Group : Prevention of stroke by antihypertensive drug treatment in older persons with isolated systolic hypertension. Résultats finaux du programme SHEP (Systolic Hypertension in the Elderly Program). JAMA 1991 ; 265 : 3255-3264.
- Beckett NS, Peters R, et al : Treatment of hypertension in patients 80 years of age or older. N Engl J Med 2008 ; 358 : 1887-1898.
- Pfeffer MA, Pitt B, McKinlay SM : Spironolactone for heart failure with preserved ejection fraction. N Engl J Med 2014 ; 371 : 181-182.
- Pfeffer MA, Claggett B, et al. : Variation régionale des patients et des résultats dans l’essai de traitement de l’insuffisance cardiaque préservée avec un antagoniste de l’aldostérone (TOPCAT). Circulation 2015 ; 131 : 34-42.
- de Denus S, O’Meara E, et al. : Spironolactone Metabolites in TOPCAT – New Insights into Regional Variation. N Engl J Med 2017 ; 376 : 1690-1692.
- Redfield MM : Insuffisance cardiaque avec fraction d’éjection préservée. N Eng J Med 2016 ; 375 : 1868-1877.
- Messerli FH, Rimoldi SF, Bangalore S : The Transition from Hypertension to Heart Failure : Contemporary Update. JACC Heart Fail 2017;5 : 541-551.
CARDIOVASC 2017 ; 16(5) : 30-35











