Les patients souffrant d’insuffisance cardiaque chronique disposent aujourd’hui d’un certain nombre d’options thérapeutiques. Il n’est pas toujours facile de faire le bon choix.
Les progrès dans le traitement médical, en particulier du syndrome coronarien aigu, ont récemment entraîné une augmentation constante de la prévalence de l’insuffisance cardiaque chronique – qui touche actuellement environ 26 millions de personnes dans le monde et environ 200 000 patients en Suisse. Comme l’évolution de la maladie ne peut être que retardée, mais que la maladie de base ne peut pas être inversée, de plus en plus de patients, même jeunes, atteignent un stade sévèrement symptomatique avec une qualité de vie fortement réduite et un taux de mortalité élevé à un an.
L’une des tâches les plus difficiles est de décider quel patient doit recevoir quel traitement complémentaire et à quel moment. La transplantation cardiaque offre généralement une très bonne qualité de vie et les patients ont une excellente survie à long terme (après 12,4 ans, 50% des patients transplantés sont encore en vie [ISHLT]). Cependant, en raison de la pénurie persistante d’organes de donneurs, ce traitement ne peut être proposé qu’à un petit nombre de patients sélectionnés, généralement plus jeunes. Avec un délai d’attente moyen de 1 à 2 ans, la transplantation n’est en outre pas une option dans la situation aiguë ; une assistance circulatoire mécanique avec un système d’assistance ventriculaire gauche (LVAD) est alors envisagée comme alternative thérapeutique à long terme (Destination-Therapy) ou comme solution de transition (Bridge-to-Transplant). T. Carrel et D. Reineke ont publié dans le
dernier numéro
ont donné un bon aperçu de l’assistance circulatoire mécanique en cas d’insuffisance cardiaque aiguë et chronique.
Qui bénéficie d’un cœur artificiel et comment reconnaître le moment optimal pour une telle thérapie ?
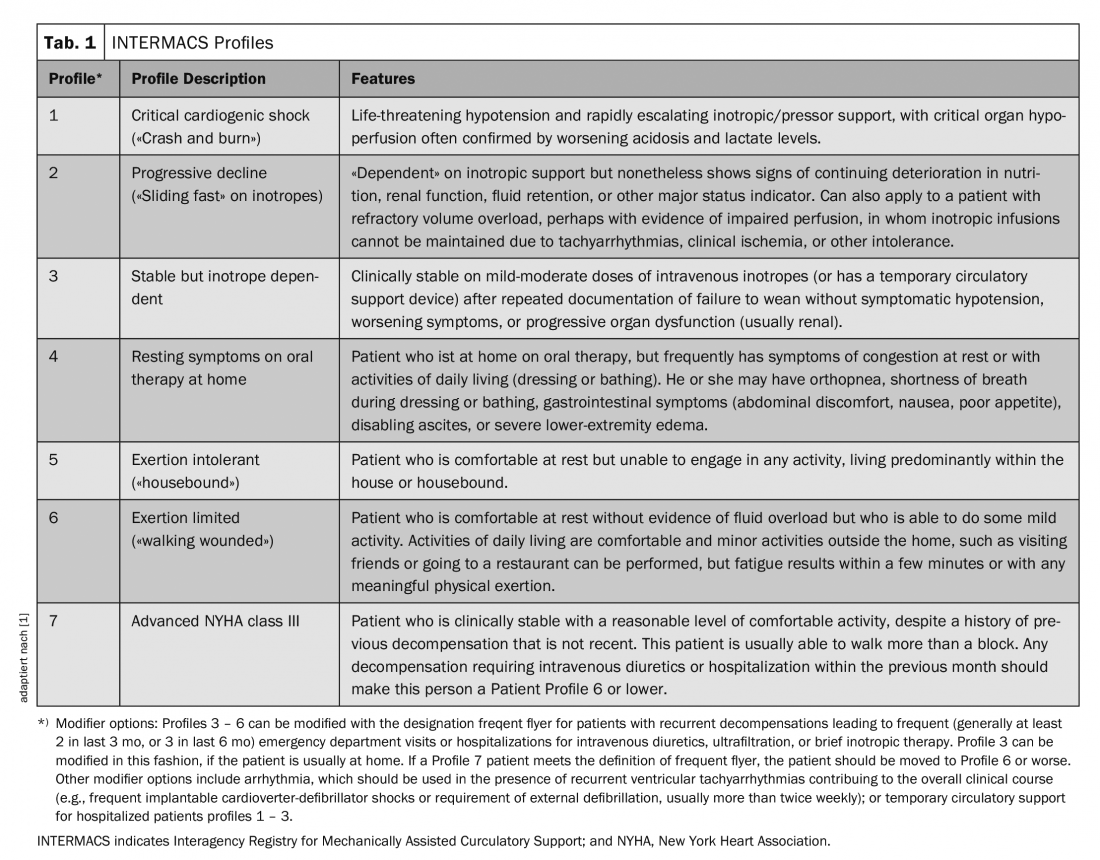
Ces dernières années, l’implantation d’un dispositif d’assistance ventriculaire gauche (DAVG) a été envisagée principalement chez les patients appartenant aux catégories 1 à 3 de l’INTERMACS (IM). (Tab.1). C’est-à-dire les patients en état de choc cardiogénique critique (profil IM 1), une détérioration rapide malgré une thérapie intensive maximale (profil IM 2) ou ceux qui ne peuvent pas être sevrés de la thérapie par inotropes (profil IM 3), c’est-à-dire les patients pour lesquels une survie en dehors de l’hôpital n’aurait pas été possible sans thérapie supplémentaire.
Le plus grand registre de patients porteurs de dispositifs d’assistance mécanique est tenu par la Société internationale de transplantation cardiaque et pulmonaire (IMACS ; International Society for Heart and Lung Transplantation Mechanical Circulatory Support Registry). Il comprend des données provenant de 35 pays ainsi que des grands registres d’Europe (EUROMACS), des États-Unis (INTERMACS) et du Japon (J-MACS) [2]. Entre janvier 2013 et décembre 2016, un total de 14 062 implantations de dispositifs ont été enregistrées, dont 93% de DAVG purs, 5% de systèmes d’assistance biventriculaire et 2% de “total artificial hearts”, c’est-à-dire de cœurs artificiels complets. 83% des patients étaient en catégorie IM 1-3, près de 28% étaient activement listés pour une transplantation cardiaque, 41% ont reçu un appareillage en tant que traitement final (Destination-Therapy).
Le taux de survie à un an et à deux ans chez les patients ayant subi une implantation d’appareillage à flux continu était respectivement de 81% et 71%. Les patients présentant un profil IM 1 avaient un taux de survie à un an nettement moins bon que ceux présentant un profil IM 3 (71% contre 84%), le meilleur taux de survie à deux et trois ans étant observé chez les patients présentant un profil IM 5-7, c’est-à-dire les patients ambulatoires souffrant d’insuffisance cardiaque sévère.
Attendons-nous trop longtemps ?
L’étude ROADMAP s’est penchée sur cette question et a inclus 200 patients ambulatoires souffrant d’insuffisance cardiaque sévère (profil IM ≥4, distance de marche lors du test de marche de 6 min (6 MWT) <300 mètres, au moins une hospitalisation ou deux présentations aux urgences pour insuffisance cardiaque au cours de la dernière année) qui ne se qualifient pas pour une transplantation cardiaque ont été inclus dans cette étude multicentrique prospective et non randomisée [3]. Les patients ont pu choisir, avec leurs médecins, entre une thérapie médicamenteuse optimale (OMT) ou une implantation d’appareillage (Destination Therapy). Le critère d’évaluation principal était la survie sous le traitement initialement choisi et une amélioration de 75 mètres ou plus dans le 6 MWT. Les critères d’évaluation secondaires comprenaient le relevé de la qualité de vie (EuroQol 5 dimensions, 5-level questionnaire, EQ-5D-5L) ainsi qu’un score de dépression (Patient Health Questionnaire, PHQ-9) au moyen d’un questionnaire, la classe NYHA et les événements indésirables.
Comme on pouvait s’y attendre, les patients qui ont initialement opté pour un LVAD étaient globalement plus malades et avaient une moins bonne qualité de vie (groupe LVAD vs groupe OMT : qualité de vie (EQ-5D VAS) 44 vs 66 points, dépression (score PHQ-9) 10 vs 7 points, NYHA IV 52% vs 25%, profil Intermacs 4 65% vs 34%, IM 5 ou plus 32% vs 64%).
Malgré une situation de départ moins favorable, davantage de patients ont montré une amélioration de leur capacité à atteindre une classe NYHA I/II deux ans après l’implantation de l’appareillage (69% vs 37% sous OMT) et la distance de marche a augmenté de manière significative. En outre, les patients ont signalé une amélioration significative de leur qualité de vie (EQ-5D VAS +27pts) et de leur humeur (score de dépression PHQ 9 -4,6pts). Aucun changement significatif n’a été détecté dans le groupe des OMT.
Il est toutefois intéressant de noter que dans les deux années qui ont suivi, près d’un quart des patients du groupe OMT (21%) ont opté pour une implantation de l’appareillage, et ce dès 4,9 mois en médiane après l’inclusion. Plus de la moitié des patients (55%) ayant subi une implantation retardée de l’appareillage étaient déjà sous traitement inotrope à ce moment-là, 70% avaient atteint le stade IV de la NYHA et la distance médiane de marche a diminué de 219 m initialement à 90 m. Les patients qui ont subi une implantation retardée de l’appareillage n’ont pas eu besoin de traitement inotrope.
Si l’on ajoute au groupe OMT (intention de traiter) ce groupe relativement important de patients ayant subi une implantation tardive de l’appareillage, aucune différence significative de survie n’apparaît entre les deux groupes. Cependant, si on les sépare en fonction du traitement effectivement reçu, on constate que seuls 41% du groupe OMT ont survécu sous le traitement initial, contre 70% du groupe LVAD.
Le nombre d’effets indésirables (EI) était plus élevé dans le groupe LVAD que dans le groupe OMT. Les EI les plus fréquents après l’implantation de l’appareillage étaient les hémorragies, les infections drivelines, les thromboses de la pompe et les accidents vasculaires cérébraux ; dans le groupe OMT, il s’agissait surtout d’une aggravation de l’insuffisance cardiaque (50% des patients). De manière surprenante, malgré les EI et les hospitalisations plus fréquentes (86% vs 78%), les patients atteints d’appareillage ont déclaré une meilleure qualité de vie et une meilleure humeur.
Si l’on répartit les patients en fonction de la gravité de leur maladie, on constate que ce sont surtout les patients atteints de MI 4 qui en ont bénéficié, ceux atteints de MI 5-7 n’en bénéficiant que s’ils avaient auparavant déclaré une qualité de vie limitée.
Si l’on résume toutes les conclusions de cette étude, on peut dire que les patients atteints de MI 5-7 qui déclarent une qualité de vie acceptable peuvent attendre avant d’être implantés sans risquer une mortalité excessive, tant qu’ils sont suivis régulièrement et étroitement dans un centre (dans cette étude, la détérioration médiane est survenue après seulement 4,9 mois).
Optimisation du traitement avant l’implantation de l’appareillage
Depuis la réalisation de l’étude ROADMAP et la dernière collecte de données du registre IMACS en 2016, les nouveaux traitements médicamenteux (sacubitril-valsartan) et interventionnels (MitraClip®, ablation de la fibrillation auriculaire) ont été de plus en plus utilisés dans la pratique quotidienne. Dans l’étude PARADIGM-HF Trial, le traitement par sacubitril-valsartan a montré une réduction relative de 20% de la mortalité et des hospitalisations pour insuffisance cardiaque chez les patients les moins malades (moins de 1% seulement avaient une NYHA IV, la majorité environ 70% une NYHA II) par rapport au traitement par énalapril [4]. Dans CASTLE-AF, un groupe de patients très sélectionnés souffrant d’insuffisance cardiaque et de fibrillation auriculaire a présenté une réduction relative de 38% du critère d’évaluation combiné de décès et de réhospitalisation pour cause d’insuffisance cardiaque après ablation de la fibrillation auriculaire [5]. L’essai COAPT a montré une réduction de la mortalité (RRR -38%) et du taux de réhospitalisation pour cause d’HI (RRR -47%) après l’implantation de MitraClip® par rapport au traitement médicamenteux chez les patients souffrant d’insuffisance mitrale secondaire sévère et d’insuffisance cardiaque [6]. Même si tous les patients ne bénéficient certainement pas de ces thérapies, nous disposons de plus en plus de moyens pour aider ces patients gravement malades.
Mais ces dernières années, de nombreux développements techniques ont également permis de réduire le taux de complications après l’implantation d’un appareillage. D’une part, des données récentes permettent une prise en charge plus optimale des patients (ainsi, l’ENDURANCE Supplemental Trial a permis d’obtenir une réduction significative du taux d’AVC grâce à un meilleur contrôle de la pression artérielle), et d’autre part, des changements techniques sont apparus avec la dernière génération de LVAD (HeartMate 3®, Abbott) [7]. Dans l’étude MOMENTUM 3, l’implantation du HeartMate 3® (une pompe centrifuge) a entraîné une réduction significative du taux global d’AVC (10 % contre 19 %, le nombre d’AVC graves (score de Rankin modifié) étant plus élevé que le nombre d’AVC légers. >3) est resté le même), ainsi qu’un taux nettement inférieur de thromboses de pompe possibles ou confirmées (1,1% vs 15,7%) par rapport au HeartMate 2®. Aucun HeartMate 3® n’a dû être remplacé ou explanté en raison d’une suspicion de thrombose de la pompe, alors que cela a été le cas pour 12% des patients avec HeartMate 2® [8].
Un traitement optimisé pour chaque patient
Avec toutes les possibilités techniques, interventionnelles et médicamenteuses, nous pouvons aujourd’hui offrir aux patients souffrant d’insuffisance cardiaque beaucoup plus d’options qu’auparavant. En même temps, cela implique aussi l’obligation de trouver pour chaque patient le traitement qui lui convient le mieux. Afin de permettre au patient et à sa famille d’examiner calmement tous les avantages et inconvénients de chaque traitement et de réaliser les interventions dans un cadre électif, il est important de rencontrer les patients à un stade précoce dans un centre pour insuffisance cardiaque sévère et de coordonner les soins ultérieurs avec les médecins traitants, les cardiologues et les autres personnes impliquées dans l’environnement.
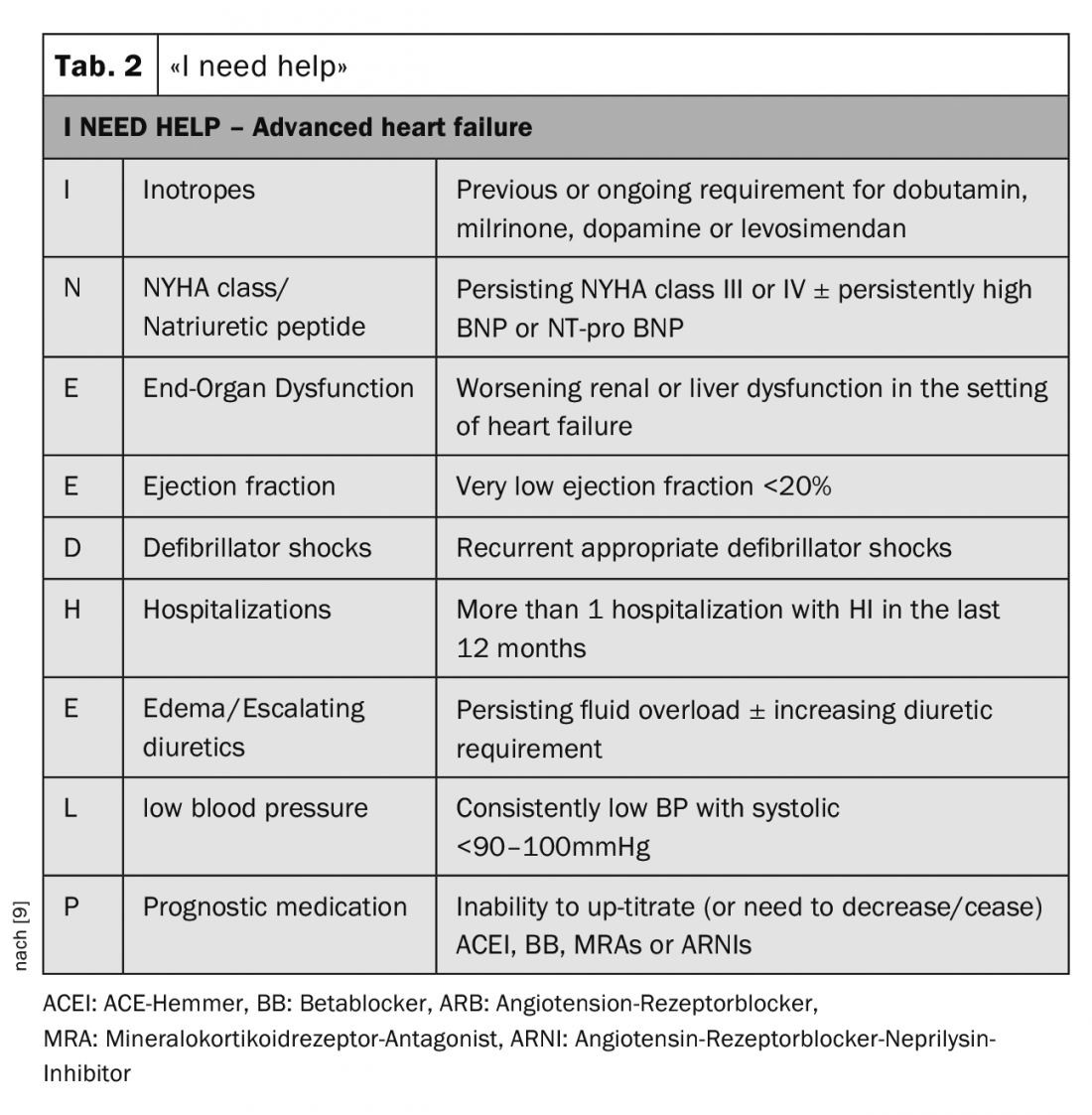
L’aide-mémoire “I need help” est très utile pour identifier les patients qui ont besoin d’une évaluation plus poussée dans un centre. (tableau 2). En particulier, les patients présentant des décompensations cardiaques récurrentes ou ceux pour lesquels il est impossible d’augmenter le traitement de l’insuffisance cardiaque, voire de le réduire, doivent être adressés à un spécialiste pour évaluation.
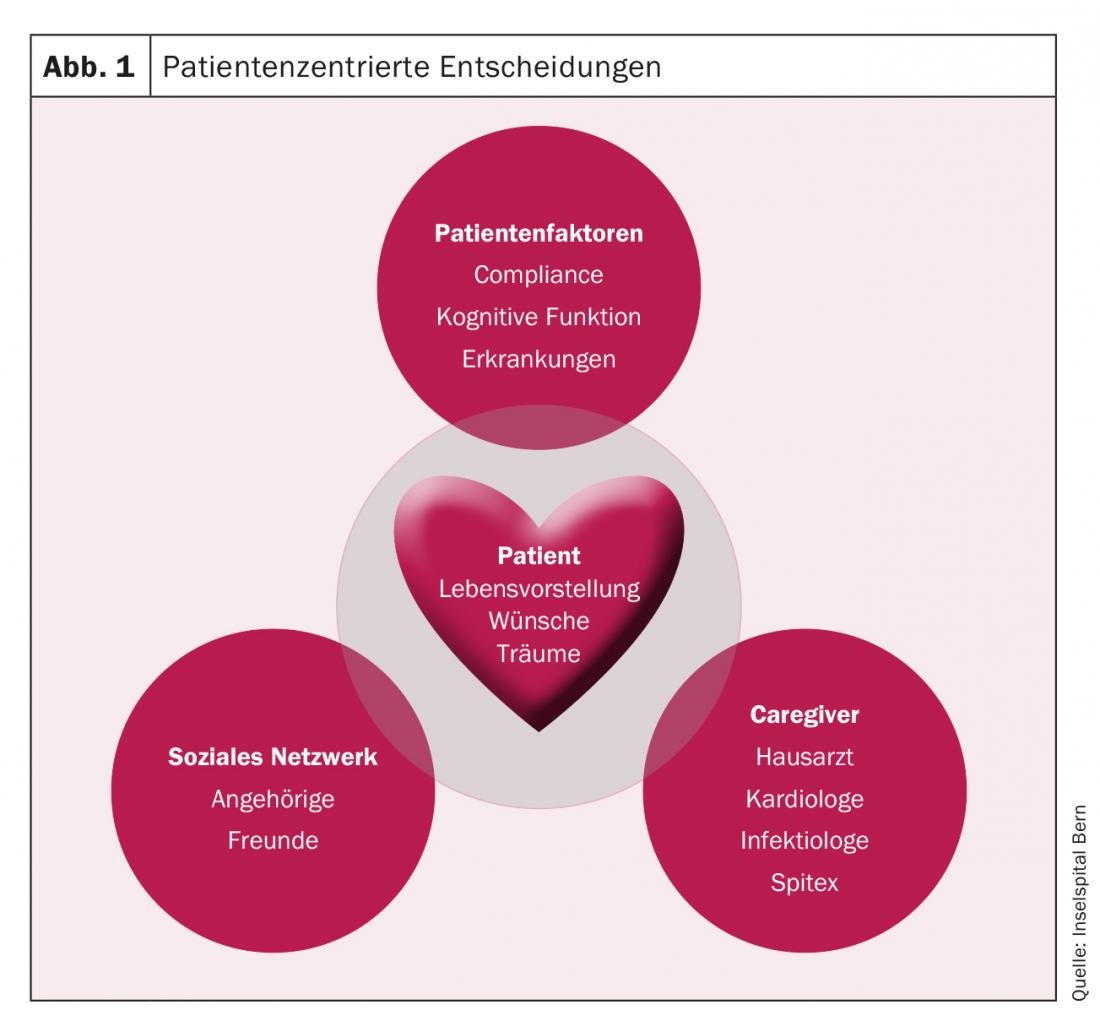
La décision finale pour ou contre un appareillage doit être prise avant tout en tenant compte des souhaits et des idées de vie du patient, en impliquant son réseau social (amis, famille), en collaboration avec le patient, sa famille et les caregiver (par ex. le médecin de famille, le cardiologue, les soins à domicile) (Fig. 1).
Messages Take-Home
- Pour les patients souffrant d’insuffisance cardiaque, nous disposons aujourd’hui d’un nombre croissant de traitements médicamenteux (sacubitril-valsartan), interventionnels (CRT, Mitralclip® en cas d’insuffisance mitrale, ablation en cas de fibrillation auriculaire) et techniques (LVAD). Afin de permettre aux patients, à leur famille ainsi qu’aux médecins traitants de discuter calmement de toutes les options thérapeutiques disponibles et de trouver le traitement optimal pour chaque patient, il est important de les présenter le plus tôt possible à un centre de l’insuffisance cardiaque.
- L’aide-mémoire “I need help” (J’ai besoin d’aide) peut servir de guide pour savoir quand les patients doivent être envoyés au plus tard chez un spécialiste de l’IH.
- Ces dernières années, une meilleure prise en charge des patients ainsi que des progrès techniques ont permis de réduire les complications graves (p. ex. thrombose de la pompe, accident vasculaire cérébral) pour les patients atteints de DAVG. En raison de la pénurie croissante d’organes de donneurs, l’implantation de l’appareillage représente une bonne alternative pour un nombre croissant de patients souffrant d’insuffisance cardiaque sévère.
- Chez les patients présentant un profil INTERMACS 5-7 et une qualité de vie préservée, il convient d’attendre avant d’implanter un appareillage. Un suivi étroit est indispensable pour ne pas passer à côté des premiers signes d’une détérioration souvent rapide et éviter ainsi des interventions à haut risque.
- Les patients présentant un profil INTERMACS 5-7 avec une qualité de vie limitée doivent évaluer s’ils sont prêts à accepter un taux accru de complications pour avoir une chance d’améliorer leur qualité de vie.
Littérature :
- Yancy CW et al : 2013 ACCF/AHA guideline for the management of heart failure : a report of the American College of Cardiology Foundation/American Heart Association Task Force on practice guidelines. (Adapté de Stevenson et al. INTERMACS profiles of advanced heart failure : the current picture. J Heart Lung Transplant. 2009;28:535-4). Circulation 2013;128(16):e240-327.
- Kirklin JK, et al : J Heart Lung Transplant 2018 ; 37(6) : 685-691.
- Starling RC, et al : Évaluation du risque et efficacité comparée du dispositif d’assistance ventriculaire gauche et de la prise en charge médicale chez les patients ambulatoires atteints d’insuffisance cardiaque : l’étude ROADMAP 2 ans de résultats. JACC Heart Fail 2017 ; 5(7) : 518-527.
- McMurray JJ, et al : Angiotensin-neprilysin inhibition versus enalapril in heart failure. N Engl J Med 2014 ; 371(11) : 993-1004.
- Marrouche NF, et al : Ablation par cathéter pour fibrillation auriculaire avec défaillance cardiaque. N Engl J Med 2018 ; 378(5) : 417-427.
- Stone GW, et al : Transcatheter Mitral-Valve Repair in Patients with Heart Failure. N Engl J Med 2018 ; 379(24) : 2307-2318.
- Milano CA, et al. : HVAD : The ENDURANCE Supplemental Trial. JACC Heart Fail 2018 ; 6(9) : 792-802.
- Mehra MR, et al : Two-Year Outcomes with a Magnetically Levitated Cardiac Pump in Heart Failure (Résultats à deux ans avec une pompe cardiaque à lévitation magnétique en cas d’insuffisance cardiaque). N Engl J Med 2018 ; 378(15) : 1386-1395.
- Baumwol J : “I Need Help”-A mnemonic to aid timely referral in advanced heart failure. J Heart Lung Transplant 2017 ; 36(5) : 593-594.
CARDIOVASC 2019 ; 18(1) : 16-19