Les multiples manifestations de la maladie du lupus érythémateux systémique (LES) sont essentiellement dues à des auto-anticorps, des complexes immuns et des cytokines. De nouvelles thérapies ciblent l’immunopathogénèse de cette maladie auto-immune complexe. Pendant longtemps, le belimumab a été le seul médicament biologique autorisé spécifiquement pour le LED. Depuis, un autre anticorps monoclonal, l’anifrolumab, a reçu une autorisation de mise sur le marché dans ce domaine d’indication et de nombreux autres candidats médicaments sont actuellement à l’étude. Dans l’optique d’une stratégie de traitement personnalisée, l’identification de biomarqueurs revêt une importance croissante.
Martin Aringer, de l’hôpital universitaire de Dresde (Allemagne) [1]. Selon les critères actuels de classification EULAR/ACR, le critère d’entrée pour le lupus érythémateux systémique (LED) est la détection d’anticorps antinucléaires (ANA) positifs [2,3,13]. D’autres paramètres immunologiques tels que les facteurs de complément – les taux sériques de complément (C3/C4) sont souvent abaissés en cas de maladie active – sont également importants, mais leur sensibilité est moindre par rapport aux ANA et ils font donc simplement partie des critères pondérés**. Ces derniers sont associés à des domaines qui sont associés à différentes manifestations du LED.
** Valeur de cut off sur 10 points
Les cellules B et les voies de signalisation de l’interféron au cœur de la recherche
L’étiopathogénie du LED n’est pas encore totalement élucidée à ce jour. Mais au cours des dernières décennies, certains mécanismes corrélés au LED ont été identifiés [4]. Il s’agit notamment de
- Facteurs contribuant à l’activation des lymphocytes B ou à la survie des lymphocytes B autoréactifs
- Perturbation de l’élimination du matériel cellulaire apoptotique, qui contient de nombreux auto-antigènes associés au LED
- influence chronique de l’interféron comme “signal de danger viral”.
On pense que les auto-anticorps pathogènes peuvent en partie agir directement sur les cellules et, sous forme de complexes immuns et avec l’aide du complément, activer les macrophages qui alimentent la réaction inflammatoire via des cytokines pro-inflammatoires. En outre, les auto-anticorps contribuent à la survie des lymphocytes autoréactifs et à la formation d’autres auto-anticorps par l’intermédiaire de la cytokine des cellules B BLyS/BAFF et des interférons dans une boucle de rétroaction positive [4]. Plusieurs nouveaux médicaments immunomodulateurs ont été développés au cours des dernières décennies. Et on espère que les études “poly-omiques” à grande échelle (génomique, protéomique et métabolomique) permettront d’en savoir plus sur les mécanismes immunologiques clés [5].
Les biothérapies sont porteuses d’espoir – le choix du traitement devient central
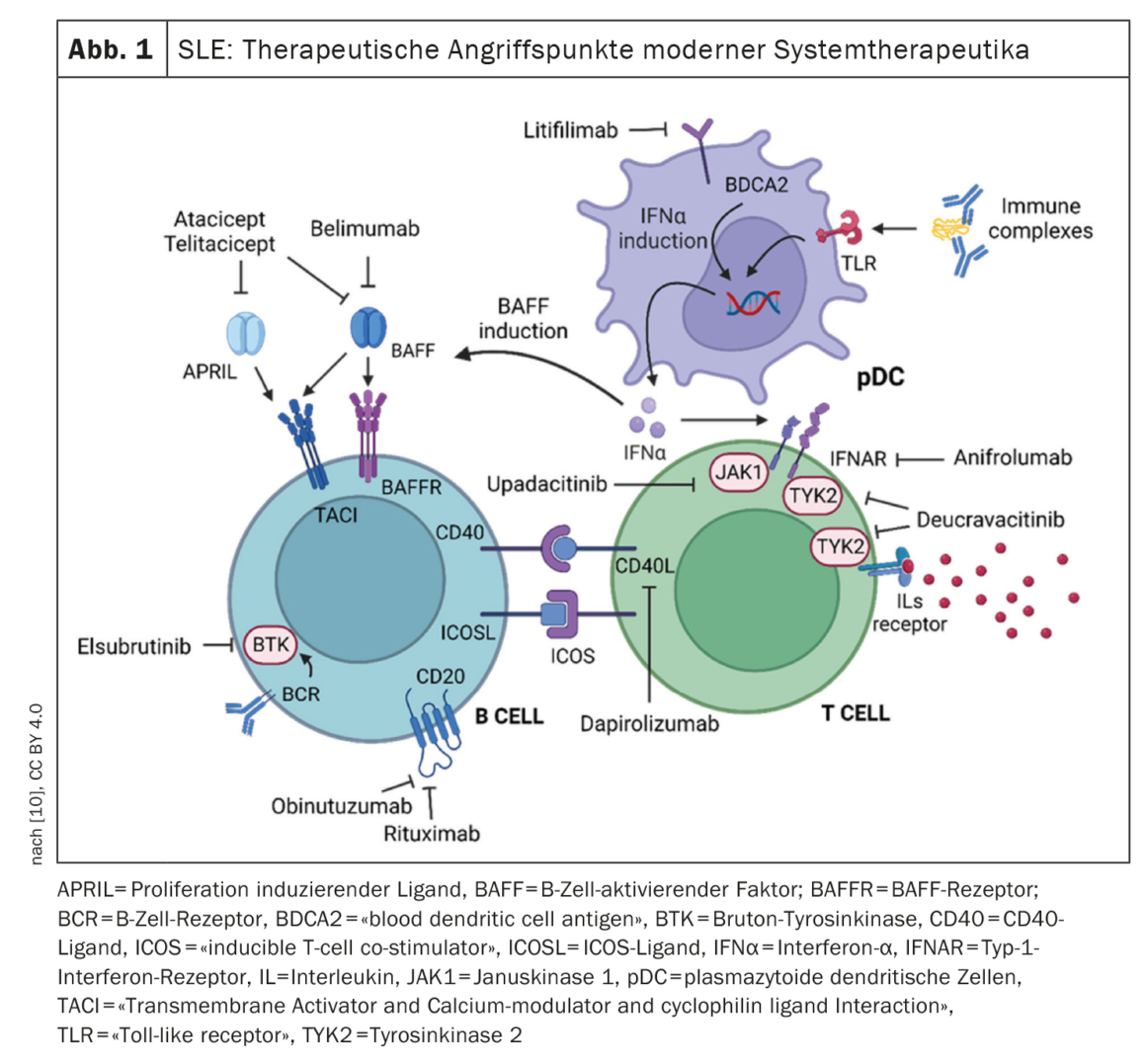
Le lupus érythémateux disséminé est considéré comme une maladie auto-immune à médiation cellulaire B. Le rituximab est un traitement de déplétion des cellules B qui empêche la formation de blastes plasmatiques. Malgré des preuves d’efficacité dans certaines études, le rituximab n’a pas été officiellement autorisé en Suisse dans le domaine d’indication du LED. Toutefois, sur demande, une garantie de prise en charge peut être accordée par la caisse d’assurance maladie [6]. Le premier médicament biologique approuvé spécifiquement pour le LED a été le bélimumab, un inhibiteur de BLyS. En inhibant BAFF/BLyS, le bélimumab provoque un blocage sélectif de l’activation des cellules B. Le bélimumab peut être utilisé dans le traitement de l’hypertension artérielle. Sous belimumab, le nombre de cellules B naïves et activées, et par conséquent de blastes plasmatiques, diminue, ce qui entraîne une baisse des taux d’auto-anticorps et une amélioration des taux de complément C3 et C4 [7]. Les produits biologiques peuvent catalyser l’obtention d’une réduction des symptômes. Mais ce n’est pas tout : “Le belimumab et l’anifromulab peuvent aider à équilibrer les glucocorticoïdes et ont été testés dans différentes populations d’étude”, a déclaré le professeur Dimitrios T. Boumpas, MD, Département de médecine, Université nationale et capodistrienne d’Athènes [8]. L’anifrolumab a été approuvé sur la base des résultats des études TULIP [9]. Il a été démontré que l’efficacité de l’anifrolumab est positivement corrélée à des taux sériques élevés d’IFN [9]. Le belimumab et l’anifrolumab se sont tous deux révélés supérieurs au placebo chez les patients atteints de LED présentant des marqueurs sérologiques anormaux à la ligne de base (C3/C4 et/ou ADN anti-ds). Le belimumab a été testé dans des études randomisées sur différentes populations. Outre le belimumab et l’anifrolumab, des biothérapies déjà approuvées, des données prometteuses de phase II ont été obtenues pour l’iberdomide, le litifilimab et le deucravacitinib. Par ailleurs, plusieurs autres candidats médicaments font l’objet de recherches [10] (Fig. 1) .
Congrès : réunion annuelle de l’EULAR
Littérature :
- “Lupus classification and diagnosis still based on clinical manifestations”, Prof Dr Martin Aringer, Universitätsklinikum Dresden, EULAR Annual Meeting, 31.05.-03.06.2023.
- Aringer M, et al : 2019 European League Against Rheumatism/American College of Rheumatology classification criteria for systemic lupus erythematosus. Arthritis Rheumatol 2019 ; 71 : 1400-1412.
- Aringer M, et al : 2019 European League Against Rheumatism/American College of Rheumatology classification criteria for systemic lupus erythematosus. Ann Rheum Dis 2019 ; 78 : 1151-1159.
- Aringer M, Finzel S, Voll RE : Immunopathogénèse du lupus érythémateux systémique. Z Rheumatol 2022. https://doi.org/10.1007/s00393-022-01214-4
- Aringer M, et al : A glimpse into the future of systemic lupus erythematosus. Ther Adv Musculoskelet Dis 2022 ; 14 : 1759720X221086719.
- Magazine pour les personnes atteintes de lupus érythémateux, 1/2017 ; www.lupus-suisse.ch,(dernière consultation 23.06.2023)
- Hiepe F : Nouvelles connaissances sur la pathogenèse du LED et leur impact sur le développement de nouveaux concepts thérapeutiques. Akt Rheumatol 2020 ; 45 : 328-333
- “Comment traiter le lupus”, professeur, Dimitrios T. Boumpas, MD, réunion annuelle de l’EULAR, 31.05.-03.06.2023.
- Morand EF, et al ; Investigateurs de l’essai TULIP-2. Essai de l’anifrolumab dans le lupus érythémateux disséminé actif. N Engl J Med 2020 ; 382(3) : 211-221.
- Venturelli V, Isenberg DA : Targeted Therapy for SLE-What Works, What Doesn’t, What’s Next. Journal of Clinical Medicine 2023 ; 12(9) : 3198.
www.mdpi.com/2077-0383/12/9/3198,(dernier appel 23/06/2023) - Ruiz-Irastorza G, Gertsias G : Rhumatologie (Oxford) 2020 ; 59(Suppl. 5) : v69-v81.
- Choi ST, et al : Analyse par sous-échelle de la qualité de vie chez les patients atteints de lupus érythémateux disséminé : association avec la dépression, la fatigue, l’activité de la maladie et les dommages. Clin Exp Rheumatol 2012 ; 30 : 665-672.
- Fanouriakis A, et al : 2019 update of the EULAR recommendations for the management of systemic lupus erythematosus.Ann Rheum Disease 2019 ; 78 : 736-745.
- Miyazaki C, et al : Modèles de traitement et coût médical des patients atteints de lupus érythémateux disséminé au Japon : une étude rétrospective de la base de données des réclamations. J Med Econ 2020 ; 23 : 786-799.
HAUSARZT PRAXIS 2023 ; 18(7) : 32-33 (publié le 12.7.23, ahead of print)