De nouvelles données confirment les résultats de la première étude de phase III publiés en début d’année. Dans les deux études, par rapport au placebo, une proportion significativement plus élevée de patients traités par baricitinib a atteint le critère d’évaluation principal de la croissance des cheveux à la semaine 36, pour les deux schémas posologiques.
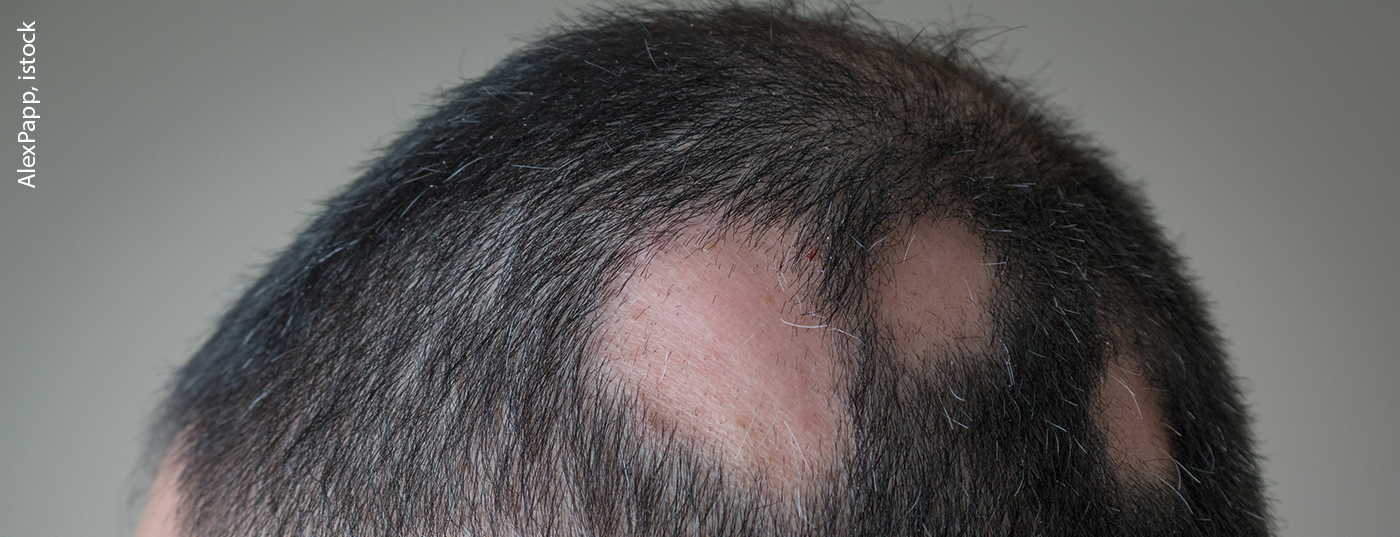
L’alopécie areata (AA*) est une maladie auto-immune qui entraîne une perte de cheveux aiguë et inflammatoire du cuir chevelu, du visage et parfois d’autres parties du corps, qui peut être progressive et pour laquelle les options de traitement sont actuellement limitées. L’étude de phase III BRAVE-AA1 a permis de reproduire le profil d’efficacité et d’innocuité avantageux du baricitinib chez les adultes atteints d’alopécie areata sévère, tel qu’il a été observé dans la première étude clinique de phase III BRAVE-AA2.
*AAA = chute de cheveux aiguë d’origine inflammatoire
Les deux dosages sont significativement supérieurs au placebo
Dans les deux études, les patients atteints d’alopécie sévère traités par baricitinib 2 mg et 4 mg une fois par jour pendant la période de traitement de neuf mois ont montré, selon l’évaluation du médecin, une croissance significativement plus importante des cheveux sur le cuir chevelu par rapport aux patients du groupe placebo. À la semaine 36, dans l’étude BRAVE-AA1, une proportion significativement plus élevée de patients traités par baricitinib a atteint une pilosité crânienne de 80% ou plus par rapport au placebo (p≤0,001). Cette proportion était de 35% chez les patients traités par baricitinib 4 mg/jour, de 22% chez les patients traités par baricitinib 2 mg/jour et de 5% dans le groupe placebo. Dans l’étude BRAVE-AA2, le pourcentage de patients ayant atteint un taux de couverture des cheveux de 80% ou plus était de 33% chez les patients traités par baricitinib 4 mg /jour et de 17% chez les patients traités par baricitinib 2 mg/jour, contre 3% des sujets du groupe placebo.
Pas de nouveaux signaux de sécurité
Les effets indésirables liés au traitement les plus fréquents dans BRAVE-AA1 et BRAVE-AA2 comprenaient des infections des voies respiratoires supérieures, des maux de tête et de l’acné. Aucun décès ou événement thromboembolique veineux n’a été rapporté dans les études. Dans les deux études, le profil de sécurité du baricitinib était conforme à son profil de sécurité connu chez les patients atteints de polyarthrite rhumatoïde (PR) et de dermatite atopique (DA).
Source : “Lilly and Incyte’s Baricitinib Improved Hair Regrowth for Alopecia Areata Patients in Second Phase 3 Study”, Eli Lilly, 20.04.2021
DERMATOLOGIE PRATIQUE 2021 ; 31(3) : 38