Bien que la démence ne soit pas l’une des maladies neurologiques les plus courantes, elle constitue déjà un problème pertinent et son importance va considérablement augmenter en raison de l’évolution démographique.
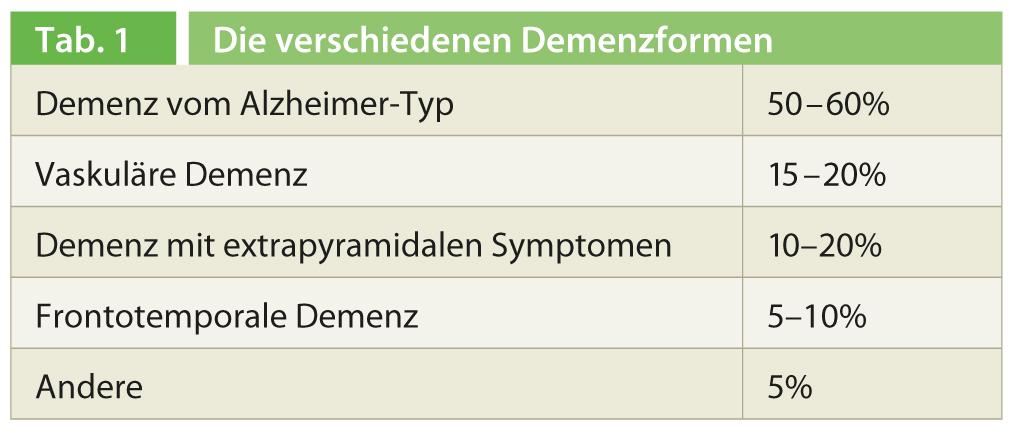
La démence est une maladie cérébrale chronique et progressive qui entraîne des troubles dans plusieurs sphères cognitives telles que la mémoire, le raisonnement, l’orientation, la compréhension, le calcul, la capacité d’apprentissage, le langage, la parole et le jugement. La conscience des personnes démentes n’est pas altérée et la perception sensorielle est préservée. En revanche, on observe des modifications du contrôle émotionnel, du comportement social et/ou de la motivation, avec les conséquences que cela implique sur la vie quotidienne. Selon la définition de la CIM-10, cet état doit persister pendant une période d’au moins six mois pour que le diagnostic de démence puisse être posé. Outre la cognition, la démence affecte plusieurs compétences quotidiennes et fonctions corporelles. La démence de type Alzheimer est de loin la forme de démence la plus fréquente, avec 50 à 60% des cas (tableau 1).
Diagnostic
“Dans le diagnostic de la démence, vous avez un rôle à jouer en tant que praticien. Vous connaissez les patients et leurs familles et, la plupart du temps, vous êtes la première personne à contacter lorsqu’une personne change de comportement”, explique le professeur Hans Jung, de l’Hôpital universitaire de Zurich. Outre l’anamnèse et l’anamnèse externe, les mesures suivantes peuvent être facilement mises en œuvre dans chaque cabinet pour un premier dépistage de la démence :
- le recueil d’un bilan interne, neurologique et psychopathologique orienté,
- Examens de laboratoire de base (électrolytes, taux thyroïdiens, taux rénaux, vitamine B12, acide folique, VIH, lues) ainsi que
- un ou plusieurs tests courts standardisés (Mini-Mental-State, test de l’horloge).
Il peut également être nécessaire de demander une imagerie. Selon la situation, d’autres étapes diagnostiques, comme des tests neurophysiologiques plus détaillés, peuvent être entreprises en collaboration avec un spécialiste. “En particulier chez les jeunes patients – et j’entends par là les patients de moins de 65 ou 70 ans ( !) – ainsi qu’en cas d’incertitude diagnostique, un diagnostic du liquide céphalo-rachidien, un EEG ou une imagerie plus poussée avec le PET ou le SPECT peuvent également être indiqués”, poursuit le professeur Jung. Lors du diagnostic du LCR, ce sont surtout les taux d’inflammation, de tau, de phospho-tau, de β-amyloïde et de protéine 14-3-3 qui sont intéressants).
Des symptômes précoces, tels que des troubles cognitifs légers n’affectant que la mémoire, peuvent dans certains cas être des signes précurseurs de la démence d’Alzheimer. 20 à 30% des patients atteints de MCI (Mild Cognitive Imp airement) finissent par développer une démence de type Alzheimer. En théorie, il serait possible d’identifier les patients qui développeront une démence d’Alzheimer à ce stade précoce à l’aide de marqueurs spécifiques dans le LCR et dans le PET/SPECT, mais en pratique, cela n’a pas de sens tant qu’aucun traitement préventif n’est disponible.
Possibilités thérapeutiques
Malgré des recherches intensives, les seuls traitements disponibles à ce jour, outre le soutien psychosocial apporté aux patients et à leurs familles, sont des médicaments destinés à traiter les symptômes. Des effets positifs significatifs sur les symptômes de démence ont été démontrés tant pour les inhibiteurs de l’acétylcholinestérase (rivastigmine, galantamine, donézépil) que pour la mémantine. Les premiers sont indiqués en cas de démence d’Alzheimer légère à modérée, les seconds en cas de démence d’Alzheimer modérée à sévère.
Les inhibiteurs de l’acétylcholinestérase permettent d’améliorer la transmission cholinergique dans le cerveau, qui est réduite en cas de démence d’Alzheimer. L’évolution de la maladie ne peut certes pas être stoppée, mais l’état peut être considérablement amélioré et stabilisé, ce qui permet de retarder l’apparition de la perte d’autonomie et de la dépendance [1, 2]. S’il existe des déficits importants, il convient donc de faire un essai avec ces médicaments relativement tôt après le diagnostic.
Les effets secondaires cholinergiques tels que les nausées, les vomissements et la diarrhée sont relativement fréquents avec les inhibiteurs de l’acétylcholinestérase, le plus souvent avec la rivastigmine, bien que cela ne soit vrai que pour la formulation orale. Sous le patch de rivastigmine, disponible depuis quelques années, le taux d’effets secondaires est significativement plus faible et seulement légèrement plus élevé que sous placebo [3]. De plus, le patch est disponible en deux dosages (9,5 mg/24h et 13,3 mg/24h), ce qui permet d’obtenir un bénéfice supplémentaire en termes d’efficacité avec le patch plus fortement dosé, tout en conservant le même taux d’effets secondaires [4].
La mémantine est surtout efficace dans les stades modérés et tardifs de la démence d’Alzheimer et peut contribuer à une nette amélioration de la situation de soins en influençant positivement les troubles du comportement. “Des études montrent clairement qu’il serait utile de combiner la mémantine avec un inhibiteur de l’acétylcholinestérase, mais malheureusement cette combinaison n’a pas encore été approuvée et vous devez donc la demander individuellement dans chaque cas”, a conclu l’orateur [5].
Source : Lunchsymposium, Medidays 2013, 2-6 septembre 2013, UniversitätsSpital Zürich.
Littérature :
- Birks J : Inhibiteurs de la cholinestérase pour la maladie d’Alzheimer. Base de données Cochrane des revues systématiques 2006 : CD005593.
- Birks J : Les inhibiteurs de la cholinestérase (ChEIs), le donépézil, la galantamine et la rivastigmine sont efficaces pour la maladie d’Alzheimer légère à modérée. Résumés Cochrane. Publié en ligne : May 16, 2012.
- Winblad B, et al : Caregiver preference for rivastigmine patch relative to capsules for treatment of probable Alzheimer’s disease. Int J Geriatr Psychiatry 2007 ; 22 : 485-491.
- Cummings J, et al : Randomized, double-blind, parallel-group, 48-week study for efficacy and safety of a higher-dose rivastigmine patch (15 vs. 10 cm2) in Alzheimer’s disease. Dement Geriatr Cogn Disord 2012 ; 33 : 341-353.
- Farrimond LE, et al : Memantine and cholinesterase inhibitor combination therapy for Alzheimer’s disease : a systematic review. BMJ Open 2012;2. pii : e000917.
HAUSARZT PRAXIS 2013, Vol. 8, n° 9