Pour la première fois après l’étude FOURIER, qui a fait couler beaucoup d’encre, un inhibiteur de PCSK9 montre désormais un bénéfice en termes de mortalité dans la prévention secondaire. Il s’agit de l’alirocumab. Les professionnels réagissent positivement et discutent déjà d’une réduction des valeurs cibles.
Brève rétrospective : Le congrès ACC 2017 a été marqué par l’étude FOURIER, qui a fourni pour la première fois des données sur les critères d’évaluation “durs” tant attendus (et réclamés avec insistance) dans le domaine de l’inhibition des PCSK9. L’ajout d’évolocumab a réduit de manière significative le risque de décès cardiovasculaire, d’infarctus du myocarde, d’accident vasculaire cérébral, d’hospitalisation pour angor instable ou de revascularisation coronarienne. L’évolocumab s’est également révélé supérieur au placebo dans le critère d’évaluation secondaire, qui ne comprenait que le décès cardiovasculaire, l’infarctus du myocarde ou l’accident vasculaire cérébral (ajouté au traitement par statine existant avec/sans ézétimibe) – concrètement, le risque a été réduit de 20%. Et ce, avec un bon profil de sécurité. L’hypothèse “the lower, the better” semblait confirmée, mais la grande question était la suivante : les résultats sont-ils suffisants pour justifier les prix non négligeables des médicaments de cette classe de substances actives et pour utiliser ces médicaments à grande (plus) échelle ?
Enfin – et c’était un “mais” décisif – le bénéfice en termes de morbidité ne s’est pas traduit par un avantage significatif en termes de survie. On sait certes, grâce à d’autres études comparant un traitement hypolipémiant plus intensif à un traitement modéré, qu’une réduction supplémentaire du cholestérol LDL n’a pas toujours un effet significatif sur la mortalité cardiovasculaire. Ou bien le bénéfice clinique complet n’apparaît qu’avec un certain retard (FOURIER était relativement court, avec une durée d’environ deux ans).
Dans la pratique clinique quotidienne, il subsistait néanmoins certains points d’interrogation et certaines restrictions quant à l’utilisation de cette nouvelle classe de médicaments coûteux, et l’on attendait avec d’autant plus d’impatience les premiers résultats du concurrent alirocumab.
ODYSSEY OUTCOMES
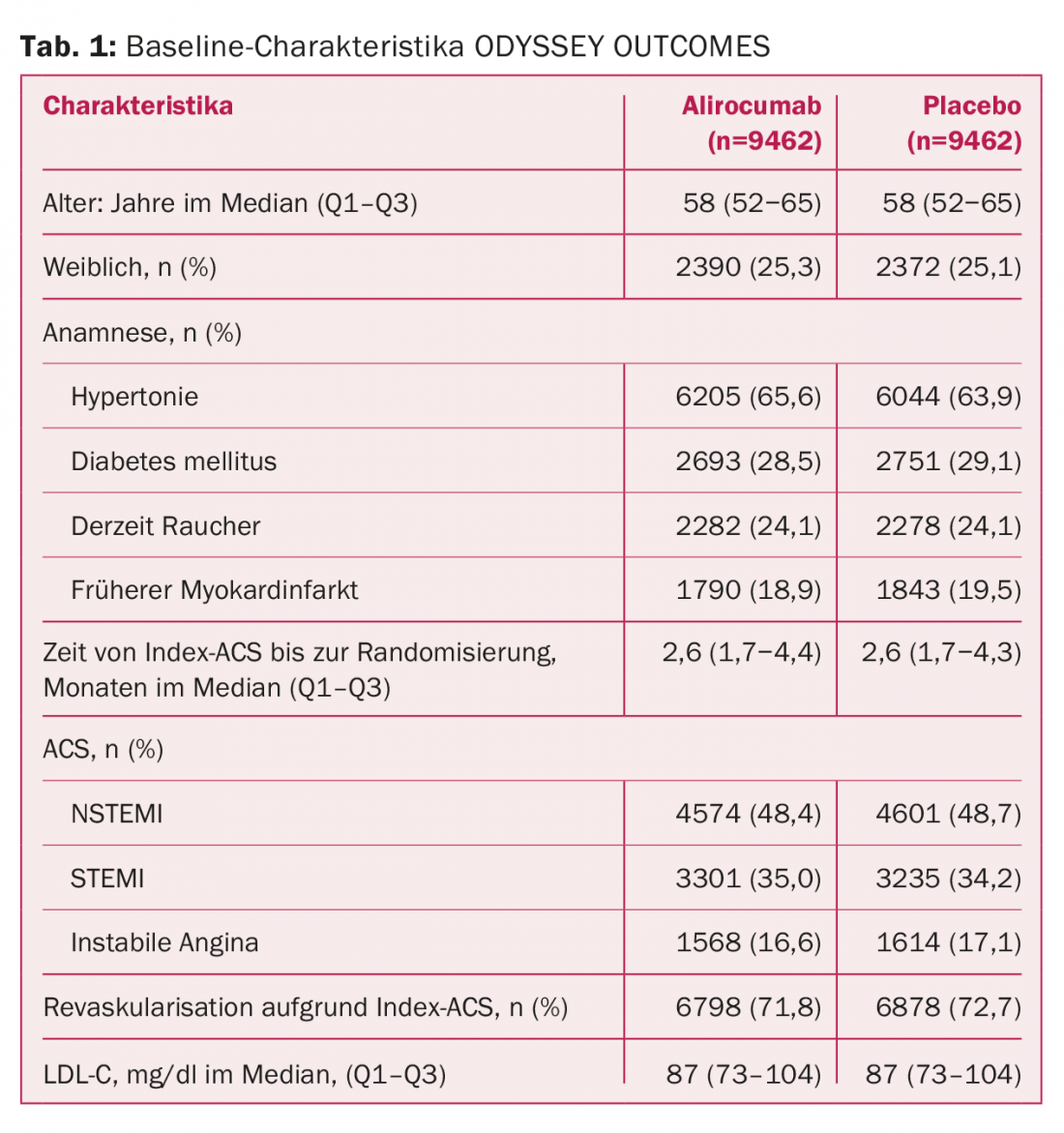
Elles sont maintenant là, sous la forme de l’étude ODYSSEY OUTCOMES. Et, pour commencer, ils ne clarifient pas non plus avec certitude tous les points en suspens concernant le traitement PCSK9. Cela s’explique d’une part par le choix différent de la population étudiée. Au lieu d’un peu plus de 27 000 patients présentant une maladie athérosclérotique stable et établie comme dans FOURIER, il s’agissait ici de près de 19 000 patients présentant un syndrome coronarien aigu (SCA) au cours des 1 à 12 derniers mois et un contrôle inadéquat des lipides, c’est-à-dire des valeurs de LDL-C ≥1,8 mmol/l malgré un traitement par statine de haute intensité ou toléré au maximum. 89% étaient sous atorvastatine/rosuvastatine à haute dose au début de l’étude, 3% recevaient de l’ézétimibe. Un échantillon présentant un risque clairement accru d’autres événements (tab. 1). Dans FOURIER, une minorité de patients présentaient un SCA au cours de l’année précédente.
Pris toutes les deux semaines, le médicament a réduit le risque d’événements cardiaques majeurs (MACE) de 15% par rapport au placebo. Il s’agissait notamment de décès dus à une maladie coronarienne, d’un infarctus du myocarde non fatal, d’un accident vasculaire cérébral ischémique ou d’un angor instable nécessitant une hospitalisation. C’est la différence suivante par rapport à FOURIER, qui incluait également la composante “plus douce” de la revascularisation coronaire dans le critère d’évaluation primaire. L’obstacle à la génération d’un avantage significatif a donc dû être un peu plus élevé cette fois-ci. La durée médiane du suivi était de 2,8 ans.
Le taux d’infarctus du myocarde et (cette fois aussi) la mortalité totale, considérés séparément, ont été également améliorés, le premier passant de 7,6% à 6,6% (p=0,006) et le second de 4,1% à 3,5% (p=0,026, réduction de 15%). Si l’on considère séparément les décès dus à une maladie coronarienne et les décès d’origine cardiovasculaire, qui sont également des critères d’évaluation secondaires, aucune différence significative n’a été observée. Il convient de noter qu’une étude globale menée dans 1 315 centres et 57 pays ne garantit pas nécessairement que les causes de décès sont toujours correctement documentées lorsque les patients meurent à domicile. En revanche, la mort elle-même peut être constatée partout avec certitude. La valeur p de 0,026 pour la mortalité totale est considérée comme “nominale”, car ce critère a été évalué statistiquement en aval (évaluation hiérarchique du critère).
Les patients ont bien toléré le traitement avec des taux comparables d’effets secondaires (y compris graves). Il n’y avait pas non plus de différences pertinentes en ce qui concerne le diabète new-onset, les réactions allergiques ou les événements neurocognitifs (le cas échéant, la substance active avait plutôt tendance à être supérieure au placebo). Après plus de trois ans de traitement dans ce grand collectif, aucun signal de sécurité n’a été observé sous alirocumab, hormis des réactions au point d’injection.
Plus c’est profond, mieux c’est
Comme FOURIER, ODYSSEY OUTCOMES est favorable à l’hypothèse “lower is better” et donc à l’adaptation du traitement aux niveaux de lipides (plutôt que de se baser uniquement sur l’intensité de la statine, voir la controverse des guidelines de ces dernières années entre les Etats-Unis et l’Europe). Mais elle laisse aussi supposer qu’en cas de maladie coronarienne, les valeurs cibles actuelles du LDL-cholestérol, inférieures à 70 mg/dl, ne sont pas encore optimales.
Au début de l’étude, le LDL-C était de 87 mg/dl. Des réductions de plus de 50 % du LDL-C ont été rapidement observées et se sont majoritairement maintenues au cours du suivi. Les réductions étaient qualitativement comparables à celles de FOURIER : après quatre mois sous alirocumab, le LDL-C était de 37,6 mg/dl, contre 93,3 mg/dl sous placebo, soit une réduction de plus de 60 pour cent. Des valeurs extrêmement claires, auxquelles l’inhibition de PCSK9 nous a désormais habitués.
On peut se demander si le succès croissant de l’inhibition de PCSK9 créera bientôt un nouveau standard, à savoir une réduction du LDL en dessous de 50 mg/dl ? Enfin, la dimension de l’amélioration clinique dans le critère d’évaluation primaire (et tout particulièrement pour les taux initiaux élevés de LDL) est remarquable. Et après FOURIER, ODYSSEY OUTCOMES est la deuxième grande étude à démontrer qu’une réduction du cholestérol LDL dans une fourchette de 25-50 mg/dl améliore le pronostic des patients atteints de maladie coronarienne.
A la fin du suivi à 48 mois, les niveaux étaient encore de 53,3 vs 101,4 mg/dl (réduction de 54,7%). L’objectif de l’étude était d’obtenir un LDL-C de 25-50 mg/dl, on a essayé activement (et avec une titration en aveugle) de maintenir le plus de patients possible dans cette fourchette cible. On ne sait donc pas si la diminution à long terme de la réduction du LDL-C est liée à la conception de l’étude (lorsque les valeurs étaient inférieures à la plage cible, la dose était ajustée ou on passait au placebo) ou au développement d’anticorps neutralisants contre la substance active, qui semblaient plus fréquents dans le groupe traité (42 contre 6 cas). Des études menées dans le cadre d’un autre programme d’étude appelé SPIRE [1,2] avec l’anticorps PCSK9 bococizumab ont été interrompues prématurément, entre autres, précisément en raison de ce problème : apparemment, l’effet de réduction du LDL a nettement diminué en raison de la formation de l’anticorps. Seuls les patients dont la LDL-C de base était supérieure à 2,6 mmol/l ont bénéficié de SPIRE 1 et 2, respectivement pour l’évolocumab et l’évolocumab. dans FOURIER, le problème ne s’est pas manifesté. Selon les auteurs d’ODYSSEY OUTCOMES, l’alirocumab ne devrait pas non plus avoir d’effet néfaste dû aux anticorps.
Qui en profite le plus ?
Les appels en faveur d’une analyse coût-efficacité des inhibiteurs de PCSK9 n’ont donc pas cessé, même après l’accueil globalement positif réservé à ODYSSEY OUTCOMES. Les évaluations réalisées jusqu’à présent ont abouti à une conclusion négative [3,4]. Il faudrait soit modifier le prix, soit définir plus précisément les patients pour lesquels le bénéfice l’emporte clairement sur les coûts, a-t-on entendu à plusieurs reprises lors du congrès. Une pression accrue sur les assureurs pour qu’ils remboursent plus largement cette classe de médicaments a également été demandée. Les analyses de sous-groupes issues d’ODYSSEY OUTCOMES indiquent que les patients présentant un LDL-C ≥100 mg/dl au moment de la ligne de base (médiane de 118 mg/dl) en tirent particulièrement profit. Chez eux, la MACE passe de 14,9% à 11,5% (HR 0,76) et la mortalité totale de 5,7% à 4,1% (HR 0,71). Des réductions de risque similaires ont été observées dans ce sous-groupe pour les décès dus à une maladie coronarienne et les décès d’origine cardiovasculaire. Cependant, aucune interaction significative n’a été observée entre les résultats primaires ou la mortalité totale et les niveaux de LDL-C de référence (p=0,09 et p=0,12). Même le groupe avec un LDL-C de base <80 mg/dl a connu une réduction du risque de 14% sur le critère d’évaluation primaire et de 11% sur la mortalité totale sous l’effet de la substance active (fig. 1 et 2).
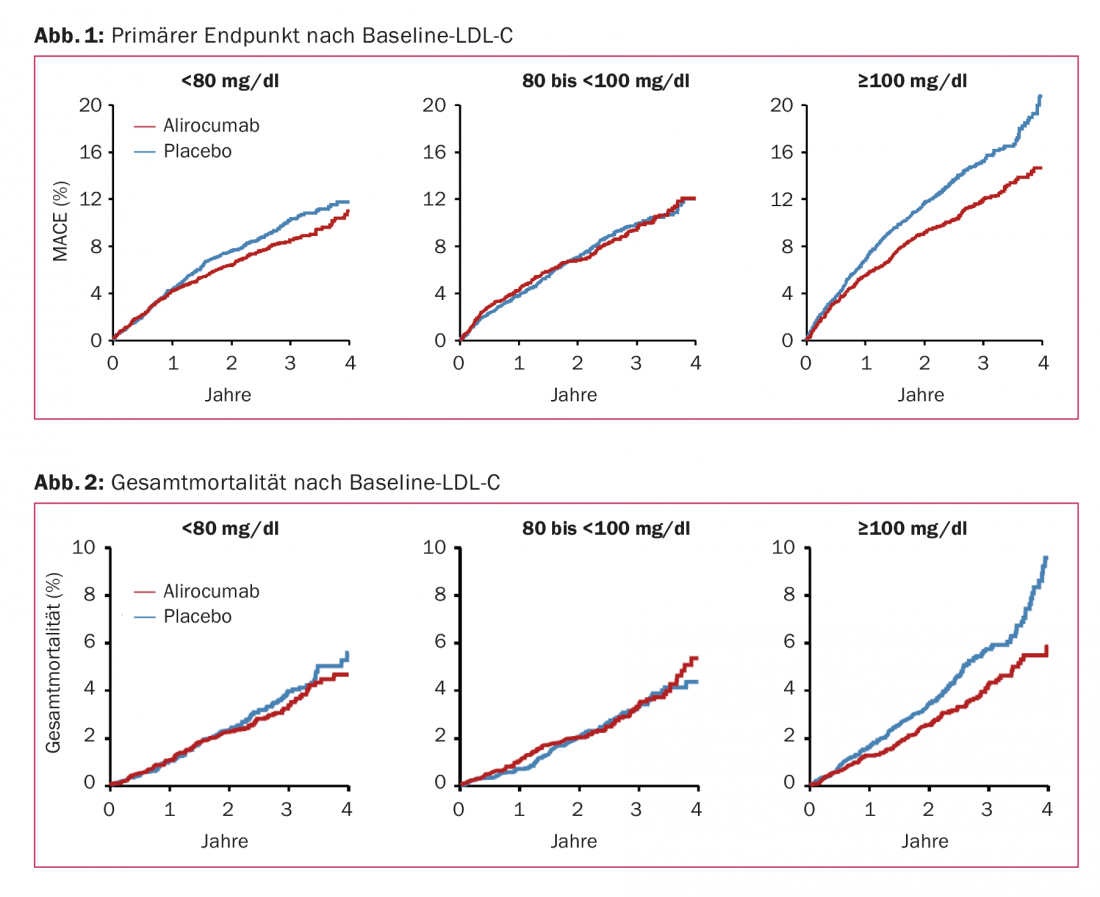
Dans l’ensemble, la population post-ACS dans ODYSSEY OUTCOMES présentait néanmoins un risque plus élevé que l’échantillon FOURIER. En effet, en dépit de stratégies préventives fondées sur des preuves, le risque résiduel reste élevé peu après un SCA et est, du moins en partie, lié aux niveaux de LDL-C. Le risque d’accident vasculaire cérébral (AVC) est donc plus élevé que le risque de décès. Si ces taux sont réduits tôt après l’événement, par exemple par un traitement par statine [5] – surtout à haute intensité [6] ou en association avec l’ézétimibe [7] -, le risque d’autres événements diminue également (remarque secondaire : l’étude SECURE-PCI, également menée à l’ACC 18, a remis en question la question de savoir si le principe “plus les statines sont précoces en cas de SCA, mieux c’est” s’applique ici). Il semble que l’effet protecteur puisse être encore renforcé par la puissante inhibition de PCSK9. Peut-être est-ce donc effectivement surtout ce groupe à haut risque qui bénéficie de l’inhibition de PCSK9, non seulement en termes de morbidité, mais aussi de mortalité, ce qui permettrait de mieux soutenir les prix élevés des médicaments. Outre la population différente de l’étude, l’allongement de la période de suivi pourrait également avoir joué un rôle dans l’amélioration de la survie.
Quoi qu’il en soit, après les deux études positives FOURIER et ODYSSEY OUTCOMES, il faut maintenant trouver une solution en termes de coûts pour pouvoir enfin donner la molécule à tous les patients qui en bénéficieraient (ce qui, selon les preuves actuelles, est le cas de beaucoup). Enfin, la sécurité, qui est généralement du côté des coûts ou des risques/bénéfices, est si bonne dans le cas de l’inhibition des PCSK9 que le pendule pencherait clairement du côté des bénéfices – si l’on ne tient pas compte du prix des médicaments.
Il est clair qu’ODYSSEY OUTCOMES fournit la prochaine pièce du puzzle dans une image globale qui devient de plus en plus claire pour cette classe de médicaments relativement nouvelle. Selon les études actuelles, l’évolocumab est indiqué pour les patients souffrant d’une maladie cardiovasculaire athéroscléreuse stable et l’alirocumab pour les patients atteints de SCA, et ce jusqu’à ce qu’un effet de classe soit confirmé.
L’alirocumab est actuellement autorisé en accompagnement d’un régime alimentaire et en complément d’une dose maximale de statine tolérée, avec ou sans autre traitement modificateur de lipides, pour le traitement des adultes atteints d’hypercholestérolémie familiale hétérozygote sévère ou d’une maladie cardiovasculaire athéroscléreuse cliniquement manifeste nécessitant une réduction supplémentaire du LDL-C. L’alirocumab est également autorisé en complément d’un régime alimentaire et en complément d’une dose maximale de statine tolérée, avec ou sans autre traitement modificateur de lipides. Selon Limitatio, son utilisation en prévention secondaire est actuellement limitée aux patients présentant un LDL-C >3,5 mmol/l et/ou une maladie cardiovasculaire athérosclérotique clinique progressive avec un LDL-C >2,6 mmol/l.
Source : American College of Cardiology (ACC) 2018 Annual Scientific Session, 10-12 mars 2018, Orlando
Littérature :
- Ridker PM, et al : Cardiovascular Efficacy and Safety of Bococizumab in High-Risk Patients. N Engl J Med 2017 ; 376 : 1527-1539.
- Ridker PM, et al : Lipid-Reduction Variability and Antidrug-Antibody Formation with Bococizumab. N Engl J Med 2017 ; 376 : 1517-1526.
- Kazi DS, et al. : Updated Cost-effectiveness Analysis of PCSK9 Inhibitors Based on the Results of the FOURIER Trial. JAMA 2017 ; 318(8) : 748-750.
- Fonarow GC, et al : Cost-effectiveness of Evolocumab Therapy for Reducing Cardiovascular Events in Patients With Atherosclerotic Cardiovascular Disease. JAMA Cardiol 2017 ; 2(10) : 1069-1078.
- Schwartz GG, et al : Effects of atorvastatin on early recurrent ischemic events in acute coronary syndromes : the MIRACL study : a randomized controlled trial. JAMA 2001 avr 4 ; 285(13) : 1711-1718.
- Cannon CP, et al : Intensive versus moderate lipid lowering with statins after acute coronary syndromes. N Engl J Med 2004 Apr 8 ; 350(15) : 1495-1504.
- Cannon CP, et al : Ezetimibe Added to Statin Therapy after Acute Coronary Syndromes. N Engl J Med 2015 juin 18 ; 372(25) : 2387-2397.
CARDIOVASC 2018 ; 17(2) : 35-38