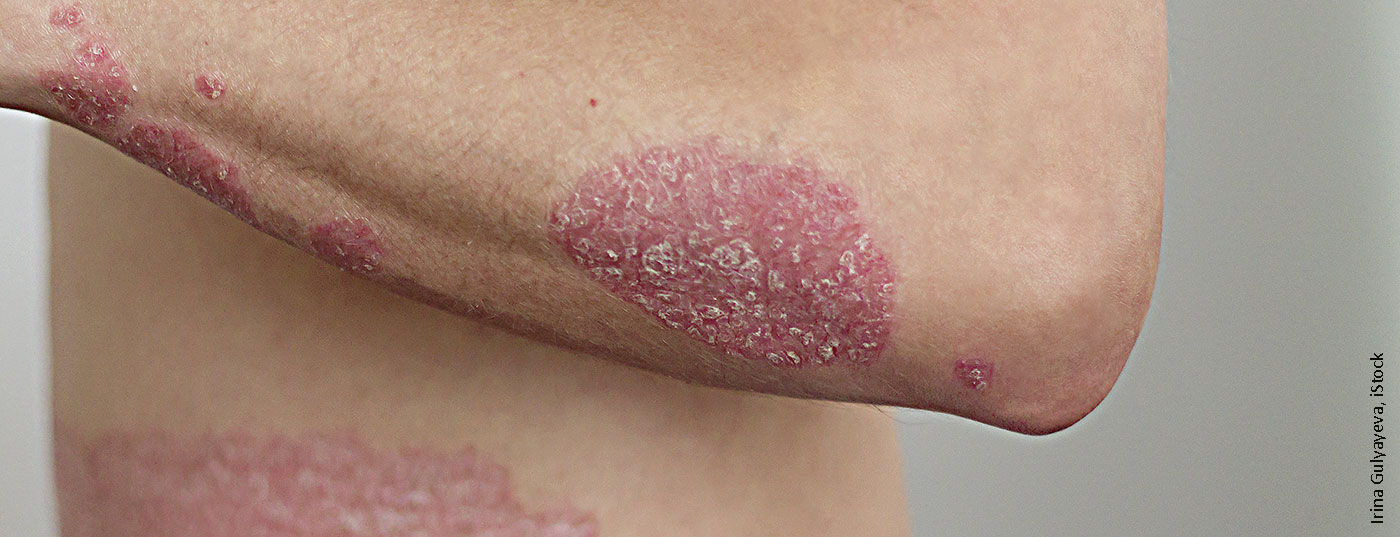
Le psoriasis est aujourd’hui bien traité par des thérapies moléculaires. Les médicaments biologiques permettent d’obtenir des taux de réponse optimisés. Par rapport à leurs prédécesseurs, les nouveaux médicaments de cette classe de substances se caractérisent par des effets durables et persistants. Cela a été objectivement prouvé à plusieurs reprises.
Les données des ECR montrent qu’en 20 ans, les taux de réponse se sont améliorés, passant de 16-25% à 90% de PASI75, et que les PASI90 et PASI100 sont aujourd’hui des objectifs thérapeutiques réalistes [1,2]. La disponibilité de thérapies biologiques ciblées va de pair avec une meilleure compréhension biologique de la pathogenèse du psoriasis, a expliqué James G. Krueger, MD, PhD, Rockefeller University (États-Unis). Il y a environ 15 ans, on s’est rendu compte que les maladies inflammatoires de la peau étaient associées à des sous-populations de lymphocytes T. Les chercheurs ont découvert que ces sous-populations de lymphocytes T avaient une influence sur les maladies inflammatoires de la peau.
Changement de paradigme du modèle explicatif pathogénétique
Le modèle de pathogenèse IL17/IL23, qui remplace depuis 2010 les concepts étiologiques antérieurs, fournit la description suivante de la cascade sous-jacente aux lésions psoriasiques [3] :
1) Les cellules dendritiques produisent de l’IL23, dont les sorties activent l’IL17, 2) L’IL17 déclenche la production de cytokines et d’autres molécules inflammatoires par les kératinocytes.
Des données montrent qu’après deux mois de traitement par risankizumab (antagoniste de l’IL23), une réduction des mécanismes d’alimentation en aval typiques du psoriasis est mesurable dans l’épiderme. Après trois mois de traitement par sécukinumab (antagoniste de l’IL17), une forte réduction de différents processus liés à l’IL17 est démontrée [2].
“Drug survival” crucial pour la stratégie à long terme
Le psoriasis est une maladie qui dure toute la vie – une question centrale est de savoir si l’on peut contrôler efficacement les symptômes du psoriasis au moyen de médicaments biologiques sur une longue période. Alors que la durée de traitement des médicaments contre le psoriasis était autrefois limitée par la toxicité, le bénéfice clinique et la “survie du médicament” (durée d’utilisation) sont aujourd’hui des facteurs déterminants. En 2010, l’une des premières études sur la durabilité des bénéfices cliniques des médicaments biologiques a été publiée. Le Dr Krueger a expliqué que cette étude a montré que la réponse au traitement par ustékinumab (antagoniste de l’IL12/IL23), mesurable à 12 et 24 semaines, pouvait être maintenue sur une période de 3 ans [1].
Après 5 ans supplémentaires, les données de registre des patients naïfs de traitement biologique ont été évaluées. Avec l’ustékinumab, les effets positifs ont pu être maintenus sur une période de 4 à 5 ans, contrairement au traitement par inhibiteurs du TNFα, où l’on a observé une chute rapide des effets sur la même période et où seuls 50% des patients ont maintenu le traitement. Ce phénomène peut s’expliquer par différents mécanismes d’action, explique le conférencier [1]. Le “drug survival” joue un rôle crucial à cet égard. Il s’agit de la durée avant l’interruption d’un traitement et est influencé, outre l’efficacité, entre autres par la tolérance d’une préparation.
|
Résumé L’obtention d’une clairance de 100% (PASI100) reflète l’activité de fond liée au psoriasis présente avant le traitement. Outre le PASI100 ou le PGA0 pour le plus grand nombre de patients possible, un autre objectif pour l’avenir est de réduire les “Molecular Scars” dans les lésions rémittentes. Cela, ainsi que la prise en compte des comorbidités associées à la maladie dans le traitement, devrait permettre d’améliorer la qualité de vie. Il existe des différences intéressantes dans les “Molecular Scars” des lésions cliniquement rémittentes entre les différents agents biologiques, les représentants de la nouvelle génération étant supérieurs à cet égard selon les analyses “responder-to-responder” [1,4–6]. Il en va de même pour la “survie au médicament” (durée d’utilisation), qui joue un rôle important dans les stratégies thérapeutiques à long terme. |
“Molecular Scars” comme indicateur d’efficacité durable
Les données à long terme issues d’ECR et d’études d’extension illustrent les effets durables des médicaments biologiques modernes. Les données à 5 ans de l’ustékinumab (antagoniste d’IL12/IL23), du brodalumab et de l’ixekinumab (tous deux antagonistes d’IL17) montrent des effets stables et durables en termes de taux de réponse PASI75/90/100. En ce qui concerne les inhibiteurs de l’IL23 seuls, les données sont moins nombreuses, car les représentants de cette classe de substances n’existent pas depuis très longtemps. Les données à 4 ans du tildrazikumab montrent une évolution similaire à celle des antagonistes de l’IL17. C’est également le cas pour les données à 3 ans du guselkumab et les données à 2 ans du risankizumab. Les “cicatrices moléculaires” sont un indicateur mesurable de l’activité inflammatoire résiduelle qui persiste malgré la suppression des processus lésionnels. Il s’agit du profil d’expression génétique pathologique restant (gènes transcriptomiques avec <75% d’amélioration au moment de l’analyse du point final). Il contient des informations inflammatoires résiduelles qui peuvent réinitialiser une poussée de psoriasis.
Il ressort d’une étude randomisée en tête-à-tête [4] que l’ustékinumab entraîne une rémission plus importante au niveau moléculaire par rapport à l’étanercept (inhibiteur du TNFα) (analyse de répondeur à répondeur). Des différences hautement significatives ont également été mises en évidence entre le risankizumab et l’ustékinumab [5]. Comparé à l’ustékinumab, le guselkumab a notamment montré une réduction plus importante des cellules T et des cellules dendritiques inflammatoires [6].
Source : EADV, Madrid
Littérature :
- Krueger JG : Biologics in Psoriasis, Training and education forum, James G. Krueger, MD, PhD, Rockefeller University (USA), EADV Madrid, 11.10.2019.
- Krueger JG, et al : JACI 2019 ; 144(3) : 750-763.
- Hawkes JE, Chan TC, Krueger JG : JACI 2017 ; 140(3) : 645-653.
- Brodmerkel C, et al : JACI 2019 ; 143(5) : 1965-1969.
- Visvanathan S, et al : JACI 2019 ; 143(6) : 2158-2169.
- Li K, et al. : www.psoriasisg2c.com, dernière consultation 10.01.2020.
DERMATOLOGIE PRAXIS 2020 ; 30(1) : 20 (publié le 25.2.20, ahead of print)