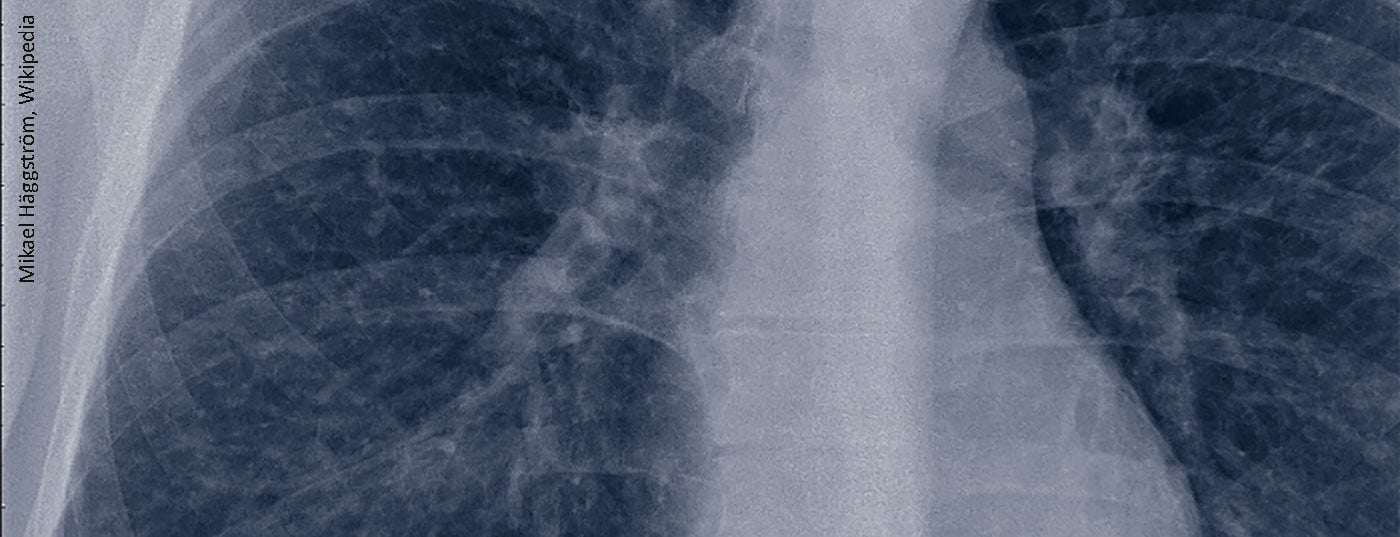
La sarcoïdose affecte le plus souvent les poumons, mais des manifestations extrapulmonaires peuvent également se produire. L’implication isolée d’un seul organe ou système d’organes est rare dans la sarcoïdose, c’est pourquoi les patients doivent être examinés de manière approfondie pour détecter d’autres manifestations de la maladie. Lors du Congrès allemand de rhumatologie, un expert a donné des recommandations actualisées sur le diagnostic et le traitement de la maladie.
En raison de l’implication fréquente des poumons (plus de 90% [2]), la sarcoïdose est souvent entre les mains des pneumologues, mais le tableau clinique est également pertinent pour les rhumatologues. En général, les maladies rhumatologiques avec atteinte pulmonaire peuvent également présenter d’autres manifestations organiques, telles qu’une atteinte des reins, des glandes salivaires, des yeux, des articulations et de la peau. La distinction avec d’autres maladies auto-immunes se fait par des examens de laboratoire, des tests d’imagerie ou une biopsie des organes concernés (aperçu 1) [3].

Recommandations actuelles en matière de diagnostic
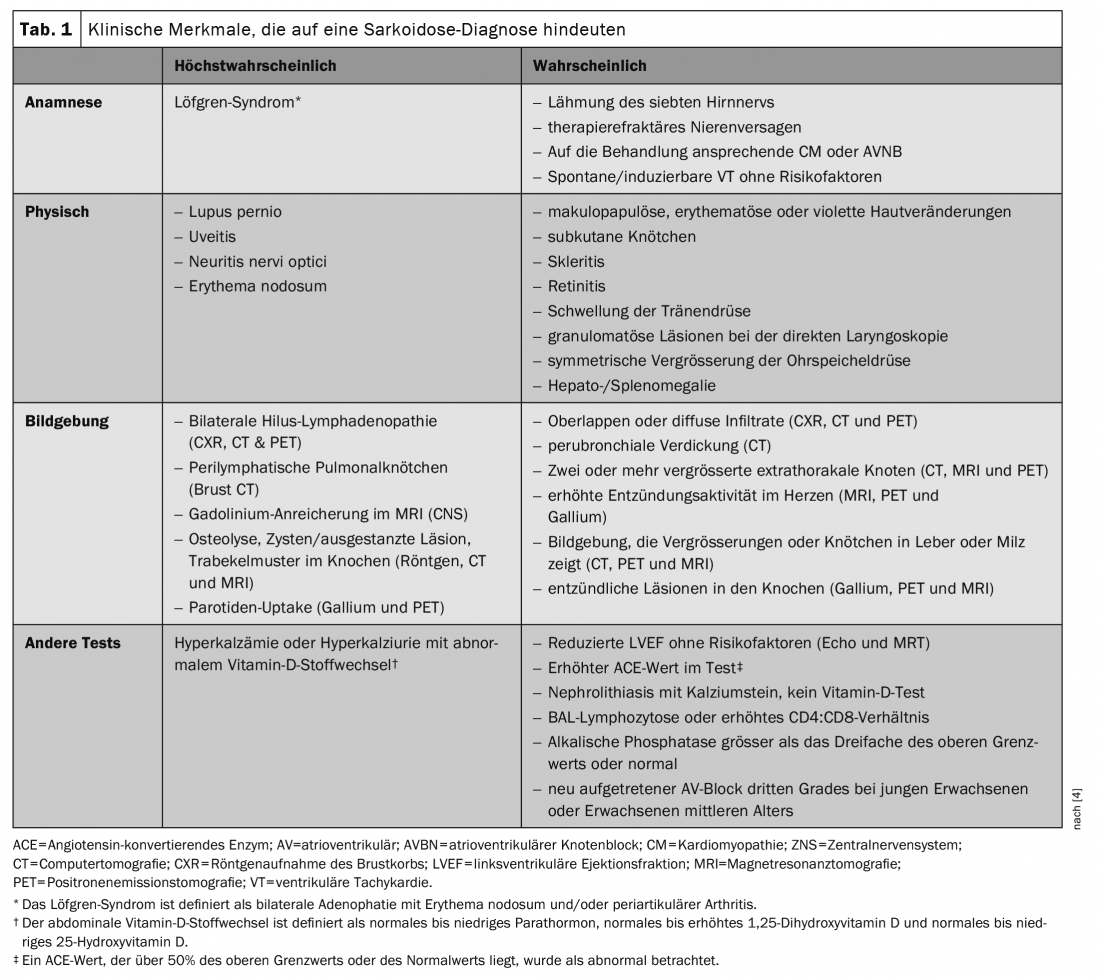
Le diagnostic de la sarcoïdose n’est pas standardisé, mais repose sur trois critères principaux : Un aspect clinique compatible, la découverte d’une inflammation granulomateuse non nécrosante dans un ou plusieurs échantillons de tissus et l’exclusion des causes alternatives de maladie granulomateuse. Il n’existe cependant pas de mesures généralement reconnues pour déterminer si chaque critère de diagnostic a été rempli. Alors que de nombreux cas de sarcoïdose posent un dilemme diagnostique, certaines caractéristiques cliniques de la sarcoïdose sont considérées comme si hautement spécifiques de la maladie qu’elles sont considérées comme diagnostiques. Il s’agit notamment du syndrome de Löfgren, du lupus pernio et du syndrome de Heerfordt. D’autres caractéristiques ont été fortement associées à la sarcoïdose, par exemple une adénopathie bilatérale de la région hilaire chez les patients ne présentant pas de symptômes B (fièvre, sueurs nocturnes et perte de poids) (tableau 1) [4]. Dans le cas du syndrome de Löfgren, du lupus pernio, de la maladie de Heerfordt et de la lymphadénopathie bihile sans symptôme B, il n’est pas nécessaire de pratiquer une biopsie de détection. Dans tous les autres cas, la sarcoïdose ne peut pas être exclue avec certitude, c’est pourquoi le diagnostic doit toujours être posé par biopsie.
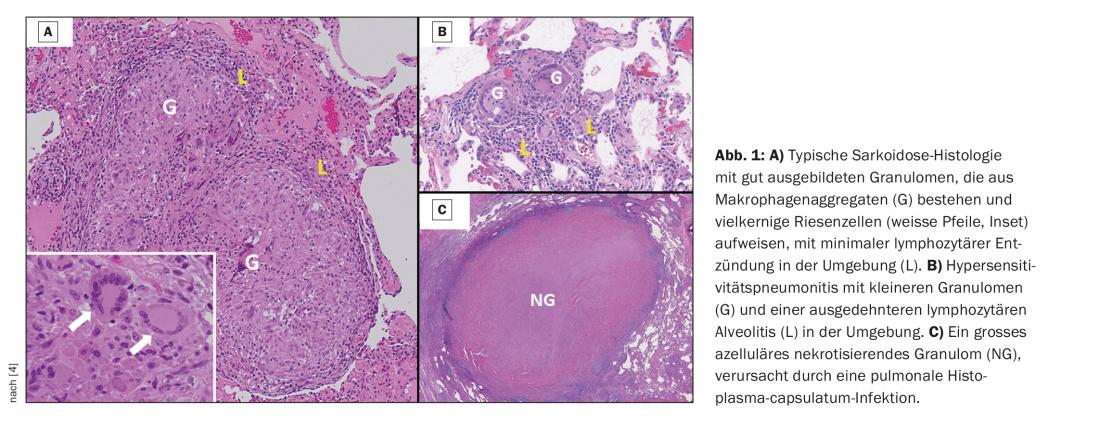
Comme les manifestations cliniques de la sarcoïdose sont souvent non spécifiques, une évaluation histologique des granulomes tissulaires est souvent nécessaire pour établir le diagnostic. Les caractéristiques histologiques typiques du granulome sarcoïdosique incluent la présence de couches concentriques bien développées de cellules immunitaires, dont le noyau central composé d’agrégats de macrophages et de cellules géantes multinucléées est le plus frappant. Une couche externe de lymphocytes peu organisés, généralement des cellules T, est souvent observée avec quelques cellules dendritiques intercalées. Dans certains cas, les granulomes sont entourés d’amas isolés de lymphocytes B. Dans d’autres cas, les granulomes sont entourés d’amas isolés de lymphocytes B. Les granulomes de la sarcoïdose ne sont pas nécrotiques dans la plupart des cas, mais des variantes de la sarcoïdose, notamment le phénotype nodulaire pulmonaire de la sarcoïdose, peuvent apparaître avec un mélange de granulomes nécrotiques et non nécrotiques. La figure 1 présente des caractéristiques histopathologiques utiles pour distinguer la sarcoïdose des autres causes, bien que les caractéristiques histopathologiques seules ne permettent pas de distinguer la sarcoïdose des autres maladies granulomateuses.
Dépistage des maladies extrapulmonaires
Chez les patients atteints de sarcoïdose, un examen oculaire de base est recommandé pour dépister la sarcoïdose oculaire. Les patients qui ne présentent ni symptômes rénaux ni sarcoïdose rénale établie doivent subir un test de base de la créatinine sérique pour dépister une sarcoïdose rénale. Chez les patients atteints de sarcoïdose qui ne présentent ni symptômes hépatiques ni sarcoïdose hépatique établie, un dosage sérique des phosphatases alcalines est recommandé pour le dépistage de la sarcoïdose hépatique. Pour les patients qui ne présentent ni symptômes hépatiques ni sarcoïdose hépatique avérée, aucune recommandation n’est formulée pour ou contre un test de base des transaminases sériques. En revanche, il convient d’effectuer un test sérique de base du calcium pour dépister un métabolisme calcique anormal. Si une évaluation du métabolisme de la vitamine D est jugée nécessaire chez un patient atteint de sarcoïdose, par exemple pour déterminer si une substitution en vitamine D est indiquée, il est recommandé de mesurer à la fois les taux de 25 et de 1,25 OH-vitamine D avant de procéder à la substitution en vitamine D. Les taux de 25 et de 1,25 OH-vitamine D peuvent être mesurés à l’aide d’un appareil de mesure de l’hémoglobine. En outre, un hémogramme complet doit être réalisé afin de détecter toute anomalie hématologique. Il est également recommandé de réaliser un ECG de base pour dépister une éventuelle implication cardiaque. En revanche, il n’est pas recommandé de pratiquer systématiquement une échocardiographie transthoracique (ETT) ou une surveillance ambulatoire par ECG sur 24 heures (Holter) pour dépister une éventuelle implication cardiaque [4].
Évaluation diagnostique d’une suspicion de maladie extrapulmonaire
En cas de suspicion d’implication cardiaque, il est recommandé de réaliser une imagerie par résonance magnétique (IRM) cardiaque plutôt qu’une tomographie par émission de positons (TEP) ou une ETT afin d’obtenir des informations à la fois diagnostiques et pronostiques. Pour les patients dont l’implication cardiaque est suspectée et qui sont traités dans un environnement où l’IRM cardiaque n’est pas disponible, il est recommandé de réaliser une TEP spécifique plutôt qu’une ETT afin d’obtenir des informations à la fois diagnostiques et pronostiques. Les patients chez qui une hypertension pulmonaire (HTP) est suspectée doivent bénéficier d’un examen initial par ETT. Si une HTP est simplement suspectée ou si l’échocardiographie transthoracique suggère une HTP, un cathétérisme cardiaque droit doit être réalisé pour confirmer ou exclure définitivement une HTP. Si une HTP est suspectée mais qu’un échocardiogramme transthoracique ne l’indique pas, la nécessité d’un cathétérisme cardiaque droit doit être décidée au cas par cas [4].
Traitement dépendant des manifestations
Les principales raisons du traitement de la sarcoïdose sont la réduction du risque de morbidité et de mortalité et l’amélioration de la qualité de vie. L’indication du traitement varie en fonction de la manifestation à l’origine des symptômes : poumons, cœur, cerveau, peau ou autres. Les manifestations de la sarcoïdose cardiaque comprennent un retard de conduction auriculo-ventriculaire, un bloc de conduction du système His-Purkinje, des tachyarythmies ventriculaires et supraventriculaires et une cardiomyopathie. L’utilisation de glucocorticoïdes est donc recommandée chez les patients présentant des signes d’anomalies cardiaques fonctionnelles, y compris un bloc cardiaque, des troubles du rythme ou une cardiomyopathie.
Les manifestations cliniques de la neurosarcoïdose symptomatique ont souvent un impact important sur la qualité de vie du patient atteint de sarcoïdose et comprennent une paralysie faciale, une névrite optique, une méningite aseptique, des séquelles graves de lésions granulomateuses massives du système nerveux central, une hydrocéphalie et une encéphalopathie/psychose. Un traitement par glucocorticoïdes est donc recommandé pour les patients présentant une neurosarcoïdose cliniquement significative. Chez les patients atteints de neurosarcoïdose qui ont été traités par des glucocorticoïdes et chez qui la maladie persiste, il est recommandé d’ajouter du méthotrexate. Si la maladie persiste, il convient d’administrer de l’infliximab.
Avant de pouvoir diagnostiquer une fatigue associée à la sarcoïdose (FAS), il faut exclure d’autres causes de fatigue. Il s’agit notamment du diabète sucré, des troubles de la fonction thyroïdienne, des troubles neuroendocriniens, des troubles mentaux (en particulier la dépression), de l’apnée obstructive du sommeil, de la neuropathie à petites fibres, de la carence en vitamine D (en particulier un faible taux de 1,25-dihydroxycholécalciférol), de l’insuffisance cardiaque et des troubles neurologiques. Chez les patients atteints de sarcoïdose qui souffrent de fatigue incommodante, il est recommandé de suivre un programme de réadaptation pulmonaire et/ou un entraînement de la force musculaire inspiratoire pendant 6 à 12 semaines pour améliorer la fatigue. Si la fatigue n’est pas liée à l’activité de la maladie et qu’un programme d’exercice ou de réadaptation pulmonaire a été testé, il est recommandé d’utiliser le D-méthylphénidate ou l’armodafinil pendant 8 semaines afin de tester l’effet sur la fatigue et la tolérance [5].
Congrès : Congrès allemand de rhumatologie 2021
Littérature :
- Dr Peter Korsten, Recommandations actuelles pour le diagnostic et le traitement de la sarcoïdose, présentation du Congrès allemand de rhumatologie 2021, 17.09.2021.
- Al-Kofahi K, et al : Management of extrapulmonary sarcoidosis : challenges and solutions. Ther Clin Risk Manag 2016, doi : 10.2147/TCRM.S74476.
- Korsten P, et al : Sarcoïdose et maladies auto-immunes : différences, similitudes et chevauchements. CURR OPIN PULM MED 2018, doi : 10.1097/MCP.0000000000000500.
- Crouser E, et al. : Diagnostic et détection de la sarcoïdose. An Official American Thoracic Society Clinical Practice Guideline. Am J Respir Crit Care Med 2020, doi : 10.1164/rccm.202002-0251ST.
- Baughman R, et al : ERS clinical practice guidelines on treatment of sarcoidosis. Eur Respir J 2021, doi : 10.1183/13993003.04079-2020.
InFo DOULEUR & GERIATRIE